非洲猪瘟病毒多基因家族成员MGF360-12L RPA检测方法的建立
2020-04-02吴映彤王西西陈鸿军朱鸿飞郭晓宇
吴映彤,王西西,吴 竞,2,陈鸿军,朱鸿飞,郭晓宇
(1.中国农业科学院北京畜牧兽医研究所,北京 100193;2.比利时列日大学 让布鲁农学院,列日 4000;3.中国农业科学院上海兽医研究所,上海 200241)
非洲猪瘟(africa swine fever,ASF)是由非洲猪瘟病毒(Africa swine fever virus,ASFV)引起的家猪和野猪的一种急性、热性和高传染性疾病,其临床症状表现为发热、呕吐、皮肤发绀、内脏器官明显出血等[1]。20世纪初,ASF病例首次发现于肯尼亚,自此ASV疫情迅速在非洲大部分地区蔓延[2]。2007年,ASF疫情在高加索地区的格鲁吉亚出现,随后迅速蔓延至俄罗斯联邦以及东欧等周边国家[3-4]。2018年8月1日,我国辽宁省沈阳市沈北区发现ASF疫情,经B646L/p72基因进化树分析发现该病毒属于基因Ⅱ型,与目前在俄罗斯和东欧流行的Georgia 2007/1毒株属于一个进化分支[5]。目前已在辽宁、河南、江苏、浙江、安徽、黑龙江、内蒙、吉林、天津等9个省直辖市发现ASF疫情。
ASFV基因组大小约为170~190 kb,含有151~167个开放阅读框(open reading frame,ORF),其中约30%的ORF存在多个拷贝,即多基因家族,包括MGF100、MGF110、MGF300、MGF360和MGF505/530,不同分离毒株的ORF拷贝数也各不相同[6],MGFs家族基因编码的多个拷贝可能为病毒提供了选择进化的优势[7]。由于ASFV中某些基因可干扰宿主免疫应答,缺失这些基因将有助于增强宿主的免疫应答[8]。已有研究发现,ASFV弱毒株OURT88/3在缺失MGF360-10L、11L、12L、13L、14L后,可分别在体内和体外诱导产生较高水平的IFN,并在免疫后提供针对同源基因Ⅰ型及其他基因型的攻毒保护[9-10]。MGFs家族基因缺失疫苗被认为是非洲猪瘟疫苗研制的主要方向之一,因此建立针对MGFs家族基因的鉴别诊断方法尤为重要。当前常用的分子诊断方法主要有PCR、实时荧光定量PCR、环介导技术等温扩增(loop-mediated isothermal amplification,LAMP)等,但这些方法大多需要昂贵的仪器设备、繁琐的实验程序、较长的检测时间[11-12]或出现检测结果不准确(LAMP)等现象[13],难以满足检测需要。重组酶聚合酶扩增(recombinase polymerase amplification,RPA)是一种新兴的核酸等温扩增技术,该技术对硬件设备的要求很低,在重组酶、单链结合蛋白(single strand DNA-binding protein,SSB)、DNA聚合酶等参与下,以恒定温度即可获得高灵敏性及特异性的核酸扩增产物[14],可用于体外诊断,适用于兽医、食品安全、生物安全、农业等领域。
鉴于此,本实验比较近年来周边国家报道的ASFV毒株序列,主要根据Georgia 2007/1毒株MGF360-12L基因的参考序列,进行RPA引物设计,筛选最适引物,对反应条件进行优化,并验证检测方法的特异性、灵敏性,为后续ASFV MGF360-12L缺失毒株的鉴别诊断提供一定的技术支持。
1 材料与方法
1.1 主要试剂与仪器 TwistAmpTMDNA amplification kit购自英国TwistDx公司;DNA纯化回收试剂盒、质粒DNA小量抽提试剂盒(OMEGA)购自北京佳诚实创科技有限公司;质粒DNA中提试剂盒(GeneMark)购自北京达科为生物技术公司;病毒RNA提取试剂盒、2× Primer STAR Mix、5×Prime Script Mix反转录试剂盒购自北京宝日医生物技术有限公司;2×Reatime PCR Mix(SYBR green)购自北京聚合美生物技术公司;2×TaqPCR Mix购自南京诺唯赞生物技术公司;引物合成与测序送至金唯智生物技术(苏州)公司。
1.2 病毒株和临床样品 含有ASFV Georgia 2007/1毒株12L基因的真核重组质粒pcDNA3.1-12L由本实验室构建并保存。猪繁殖与呼吸综合征病毒(Porcine reproductive and respiratory syndrome,PRRSV)、猪流行性腹泻病毒(Porcine epidemic diarrhea virus,PEDV)基因组RNA和伪狂犬病毒(Pseudorabies virus,PRV)、猪圆环病毒2型(Porcine circovirus 2,PCV-2)基因组DNA由本实验室保存;猪瘟病毒(Classical swine fever virus,CSFV)基因组RNA提取自瑞普商品化兔脾淋活疫苗;O型口蹄疫病毒(Foot-and-mouth disease virus,FMDV)基因组RNA提取自中农威特猪口蹄疫灭活疫苗。15份未知病原的临床样品由本实验室保存。
1.3 标准质粒的构建及拷贝数确定 根据GenBank中ASFV Georgia 2007/1株(GenBank登录号:FR682468.1)参考序列,确定MGF360-12L基因序列信息,合成并克隆至pUC57载体。将目的基因连接至真核载体pcDNA3.1,构建标准重组质粒pcDNA3.1-12L。拷贝数(copies/μL)=6.02×1023×[质粒浓度(ng/μL)×10-9/(质粒碱基数×660)]。
1.4 病毒RNA的提取 根据病毒RNA提取试剂盒提取病毒核酸。按照反转录说明书,将PRRSV、CSFV、FMDV和PEDV基因组RNA反转录为cDNA,并测定其浓度;所有病毒DNA和cDNA模板保存于-20℃备用。
1.5 RPA引物设计 参考GenBank中ASFV Georgia2007/1株MGF360-12L基因序列,设计RPA引物,目的片段大小为216 bp。同时设计普通PCR和实时荧光定量PCR引物,具体见表1。
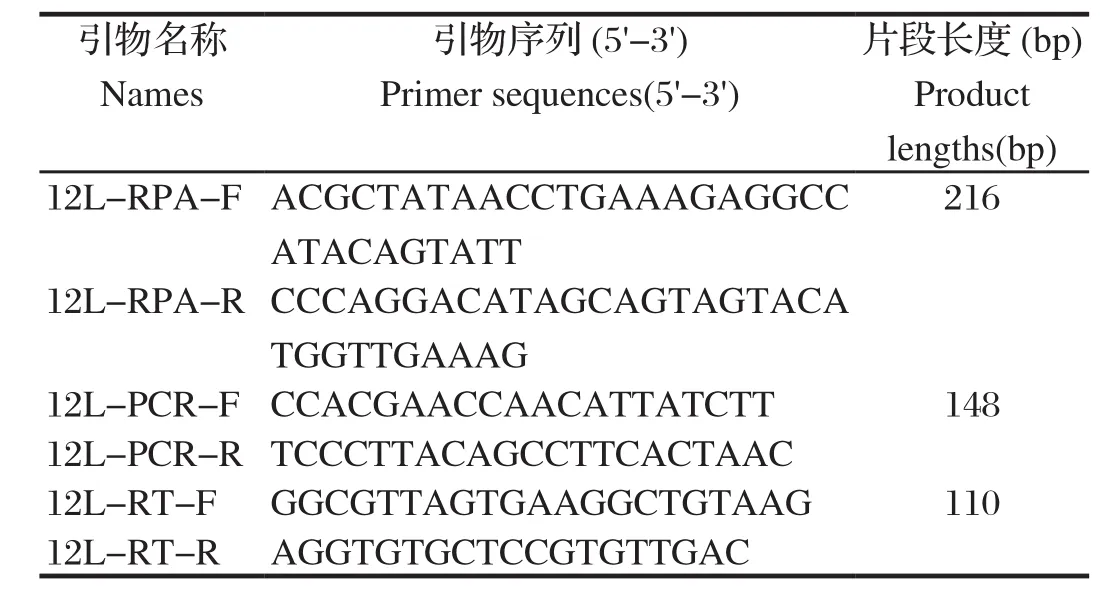
表1 本研究引物Table 1 The primers used in this study
1.6 RPA检测方法的建立与条件优化 使用TwistAmpTMDNA amplification kit配制50 μL RPA反应体系,其中上、下游引物12L-RPA-F/12L-RPA-R(10 μmol/L)各2.4 μL,rehydration buffer 29.5 μL,DNase/RNase Free H2O 11.2 μL,模板2 μL。将以上试剂预混后转入含冻干酶制剂的反应管中,将2.5 μL 280 mmol/L MgAc加于反应管盖上,盖紧后瞬时离心混匀,分别于38℃反应5、10、20、30 min,RPA产物经回收纯化后,取5 μL进行2%琼脂糖凝胶电泳,紫外灯下观察结果,确定最适反应引物组合。为筛选RPA最佳反应温度和时间,以标准质粒pcDNA3.1-12L为模板,分别在30℃、35℃、37℃、39℃、40℃、42℃条件下扩增30 min。再将标准质粒置于最适温度,反应5、10、15、20、25、30、35、40 min,以确定最佳反应时间。
1.7 特异性和敏感性试验 分别以PEDV、FMDV、CSFV、PRRSV的cDNA,PRV、PCV-2的DNA,以及pcDNA 3.1-12L为模板,进行RPA反应,确定该方法特异性。此外,将标准质粒进行10倍倍比稀释,使其浓度为100~106copies/μL,以此为模板进行RPA反应,确定方法的最低检测限。
1.8 普通PCR和实时荧光定量PCR扩增 普通PCR扩增体系(20 μL):2×TaqMix 10 μL,上下游引物各1 μL,DNA模板1 μL,ddH2O补齐。PCR反应程序为:98℃预变性10 min;98℃变性10 s,60℃退火15 s,72℃延伸90 s,共35个循环;72℃延伸10 min。实时荧光定量PCR 扩增体系(20 μL):2×Realtime PCR Mix (SYBRgreen)10 μL,上下游引物各0.8 μL,模板DNA 2 μL,ddH2O补齐。实时荧光定量PCR反应程序为:95℃预变性1 min;95℃变性15 s,60℃退火15 s,72℃延伸45 s,共40个循环。将pcDNA3.1-12L标准质粒10倍比稀释(100~106copies/μL)进行普通PCR及实时荧光定量PCR,比较3种检测方法的敏感性。
1.9 临床样品的检测 对实验室保存的15份未知病原的病死猪样品进行处理,提取其RNA、反转录为cDNA,采用RPA和实时荧光定量PCR同时检测,比较两种检测方法的结果是否一致。
2 结果
2.1 标准质粒鉴定及拷贝数的计算 对标准质粒进行双酶切鉴定,结果见图1,大小与预期相符(12L为1053 bp,pcDNA3.1为5428 bp)。鉴定正确的阳性质粒浓度为682 ng/μL,重组质粒碱基数为6423 bp,经计算得知质粒的拷贝数为9.68×1010copies /μL。
2.2 RPA反应引物筛选 以106copies/μL的pcDNA3.1-12L质粒为模板,使用4组引物,进行RPA引物筛选(图2)。结果显示,阳性对照扩增成功;在实验组中,虽然引物组合1首先出现扩增条带,但扩增30 min时出现非特异性条带,而引物组合4扩增目的条带较为单一、亮度较强,因此选取引物组合4用于后续实验。
2.3 RPA反应条件的优化 为筛选反应最佳温度,以106copies/μL的pcDNA3.1-12L为模板,使用上述最适引物进行RPA扩增,在30℃~42℃下最长反应30min。经半定量分析发现,12L基因在35℃时扩增条带较强(图3)。为筛选反应最适时间,将106copies/μL的模板在35℃下扩增5~40 min后发现,反应30 min的样品出现较为稳定的阳性条带(图4),因此选取30 min为最适反应时间。

图1 真核重组质粒酶切结果Fig.1 Enzyme digestion identification results of recombinant eukaryotic vector
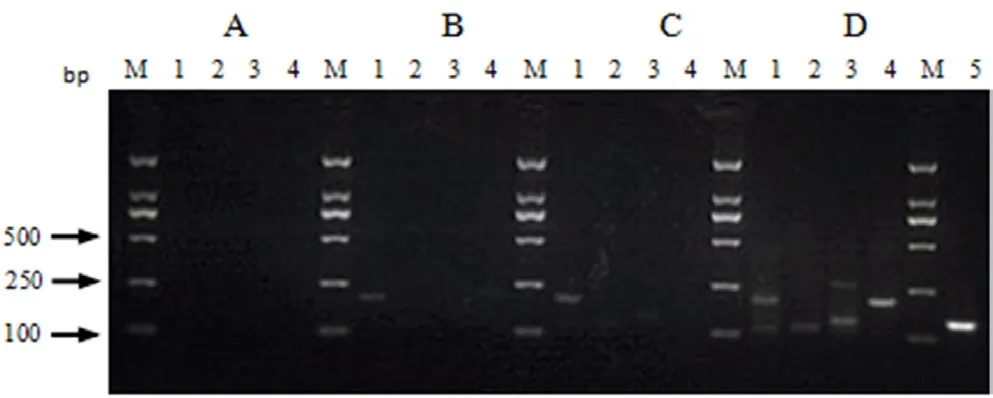
图2 12L-RPA扩增引物筛选Fig.2 The selection of 12L-RPA primers

图3 12L-RPA反应温度优化Fig.3 12L-RPA reaction temperature optimization
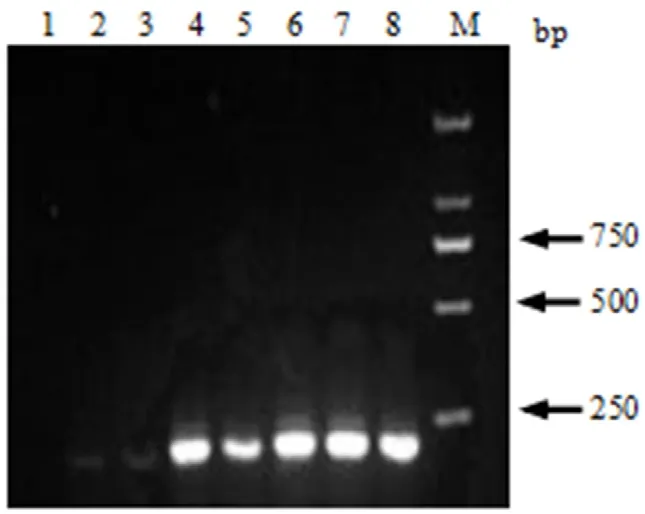
图4 12L-RPA反应时间优化Fig.4 12L-RPA reaction time optimization
2.4 特异性和灵敏性实验 以pcDNA3.1-12L质粒以及PEDV、FMDV、CSFV、PRRSV的cDNA,PRV、PCV-2的DNA为模板,扩增后发现只有12L基因出现扩增条带,说明该方法具有良好的特异性(图5)。为确定RPA方法的最小检出量,以100~106copies/μL的pcDNA3.1-12L为模板,扩增后发现,RPA最低可以检测到1×103copies质粒(图6A),与普通PCR(图6B)检测限相同,与荧光定量PCR检测限相近(图6C)。
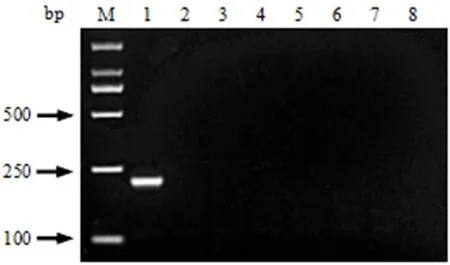
图5 12L-RPA特异性检测Fig.5 12L-RPA specificity test
2.5 RPA检测方法的应用 通过本研究建立的RPA方法,对15份样品进行检测,结果显示所有样品均为ASFV阴性,与实时荧光检测结果一致。
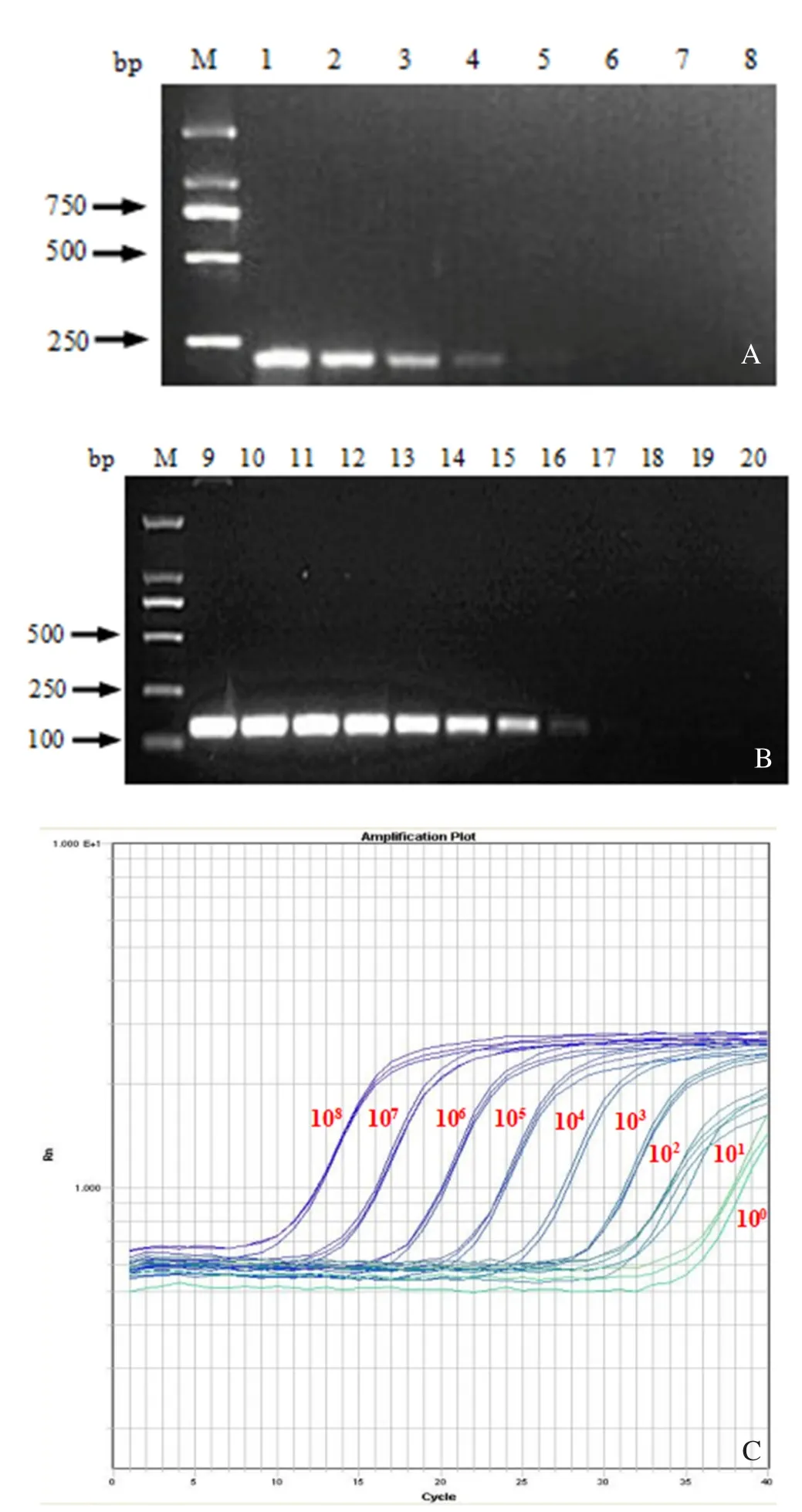
图6 敏感性检测Fig.6 Sensitivity test results
3 讨论
由于发病病程短、致死率高等特点,ASF已成为危害养猪业的重要疫病之一。该病毒免疫逃逸机制复杂、基因型较多(24个基因型)[15],目前并未研制出有效的疫苗。研究发现,删除毒株Benin 97/1 MGF360-10L、11L、12L、13L、14L和MGF505-1R、2R、3R及部分基因(MGF360-9L和MGF530/505-4R)后,缺失毒株和亲本病毒在猪巨噬细胞体外的生长特性基本相似;此外,动物免疫攻毒保护实验结果也表明,缺失毒株可以保护实验猪只免受强毒株Benin97/1的攻击[16]。随着缺失疫苗毒株的广泛研究,对此建立快速准确的检测方法同样重要。
对比当前常见的检测方法,RPA主要优势如下:第一,RPA反应中关键酶以冻干颗粒形式存在,易于保存;第二,RPA反应时间一般不超过30 min;第三,RPA属于等温扩增技术,不需要复杂的变温过程,对仪器设备要求较低[17]。目前RPA方法已经广泛应用于多种病原微生物的检测,如PCV-2[18]、猪细小病毒[19]、FMDV[20]、致病性钩端螺旋体[21]、B组链球菌[22]、疟原虫[23-24]等病原检测。此外,在食品安全、生物安全和癌症等领域RPA技术都也已有相关研究。
本研究根据实验构建了pcDNA3.1-12L真核重组质粒,并以此作为标准质粒进行RPA扩增。在引物设计方面,12L-RPA引物长度约为30~35 bp,因为这将有利于单链结合蛋白与寡核苷酸(引物)的结合,使其有效的整合到双链DNA[25]。筛选得到最适引物后,对RPA反应组分引物浓度与模板量进行优化,发现当模板拷贝数较低时,加入引物量越小、模板量越大时,扩增效果较为明显。优化温度区间为30℃~42℃,由图3可知,12L基因在35℃、37℃扩增效果较好,经半定量分析发现,35℃产物量与37℃时的产物量虽相差无几,但35℃下反应重复性、灵敏性较37℃效果更好。建立的RPA检测方法特异性针对ASFV Georgia 2007/1毒株12L基因缺失毒株进行检测,检测限为1×103copies/μL,但反应时间仅为普通PCR的1/4,可初步应用于ASFV Georgia 2007/1 MGF360-12L缺失毒株的鉴别诊断。
