自搅拌下CoB/SiO2 催化剂催化硼氢化钠水解制氢研究
2020-03-21孙海杰陈志浩陈凌霞刘冉冉蔡文娟
孙海杰,陈志浩,陈凌霞,刘 聪,刘冉冉,蔡文娟
(1.郑州师范学院化学化工学院,河南郑州450044;2.中国烟草总公司郑州烟草研究院)
近年来,能源需求量日益增长,传统化石能源不但存量有限而且使用过程中带来了严重的环境污染和温室效应等问题。因此,寻找新的可再生的绿色替代能源迫在眉睫。氢气是一种新型的清洁能源,能量密度大、来源广、燃烧产物无污染,近年来备受人们的关注[1-2];并且氢气是燃料电池这种新兴的发电方式和动力源的最优燃料。 所以,如何在温和条件下快速制氢、 安全高效地储氢是急需解决的问题[3]。NaBH4水解反应是一种较好的制氢方法, 反应方程式为NaBH4+2H2O→4H2↑+NaBO2[4]。 这种制氢方式安全、高效,副产物偏硼酸钠对环境友好,没有其他气体副产物[5]。然而,硼氢化钠水解制氢需要高效的催化剂。因此,NaBH4水解制氢催化剂的研发是硼氢化钠储氢技术的关键。
当前普遍认为纳米非晶态合金CoB 催化剂应用前景较好[4],但是纳米尺度的CoB 颗粒容易团聚,而且CoB 本征磁性加剧了团聚, 使催化剂效率降低。 高比表面积的载体既可以提高活性组分的分散度,又可以弱化CoB 磁性。因此,制备负载型CoB 催化剂是硼氢化钠水解制氢的研究热点。 梁志花等[6]用化学浸渍-原位化学还原法制备了丝光沸石负载的Co-B 非晶态合金催化剂, 发现其催化硼氢化钠水解制氢反应的活化能为53.18 kJ/mol,低于纯CoB的活化能。 他们又用化学浸渍-还原法制备了沸石咪唑酯骨架材料ZIF-负载CoB 催化剂,发现在该催化剂上硼氢化钠水解制氢反应为一级反应,表观活化能为51.48 kJ/mol[7]。赵士夺等[8]用浸渍-化学还原法制备了USY 型分子筛负载CoB 催化剂, 发现其催化硼氢化钠水解产氢的活化能为65.9 kJ/mol。 然而,负载型催化剂质量一般比较大,需要合适的搅拌消除外扩散的影响,这无疑增加了硼氢化钠储氢技术工业化的成本。
硼氢化钠水解产氢的同时会产生很大的瞬时动量,如何利用这些瞬时动量消除外扩散,开发适宜负载型CoB 纳米非晶态合金催化剂是关键。 笔者利用价格低廉的纳米SiO2为载体,系统研究了SiO2粒径、Co 负载量和还原剂NaBH4用量等条件对制备的CoB/SiO2催化剂催化硼氢化钠水解产氢性能的影响,开发出了自搅拌条件下高效催化硼氢化钠水解产氢的CoB/SiO2催化剂。
1 实验部分
1.1 实验原料
六水合硝酸钴(分析纯),氢氧化钠(分析纯),硼氢化钠(分析纯),二氧化硅(分析纯,粒径为15 nm±5 nm、30 nm±5 nm、50 nm±5 nm)。
1.2 催化剂的制备
称取0.78 g Co(NO3)2·6H2O 置于烧杯中,用20 mL蒸馏水搅拌溶解。向上述溶液中加入粒径为15 nm±5 nm 的SiO21.00 g, 置于恒温磁力搅拌水浴锅中于303 K、420 r/min 条件下恒温水浴搅拌30 min。 称取0.49 g NaBH4,溶于10 mL 蒸馏水中。 将NaBH4溶液置于滴液漏斗中,逐滴滴入上述Co(NO3)2·6H2O 和SiO2的混合溶液中,滴加完成后继续恒温搅拌10 min。抽滤并洗涤至洗出液pH 为7。将固体置于330 K 真空干燥箱中干燥4 h,研成粉末备用。 将粒径为15 nm±5 nm 的SiO2换成粒径为30 nm±5 nm、50 nm±5 nm的SiO2,考察SiO2粒径对催化剂性能的影响。 调整Co(NO3)2·6H2O 用量,考察CoB 负载量对催化剂性能的影响。 调整NaBH4用量,考察还原剂NaBH4用量对催化剂性能的影响。
1.3 催化剂的评价
采用排水集气法进行催化剂的性能评价。 取30 mL NaBH4(0.15 mol/L)和NaOH(0.03 mol/L)的混合溶液加入250 mL 三颈烧瓶中,置于恒温磁力搅拌水浴锅中。 在303 K、420 r/min 条件下将0.40 g 的CoB/SiO2催化剂倒入上述三颈烧瓶中,每隔60 s 记录排出水的质量。
1.4 催化剂的表征
采用D/max 2550V 型X 射线衍射仪 (XRD)进行催化剂的物相分析。 采用JEOL JEM 2100 型透射电子显微镜(TEM)观察催化剂的形貌。 采用PHI Quantera SXM 型X 射线光电子能谱仪(XPS)测定催化剂中元素的价态。
2 结果与讨论
2.1 催化剂制备条件对其性能的影响
2.1.1 SiO2粒径的影响
图1a 为不同粒径SiO2负载CoB 催化剂XRD 谱图。 由图1a 看出,所有样品都在22、33、59°处出现3 个特征衍射峰, 其中22°处衍射峰归属于非晶态SiO2特征衍射峰,33°处衍射峰归属于CoB 特征衍射峰。 随着SiO2粒径增大,33°处衍射峰强度逐渐增加,宽度逐渐减小,说明CoB 催化剂的粒径逐渐增大。这说明粒径小的SiO2上CoB 催化剂的粒径较小。
图1b 为不同粒径SiO2负载CoB 催化剂催化硼氢化钠水解产氢的性能。 由图1b 看出,随SiO2粒径增大,CoB/SiO2催化剂催化硼氢化钠水解产氢的速率逐渐减慢。由XRD 表征结果可知,SiO2粒径越小,制备的CoB 催化剂粒径越小。 CoB 催化剂粒径越小,催化硼氢化钠水解产氢的速率越快。 Wang 等[9]也发现制备的NiB 催化剂粒径越小,其催化硼氢化钠水解产氢的速率越快。
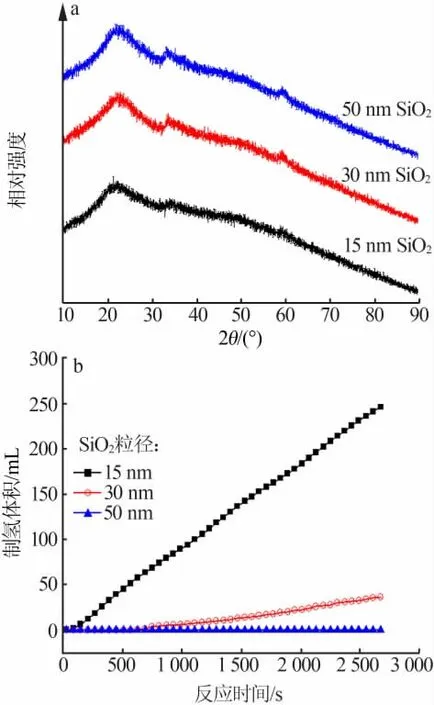
图1 不同粒径SiO2 负载CoB 催化剂XRD 谱图(a)及其催化硼氢化钠水解产氢的性能(b)
2.1.2 Co 负载量的影响
图2a 为不同Co 负载量制备CoB/SiO2催化剂的XRD 谱图。 由图2a 看出,所有样品在22°处都出现了非晶态SiO2特征衍射峰;随Co 负载量增大,33°处CoB 特征衍射峰从无到有, 衍射峰强度逐渐变大,说明CoB 活性组分逐渐聚集长大。
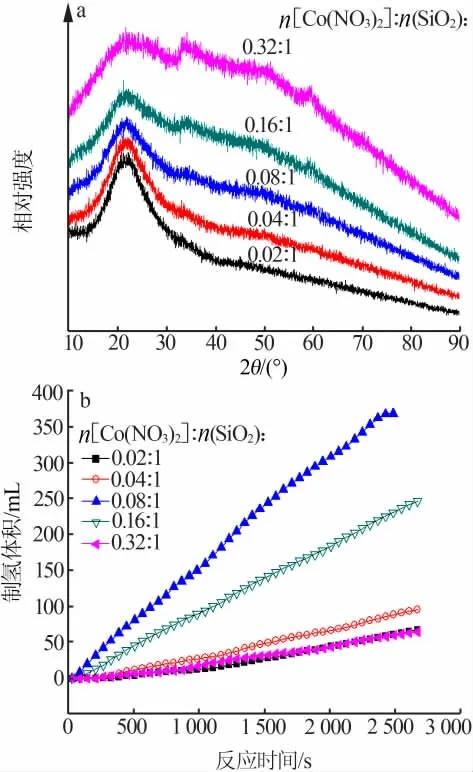
图2 不同Co 负载量制备CoB/SiO2 催化剂XRD 谱图(a)及其催化硼氢化钠水解制氢的性能(b)
图2b 为不同Co 负载量制备CoB/SiO2催化剂催化硼氢化钠水解产氢的性能。 由图2b 看出,随着Co 负载量增加,催化剂催化硼氢化钠水解制氢的速率先加快后减慢,n[Co(NO3)2]∶n(SiO2)=0.08∶1 为最佳比例。Co 负载量增加,催化剂活性组分增加,催化剂活性增加。 而由XRD 表征结果可知,随着Co 负载量增大,CoB 催化剂逐渐在SiO2表面聚集长大。CoB 催化剂粒径越大,催化剂活性越低。 当Co 负载量适中时,即n[Co(NO3)2]∶n(SiO2)=0.08∶1 时,活性组分CoB 含量适中, 粒径适中,CoB/SiO2催化剂催化硼氢化钠水解产氢的速率最快。
2.1.3 NaBH4用量的影响
图3a 为不同NaBH4用量制备CoB/SiO2催化剂XRD 谱图。由图3a 看出,所有样品都在22°处出现了SiO2特征衍射峰,在33°处出现了CoB 催化剂特征衍射峰,且33°处衍射峰很弱,说明CoB 催化剂粒径很小。
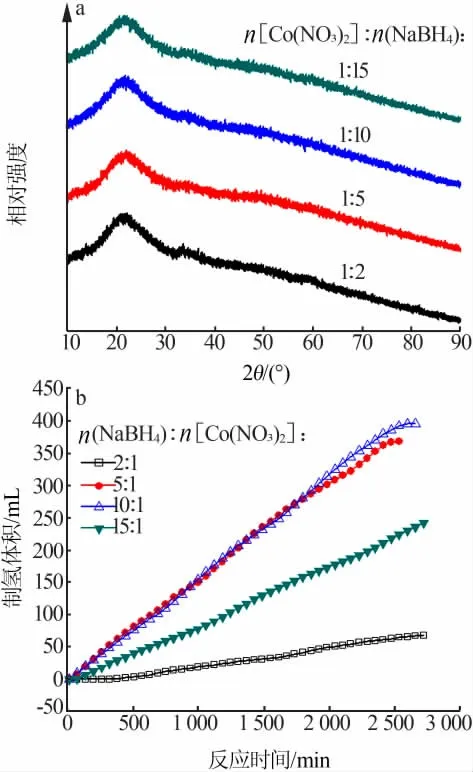
图3 不同NaBH4 用量制备CoB/SiO2 催化剂XRD谱图(a)及其催化NaBH4 水解产氢的性能(b)
图3b 为不同NaBH4用量制备CoB/SiO2催化剂催化硼氢化钠水解产氢的性能。 由图3b 可知,随着n(NaBH4)∶n[Co(NO3)2]增 加,硼 氢 化 钠 水 解 产 氢的速率呈现先增加后减慢的趋势,当n(NaBH4)∶n[Co(NO3)2]=5∶1 时硼氢化钠水解产氢的速率最快。这是因为,当硝酸钴用量一定时,增加NaBH4的比例,还原得到的CoB 活性成分增加,所以硼氢化钠水解速率加快。 当n(NaBH4)∶n[Co(NO3)2]=5∶1 时,活性组分前体Co(NO3)2可能被完全还原为Co,硼氢化钠水解速率最快,制备的CoB/SiO2催化剂催化硼氢化钠水解产氢的速率为45.6 mL/(min·g)。 继续增大n(NaBH4)∶n[Co(NO3)2],过多的硼氢化钠会被所得的CoB/SiO2催化剂催化水解,生成的产物偏硼酸钠易吸附至催化剂表面,使催化剂催化活性降低,故硼氢化钠水解产氢速率降低。
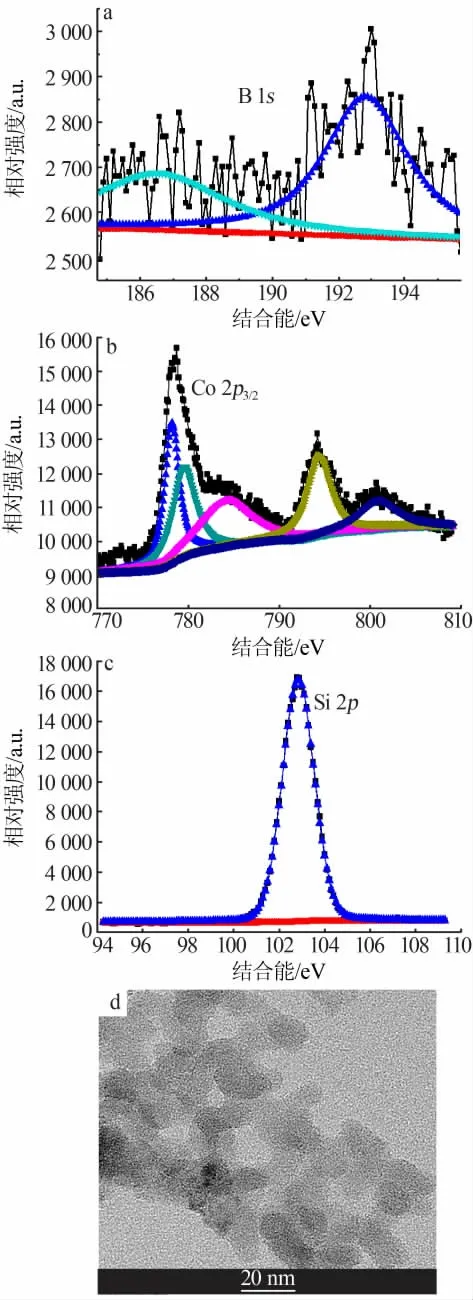
图4 n[Co(NO3)2]∶n(NaBH4)=1∶5 制备CoB/SiO2 催化剂XPS 图及TEM 照片
图4 为n[Co(NO3)2]∶n(NaBH4)=1∶5 时制备CoB/SiO2催化剂的XPS 图及TEM 照片。图4a 为B 1s的XPS 图,可以看出在186.5 eV 和192.8 eV 处出现了两个峰,分别对应元素态B[10]和氧化态B3+[11]。 图4b为Co 2p的XPS 图,可以看出Co 2p3/2由778.6、780.0、784.8 eV 处3 个峰组成, 分别归属于元素态Co[12]、氧化态Co2+[13]和Co2+的卫星峰[1],元素态Co 的电子结合能比文献报道的778.3 eV 略高。 图4c 为Si 2p的XPS 图,可以看出Si 2p电子结合能为102.8 eV,比文献[14]报道的SiO2给合能为103.2 eV 低。这说明活性组分Co 与载体SiO2之间存在电子作用,活性组分Co 将一部分电子转移给了载体SiO2。
图4d 为n[Co(NO3)2]∶n(NaBH4)=1∶5 时制备的CoB/SiO2催化剂的TEM 照片。 在图4d 中只观察到10~15 nm SiO2晶粒,没有观察到Co 活性组分。 这说明Co 活性组分粒径很小,与XRD 表征结果一致。
2.2 反应条件对硼氢化钠水解产氢的影响
2.2.1 搅拌转速的影响
表1 为不同搅拌转速条件下CoB/SiO2催化剂催化硼氢化钠水解产氢的性能。由表1 看出,随着搅拌转速增加, 硼氢化钠产氢速率和最大产氢量没有明显改变, 说明搅拌转速对硼氢化钠产氢速率的影响不大。 这可能是由于催化剂粒径小,催化活性高,伴随快速产氢产生的动量完全消除了外扩散的影响。 故利用制备的CoB/SiO2催化剂催化硼氢化钠水解产氢无需机械搅拌, 这样可以大幅度降低硼氢化钠水解产氢装置的成本。
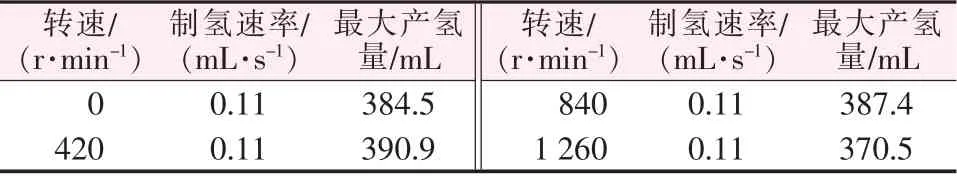
表1 不同搅拌转速条件下CoB/SiO2 催化剂催化硼氢化钠水解产氢的性能
2.2.2 催化剂用量的影响
图5 为不同CoB/SiO2催化剂用量催化硼氢化钠水解制氢的性能。 由图5 看出,催化剂用量越多,相同时间内产生氢气的量越多。 产氢速率与催化剂用量成正比, 这也表明在无搅拌条件下外扩散限制已经消除[15]。同时这也表明,可以通过调整催化剂用量来调控硼氢化钠产氢速率, 这为调整硼氢化钠产氢速率提供了简便的方法。
2.2.3 反应温度的影响及动力学分析
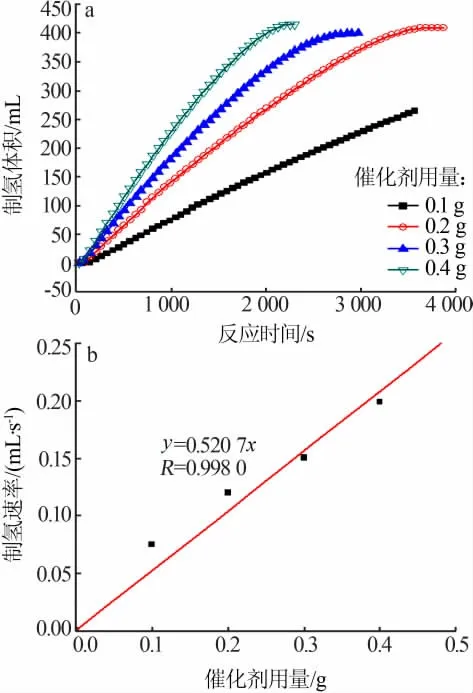
图5 不同用量CoB/SiO2 催化剂催化硼氢化钠水解制氢性能(a)以及产氢速率与催化剂用量的关系(b)
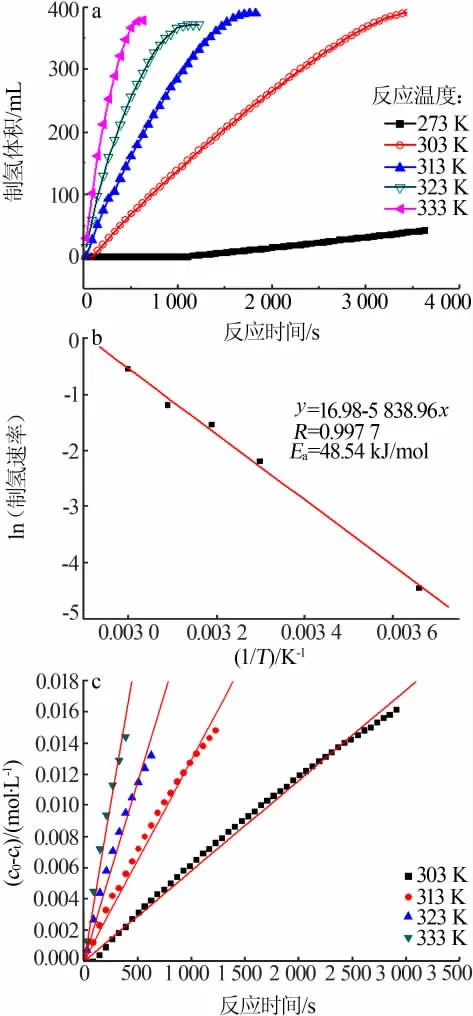
图6 不同反应温度CoB/SiO2 催化剂催化硼氢化钠水解制氢的性能(a)、Arrhenius 曲线(b)及其零级反应模型(c)
图6a 为不同反应温度条件下CoB/SiO2催化剂催化硼氢化钠水解产氢的性能。 由图6a 看出,随着反应温度升高,硼氢化钠产氢速率急剧增加。这可以从两个方面解释:一是反应温度升高,反应物分子的动能增大,活化分子数目增多,使催化剂与反应物的碰撞机率增加[2],同时传质过程的加快使产生的氢气和副产物NaBO2得以及时地从催化剂表面脱附,从而使硼氢化钠产氢速率增大;二是温度升高,副产物NaBO2的溶解度变大,这避免了反应过程中析出的NaBO2吸附在催化剂表面导致催化剂活性降低,故而硼氢化钠析氢速率增大。
图6b 为CoB/SiO2催化剂催化硼氢化钠水解产氢的阿伦尼乌斯(Arrhenius)曲线。 由图6b 看出,ln(产氢速率)和1/T呈线性关系,根据Arrhenius 公式lnk=-Ea/RT+lnA(式中:k为速率系数;Ea为活化能;R为摩尔气体常数;T为温度;A为指前因子),计算出CoB/SiO2催化剂催化硼氢化钠水解产氢的活化能为48.54 kJ/mol,为文献报道的低活化能之一[16]。 这表明CoB/SiO2催化剂降低了硼氢化钠水解产氢的活化能。 图6c 为CoB/SiO2催化剂催化硼氢化钠水解产氢的零级反应模型。 由图6c 看出,硼氢化钠浓度差c0-ct与时间t呈线性关系,这表明CoB/SiO2催化剂催化硼氢化钠水解产氢反应时硼氢化钠反应级数为零。
2.3 催化剂重复使用性能
表2 为CoB/SiO2催化剂重复使用性能。 由表2看出,CoB/SiO2催化剂重复使用5 次过程中产氢速率稳定0.12 左右,最高产氢量稳定在375 mL 左右,表明CoB/SiO2催化剂具有良好的重复使用性能和稳定性。
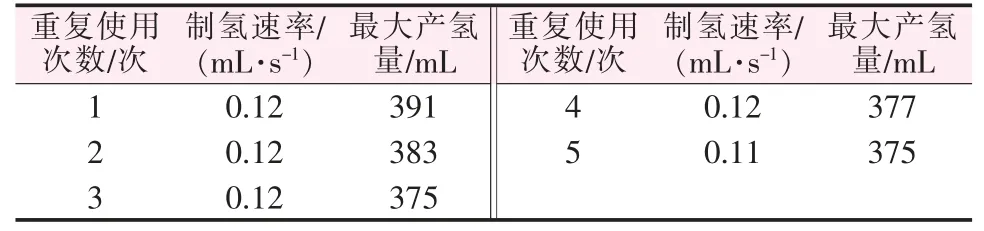
表2 CoB/SiO2 催化剂催化硼氢化钠水解产氢的重复使用性能
3 结论
1)在 二 氧 化 硅 粒 径 为15 nm、n[Co(NO3)2]∶n(SiO2)=0.08∶1、n[Co(NO3)2]∶n(NaBH4)=1∶5 条件下制备的催化剂CoB/SiO2催化剂活性最高。
2)因为催化剂粒径很小,伴随NaBH4水解产生氢气产生的动量可以完全消除外扩散速率的影响,搅拌转速对NaBH4水解速率的影响很小,NaBH4水解速率随CoB/SiO2催化剂用量的增加而变大。
3)随着温度的升高,CoB/SiO2催化剂催化硼氢化钠水解产氢反应速率增加,NaBH4水解反应的表观活化能为48.54 kJ/mol, 硼氢化钠反应级数为零。而且CoB/SiO2催化剂具有良好的重复使用性能和稳定性。
