可见光驱动Z-scheme g-C3N4/α-Fe2O3催化剂高效产H2*
2020-02-13王宇晶宋荷美张新东柴守宁
王宇晶,宋荷美,张新东,柴守宁
(1. 西安工业大学 材料与化工学院,西安 710021;2. 西安建筑科技大学 环境与市政工程学院,西安 710055)
0 引 言
近年来,严峻的环境污染和化石能源严重消耗带来的能源短缺,成为当今社会发展中亟待解决的问题[1-2]。因此,清洁能源的开发势在必行。氢气,一种理想的二次能源,被认为是满足未来能源和环境要求的最为理想的一种清洁和可持续能源[3]。此外,光催化剂在光照激发下通过裂解H2O产生H2,实现了光能转化为化学能和减少了化石燃料的消耗[4-6]。但是目前,开发出的光催化主要为紫外光(占太阳光总能量的4%)响应催化剂且光生电子与空穴复合高,导致氢气产率低[7-9]。为了更好的利用太阳光,开发可见光(占太阳光总能量的43%)响应催化剂加速H2O裂解反应是当务之急。
石墨相氮化碳(g-C3N4)作为一种无机非金属光催化剂,由C、H两种元素以sp2杂化形成的C3N3或C6N7环构成,环与环之间通过N原子相连,形成无线扩展的平面,具有良好的化学稳定性和热稳定性[10-11]。更重要的是,g-C3N4是典型的中宽带隙半导体,禁带宽度为2.7 eV,带隙吸收约为460 nm,具有良好的可见光吸收能力[12]。2009年,由Wang等[13]首次报道了铂改性g-C3N4在可见光照射下(可见光420~460 nm范围吸收约0.1%),可光解水制取H2,为功能材料在能源生产方面开辟了新的前景。但是,g-C3N4亦存在自身的缺陷,激子结合能较高,结晶度较低,这两点导致g-C3N4光生电子和空穴的大量复合;g-C3N4粉体比表面积较小,约10 m2/g左右,易团聚回收再利用困难;带隙宽度相对可见光依然较宽,只能响应可见光当中的蓝紫部分,实际的可见光利用率低[14]。为了克服这些缺陷,研究者尝试利用窄隙半导体将g-C3N4进行改性,形成Z-scheme的复合g-C3N4,来提高电子传递效率和延长载流子复合,从而提高制氢效率。目前,α-Fe2O3作为一种化学稳定性(pH值>3)、成本低的光催化剂,由于禁带宽度较窄(2.0~2.2 eV),在可见光范围内有很强的吸收(λ>600 nm),能够收集40%的太阳能谱能量。若将其与g-C3N4复合形成Z-scheme复合体系,可望拓宽对可见光的波长响应,促进电荷的有效分离以及提高光子吸收率,从而提高产氢效率[15-16]。
本文以三聚氰胺、尿素和FeCl3·6H2O为原料,通过水热合成法制备出一种纳米晶胶体g-C3N4/α-Fe2O3,促进了光生电子和空穴的有效分离和增强了对可见光吸收性能。通过SEM、TEM、XPS、PL、DRS、EIS和PC等手段进行形貌、结构和光催化活性测试。实验中以NaBH4为产氢底物,考察了温度、Fe元素掺杂比和NaBH4浓度等各种因素对产氢性能的影响,并对产氢活性提高的机理进行了探讨。
1 实 验
1.1 催化剂的制备
1.1.1 g-C3N4的制备
g-C3N4采用前驱体热解聚合法。称取3 g三聚氰胺和7 g尿素(分析纯)添加到20 mL去离子水中,在80 ℃水浴条件下搅拌直至水分蒸干,将上述混合物置于马弗炉中加热至520 ℃,升温速率为5 ℃/min,保温时间为2 h,待马弗炉恢复室温时将坩埚取出,得到淡黄色粉末状的g-C3N4。
1.1.2 g-C3N4/α-Fe2O3的制备
0.06 g g-C3N4加入20 mL去离子水和0.00356 g FeCl3·6H2O加入20 mL去离子水混合磁力搅拌10 min,放入超声清洗器中超声1 h,向上述混合物中缓慢加入20 mL溶于3.96 g的聚乙烯比咯烷酮,将分散均匀的混合液置于体积为80 mL的水热反应釜中,在180 ℃高温下反应12 h,得到g-C3N4/α-Fe2O3胶体催化剂。
1.2 g-C3N4/α-Fe2O3 光催化剂形貌及结构表征
利用扫描电子显微镜(SEM Quanta-400F)观察g-C3N4/α-Fe2O3复合物的形貌,测试前样品经烘干处理。透射电子显微镜(TEM JEM-2010)测定g-C3N4/α-Fe2O3复合物内部精细结构,加速电压200 kV,点分辨率0.23 nm。X射线衍射(XRD-6000)测定样品衍射峰的出峰位置和出峰强度,与XRD标准卡片特征峰对比,得到样品的物质组成。其辐射源为CuKα,工作电压40 kV,管电流30 mA,扫描范围10~70°,扫描速度为4°/min。X射线光电子能谱(XPS AXIS-ULtrabld Kratos)测定样品所含元素及其元素价态。其辐射源为AlKα,扫描范围0~1 000 eV。紫外可见漫反射光谱(UV-Vis-2550)分析样品的光吸收性能,吸收范围250~600 nm。光致发光光谱(PL-LS55)测定样品的光生电子空穴复合率,侧面反映样品光催化活性。以Xe灯作为激发光源,激发波长360 nm,激发和发射狭缝均为5 nm。
1.3 可见光驱动g-C3N4/α-Fe2O3 产氢性能研究
以250 W的汞坞混光灯为可见光光源,光催化NaBH4来完成对胶晶g-C3N4/α-Fe2O3催化活性的探索。量取10 mL浓度为30 mmol/L的NaBH4溶液于三颈烧瓶中,pH值为12。随后,将三颈烧瓶置于30 ℃水浴条件下搅拌10 min以排尽残余气体。接着,将30 mg经研磨的光催化加入到反应器中,持续搅拌并光照15 min,每隔1 min记录产氢数据。
1.4 g-C3N4/α-Fe2O3 光催化剂电化学性能分析
采用电化学表征分析方法测试催化剂的产氢活性与催化反应中电子传输情况,所用仪器为上海辰华的600D CHI分析仪。其工作电极为附着催化剂的ITO导电玻璃,参比电极为饱和甘汞电极,对电极为铂丝,电解液为0.1 mol/L的Na2SO4。电化学交流阻抗(EIS)反应催化剂的光生电子和空穴的分离效率。测试条件:初始电压为0 V,测定电压范围为-1~1 V,振幅为5 mV。瞬态光电流测试(PC)反应催化剂的光响应能力。测试条件:初始电压为0 V,每隔50 s开关灯,测定范围为-1~1 V,敏感度为1×10-6。
2 结果与讨论
2.1 g-C3N4/α-Fe2O3光催化剂形貌及结构表征
图1是g-C3N4/α-Fe2O3复合催化剂的SEM图、TEM图和EDS图谱。图1(a)为g-C3N4/α-Fe2O3的SEM图。从图1(a)可看出,α-Fe2O3颗粒均匀的分散在g-C3N4表面,抑制了α-Fe2O3的团聚。从TEM图谱(图1(b))g-C3N4片层上分散一些小颗粒,两组份之间形成异质结构有利于加速光催化反应过程中电子和空穴对的分离[17]。图1(c)是样品g-C3N4/α-Fe2O3的EDS光谱,EDS光谱中出现了C、N、O和Fe元素,4种元素的共存证明形成了g-C3N4/α-Fe2O3复合材料[18-19]。

图1 g-C3N3/α-Fe2O3 的SEM图谱、TEM谱图和EDS图Fig 1 SEM image, TEM image and EDS spectrum of the g-C3N3/α-Fe2O3sample
图2为g-C3N4和g-C3N4/α-Fe2O3复合材料的XRD图。图2中显示纯g-C3N4在13.2和27.5°处出现两个明显的特征衍射峰,分别对应于(100)和(002)晶面。2θ在27.5°的强峰是由共轭芳香环的堆垛形成的[20]。另一个较弱的衍射峰13.2°是melon类物质的特征峰,是由平面结构内的堆垛3-s三嗪结构单元聚合所形成的[21]。当负载有α-Fe2O3颗粒后,g-C3N4/Fe2O3的XRD图还显示了9个其它的特征峰,分别位于24.2,33.1,35.5,40.7,49.5,53.8,57.5,62.4以及64.1°,这些衍射峰分别与α-Fe2O3(JCPDS33-0664)的(012)、(104)、(110)、(113)、(024)、(116)、(018)、(214)以及(300)晶面完整对应[22]。结果表明g-C3N4/α-Fe2O3复合材料的XRD图谱同时含有g-C3N4和α-Fe2O3衍射峰,但是衍射峰强度有所改变,说明二者形成了复合材料。
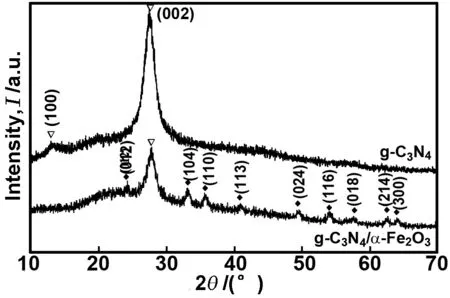
图2 g-C3N4和g-C3N3/α-Fe2O3 的XRD表征图谱Fig 2 X-ray diffraction patterns of g-C3N4 and g-C3N4/α-Fe2O3


图3 g-C3N3/α-Fe2O3 样品的XPS图谱Fig 3 XPS spectra of g-C3N3/α-Fe2O3 composite
2.2 可见光驱动g-C3N4/α-Fe2O3 产氢性能研究
图4为g-C3N4/α-Fe2O3复合材料在光照和避光条件下的产H2效果图。由图4可知,光照条件下,g-C3N4/α-Fe2O3催化剂在10 min后产H230 mL,是避光环境下产H2的1.67倍。这归因于g-C3N4受到光激发后,光生电子空穴在α-Fe2O3助催化剂的帮助下加速分离,空穴裂解NaBH4产生H+以及电子与H2O反应生成H2,提高了H2的产生。
图5(a)为不同温度对g-C3N4/α-Fe2O3复合物催化NaBH4产H2性能影响和产H2拟合的动力学曲线。由图5(a)可知,溶液温度从20 ℃(23.3 mL)升至40 ℃(33.8 mL),产H2量增加了45%,这主要归因于温度越高,催化剂的活化程度越高。当溶液温度为30 ℃,产H2量可达30 mL,仅比40 ℃产H2量低11%,但产H2效率相当,且高的温度易加速催化剂的团聚失活,不利于催化剂的长期使用[28]。因此溶液温度为30 ℃时,产H2性能最好。

图4 g-C3N3/α-Fe2O3复合物的光响应能力Fig 4 The photocatalytic activity of the g-C3N3/α-Fe2O3
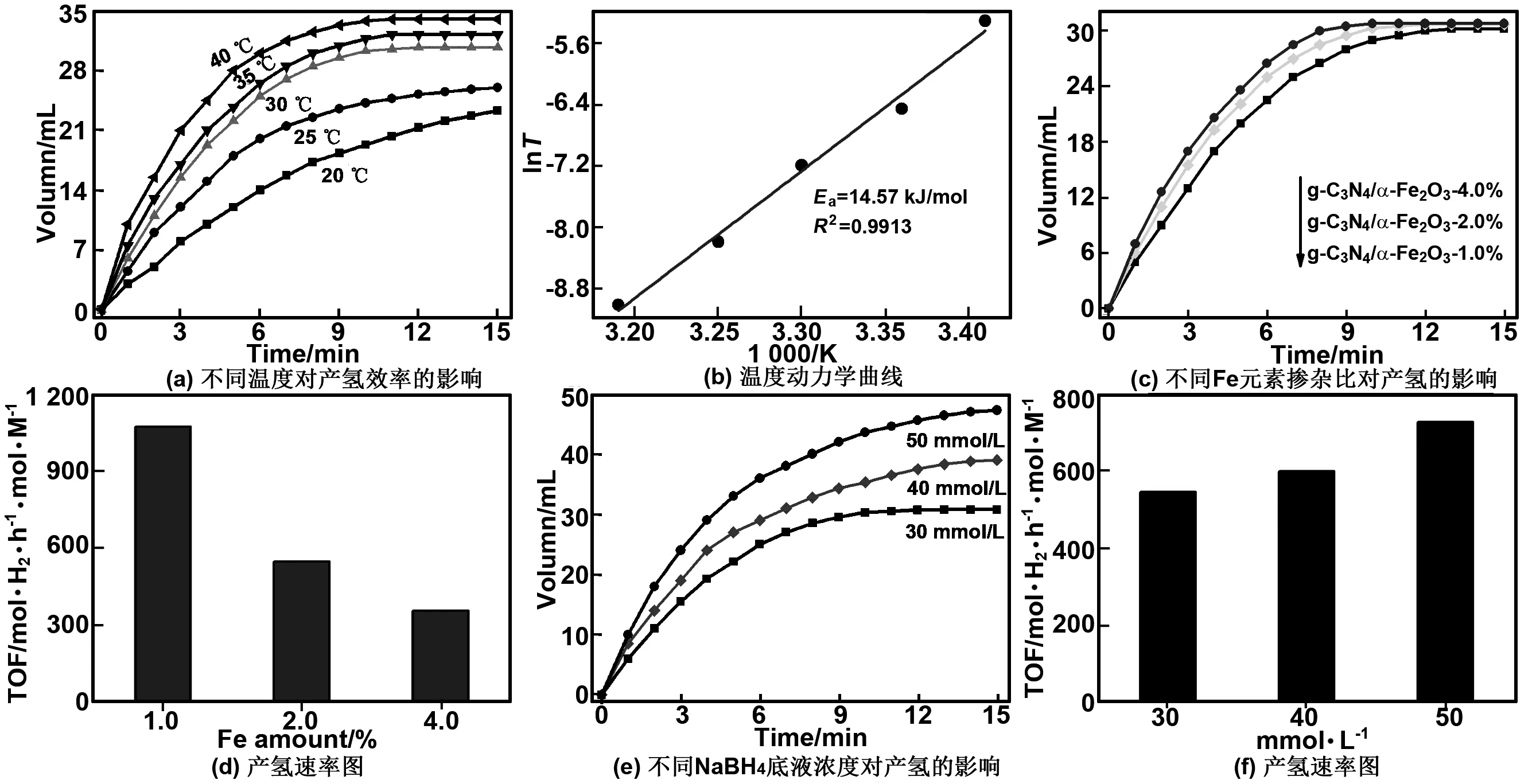
图5 不同温度对产氢效率的影响、温度动力学曲线、不同Fe元素掺杂比对产氢的影响和产氢速率图、不同NaBH4底液浓度对产氢的影响和产氢速率图
Fig 5 Effect of temperature on H2production, temperature kinetics curve, the influence of different Fe doping ratio on H2production and H2production rate, the influence of different NaBH4concentration on H2production and hydrogen production rate
图5(b)为g-C3N4/α-Fe2O3复合物不同温度下动力学曲线。通过对不同温度条件下g-C3N4/Fe2O3催化剂催化NaBH4产H2数据进行拟合得出催化剂活化能为14.57 kJ/mol,低于大部分已发表的催化剂的活化能。图5(c)为不同Fe掺杂量对光催化产H2性能的影响。研究了可见光照射15 min后H2的产生量。采用0.01,0.02和0.04的摩尔质量比例添加Fe的g-C3N4,使自产H2能力分别提高到29,30和30.8 mL。这种显著的改善是由于α-Fe2O3可以提供电荷转移的载体,改善光生电子-空穴对的分离和转移。更重要的是,g-C3N4/α-Fe2O3-1%产H2速率达到1 072 mol-H2·h-1·mol-M-1,是掺杂量2%和4%产H2速率的3.01和1.95倍,如图5(d)所示。这主要归因于大量Fe含量的掺杂,覆盖了g-C3N4片层,造成了活性位点的缺失,从而导致产H2速率的降低[29]。
图5(e)为不同NaBH4底物浓度对催化剂产H2性能的影响。由图5(e)可知,在反应进行到15 min时,30,40以及50 mmol/L的NaBH4溶液中,H2的产量分别为30,40以及50 mL,实现了NaBH4的完全催化水解。这主要归因于当α-Fe2O3助催化剂的存在能够及时转移g-C3N4导带上的电子,抑制了光生电子空穴的复合,大量空穴的存在有效的催化了NaBH4提高了催化产氢活性。图5(f)为不同浓度的NaBH4产氢速率图(TOF)。由图5(f)可知,硼氢化钠的浓度越高,反应速率越大,与图5(e)中的结论一致。当浓度为30,40以及50 mmol/L时,反应速率分别达到了547,600和728 mol-H2·h-1·mol·M-1,再次证明所制备的g-C3N4/Fe2O3催化剂有效的抑制了光生电子空穴的复合和具有更高的催化产氢活性。
光催化剂的循环稳定性是评价其适用性的关键标准[30]。图6为g-C3N4/Fe2O3光催化剂的循环寿命图。
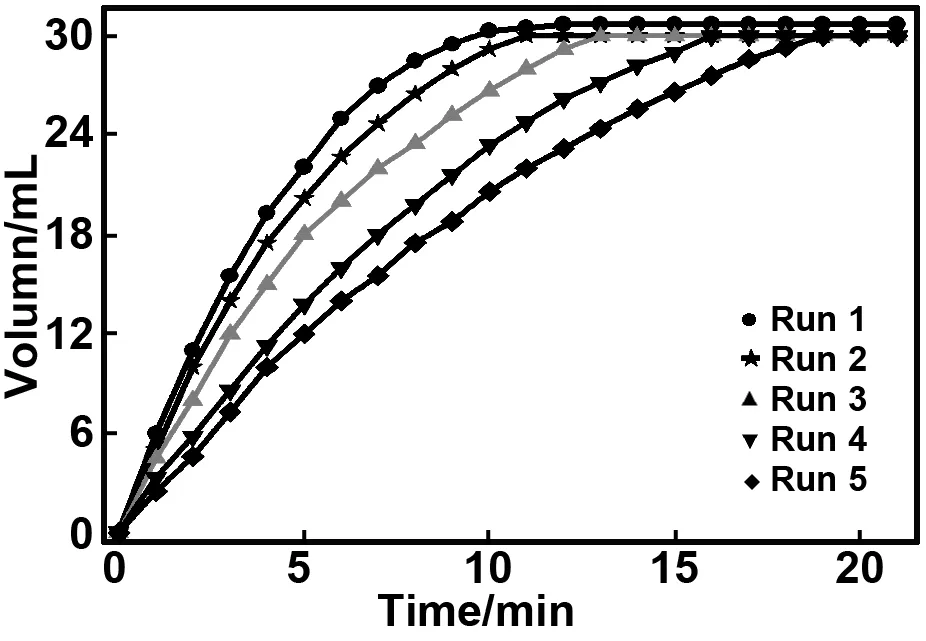
图6 g-C3N3/α-Fe2O3 光催化循环寿命图Fig 6 Recyclability of g-C3N3/α-Fe2O3 photocatalyst
由图6可知,在光催化反应20 min时,产氢量可达30.7 mL。5次重复使用后,光催化剂产氢30 mL,表明所制备的g-C3N4/α-Fe2O3光催化剂具有较高的稳定性。另外,在产氢过程中剧烈搅拌,一些α-Fe2O3颗粒可能从g-C3N4片层中分离,从而导致光催化性能略有下降。
光吸收性能是影响催化剂光催化活性的重要因素。图7(a)为g-C3N4和g-C3N4/α-Fe2O3复合材料的DRS谱图。由图7(a)可知,g-C3N4和g-C3N4/α-Fe2O3的吸收边主要集中在460 nm左右,利用公式
计算出带隙在2.70 eV左右[31-32]。g-C3N4/α-Fe2O3的DRS光谱相对g-C3N4的光谱有小幅度的红移,使得材料具有更强的光催化活性,从而提高了g-C3N4/α-Fe2O3对光的利用率。图7(b)为g-C3N4和g-C3N4/α-Fe2O3复合材料的PL谱图,激发光谱为325 nm。g-C3N4和g-C3N4/α-Fe2O3复合材料在460 nm左右出现一个较宽的发射峰,说明光生电子经历了从n→π*的跃迁[33]。g-C3N4/α-Fe2O3的PL强度较g-C3N4显著降低。这主要是由于形成异质结后,光生电子很容易的从g-C3N4的导带转移至α-Fe2O3的导带上,而光生空穴容易从α-Fe2O3的价带转移至g-C3N4的价带上,使得电子空穴分离加速,光生电子空穴复合率降低,从而参与光催化的有效电子和空穴更多,具有更好的产氢效果。图7(c)为g-C3N4和g-C3N4/α-Fe2O3复合材料的PC谱图。由图7(c)可知,当光辐射中断时,光电流迅速下降到几乎为零(稳态值),一旦打开灯,光电流恢复到原始值[34]。可见光下g-C3N4/α-Fe2O3的光电流密度约为0.36 μA,是纯g-C3N4(0.08 μA)的4倍,说明异质结构的生成加速了催化剂界面电荷转移速率。为了深入了解g-C3N4/α-Fe2O3异质结中的电荷传输行为,进行了EIS测试(图7(d))。在奈奎斯特图中,每条弧的半径与相应电极、电解质界面上的电荷转移过程有关,半径越小,电荷转移电阻越低[35]。g-C3N4/α-Fe2O3电极的弧半径小于纯g-C3N4电极,表明复合物具有良好的电荷分离和电子转移性能,这与PL及PC的结果一致。也就是说,当在纯g-C3N4引入α-Fe2O3可以有效抑制光生电荷载流子的复合,光生空穴数目的增多促进了NaBH4的分解,从而增强了体系产氢的能力。
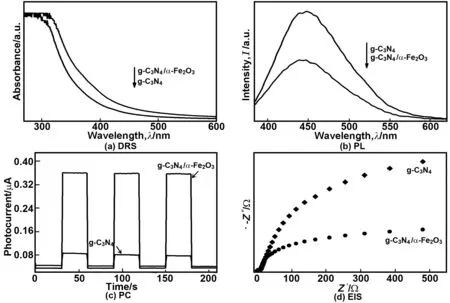
图7 g-C3N3和g-C3N3/α-Fe2O3复合物DRS、PL、PC和EISFig 7 DRS, PL spectra, EIS and transient photocurrents for as-synthesized pure g-C3N4 and g-C3N3/α-Fe2O3 composites
基于以上实验研究结果, g-C3N4/α-Fe2O3复合物符合Z型载流子电荷转移途径,以提高光催化产H2的性能更为合理,如图8所示。当g-C3N4/α-Fe2O3中的两个组分被可见光激发后,吸收光子激发价带(VB)上带有负电的电子(e-)跃迁到导带(CB)上,同时在VB上留下带有正电的空穴(h+)。α-Fe2O3的CB中的e-通过复合界面迁移到g-C3N4的VB上,并与残余h+复合,从而抑制了光生电荷在一个组分中的自复合。此时,e-和h+分别聚集在g-C3N4的CB中和α-Fe2O3的VB中,所以g-C3N4/α-Fe2O3既能具有g-C3N4的强还原能力,还具有α-Fe2O3的强氧化能力。在α-Fe2O3的VB中积累的h+会将吸附在催化剂表面的NaBH4直接氧化,产生大量H+,而在g-C3N4的CB中积累的e-可通过裂解H2O产生H+,进而提高H2的产率。显然,Z型-g-C3N4/α-Fe2O3显著提高了电荷分离效率,为光催化NaBH4氧化反应提供了较大的驱动力,从而提高了光催化NaBH4裂解性能。

图8 g-C3N3/α-Fe2O3复合材料光催化制氢机理图Fig 8 The schematic illustration of photocatalytic hydrogen production reaction over g-C3N3/α-Fe2O3
3 结 论
(1) 采用水热合成法成功的制备出Z型-g-C3N4/α-Fe2O3纳米晶胶体光催化剂,其平均粒径为17 nm,α-Fe2O3纳米颗粒均匀分布在g-C3N4片层基底上。
(2) 将g-C3N4/α-Fe2O3复合物应用于NaBH4产氢体系中,当溶液温度为30 ℃、Fe元素摩尔质量为1%,NaBH4浓度为50 mL时,其在10 min可产H230 mL,实现了100%的理论产H2效率。
(3) 与传统的g-C3N4材料相比较g-C3N4/α-Fe2O3复合物在可见光区有更强的吸收峰,电子-空穴复合率低和电子传输阻力更小、更快。
(4) Z型载流子转移途径,赋予了g-C3N4/α-Fe2O3复合物较强的氧化能力,为光催化裂解NaBH4提供了较大的驱动力。
