原发性干燥综合征合并肺受累高分辨CT特点及相关危险因素探讨
2019-11-12徐艳臧银善高玲于哲
徐艳 臧银善 高玲 于哲
【摘 要】目的:分析原发性干燥综合征(pSS)肺受累的高分辨CT(HRCT)表现,探讨pSS发生肺脏受累的临床特点以寻找危险因素,为其治疗及预后提供理论依据。方法:回顾性分析153例pSS患者,根据有无肺脏受累分组,31例肺脏受累为观察组,122例无明显肺脏受累为对照组。利用横断面研究探讨pSS患者肺脏受累的HRCT特点、类型,采用病例对照及回归分析肺脏受累的可能危险因素。结果:肺脏受累在pSS中发生率为20.26%,其中以非特异性间质性肺炎和淋巴细胞性间质性肺炎较高,同时也发现既往报道较少的结节性病变;病例对照分析发现,年龄≥50岁(OR = 1.08)、病程(OR = 3.29)、雷诺现象(OR = 7.56)、抗着丝点抗体(OR = 8.56)、白细胞(OR = 2.36)、D-二聚体(OR = 1.01)可能为pSS患者肺脏受累的独立危险因素。结论:肺受累在pSS中很常见,年龄、病程、雷诺现象、抗着丝点抗体、白细胞数、D-二聚体可能是pSS肺脏受累的危险因素。
【关键词】 干燥综合征;原发性;肺脏;高分辨CT;危险因素
原发性干燥综合征(primary Sj?gren's syndrome,pSS)是主要侵犯外分泌腺的自身免疫性疾病,临床主要表现为口干、眼干,也常累及其他系统。肺脏是血管及结缔组织较多的器官,故为最易受累的器官之一,因研究方法及样本量的差异,大量研究显示,肺受累发生率波动于9%~75%[1]。长期随访发现,肺损伤发生率随病程及年龄的增加有增加的趋势[2-3],肺脏受累对患者的生活质量和生存期均有明显的影响,甚至增加患者死亡风险达5.5倍[4]。
随着影像学技术的发展,高分辨CT(HRCT)能早期发现pSS肺脏病变,但目前关于pSS肺受累HRCT的特点及危险因素相关研究较少。有研究报道,抗SSA抗体、抗SSB抗体是肺脏受累的危险因素,然而国内许多研究表明两者无显著差异[2],甚至有学者报道受累组有较低的抗体阳性率[4-5]。目前,关于pSS肺受累的相关危险因素研究较少,关于雷诺现象、抗着丝点抗体、白细胞数、D-二聚体(DD)和肺脏受累的关系报道更少。故本研究旨在进一步明确肺脏受累相关危险因素和特点,为早期发现、早期干预提供更多理论依据。
1 资料与方法
1.1 临床资料 回顾性分析2015年1月至2019年
12月在宿迁市第一人民医院风湿免疫科就诊的门诊及住院pSS患者153例,均符合2002年美国风湿病学会(ACR)/欧洲抗风湿病联盟(EULAR)协作组制定的pSS分类标准;排除合并肿瘤、丙肝等患者。肺脏受累定义:有气短、咳嗽等呼吸系统症状,同时伴有肺功能受损和(或)HRCT异常。HRCT显示以下异常提示为pSS肺脏受累,包括磨玻璃影、馬赛克线样影、胸膜受累、肺动脉扩张、网格状影、肺气肿、支气管扩张、实变、肺大疱、蜂窝样变、支气管壁增厚、结节影、纵膈淋巴结肿大。除外与pSS不相关的肺部病变,如慢性阻塞性肺病、肿瘤、支气管哮喘、肺结核,以及早于pSS发病的支气管扩张等。153例患者均行HRCT检查,其中31例有肺脏受累(观察组),122例无肺脏受累(对照组),分析2组临床免疫及HRCT特点和差异。
1.2 研究方法 收集所有患者的临床及实验室指标结果,一般资料包括年龄、性别、病程,临床表现包括雷诺现象、皮疹、关节炎等,实验室指标包括血常规、抗核抗体(ANA)、抗SSA抗体、抗SSB抗体、抗着丝点抗体、免疫球蛋白(IgG、IgM及IgA)、类风湿因子(RF)、补体C3、补体C4、C-反应蛋白(CRP)、红细胞沉降率(ESR),所有HRCT均由阅片经验丰富的临床医生和放射科医生共同协商判定。
收集资料后,计算pSS肺脏受累发生率;总结pSS患者肺脏受累的临床和实验室指标特点;采取单因素对比观察组和对照组的各项差异,把临床重要的变量及差异有统计学意义的变量纳入多因素Logistic回归模型,研究肺脏受累的危险因素。
1.3 统计学方法 采用SPSS 19.0软件进行统计分析。计量资料以表示,组间比较采用t检验;计数资料以例(%)表示,采用χ2检验。多因素分析采用Logistic回归分析,拟合Logistic回归模型时,采用逐步回归法筛选变量。以P < 0.05为差异有统计学意义。
2 结 果
2.1 pSS肺脏受累的HRCT表现及构成比 pSS肺脏受累患者的HRCT表现有如下特点:多发性结节2例(1.31%)(活检已排除肿瘤,提示为淋巴细胞浸润性炎症),肺动脉高压2例(1.31%),支气管扩张4例(2.61%),胸膜增厚3例(1.96%),多发性薄壁囊性改变7例(4.58%),肺底磨玻璃影11例(7.19%),弥漫性磨玻璃影2例(1.31%)。
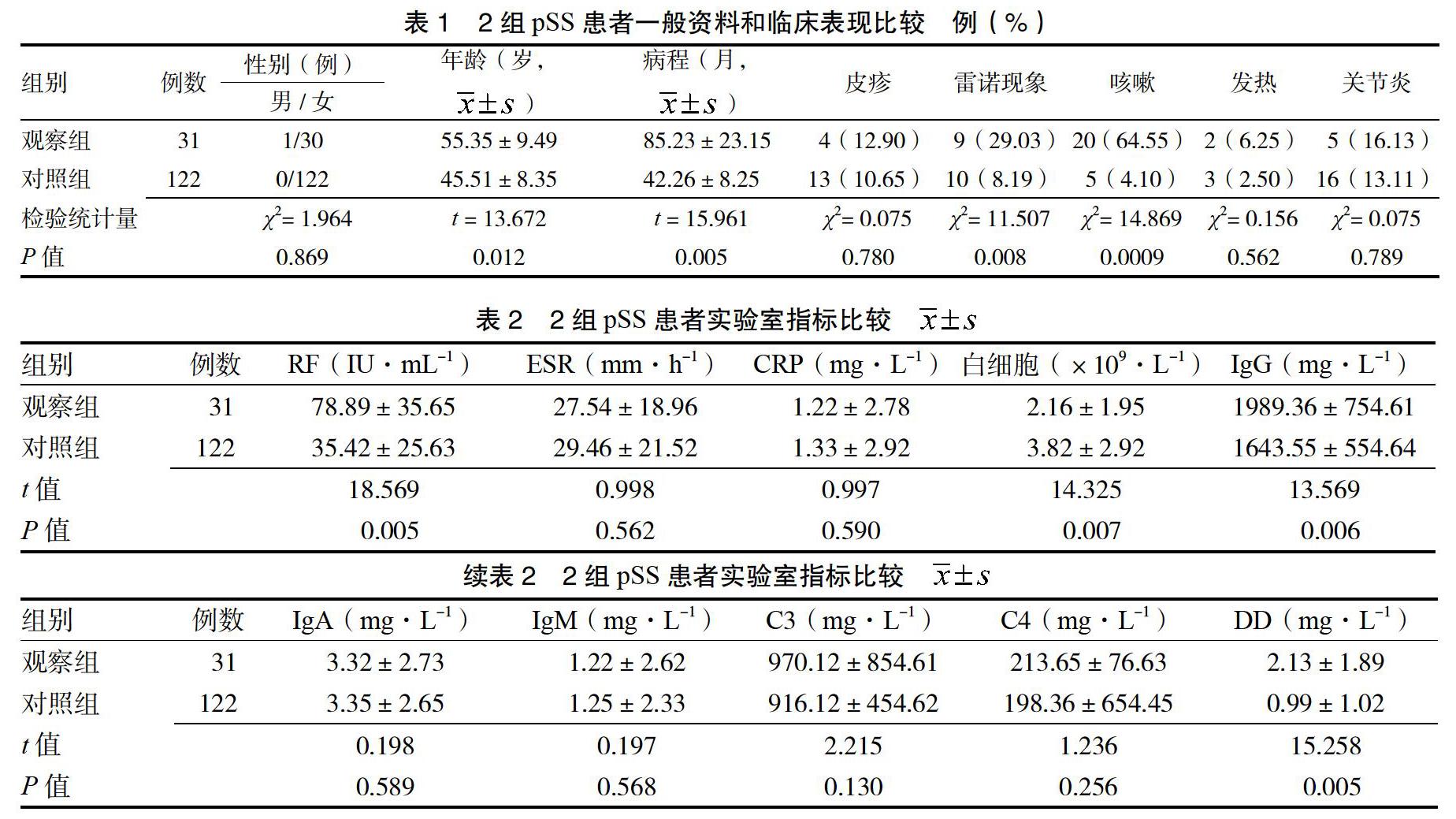
2.2 2组患者一般资料和临床表现比较 本研究153例患者中,31例肺脏受累(20.26%),其中女性30例(96.77%),男性1例(3.23%);而对照组均为女性。2组临床表现有所不同,观察组雷诺现象、咳嗽发生率相对较高。见表1。
2.3 2组患者实验室指标及抗体阳性情况比较 与对照组比较,观察组RF、DD、IgG均显著升高,抗着丝点抗体阳性率更高,白细胞更低,差异均有统计学意义(P < 0.05)。见表2、表3。
2.4 肺受累的多因素分析 把单因素分析时差异有统计学意义的变量(年龄、病程、雷诺现象、白细胞、DD、RF、IgG、着丝点抗体)进行多因素Logistic回归分析,通过逐步回归法筛选变量,RF和IgG被剔出回归模型,而年龄≥50岁(OR =
1.08)、病程(OR = 3.29)、雷诺现象(OR = 7.56)、抗着丝点抗体(OR = 8.56)、白细胞(OR = 2.36)、DD(OR = 1.01)是pSS患者中肺脏受累的独立危险因素。见表4。
[7] KINDER BW,COLLARD HR,KOTH L,et al.Idiopathic nonspecific interstitial pneumonia:lung manifestation of undifferentiated conn ective tissue disease?[J].Am J Respir Crit Care Med,2007,176(7):691-697.
[8] PALM O,GAREN T,BERGE ENGER T,et al.Clinical pulmonary involvement in primary Sj?gren's syndrome:prevalence,quality of life and mortalityfl retrospective study based on registry data[J].Rheumatology(Oxford),2013,52(1):173-179.
[9] MANFREDI A,SEBASTIANI M,CERRI S,et al.Prevalence and characterization of non-sicca onset primary Sj?gren's syndrome with interstitial lung involvement[J].Clin Rheumatol,2017,36(6):1261-1268.
[10] FLAMENT T,BIGOT A,CHAIGNE B,et al.Pulmonary manifestations of Sj?gren's syndrome[J].Eur Respir Rev,2016,25(140):110-123.
[11] SEBASTIAN A,MISTERSKA-SK?RA M,SILICKI J,et al.Chest HRCT findings in patients with primary Sj?gren's syndrome[J].Adv Clin Exp Med,2017,26(7):1101-1106.
[12] YAZISIZ V,ARSLAN G,OZBUDAK IH,et al.Lung involvement in patients with primary Sj?gren's syndrome:what are the predictors?[J].Rheumatol Int,2010,30(10):1317-1324.
[13] ROCA F,DOMINIQUE S,SCHMIDT J,et al.Interstitial lung disease in primary Sj?gren's syndrome[J].Autoimmun Rev,2017,16(1):48-54.
[14] 范海霞,刘健,黄传兵,等.新风胶囊对干燥综合征肺功能的影响及其机制研究[J].风湿病与关节炎,2015,4(1):14-17.
[15] DALVI V,GONZALEZ EB,LOVETT L.Lymphocytic interstitial pneumo nitis(LIP)in Sj?gren's syndrome:a case report and a review of the literature[J].Clin Rheumatol,2007,26(8):1339-1343.
[16] STRIMLAN CV.Interstitial lung disease in primary Sj?gren's syndrome.Clinical-pathological evaluation and response to treatment[J].Am J Respir Crit Care Med,1997,155(4):1489.
[17] 高辉,何菁,张学武,等.原发性干燥综合征肺脏受累及其危险因素分析[J].中华风湿病学杂志,2015,19(5):306-312.
[18] ZHANG R,SUN T,SONG L,et al.Increased levels of serum galectin-3 in patients with primary Sj?gren's syndrome:associated with interstitial lung disease[J].Cytokine,2014,69(2):289-293.
[19] NANNINI C,JEBAKUMAR AJ,CROWSON CS,et al.Primary Sj?gren's syndrome 1976-2005 and associated interstitial lung disease:a populat on-based study of incidence and mortality[J].BMJ Open,2013,3(11):356-369.
[20] KOKOSI M,RIEMER EC,HIGHLAND KB.Pulmonary involvement in Sj?gren's syndrome[J].Semin Respir Crit Care Med,2014,35(2):255-264.
[21] TAKAHASHI T,WADA I,OHTSUKA Y,et al.Autoantibody to alanyl-tRNA synthetase in patients with idiopathic pulmonary fibrosis[J].Respirology,2007,12(5):642-653.
[22] ZHAO Y,LI Y,WANG L,et al.Primary Sj?gren's syndrome in Han Chinese:clinical and immunological characteristics of 483 patients[J].Medicine (Baltimore),2015,94(16):594-606.
[23] ROBINSON CM,NEARY R,LEVENDALE A,et al.Hypoxiainduced DNA hypermethylation in human pulmonary fbroblasts is associated with Thy-1 promoter methylation and the development of a pro-fbrotic phenotype[J].Respir Res,2012,31(13):74.
[24] 何愛芹,陈秀梅.D-二聚体检测及其临床意义[J].中华中西医杂志,2006,7(11):8.
收稿日期:2019-03-01;修回日期:2019-05-25
