高效液相色谱-示差折光检测器法测定聚多卡醇注射液的有关物质和含量
2019-10-30杨梅欧嘉娜
杨梅 欧嘉娜

[摘要]目的 建立一种测定聚多卡醇注射液有关物质和聚多卡醇含量的方法。方法 采用高效液相色谱-示差折光检测器法进行测定。色谱柱为Nucleosil-120 C18柱(250 mm×4 mm,5 μm)或效能相当的色谱柱;流动相为乙腈-甲醇-水=20∶68∶12;流速為1.0 ml/min;柱温和检测器温度均为45℃;进样量为20 μl。按不加校正因子的主成分自身对照法测定聚多卡醇注射液中的已知杂质[正十二醇、C10(EO)nOH、C14(EO)nOH]和未知杂质,采用外标法测定聚多卡醇注射液中聚多卡醇的含量。结果 有关物质中主成分检测质量浓度线性范围为2.7316~109.2638 μg/ml(r=0.99997),相应的杂质限度范围为0.05%~2.00%,检测限为0.6829 μg/ml。聚多卡醇含量测定中主成分检测质量浓度线性范围为0.98~2.93 mg/ml(r=0.99996),平均回收率为99.3%(RSD=0.9%,n=9)。测定两个规格6批聚多卡醇注射液样品的含量分别为100.6%、101.3%、102.0%、100.1%、100.8%、101.2%。结论 本文建立的聚多卡醇注射液中的聚多卡醇含量和有关物质测定方法,简单可行,可有效控制聚多卡醇注射液的质量。
[关键词]高效液相色谱法;聚多卡醇注射液;有关物质;含量
[中图分类号] R543 [文献标识码] A [文章编号] 1674-4721(2019)8(a)-0015-04
[Abstract] Objective To establish a method for the determination of related substances and Polidocanol contents in Polidocanol Injection. Methods The method of high performance liquid chromatography-differential refractive index detector method was adopted. The determination was performed on a Nucleosil-120 C18 column (250 mm×4 mm, 5 μm), or a chromatographic column of comparable potency; the mobile phase consisted of acetonitril-methanol-water was 20∶68∶12; the flow rate was 1.0 ml/min; the temperatures of both the column and the detector were 45℃; the injection volume was 20 μl. The known impurities, such as n-dodecyl alcohol, C10(EO)nOH, C14(EO)nOH), and unknown impurities in Polidocanol Injection were determined by principal component self-control method without correction factor, and the Polidocanol contents of Polidocanol Injection was determined by external standard method. Results The linear range of main component in related substances test were 2.7316-109.2638 μg/ml (r=0.99997), and the limits of related impurity were 0.05%-2.0%, the detection limits was 0.6829 μg/ml. The linear range of main component in polidocanol content test were 0.98-2.93 mg/ml (r=0.99996), the rate of average recovery was 99.3% (RSD=0.9%, n=9). The contents of 6 batches of Polidocanol Injection samples were determined as 100.6%, 101.3%, 102.0%, 100.1%, 100.8% and 101.2%, respectively. Conclusion The method for determination of Polidocanol contents and related substances in Polidocanol Injection is simple and feasible, which can effectively control the quality of Polidocanol Injection.
[Key words] High performance liquid chromatography method; Polidocanol Injection; Related substances; Content
下肢静脉曲张是周围血管疾患中最常见的疾病之一,多见于长期从事持久体力劳动或站立工作的人员,已成为各地血管外科门诊或病房的首要病种,而且就诊人数呈逐年递增的趋势。针对此类疾病,现代医学治疗方法包括保守压包扎和弹力绷带治疗、传统手术治疗和硬化剂注射治疗,但其术后复发率在20%~30%,且恢复较慢,溃疡复发率极高[1-2]。聚多卡醇注射液是目前公认的安全有效的硬化剂,临床上主要用于下肢静脉曲张硬化治疗[3-7]、近年来逐渐用于静脉畸形[8-9]、淋巴管畸形[10]、普通婴幼儿血管瘤[11-12]、盆腔淤血综合征[13]、化脓性肉芽肿[14]、男性精索静脉曲张[15],已于2010年3月31日获美国批准用于治疗小血管静脉曲张。聚多卡醇作为血管硬化剂,静脉内注射后,通过化学作用刺激囊壁,使囊壁上皮细胞变性、脱水、坏死,并产生无菌性炎症、纤维组织增生,从而使囊腔粘连、缩小、闭合,逐步吸收并消失[16]。由于中国药典并未收载聚多卡醇注射液,EP9.0[17]、BP2019[18]和JP17[19]也只有原料药的标准,因此,为了更好地保证药品质量,本研究通过参考英国药典原料药质量标准与本制剂相关文献[20-21],对现行进口药品质量标准(JX20150310)[22]进行改进和完善,结合聚多卡醇注射液的工艺过程,建立了有关物质的检查方法,并使用同一色谱条件测定聚多卡醇的含量,以更好地对聚多卡醇注射液的质量情况进行评价,现报道如下。
1仪器与试药
1.1仪器试剂
岛津LC-20A型高效液相色谱仪;示差折光检测器;LC-solution工作站;乙腈、甲醇均为色谱纯,其他试剂均为分析纯;水为纯化水。
1.2試药
聚多卡醇注射液样品及空白辅料(上海某公司,批号:7E15110、6K28109、7H23100,规格:2 ml∶20 mg;批号:7B13106、6I05107、7H02100,规格:2 ml∶60 mg);聚多卡醇对照品(上海某公司企业工作对照品,批号:PD-16041-R9,含量:98.1%);正十二醇对照品(sigma公司,批号:BCBW5085,含量100.0%);C10(EO)nOH对照品(sigma公司产品分装,批号:74716,分子式:C26H54O9,CAS:24233-81-6,含量100.0%);C14(EO)nOH对照品(sigma公司产品分装,批号:74719,分子式:C30H62O9,CAS:27847-86-5,含量100.0%)。
2方法与结果
2.1色谱条件
色谱柱:Nucleosil-120 C18(250 mm×4 mm,5 μm);流动相:乙腈-甲醇-水(20∶68∶12);流速:1.0 ml/min,柱温及检测器温度:45℃;进样量:20 μl。
2.2溶液的制备
2.2.1供试品溶液的制备 精密量取聚多卡醇注射液样品适量,加水稀释制成每1 ml中含5 mg的溶液,作为有关物质测定的供试品溶液;精密量取聚多卡醇注射液样品适量,加水稀释制成每1 ml中含2 mg的溶液,作为含量测定的供试品溶液。
2.2.2对照品溶液及灵敏度溶液的制备 精密量取供试品溶液适量,用水定量稀释制成每1 ml中含25 μg的溶液,作为有关物质测定的对照品溶液;取聚多卡醇对照品适量,精密称定,加水溶解并稀释制成每1 ml中含2 mg的溶液,作为聚多卡醇含量测定的对照品溶液。精密量取对照溶液适量,用水定量稀释制成每1 ml中含2.5 μg的溶液,作为灵敏度试验溶液。
2.2.3空白辅料溶液的制备 按“2.2.1”项下的供试品溶液制备方法,制备不含聚多卡醇的空白辅料溶液。
2.2.4系统适用性溶液的制备 取聚多卡醇对照品和正十二醇对照品适量,加入异丙醇溶解并稀释,制成每1 ml中含50 mg聚多卡醇和0.75 mg正十二醇的混合溶液,摇匀,量取1 ml,置于10 ml的量瓶中,用水稀释至刻度,摇匀,作为系统适用性溶液。
2.3系统适用性试验
取“2.2.4”项下的系统适用性溶液20 μl,注入高效液相色谱仪,按照“2.1”项下的色谱条件进样。正十二醇峰和聚多卡醇峰的分离度应符合要求;聚多卡醇峰的拖尾因子不得超过2.5;理论板数按聚多卡醇峰计应不低于1000。
有关物质检查中,灵敏度是重要的检测因素。研究结果提示,柱温和检测器温度对检测灵敏度有较大的影响。随着柱温和检测器温度的升高,正十二醇和聚多卡醇峰的分离度逐渐变小,但主峰(聚多卡醇峰)拖尾因子亦变小,峰形趋于对称,灵敏度提高(表1)。综合各种因素,选择柱温和检测器温度均为45℃作为实验条件。
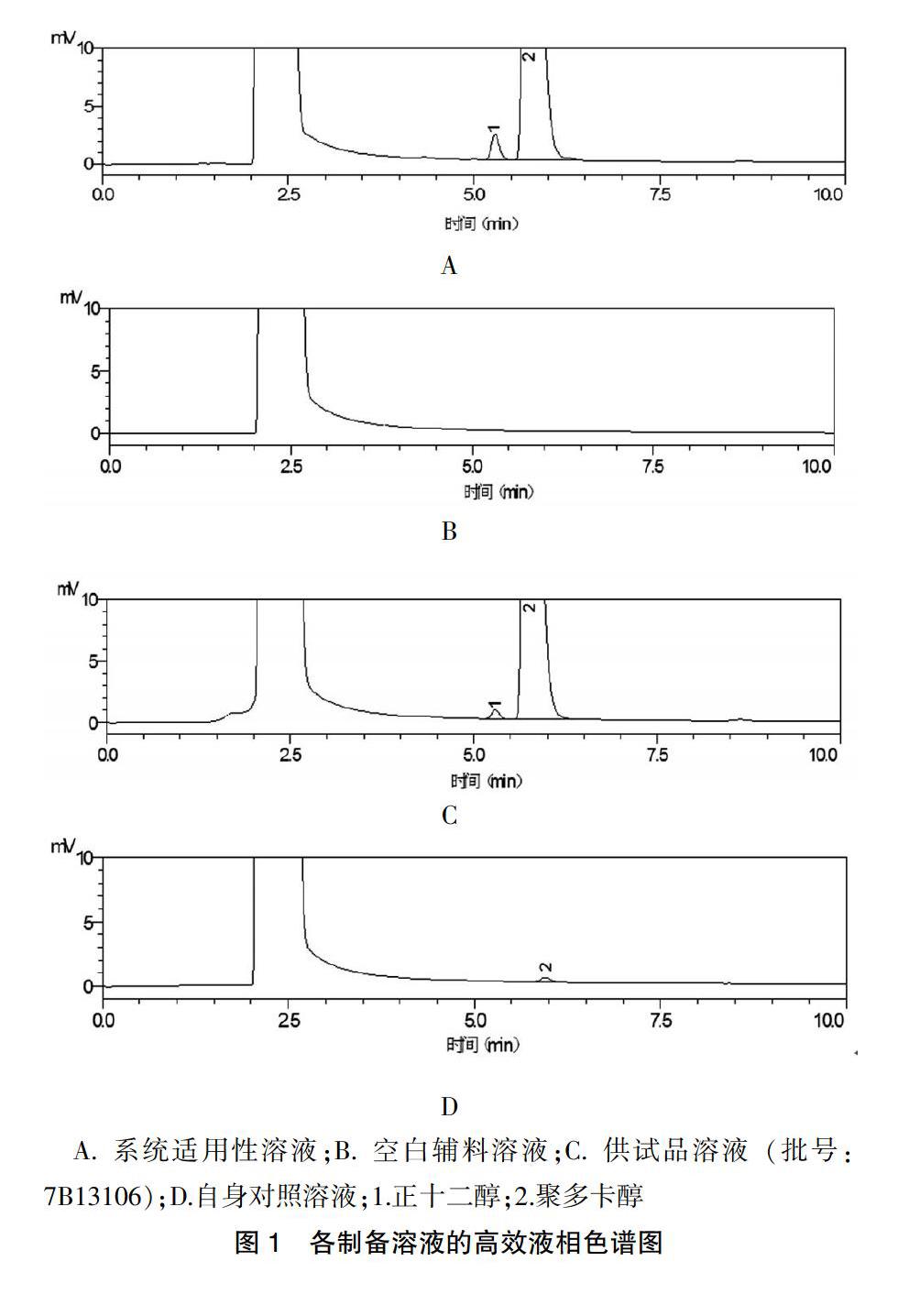
精密量取系统适用性溶液、空白辅料溶液、供试品溶液(批号:7B13106)和自身对照溶液各20 μl进行测定,色谱图见图1。结果显示,聚多卡醇峰与杂质峰及杂质峰之间分离度均>1.5,空白辅料对测定无干扰,表明该方法专属性良好。
2.4线性关系及检出限试验
有关物质采用主成分自身对照法进行计算,对主成分作线性分析,以浓度(X)为纵坐标,峰面积(Y)为横坐标,计算得到线性方程为Y=0.006 777 74X+0.627 938,r=0.999 97(n=6),主成分在2.7316~109.2638 μg/ml范围内线性关系良好,检出限(S/N=3)为0.6829 μg/ml,相应的杂质限度范围为0.05%~2.00%。
检测聚多卡醇含量的质量浓度线性范围为0.98~2.93 mg/ml,计算得到线性方程为:Y=167 916.2X-221.5,r=0.999 96(n=5),限度范围为95.0%~105.0%。
2.5精密度试验
取“2.2.2”项下的有关物质对照品溶液,连续进样6次,记录峰面积,分别为3640、3643、3658、3635、3677、3651,计算RSD值,聚多卡醇峰面积RSD为0.4%,表明该方法精密度良好。
2.6稳定性试验
取“2.2.1”项下的有关物质供试品溶液,分别于1、2、6、8、16、20、24 h时按照“2.1”项下的色谱条件进样,记录色谱图,测定峰面积值,依次为714 444、713 070、712 900、714 807、711 812、714 059、712 441,峰面积RSD=0.2%。各杂质及主峰面积均无显著性变化,RSD均<2.0%。表明供试品溶液在24 h内稳定性良好。
2.7有关物质的测定方法及限度
精密量取“2.2.2”项下的灵敏度试验溶液20 μl,按照“2.1”项下的色谱条件注入高效液相色谱仪,聚多卡醇峰的S/N应>10。精密量取“2.2.1”项下的供试品溶液和“2.2.2”项下的对照品溶液各20 μl,分别按照“2.1”项下的色谱条件注入高效液相色谱仪,记录色谱图至主峰保留时间的3倍。供试品溶液色谱图中如有杂质峰,正十二醇峰面积≤对照溶液主峰面积的3倍(1.5%),C10(EO)nOH(相对保留时间0.75)和C14(EO)nOH(相对保留时间1.5)峰面积分别≤对照溶液主峰面积的2倍(1.0%),其他单个杂质峰面积≤对照溶液主峰面积的0.2倍(0.1%),其他杂质峰面积之和≤对照溶液主峰面积的0.6倍(0.3%)。
2.8加样回收率试验
按含量测定供试品溶液浓度的80%、100%、120%各制备3份聚多卡醇回收试验溶液,测定溶液中主成分含量,计算得到平均回收率为99.3%,RSD=0.9%(n=9),回收率良好。
2.9样品有关物质及聚多卡醇含量测定结果
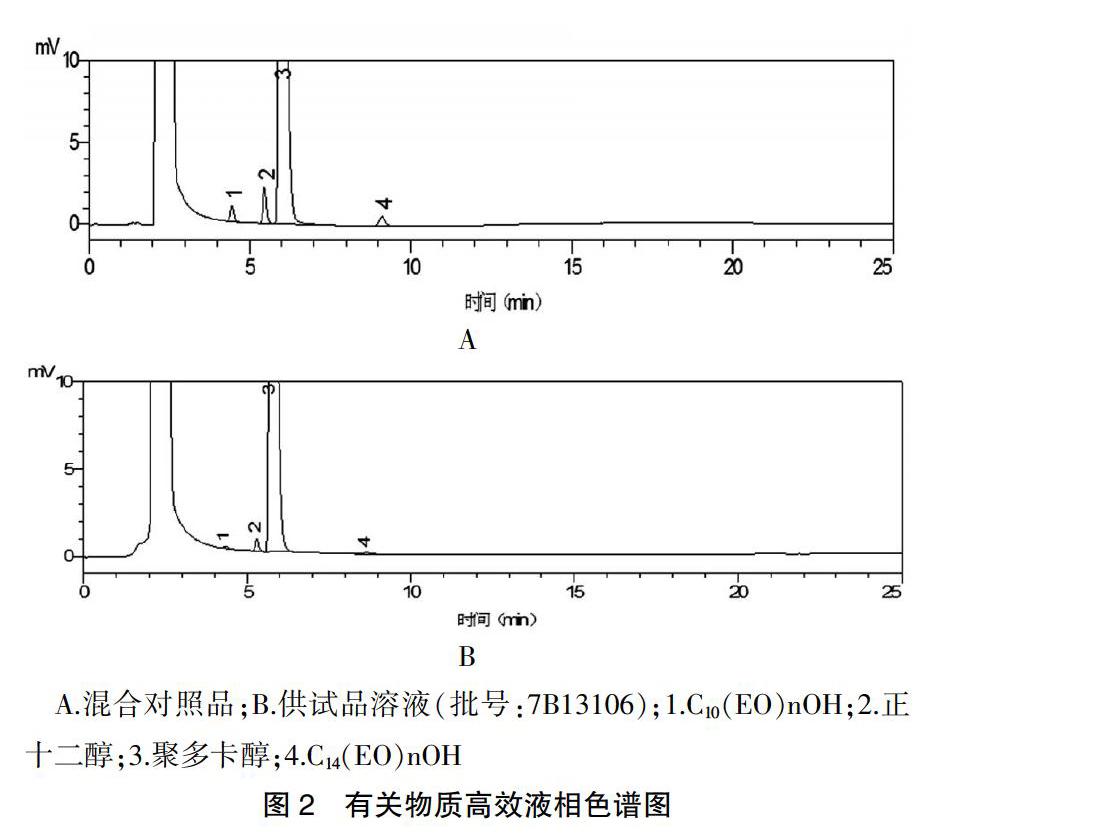
按照“2.1”項下的色谱条件对两个规格6批聚多卡醇注射液样品进行有关物质测定,聚多卡醇峰与杂质峰及各杂质峰之间均得到较好的分离(分离度均>1.5),色谱图见图2。
两个规格6批注射液正十二醇均不过1.0%,C10(EO)nOH均不过0.1%,C14(EO)nOH均不过0.2%,其他单个杂质均不过0.1%,其他杂质总量均为0.1%(表2)。
按照“2.1”项下的色谱条件,取“2.2.1”项下的供试品溶液和“2.2.2”项下的对照品溶液进行测定,按外标法以峰面积计算聚多卡醇含量。两个规格6批聚多卡醇注射液样品的聚多卡醇含量分别为100.6%、101.3%、102.0%、100.1%、100.8%、101.2%,均在规定限度范围内(表2)。
A.混合对照品;B.供试品溶液(批号:7B13106);1.C10(EO)nOH;2.正十二醇;3.聚多卡醇;4.C14(EO)nOH
3讨论
3.1检测器的选择
由于聚多卡醇在紫外检测器没有吸收,所以本实验采用示差折光检测器作为本研究的检测器,通过控制色谱条件,对样品的主成分聚多卡醇和相邻杂质进行了有效分离,检测器的灵敏度和精密度均符合实验要求。示差折光检测器,其折射率与温度有关,因此,实验过程中应注意环境温度,以免温度变化影响保留时间漂移和测定结果。
3.2已知杂质和未知杂质的选择
本次实验得到了企业的大力支持,企业提供了聚多卡醇注射液的工艺过程,合成聚多卡醇的起始原料为正十二醇,正十二醇中主要含有正癸醇和正十四醇两个杂质,在合成过程中,正癸醇和正十四醇和环氧乙烷生成相应的乙氧化脂肪醇,如C10(EO)nOH和C14(EO)nOH,这两个有关物质并非聚多卡醇的降解产物,在制剂中的含量保持不变,故正十二醇、C10(EO)nOH和C14(EO)nOH分别作为已知杂质进行控制,其他杂质则为未知杂质。
3.3已知杂质的相对校正因子测定
本实验采用企业提供的对照品,对已知杂质进行了峰确证,并采用外标法,以峰面积计算,测定了3个已知杂质正十二醇、C10(EO)nOH和C14(EO)nOH的响应因子。但考虑到今后难以提供这些对照品,故对其采用了相对保留时间定位,由于3个已知杂质相对于主成分(聚多卡醇)的校正因子(乘法)分别约为1.2、1.0和1.2,因此采用了不加校正因子的主成分自身对照法计算杂质量。
本文建立的聚多卡醇注射液中的聚多卡醇含量和有关物质测定方法,简单可行,可有效控制聚多卡醇注射液的质量,值得进行进一步深入研究。
[参考文献]
[1]周晓东,张有福,杨勇.中医防治下肢静脉曲张术后并发症的研究进展[J].世界最新医学信息文摘,2018,18(86):72-73.
[2]司富春,宋雪杰.下肢静脉曲张中医证型和方药临床研究的数据挖掘[J].世界中西医结合杂志,2015,10(4):449-455.
[3]李小红,刘春梅.聚多卡醇泡沫硬化剂治疗下肢静脉曲张50例[J].现代医学与健康研究,2018,2(15):26-28.
[4]张矛,刘洪,王寒琛,等.超声引导下泡沫硬化治疗老年下肢静脉曲张疗效观察[J].实用医院临床杂志,2018,15(4):174-176.
[5]马博,叶志东,陈洁,等.聚多卡醇硬化剂门诊治疗下肢静脉曲张的安全性[J].中日友好医院学报,2018,32(2):75-78.
[6]王林君,董阳民,王松茂,等.超声引导下聚多卡醇泡沫硬化剂治疗大隐静脉曲张的早期临床疗效分析[J].中国普通外科杂志,2016,25(6):931-934.
[7]章永萍,林勇强,魏晓建.激光联合泡沫硬化剂腔内闭合及点对点抽剥术治疗原发性大隐静脉曲张160例[J].中国乡村医药,2018,25(7):12-13.
[8]李国文,古善智,黄满平,等.聚桂醇泡沫硬化剂治疗静脉畸形效果与安全性评价[J].介入放射学杂志,2018,27(7):680-684.
[9]牛传强,李海波,刘浪,等.经皮硬化疗法治疗手部静脉畸形37例[J].介入放射学杂志,2018,27(9):832-835.
[10]林文雄,苏振民,汪城河,等.负压吸引联合硬化剂治疗微囊型淋巴管畸形[J].中国美容医学,2017,26(11):48-50.
[11]刘珍银,夏杰军,徐文婵.1%聚多卡醇局部注射治疗普通婴幼儿血管瘤疗效观察[J].现代医院,2017,17(3):390-392.
[12]中华口腔医学会口腔颌面外科专业委员会脉管性疾病学组.聚桂醇硬化剂治疗口腔颌面部血管瘤和脉管畸形专家共识[J].中国口腔颌面外科杂志,2018,16(3):275-278.
[13]王书新,梁奇伟,黄益,等.聚多卡醇治疗盆腔淤血综合征1例[J].医学影像学杂志,2017,27(3):578-579.
[14]丁语,陆信武,郑家伟,等.聚多卡醇治疗化脓性肉芽肿11例临床观察[J].中国皮肤性病学杂志,2017,31(9):1052-1053.
[15]Ali A,Wirth S,Treitl KM.Treatment of male varicoceles by transcatheter polidocanol foam sclerotherapy:evaluation of clinical success,complications,and patients satisfaction with regard to alternative techniques[J].Eur Radiol,2015,25(10):2889-2897.
[16]黎永滨,谢婷婷,钟洁瑜.聚桂醇在囊肿硬化的临床应用文献综述[J].罕少疾病杂志,2018,25(4):73-74.
[17]欧洲药典委员会.欧洲药典[S].9.0版.欧洲药品质量管理局,2016.
[18]英国药典委员会.英国药典[S].2019版.The Stationery Office,2018.
[19]日本药局方编辑委员会.日本药局方[S].17版.日本厚生劳动省颁布执行,2016.
[20]王发,徐长根,孟新芳,等.HPLC法测定聚桂醇原料药的含量[J].中国药事,2013,27(6):617-619.
[21]王红梅,黄剑英,陈素俭,等.聚桂醇400注射液的HPLC测定[J].中国医药工业杂志,2003,34(11):577-278.
[22]国家药品监督管理局.JX20150310国家食品药品监督管理局进口药品注册标准[S].国家食品药品监督管理局,2015.
(收稿日期:2019-01-07 本文编辑:孟庆卿)
