重症患者合并用药致不良事件1例
2019-10-12俞婷婷邓霖芳
俞婷婷,邓霖芳
(浙江中医药大学附属第三医院药剂科,杭州 310005)
1 病例资料
患者,男,75岁。有“四环素、土霉素、地红霉素、青霉素、庆大霉素”过敏史,具体不详,否认肝炎、肾病等疾病史。2018年2月5日入院,2018年2月7日转入重症监护室,诊断“①社区获得性肺炎,重症呼吸衰竭;②慢性支气管炎;③高血压病;④骨质疏松”。经验性予注射用美罗培南1.0 g,静脉推注,q8h(2018年2月7—23日)抗感染治疗,后因痰培养多次回报为白假丝酵母、泛耐药鲍曼不动杆菌(仅替加环素敏感)与肺炎克雷伯菌(仅替加环素及氨基苷类敏感),先后予注射用亚胺培南西司他丁0.5 g,静脉滴注,q6h(2018年2月23日—3月9日),利奈唑胺注射液0.6 g,静脉滴注,q12h(2018年2月7日—2月20日),注射用替加环素100 mg,静脉滴注,q12h(2018年2月20日—3月1日)、50 mg,静脉滴注,q12h(2018年3月2日),联合注射用卡泊芬净50 mg(首剂70 mg),静脉滴注,qd(2018年2月8—23日)、注射用伏立康唑0.2 g,静脉滴注,q12h(首日加倍,2018年2月24日—3月1日)抗感染及泮托拉唑针(2018年2月6日—3月9日)抑酸护胃、甲泼尼龙针抗炎等对症支持治疗。患者入院时肝、肾功能基本正常,2018年2月6日生化指标结果:丙氨酸氨基转移酶(ALT)26 U·L-1,天冬氨酸氨基转移酶(AST)49 U·L-1,碱性磷酸酶(ALP)42 U·L-1,总胆红素(T-BiL)9.3 μmol·L-1,直接胆红素(D-BiL)4.2 μmol·L-1,间接胆红素(I-BiL)5.0 μmol·L-1,肌酐(Scr)95 μmol·L-1。2018年2月26日出现肝转氨酶异常,予注射用还原型谷胱甘肽1.2 g,静脉推注,qd(2018年2月27日—3月9日)护肝治疗。2018年2月28日,患者转氨酶继续升高的同时伴随胆红素异常,评估病情后停用伏立康唑,替加环素减量为50 mg,q12h,并加用注射用腺苷蛋氨酸1.0 g,iv,qd(2018年3月1—9日)护肝治疗(表1)。患者入院后大便较少,每2~3 d一次黄软便,2018年2月22日开始逐渐增多,至2018年2月27日达9次,但粪便常规及性状均正常,临床药师考虑为替加环素所致的腹泻,但临床医师考虑抗生素相关性腹泻不能排除,2018年3月1日开始予甲硝唑片0.5 g,tid,po治疗。2018年3月2日患者仍有明显腹泻,结合患者肝功能及感染情况,临床药师建议停用替加环素,临床医师采纳。停药后患者腹泻好转,至2018年3月5日恢复正常。患者使用甲硝唑前白细胞(WBC)正常,红细胞(RBC)、血小板(PLT)略减少,使用3 d后血小板进一步下降,并伴随白细胞低下,临床药师考虑与甲硝唑相关,且患者大便已恢复正常,建议停用,临床医师采纳(2018年3月5日仅使用一次)。患者停用甲硝唑后白细胞、血小板逐渐恢复正常(表1)。2018年3月9日患者病情好转,转下级医院继续治疗。
2 讨论
2.1替加环素与伏立康唑致肝功能异常 患者入院时肝功能正常,使用替加环素6 d、伏立康唑3 d后出现ALT异常,第8天与第5天后出现ALP、胆红素异常,此后胆红素较转氨酶升高更快、更明显,有与药物性肝损伤发病规律相一致的潜伏期(5~90 d内)。患者否认“肝炎”病史,病情好转后肝功能出现异常,可排除其他病因或疾病所致的肝损伤。替加环素及伏立康唑说明书均有提及肝脏方面的不良反应,且作者在药物治疗中也碰到多例替加环素致胆汁淤积性肝损伤的患者[1]。根据《药物性肝损伤诊治指南》[2],患者很可能为替加环素与伏立康唑引起的药物性肝损伤。临床药师与医师进行积极沟通,及时护肝,并先后停用伏立康唑、替加环素后肝转氨酶下降,胆红素稳定。临床药师分析造成患者药物性肝损伤的原因有:①高龄[3]。②大剂量使用替加环素:说明书批准的适应证为复杂性腹腔内感染、复杂皮肤及软组织感染和社区获得性肺炎,推荐的给药方案为首剂100 mg,维持50 mg,q12h,疗程5~14 d。随着耐药菌的出现,替加环素超适应证用于医院获得性或呼吸机相关性肺炎及超剂量给药(首剂200 mg,维持100 mg,q12h)现象较普遍,但该方案的有效性及安全性一直饱受争议,尚需更多的循证证据支持[4-5]。③高敏体质:患者对多种药物过敏,尤其有“四环素”过敏史,而替加环素在结构上与四环素类似,不排除特异质性药物性肝损伤[2]的可能。④基因多态性:伏立康唑在体内呈非线性药动学特性,主要通过有基因多态性的CYP2C19代谢,相同剂量下,中间代谢型与弱代谢型较强代谢型患者血药浓度较高,发生肝毒性的概率增加[6],而与慢代谢者基因型相关的CYP2C19的无功能突变体在亚洲人群中发生频率较高,为13%~23%[7]。不排除患者为慢代谢者。⑤药物相互作用:伏立康唑不仅是CYP2C19、CYP2C9和CYP3A4的底物,也是其抑制剂;质子泵抑制剂通过CYP2C19和CYP3A4代谢,其中有些还是CYP2C19抑制剂。泮托拉唑在肝细胞内通过CYP酶双系统代谢,被认为不易发生药物相互作用,但文献表明亦不能排除其抑制伏立康唑代谢而导致不良反应的发生[8]。
2.2替加环素与伏立康唑致腹泻 替加环素为米诺环素的衍生物,与四环素类药物存在相似不良反应,胃肠道不良反应发生率较高,在临床试验中[9],替加环素相关腹泻发生率为7.4%,说明书不良反应亦有腹泻、排便异常、艰难梭菌相关性腹泻。伏立康唑说明书同样提到腹泻为其很常见的不良反应。患者使用替加环素前大便正常,使用2 d后出现次数增多,而此时又加用伏立康唑,两药联用5 d后出现严重腹泻,停用伏立康唑4 d,替加环素3 d后大便恢复正常,根据国家药品不良反应监测中心药品不良反应/事件关联性评价,该患者的腹泻很可能为替加环素与伏立康唑联用的结果。
2.3甲硝唑联用伏立康唑致白细胞、血小板减少 患者使用甲硝唑前白细胞正常,血小板略减少,使用3 d后血小板进一步下降,并伴随白细胞低下,停用甲硝唑后白细胞、血小板逐渐恢复正常,且患者在出现白细胞、血小板减少期间,感染好转,其他治疗方案并未做调整,包括可使白细胞计数升高的激素方案亦未做调整。甲硝唑说明书不良反应项有白细胞减少,且临床药师查阅文献[10-12]亦有相关报道,故临床药师认为患者白细胞、血小板减少很可能与甲硝唑有关。导致本例患者血液系统不良反应的高危因素有:①高龄,肾功能生理性减退,而甲硝唑及其代谢物主要通过尿液消除(60%~80%)。②用药剂量偏大:甲硝唑片常用剂量为0.6~1.2 g·d-1,而患者采用1.5 g·d-1的大剂量。③肝功能不全:甲硝唑通过肝脏代谢,肝功能不全时,药物代谢酶活性受损,代谢功能降低,药物易在体内蓄积。④药物相互作用:甲硝唑通过肝脏细胞色素P450(CYP)系统代谢,为CYP2C9抑制剂,但并不是CYP1A2,2C10,2D6,2E1和 3A3的底物[13]。伏立康唑经肝CYP同工酶(CYP2C19,2C9,3A4)代谢,并抑制这些酶的活性,因此可抑制甲硝唑的代谢。患者甲硝唑于伏立康唑停用当天开始使用,虽然两者仅同时使用1 d,但伏立康唑的代谢具可饱和性,药动学呈非线性,在体内有较长时间的蓄积,且患者肝功能不全,导致伏立康唑在体内代谢缓慢,蓄积时间更长。因此,伏立康唑与甲硝唑虽仅同时使用1 d,但仍存在较长时间的药物相互作用。
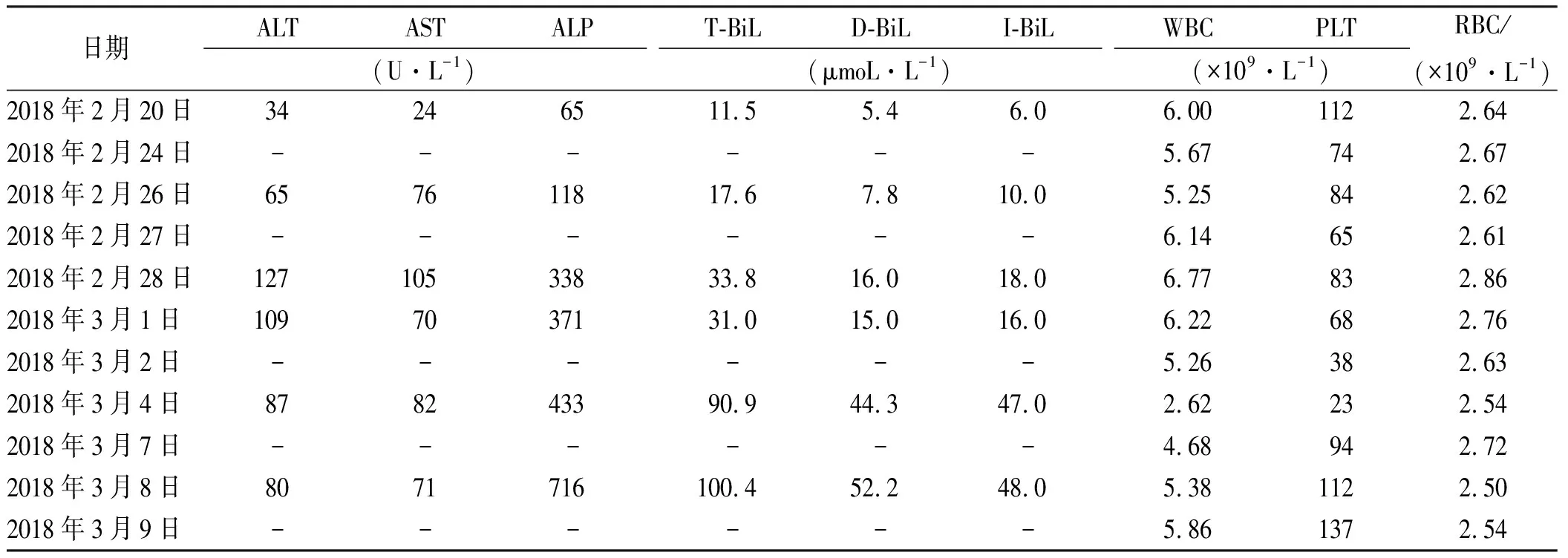
表1 患者住院期间血常规及生化指标检测结果
患者超说明书剂量使用替加环素导致不良事件发生概率增加,且替加环素代谢缓慢,血浆半衰期42.4 h,8~10 d才能从体内完全清除,导致停药后不良事件仍可持续存在较长时间。通常胆汁淤积型药物性肝损伤恢复时间约(6.6±4.2)周[5],替加环素可能需要更长的时间,这也是本例患者停药后胆红素未能及时下降的原因,提示临床在使用替加环素的过程中应严格掌握适应证,避免超剂量用药,尤其是老年患者,一旦出现肝功能损伤症状或(和)肝脏生化检测异常应及时停药,以免引起急性重症药物性肝损伤。伏立康唑肝毒性与血药浓度呈正相关,当血药浓度>5.5 mg·L-1,肝功能损伤的发生率明显增加。由于我院尚未开展伏立康唑血药浓度检测,故无法评估患者的肝损伤是否与伏立康唑血药浓度过高有关,有条件的医院在进行伏立康唑治疗时可以进行血药浓度监测,实现个体化给药,从而在保证伏立康唑治疗效果的同时,避免或减少不良反应的发生。患者仅用药 3 d就出现明显的白细胞和血小板减少,提示甲硝唑短期应用亦可致明显的血液系统不良反应。虽然经停药后恢复正常,但仍应引起临床医师的高度重视。临床药师融入临床治疗团队,并共同参与到用药方案的制定中,可以弥补临床医师在药学知识方面的不足,及时对发生不良反应的药物进行排查、分析,减少甚至避免不良事件的发生,从而切实有效地维护患者安全、合理用药。
