健脾补血颗粒微生物限度检查方法的验证
2019-06-29孙乃霞郭社民
孙乃霞 郭社民
药品的检查项目中,微生物限度检查是一项重要的指标,为了使检验方法更合理,更能真实地考察药物的微生物污染情况,国家药典委员会也不断地完善微生物检查法。该法2015年版《中华人民共和国药典》收载的方法较之前的版本变化较大,比如培养基、培养方法、培养条件等方面,所以为了检验结果的准确可靠,样品检验时需要重新建立合适的检验方法[1,2]。健脾补血颗粒是比较常见、应用也比较广泛的中药制剂,它收载在《卫生部药品标准中药成方制剂》第十七册中。相关组份有皂矾、党参、茯苓、黑豆(炒)、神曲茶、甘草、白术、陈皮等,功能主治为各种类型的贫血,也能和胃、健脾、助消化。本文依照《中华人民共和国药典》2015年版规定的检验方法对健脾补血颗粒微生物限度检查方法进行试验,寻找合适的检验方法,不仅使本样品检验结果准确可靠,也希望能对药品生产企业和检验监督机构提供一些参考。
1 实验材料
1.1 仪器设备电热恒温培养(上海跃进医疗器械厂,型号:HHBII500-S、扬州慧科电子有限公司,型号:GHP-9162)、生化培养箱(扬州慧科电子有限公司,型号:SPX-150)、立式灭菌器(上海博讯实业有限公司医疗设备厂,型号:YXQ-LS-50SII)、生物安全柜(苏净集团安泰空气技术有限公司,型号:BSC-1600IIA2、电子天平(福州华志科学仪器有限公司,型号:HZF-AE200)。
1.2 培养基胰酪大豆胨琼脂培养基(批号:20170607)、胰酪大豆胨液体培养基(批号:20170218)、沙氏葡萄糖琼脂培养基(批号:20170525)、沙氏葡萄糖液体培养基(批号:20170605)、肠道菌增菌液体培养基(批号:20170603)、紫红胆盐葡萄糖琼脂培养基(批号:20171200)、麦康凯琼脂培养基(批号:20180220)、麦康凯液体培养基(批号:20171212)、RV沙门增菌液体培养基(批号:20180402)、木糖赖氨酸脱氧胆酸盐琼脂培养基(批号:20180623)、三糖铁琼脂(批号:20180620)。生产厂家:青岛高科园海博生物技术有限公司。以上培养基的适用性试验均符合现行《中华人民共和国药典》规定。
1.3 试验样品健脾补血颗粒厂家:河南华峰制药有限公司,批号:20180401(1号)、20180402(2号)、20180403(3号)。
1.4 试验菌大肠埃希菌[CMCC(B)44102]、铜绿假单胞菌[CMCC(B)10104]、枯草芽孢杆菌[CMCC(B)63501]、乙型副伤寒沙门菌[CMCC(B)50094]、金黄色葡萄球菌[CMCC(B)26003]、黑曲霉菌[CMCC(F)98003]、白色念珠菌[CMCC(F)98001],购自广东环凯微生物科技有限公司。
2 实验方法
2.1 菌液的制备金黄色葡萄球菌菌悬液的制备:Ⅰ将金黄色葡萄球菌接种到胰酪大豆胨液体培养基中,33℃培养20 h,取该培养物适量;Ⅱ用0.9%的无菌氯化钠溶液配制成菌悬液,再用0.9%的氯化钠溶液分步稀释,选取1 ml的含菌量不超过100 cfu的菌悬液备用。枯草芽孢杆菌菌悬液的制备:将枯草芽孢杆菌接种到胰酪大豆胨液体培养基中,33℃培养20 h,取该培养物适量,余下配制方法同上述Ⅱ的操作。铜绿假单胞菌菌悬液的制备:将铜绿假单胞菌接种到胰酪大豆胨液体培养基中,33℃培养20 h,取该培养物适量,余下配制方法同上述Ⅱ的操作。黑曲霉菌悬液的制备:将黑曲霉菌接种到沙氏葡萄糖琼脂培养基上,23℃培养6 d,加0.9%无菌氯化钠溶液5 ml,洗脱孢子,制成孢子悬液。取孢子悬液适量,余下配制方法同上述Ⅱ的操作。白色念珠菌菌悬液的制备:将白色念珠菌接种到沙氏葡萄糖液体培养基中,23℃培养2 d,取该培养物适量,余下配制方法同上述Ⅱ的操作。大肠埃希菌菌悬液的制备:将大肠埃希菌接种到胰酪大豆胨液体培养基中,33℃培养20 h,取该培养物适量,余下配制方法同上述Ⅱ的操作。沙门菌菌悬液的制备:将沙门菌接种到胰酪大豆胨液体培养基中,33℃培养20 h,取该培养物适量,余下配制方法同上述Ⅱ的操作。
2.2 供试液的制备与稀释取样品1号、2号、3号,各称取10 g分别置于3个匀浆杯中,各加胰酪大豆胨液体培养基100 ml作为稀释液,混匀,制成稀释浓度为1∶10溶液。取上述溶液适量,分别用胰酪大豆胨液体培养基分步稀释,将三批样品均依次制成1∶50、1∶100、1∶1000的供试液备用。
2.3 微生物回收试验用供试液的制备试验组:取2.2项制备的三批样品的4个不同浓度供试液各100 ml,加入2.1项配制的相关菌液各1 ml,混匀备用。供试品对照组:取2.2项制备的三批样品的4个不同浓度供试液各100 ml,加入稀释液代替菌液,与试验组平行操作,混匀备用。菌液对照组:取稀释液各100 ml代替供试品,分别加入2.1项配制的相关菌液各1 ml,与试验组平行操作,混匀备用。
2.4 供试品中微生物回收(平皿-倾注法)取2.3项制备的三批样品的试验组、供试品对照组、菌液对照组各2 ml,注入2个平皿,一个平皿1 ml,倾注相应的培养基(温度不超过45℃),摇匀,待凝固后倒置在培养箱中培养。培养条件:胰酪大豆胨琼脂培养基平板为33℃培养3 d,沙氏葡萄糖琼脂培养基平板为23℃培养5 d。观察,计数。
2.5 计算回收比值计算方法:试验组的平均菌落数减去供试品对照组的平均菌落数,所得差值除以菌液对照组的平均菌落数。见表1、表2。

表1 需氧菌验证回收率

表2 霉菌和酵母菌验证回收率
2.6 计数方法的确立根据规定,比值应在0.5~2 范围内[3]。观察表1:三批样品均是稀释级别为1∶100时,胰酪大豆胨琼脂培养基平板上培养的5种试验菌株的回收率都符合规定;观察表2:稀释级别在1∶10时,沙氏葡萄糖琼脂培养基平板上培养的2种菌株的回收率都符合规定。所以健脾补血颗粒需氧菌总数计数检查是应选择最低稀释级别为1∶100的平皿倾注法;而霉菌和酵母菌总数计数检查则宜选取最低稀释级别为1∶10的供试液的平皿倾注法。
2.7 控制菌检验方法适应性试验
2.7.1 大肠埃希菌实验步骤以一批样品叙述,其余两批同法试验(下同)。取2.2中制备的1∶10的供试液30 ml,分别接种至3份各含100 ml胰酪大豆胨液体培养基的三角瓶中,每瓶10 ml供试液。其中瓶1加入2.1中制备的大肠埃希菌菌悬液1 ml,作为试验组;瓶2加入2.1中制备的金黄色葡萄球菌菌悬液1 ml,作为阴性菌对照组;瓶3为供试品组。将上述培养液混匀,33℃培养20 h后,分别将上述培养物接种至100 ml麦康凯液体培养基中,接种量为1 ml。43℃培养30 h后,将麦康凯液体培养基的培养物用接种环划线接种在麦康凯琼脂培养基平板上,33℃培养68 h,观察,根据上述3组对应平板的菌落生长情况,判断该法是否可行。
2.7.2 耐胆盐革兰阴性菌取2.2中制备的1∶10的供试液10 ml,置23℃培养2 h,使其中的细菌充分恢复。取供试液4 ml,分别接种至4支盛有10 ml肠道菌增菌液体培养基的试管中,每支1 ml供试液,其中管1加入2.1中制备的大肠埃希菌菌悬液1 ml作为试验组a;管2加入2.1中制备的铜绿假单胞菌菌悬液1 ml为试验组b;管3加入2.1中制备的金黄色葡萄球菌菌悬液1 ml为阴性菌对照组;管4为供试品组。将4管置33℃培养38 h,然后划线接种在紫红胆盐葡萄糖琼脂培养基上,置33℃培养22 h。观察,根据4组对应平板上菌落生长情况,判断该法是否可行。
2.7.3 沙门菌取样品30 g,分别接种于3瓶含胰酪大豆胨液体培养基100 ml的三角瓶中,每瓶样品10 g,混匀,其中瓶1加入2.1中制备的沙门菌菌悬液1 ml作为试验组;瓶2加入2.1中制备的金黄色葡萄球菌菌悬液为阴性菌对照组;瓶3为供试品组。将各组混匀,33℃培养22 h。将3组培养物各取0.1 ml,分别接种至含10 ml RV沙门增菌液体培养基的试管中,33℃培养22 h。取RV沙门菌增菌液体培养物用接种环接种于木糖赖氨酸脱氧胆酸盐琼脂培养基平板之上,置33℃培养45 h。观察,根据3组对应平板上的菌落生长情况,判断该法是否可行。
2.7.4 大肠埃希菌试验结果三批样品中:加入阳性菌的试验组经过培养,平板上均有菌生长,且经鉴定,该菌即为所加阳性菌;而加入阴性对照菌的一组和供试品一组经培养,平板上均未见有菌生长,说明本次试验建立的常规法对大肠埃希菌的选择性很好,此法可行,可用于该项目的检验。见表3。

表3 大肠埃希菌试验结果
2.7.5 耐胆盐革兰阴性菌试验结果3批样品中,加入阳性菌的2个试验组a、b经过培养,平板上均有菌生长,且经鉴定,该菌即为所加阳性菌;而加入阴性对照菌的一组和供试品一组经培养,平板上均未见有菌生长,说明本次试验建立的常规法对大肠埃希菌和铜绿假单胞菌的选择性都良好,此法可行,可用于该项目的检验。见表4。

表4 耐胆盐革兰阴性菌试验结果
2.7.6 沙门菌试验结果三批样品中:加入阳性菌的试验组经过培养,平板上均有菌生长,且经鉴定,该菌即为所加阳性菌;而加入阴性对照菌的一组和供试品一组经培养,平板上均未见有菌生长,说明本次试验建立的常规法对沙门菌的选择性很好,此法可行,可用于该项目的检验。见表5。
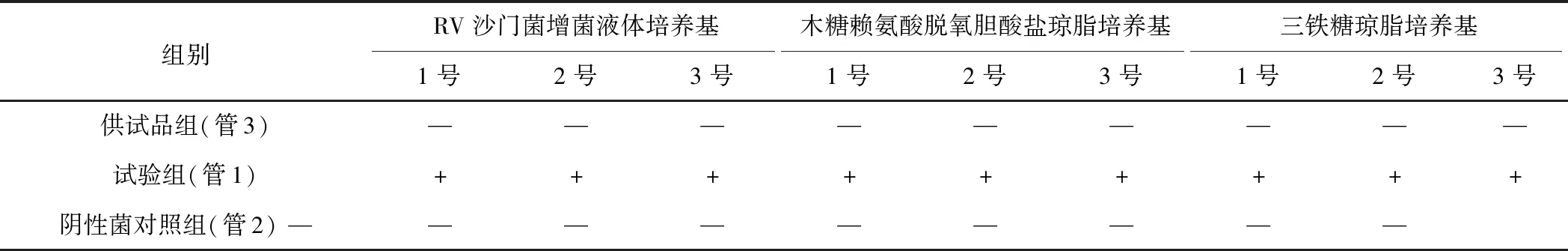
表5 沙门菌试验结果
3 讨论
微生物限度检查法是从《中华人民共和国药典》2005年版开始引入方法验证试验[4],方法验证的提出,使检验更有逻辑性,也使检验结果更加真实可靠。近十几年来,中国药典委员会不断对方法验证的实验体系进行改进、完善,相对于前版来说,现行《药典》在非无菌产品微生物限度检查部分,变动较大,为了确保检验结果的准确性,检验方法都需要重新验证[5]。
本样品是颗粒剂,通常颗粒剂是经过提取,检验时相对来说影响因素较少,干扰因素也少,可本样品不同,为了使菌落能更好的生长,本文选择了胰酪大豆胨液体培养基作为稀释液[6]。
为了更方便计数,检查需氧菌总数计数时可以用陶瓦盖代替平皿的玻璃盖[7]。
本版《药典》在控制菌检查方法适用性试验中首次提出了阴性菌对照,同供试品检查方法中的阴性对照不同,阴性对照菌更加体现了培养体系的专属性,也使检验结果更加准确、可靠[8]。
