[Ru(bpy)2dppz]2+的合成及其与DNA的相互作用研究
2019-04-09梁霞霞黄荣富
梁霞霞,周 兵,黄荣富
(成都理工大学材料与化学化工学院,四川 成都 610059)
0 前言
钌配合物是具有丰富的光化学、光物理和电化学等性质,因此,可用作DNA的结构探针。例如,Δ-Ru (phen)32+作为 B-DNA 结构探针, 用于DNA 结构的研究[1];此外,[Ru(bpy)2dppz]2+和[Ru(phen)2dppz]2+,因具有刚性、共平面的电子共轭体系,与DNA结合力强,能插入DNA碱基对之间[2-4]。同时,[Ru(bpy)2dppz]2+及其衍生配合物作为核酸探针还具有无毒、性质稳定、灵敏度高、选择性好、使用方便等优点。在金属抗癌药物方面,[Ru(bpy)2dppz]2+及其衍生物具有较高的抗肿瘤活性,并将其大量用于临床研究之中[5-7]。荧光光谱是一种光致发光方法,是研究小分子与DNA之间作用方式的方法之一,它是一种比较灵敏的分析方法。 本文通过两步反应合成了[Ru(bpy)2dppz]2+,并分别用紫外-可见吸收光谱法、核磁共振和质谱对Ru-dppz进行结构表征,利用荧光法考察了Ru-dppz与双链DNA(dsDNA)的相互作用。
1 实验部分
1.1 仪器及试剂
F-4600荧光光谱仪(日立),UV-2700紫外分光光度计 (日本岛津公司),LC/MSD-VL液质联用仪(安捷伦公司);邻苯二胺、1,10-邻菲罗啉-5,6-二酮、二水合顺-双(2,2’-二吡啶基)二氯化钌([Ru(bpy)2]Cl2·2H2O)(购自上海阿拉丁)、小牛胸腺DNA(Calbiochem,德国)、其它化学试剂均购自于成都科隆化学试剂公司。所有试剂均属分析纯无需进一步纯化。
1.2 Ru-dppz的合成
分别称取0.4997 g邻苯二胺、0.4998 g 1,10-邻菲罗啉-5,6-二酮置于烧杯中,加入适量乙醇(约30 mL)微热使其完全溶解,将邻苯二胺溶液缓慢加入到 1,10-邻菲罗啉-5,6-二酮溶液中,边加入边搅拌,然后在温水浴中加热至沸腾,保持沸腾5 min;在冰水浴中冷却结晶(红棕色),过滤后再重结晶得到棕黄色针状产物(Dppz)。
称取0.4852 g顺-双(2,2'-二吡啶基)二氯化钌 (II)与上步制备的配体0.2913 g于250 mL锥形瓶中,加入120 mL甲醇和水的混合溶剂(V水∶V甲醇=2∶1)溶解。在恒温磁力搅拌器上恒温加热并搅拌回流4.5 h,得到深红色溶液,保持恒温蒸发至15 mL,加入45 mL蒸馏水,继续煮沸10 min。将溶液在冰水浴中冷却沉淀,过滤沉淀。在滤液中加入10 mL 10%的氟硼酸钠溶液以沉淀合成的[Ru(bpy)2dppz]2+,过滤得到红棕色粗产物[Ru(bpy)2dppz](BF4)2沉淀。 将所合成的粗产物于30 mL 80%的乙醇中微热溶解,并于水浴中冷却结晶,过滤得深红色粉末状沉淀,以此方法再次重结晶以提纯产物而获得终产物。
2 结果与讨论
2.1 Ru-dppz的合成
Ru-dppz的合成可以通过两步反应制得:首先,1,10-邻菲罗啉-5,6-二酮与邻苯二胺反应制备联吡啶体配合物二吡啶[3,2-a;2',3'-c]吩嗪(Dppz);第一步的产物 Dppz再与顺-双(2,2'-二吡啶基)二氯化钌(II)二水合物(Ru (bpy)2Cl2)反应制备二联吡啶二吡啶[3,2-a;2',3'-c]吩嗪钌(Ru-dppz)。反应方程式如图1所示。
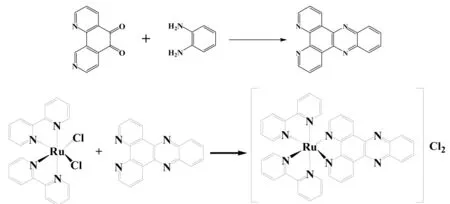
图1 Ru-dppz的合成途径
2.2 Ru-dppz的核磁共振谱(NMR)
首先,将所合成的产物使用核磁共振进行表征,结果如图2所示:δ=8.033~8.313的两组多重峰为 (2,7,10,11,12,13 位质子峰),δ=9.284~9.300 的二重峰为(1,8 位质子峰),δ=9.758~9.778的二重峰为 (3,6 位质子峰),δH(CD3CN),7.28(2H,td,J=1.2,6.4 Hz),7.49(2H,td,J=1.2,6.0 Hz),7.75(2H,d,J=5.2 Hz),7.88(2H,d,J=4.8 Hz),7.91(2H,dd,J=6.0,8.0 Hz),8.04 (2H,td,J=1.2,7.6~8.4 Hz),8.12~8.20(6H,多重重叠),8.50(2H,dd,J=3.6,6.4 Hz),8.56 (4H,dd,J=8.4,13.2 Hz),9.69(2H,dd,J=1.2,8.4 Hz)。 表征结果与文献值一致[8-10]。
2.3 Ru-dppz的紫外-可见吸收光谱图
我们研究了Ru-dppz的紫外-可见吸收光谱,如图(3)所示,Ru-dppz在 281 nm、368 nm、440 nm分别出现3个吸收峰,与所参考文献紫外吸收谱图的吸收峰一致[11]。
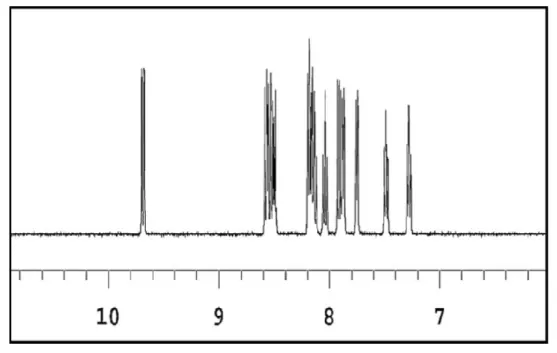
图2 Ru-dppz核磁共振氢谱图(溶剂为CD3CN)
此外,我们还利用质谱测得Ru-dppz的质荷比(m/z)为 346,与我们理论计算的[Ru(bpy)2dppz]2+的质荷比一致。综合这三种方法的表征结果,由Ru-dppz的紫外可见光吸收谱图中出现的3个特征吸收峰,核磁共振氢谱图的解析,以及质谱所得其分子量信息,证明成功合成了Ru-dppz。
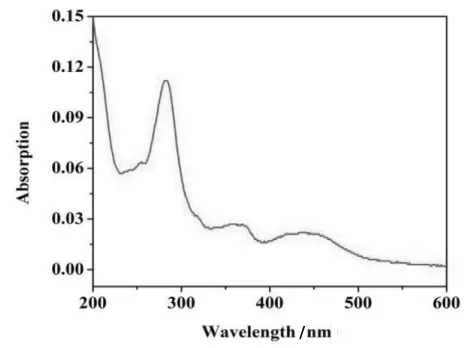
图3 Ru-dppz的紫外可见吸收光谱图
2.4 Ru-dppz的荧光特性研究
2.4.1 Ru-dppz的“光开关”行为研究
从谱图(图4)可知最大发射波长在615 nm左右,并且荧光强度随着dsDNA的浓度增加而增强。根据荧光性质的研究可以得出结论,本实验合成的产物Ru-dppz具有荧“光开关”分子的性质,即单独的Ru-dppz荧光信号很微弱,当与ds-DNA相互作用以后产生强烈的荧光。
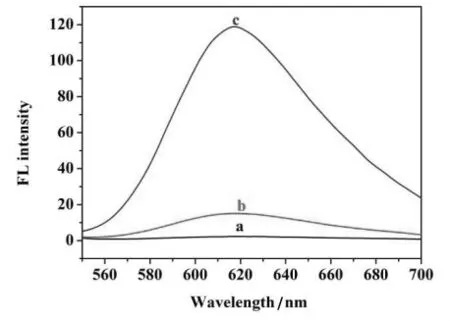
图4 10 μmol/L 的 Ru-dppz(a)在加入 10 μg/mL(b)和 100 μg/mL(c)的 dsDNA 前后的荧光光谱图(激发波长:460 nm)
2.4.2 Ru-dppz与dsDNA的相互作用研究
图5是Ru-dppz与dsDNA的荧光滴定曲线。从图5可以看出,初始阶段荧光强度随着Rudppz浓度的增加而增加,最后趋于饱和达到平台。以荧光强度增加部分拟合一条直线,其斜率为K1=2.8461×108。将拐点处的点分别计算binding值,b=信号/K1,在分别用该拐点Ru-dppz的实际浓度减去binding值,以Free表示。然后以b对b/Free作直线,可以得到一条斜率K2=-6.7953×10-8的直线L2,对K2求负倒数即为Ru-dppz的结合常数。带入斜率K2,计算得到结合常数K=1.5×107L/mol。
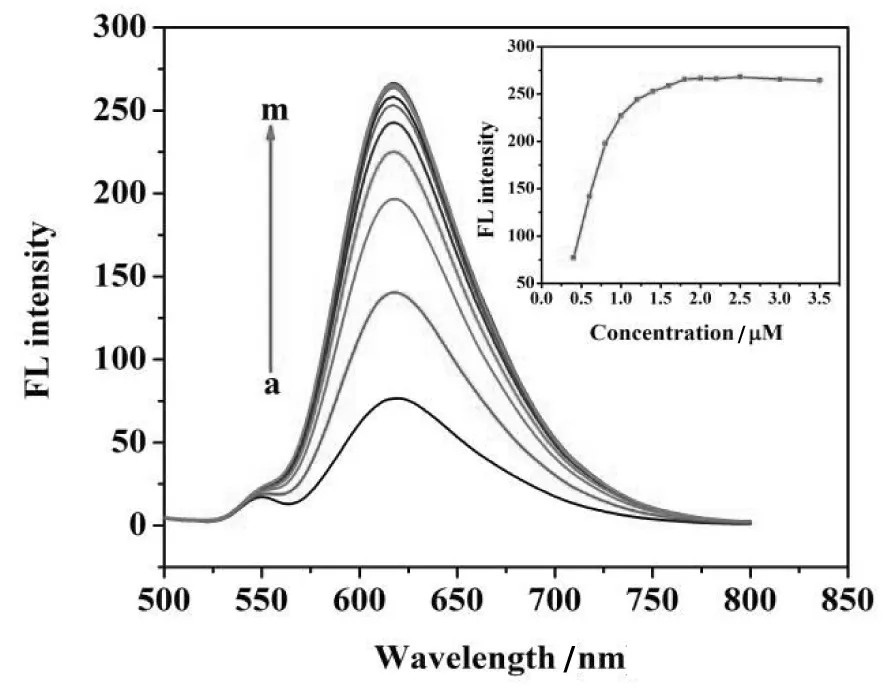
图5 不同浓度Ru-dppz与 dsDNA(5.1 μg/mL)相互作用后的荧光谱图(a至m浓度依次为0.430、0.644、0.854、1.064、1.274、1.484、1.694、1.904、2.114、2.324、2.639、3.164、3.689 μmol/L)激发波长:460 nm)。插图为对应的Ru-dppz的浓度信号曲线。
由Ru-dppz的浓度曲线图可以获得在荧光强度达平台后的平均荧光强度为266.2,直线L1与平台的交点所对应的浓度为Ru-dppz与小牛胸腺DNA的最大结合浓度,即将平台信号266.2带入L1计算获得浓度Cmax=1.09×10-6mol/L。且dsDNA的校正浓度按每个碱基对的平均分子量为 325,则换算为碱基的摩尔浓度为C碱基=15.69 μmol/L。则该结合比 CRu-dppz:C碱基=0.07,染料与碱基对之比为0.14,即 7.14个碱基对结合1个Ru-dppz分子。
3 结论
本文通过两步反应合成了 “光开关”分子,Ru-dppz,并通过三种不同的方法表征了本物质的结构。产物的紫外-可见吸收光谱、核磁共振氢谱和质谱表征结果与理论结果一致,说明实验中成功合成Ru-dppz。Ru-dppz与dsDNA相互作用研究表明,Ru-dppz与dsDNA结合后,荧光信号得到恢复。通过荧光滴定实验,测得Ru-dppz与dsDNA的结合常数为1.5×107L/mol,染料与碱基对之间的结合比为0.14。
