N-(3-(2-呋喃基)丙烯酰基)苯丙氨酸的合成
2019-01-25黄朋勉陈金星熊前政郑晓斌周智慧王梓鉴吕彦博周胜
黄朋勉,陈金星,熊前政,郑晓斌,周智慧,王梓鉴,吕彦博,周胜
(1.长沙理工大学化学与生物工程学院,湖南 长沙 410114;2.湖南斯派克科技股份有限公司,湖南 长沙,410000;3.连云港笃翔化工有限公司,江苏 连云港,223500)
心血管疾病是人类身体健康的第一大杀手,因此检测治疗心血管疾病具有重大的社会意义和经济价值。N-[3-(2-呋喃基)丙烯酰]-L苯丙氨酰-甘氨酰-甘氨酸(FAPGG)广泛应用于检测血管紧张素转换酶(ACE)的活性[1],具有灵敏、快速、重复性好等突出特点[2-3],是测定ACE活性不可或缺的手段[4]。另外,FAPGG也广泛应用于肺部[5-6]、肝脏、肾脏和甲状腺等疾病的诊断[7-9],因此FAPGG的制备工艺研究意义重大。N-(3-(2-呋喃基)丙烯酰基)苯丙氨酸(FA-PHE-OH)是合成FAPGG的关键中间体,其质量与成本对FAPGG的质量和成本具有重要影响。
目前国内外制备FA-PHE-OH的研究报道很少。其中Jean等[10]以2-呋喃丙烯酸为原料,BOP为缩合剂,经过酰基化反应和水解反应,二步反应得到产物,纯度低,收率仅为51.9%,该合成路线具有原料成本高的不足。
本文设计新的工艺路线,以糠醛、丙二酸、L-苯丙氨酸为起始原料,经过Knoevenagel反应、甲酯化反应、酰基化反应和水解反应得FA-PHE-OH,纯度99.5%,总收率为80.2%,较文献报道收率提高54.5%。本工艺具有原材料易得,操作简单,收率和纯度高,是一条适合工业化的路线。
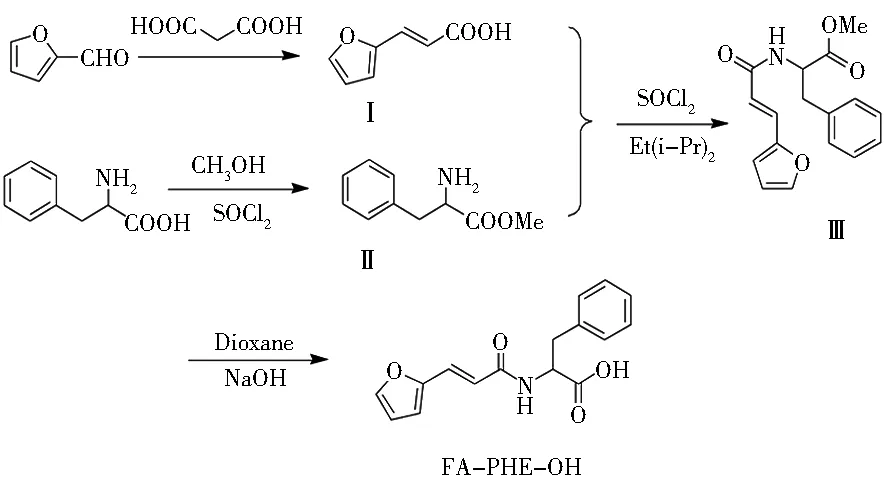
图1 FA-PHE-OH的制备工艺路线
1 实验部分
1.1 试剂与仪器
糠醛(99%),天津市大茂化学试剂厂;丙二酸(98%),西陇科学股份有限公司;L-苯丙氨酸(98.5%)、N,N-二异丙基乙胺(99%)、BOP(99%),苏州亚科科技股份有限公司;二氯亚砜(99.5%),无锡海伦生物科技有限公司。
SPD-20A高效液相色谱仪,日本岛津公司;WRS-1B数字熔点仪,上海精科;DZ-1BC真空干燥箱,天津市泰斯特仪器有限公司;Avance Ⅲ 核磁共振仪(500 MHz),布鲁克(北京)科技有限公司。
1.2 实验步骤
1.2.12-呋喃丙烯酸(Ⅰ)的合成
分别向干燥洁净的250 mL三口烧瓶中加入9.6 g(0.1 mol)新蒸糠醛、12.5 g(0.12 mol)丙二酸和15.8 g(0.2 mol)吡啶,在氮气氛围搅拌,加热至95 ℃回流反应4 h,降至室温,加20 mL去离子水搅拌15 min,用1 mol/L NaOH溶液调pH至10,过滤收集滤液,用5 mol/L HCl调pH至3,析出白色固体,过滤得Ⅰ,真空干燥得到12.5 g白色Ⅰ。含量(HPLC)98.8%,收率90.6%,m.p.140.2~142.6 ℃(文献值[11]:139~141 ℃)。1H NMR(500 MHz,CDCl3),δ:7.51(t,J=12.0,3.5 Hz,2H),6.66(d,J=3.0 Hz,1H), 6.48(dd,J=3.0,1.5 Hz,1H),6.30(d,J=15.5 Hz,1H)。
1.2.2L-苯丙氨酸甲酯盐酸盐(Ⅱ)的合成
向干燥洁净的250 mL三口烧瓶中加入10 g(0.06 mol)L-苯丙氨酸,36 g(1.13 mol)无水甲醇,置于低温浴(-5 ℃)搅拌,缓慢滴加13 g(0.11 mol)的二氯亚砜,滴完后自然升至室温,搅拌反应20 h,旋蒸除去溶剂,过滤得白色固体,真空干燥得到12.4 g白色Ⅱ,收率96.1%,m.p.156.4~158.1 ℃(文献值[12]:155~157 ℃)。1H NMR(500 MHz,D2O),δ:7.46~7.30(m,5H),4.46~4.43(m,1H),3.85(s,3H),3.38~3.22(m,2H)。
1.2.33-(2-呋喃基)丙烯酰基-L-苯丙氨酸甲酯(Ⅲ)的合成
依次向干燥洁净的250 mL三口烧瓶加入6.9 g(0.05 mol)Ⅰ,40 mL CH2Cl2,5 ℃搅拌,缓慢滴加7.1 g(0.06 mol)的SOCl2,自然升至室温,40 ℃回流反应5 h,旋蒸除溶剂得到反应液1;向另一个250 mL的三口烧瓶中依次加入12.9 g(0.06 mol)Ⅱ,20 mL CH2Cl2,5 ℃搅拌,缓慢滴加7.7 g(0.06 mol)二异丙基乙胺,得到反应液2。-5 ℃搅拌下,将反应液2缓慢滴加到反应液1中,自然升至室温,反应10 h,除溶剂,得到油状物,依次加入15 mL乙酸乙酯和10 mL去离子水,分别用1 mol/L盐酸、20%碳酸钠和饱和食盐水洗涤,旋蒸除溶剂,过滤得白色固体,真空干燥得到14.6 g白色Ⅲ。含量99.2%,收率97.3%,m.p.108.6~110.5 ℃(文献值[13]:109 ℃)。1H NMR(500 MHz,CDCl3),δ:7.44~7.12(m,7H),6.56(d,J=3.5 Hz,1H),6.45(dd,J=3.0,1.5 Hz,1H),6.31(d,J=15 Hz,1H),6.13(d,J=7.5 Hz,1H),5.03(dd,J=13.5,6.0 Hz,1H),3.76(s,3H),3.26~3.16(m,2H).13C NMR(500 MHz,CDCl3),δ:172.02,165.23,151.18,144.15,135.86,129.32,128.59,127.14,117.68,114.11,112.18, 53.34,52.35,37.95。
1.2.4N-(3-(2-呋喃基)丙烯酰基)苯丙氨酸(FA-PHE-OH)的合成
依次向干燥洁净的100 mL的三口烧瓶加入3 g(0.01 mol)Ⅲ,5 mL去离子水和20 mL二氧六环,搅拌溶解,5 ℃下用1 mol/L氢氧化钠调pH至10,室温反应12 h,旋蒸除溶剂,用去离子水和CH2Cl2萃取,得水相,5 ℃下用2 mol/L盐酸调pH至4,析出固体,过滤、真空干燥得2.7 g白色FA-PHE-OH。含量99.5%,收率94.7%。m.p.206.2~208.1 ℃(文献值[10]:206 ℃)。1H NMR(500 MHz,CDCl3),δ:7.39~7.16(m,7H),6.52~6.28(m,4H),4.96(dd,J=15.0,5.0 Hz,1H),3.29~3.14(m,2H).13C NMR(500 MHz,CDCl3),δ:174.47,166.47,151.03,144.34,135.90,129.41,129.01,128.62,127.11,117.23,114.58,112.25,53.78,37.34。
2 结果与讨论
2.1 2-呋喃丙烯酸(Ⅰ)的制备
2.1.1原料摩尔比对2-呋喃丙烯酸收率的影响
为提高产物的收率,常采用反应物之一过量的方法。若选用糠醛过量,存在以下问题:1)过量的糠醛易被氧化,生成糠酸副产物;2)过量的糠醛,可以和Ⅰ上的羧基继续缩合,生成副产物;3)过量的糠醛在高温下可开环聚合,生成带有颜色的高聚物。而选用丙二酸过量可以避免这些问题,并且提高糠醛的转化率。本工艺重点考察了原料摩尔比对Ⅰ收率的影响,结果见表1。由表1可知,当n(糠醛)∶n(丙二酸)=1∶1.2时,Ⅰ的收率最高为90.6%。

表1 原料摩尔比对Ⅰ收率的影响
2.1.2反应温度对2-呋喃丙烯酸收率、颜色的影响
温度是决定Ⅰ颜色变化的主要因素,酸性条件下,温度升高会导致产品聚合,颜色加深,会使后续产品Ⅲ和FA-PHE-OH的颜色加深,增加产品的提纯难度和降低产品的收率,因此,本工艺重点考察了温度对Ⅰ收率和颜色的影响。结果见表2。

表2 反应温度对Ⅰ收率和颜色的影响
由表2可知,当反应温度为95 ℃时,收率和颜色最佳。当温度低于95 ℃时,缩合反应不完全,且由于糠醛过量,会被氧化生成糠酸和黑色的糠醛开环聚合杂质[14],导致产品收率低,提纯难度大。
2.1.3反应时间对2-呋喃丙烯酸收率的影响
以吡啶为溶剂,反应温度95 ℃,n(糠醛)∶n(丙二酸)=1∶1.2,氮气氛围保护,考察反应时间对Ⅰ收率的影响,结果见表3。

表3 反应时间对Ⅰ收率的影响
由表3可知,糠醛和丙二酸的Knoevenagel反应,前期反应速度快,反应2 h,收率超过70%;而后反应速度逐渐减缓,反应时间为5 h时,Ⅰ的收率最高;在延长反应时间,收率反而有所下降,这可能是由于Ⅰ的结构不稳定,长时间在高温下有部分聚合导致的。
2.2 3-(2-呋喃基)丙烯酰基-L-苯丙氨酸甲酯(Ⅲ)的制备
2.2.1原料摩尔比对3-(2-呋喃基)丙烯酰基-L-苯丙氨酸甲酯收率的影响
Ⅰ先用二氯亚砜制备成酰氯,然后采用一锅法制备Ⅲ。选用Ⅱ过量以提高酰氯的转化率,该工艺有以下优点:1)减少酰氯的副反应,提高Ⅲ的收率;2)一锅法操作简单,收率高。本工艺重点考察Ⅰ与Ⅱ的摩尔比对产品Ⅲ收率的影响,结果见表4。
由表4可知,当n(Ⅰ)∶n(Ⅱ)低于1∶1.2时,收率随摩尔比的增大而增加,原因是Ⅱ用量的增加使Ⅰ的转化率提高;当n(Ⅰ)∶n(Ⅱ)为1∶1.2时,Ⅲ收率最高;当n(Ⅰ)∶n(Ⅱ)大于1∶1.2时,收率随着摩尔比的增大而降低,原因是Ⅱ过多会导致二异丙基乙胺用量增加,使其在反应体系中以二异丙基乙胺盐酸盐的形式存在,不利于发生酰基化反应,并加大了产品的精制难度。
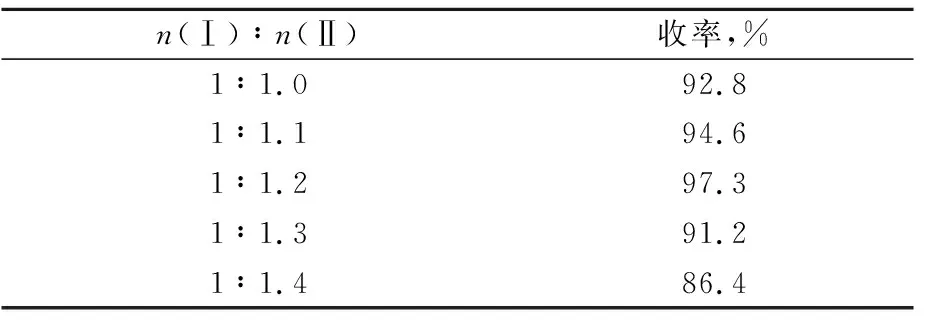
表4 原料摩尔比比对Ⅲ收率的影响
2.2.2反应温度对3-(2-呋喃基)丙烯酰基-L-苯丙氨酸甲酯收率的影响
本工艺采用一锅法制备Ⅲ。由于酰基化反应是放热反应,为保证产品质量,要控制反应温度,所以本工艺重点考察了反应温度对Ⅲ收率的影响,结果见表5。
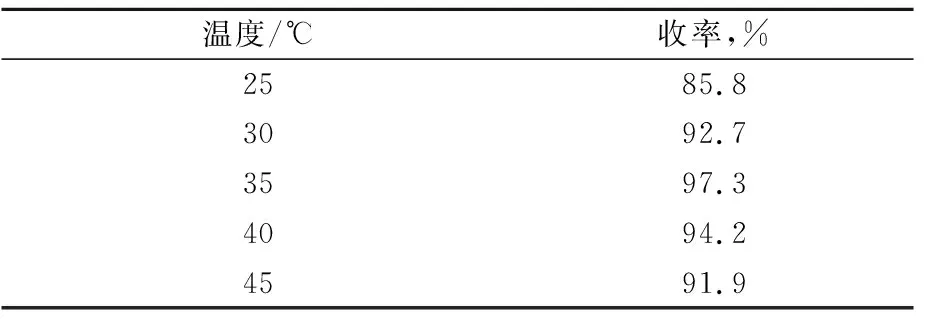
表5 反应温度对Ⅲ收率的影响
由表5可知,当反应温度低于35 ℃时,收率随温度的升高而增加;当反应温度高于35 ℃时,收率随温度的升高而降低,原因可能是,温度过高酰氯易分解,且Ⅱ上的氮原子被氧化,导致产品颜色深及收率降低。
2.2.3反应时间对3-(2-呋喃基)丙烯酰基-L-苯丙氨酸甲酯收率的影响
本工艺采用一锅法制备Ⅲ,重点考察了反应时间对Ⅲ收率的影响,结果见表6。
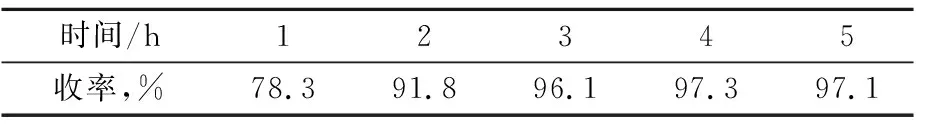
表6 反应时间对Ⅲ收率的影响
由表6可知,反应1 h,反应物有78.3%转化为产物,是因为酰氯活性高,导致反应速度快;反应时间为4 h时,Ⅲ收率最大;在延长反应时间,收率基本上保持不变,故最佳反应时间为4 h。
2.2.4缩合剂对3-(2-呋喃基)丙烯酰基-L-苯丙氨酸甲酯收率的影响
文献报道[10]BOP缩合剂是一锅法制备Ⅲ的关键因素之一,但考虑到BOP成本高,且收率偏低,本工艺设计先与SOCl2反应制备酰氯,再缩合,考察二者的收率和产品质量,结果见表7。

表7 缩合剂对Ⅲ收率的影响
由表7可知,将Ⅰ与SOCl2反应制备酰氯,在不用BOP缩合剂的条件下,与Ⅱ反应得到Ⅲ,收率高达97.3%,收率大幅增加76.6%,增幅明显,而且产品质量好,取得大的突破。具体体现为:1)把Ⅰ用SOCl2制备成酰氯,与Ⅱ缩合得到Ⅲ,收率高,条件温和;2)SOCl2成本低,收率高;3)过量的SOCl2挥发,易除去。目前,文献报道Ⅲ的合成研究,都是以BOP为缩合剂,收率仅为59%,且BOP不适用于有空间位阻多肽的合成,在活化羧基的过程中会产生有毒致癌物质六甲基磷酰亚胺[15],故选用SOCl2为缩合剂。
3 结 论
a.以糠醛和丙二酸为原料,经过Knoevenagel、甲酯化、酰基化及水解反应新路线制备FA-PHE-OH,总收率为80.2%,纯度为99.5%。该工艺具有产品质量好,收率高,成本低的优势。
b.酰基化反应以SOCl2代替BOP制备3-(2-呋喃基)丙烯酰基-L-苯丙氨酸甲酯,收率提高76.6%,且成本大幅降低。
c.合成2-呋喃丙烯酸的最佳条件为:反应温度95 ℃,反应时间5 h,n(糠醛)∶n(丙二酸)=1∶1.2。
d.合成3-(2-呋喃基)丙烯酰基-L-苯丙氨酸甲酯最佳条件为:反应温度35 ℃,反应时间4 h,n(2-呋喃丙烯酸)∶n(L-苯丙氨酸甲酯盐酸盐)=1∶1.2。
