瑞舒伐他汀对75岁及以上高龄老人肾功能的影响
2018-11-23邓慧戴阳陆昊王春
邓慧 戴阳 陆昊 王春
动脉粥样硬化性心血管疾病(ASCVD)是老年人群患病率最高的疾病,他汀类药物作为治疗ASCVD的基础用药,随着我国老龄化进展,应用人群将十分庞大。目前,瑞舒伐他汀是我国用量最多的他汀类药物之一,从其上市一直延续至今的争议是对肾脏功能包括肾小球滤过率(GFR)与蛋白尿的影响。老年人群慢性肾脏病(CKD)患病率高,且即使未合并CKD,肾脏结构已发生了衰老性结构改变,结构的异常使得衰老的肾脏更易受外界因素的影响[1]。有研究表明,在年龄>75岁的老年人中,47%的老年人日常用药超过5种[2]。因此,该类人群在治疗基础疾病的同时,选择具备肾脏安全性的他汀类药物非常重要。而瑞舒伐他汀在≥75岁高龄老人中应用时肾脏安全性的相关研究较少,且对肾脏功能评估时多采用血肌酐、尿微量白蛋白,评价指标少。因此,本研究选取≥75岁高龄老人作为观察对象,联合多项肾脏功能指标进行评估,以期更全面地反映瑞舒伐他汀在该类人群中应用的肾脏安全性。
1 对象与方法
1.1 研究对象 选择2014年12月至2016年12月我院老年科住院的病人16例,其中男14例,女2例,年龄75~94岁,平均(85.31±6.23)岁,病人均合并颈动脉粥样硬化,有他汀治疗的适应证。纳入标准:(1)年龄≥75岁;(2)已应用阿托伐他汀(立普妥)治疗至少8周。排除标准:(1)不能正常进食、活动者;(2)CKD Ⅲ期及以上的病人;(3)急性炎症期病人;(4)服用血管紧张素转化酶抑制剂、血管紧张素Ⅱ受体阻滞剂、利尿剂<3个月;(5)心功能Ⅳ期病人;(6)休克与重症病人;(7)肝脏转氨酶明显升高2倍及以上;(8)患自身免疫系统疾病;(9)正在服用各类肾毒性药物;(10)双侧肾脏占位、肾脏结石病变。
1.2 研究方法 根据瑞舒伐他汀与阿托伐他汀临床降脂疗效关系,将阿托伐他汀等作用剂量调整为瑞舒伐他汀(20 mg阿托伐他汀=10 mg瑞舒伐他汀),保持其他治疗方案不变。于入组时及瑞舒伐他汀治疗1周后分别采集病人的血液、尿液样本并进行指标检测,收集病人的基本临床资料及一般实验室检查结果。应用99mTc-DTPA 肾动态显像法(ECT)检测GFR水平,以评估病人肾小球滤过功能。估算的肾小球滤过率(eGFR)应用我国人群肾脏病膳食改善研究校正方程 (MDRD) 简化公式eGFR[mL/(min·1.73 m2)]=175×血肌酐-1.234×年龄-0.179×0.79(女性)估算[3]
1.3 检测指标
1.3.1 一般实验室检查指标:(1)肝功能:丙氨酸氨基转移酶(ALT)、天冬氨酸氨基转移酶(AST)、总胆红素(TB)、白蛋白(ALB);(2)肌酶:肌酸激酶(CK)、肌酸激酶同工酶(CK-MB);(3)血糖与甲状腺功能:糖化血红蛋白(HbA1c)、空腹血糖(FPG)、促甲状腺激素(TSH)、血清游离三碘甲状腺素原氨酸(FT3)、血清游离甲状腺素(FT4);(4)血脂:低密度脂蛋白胆固醇(LDL-C)、高密度脂蛋白胆固醇(HDL-C)、载脂蛋白A(ApoA)、载脂蛋白B(ApoB)。
1.3.2 肾脏相关指标:(1)肾小管重吸收指标:血尿素氮(BUN)、血肌酐、尿微量白蛋白、尿微量白蛋白/肌酐、尿N-乙酰-β-D-氨基葡萄糖苷酶(NAG);(2)反映肾脏损害的新型生物标志物:收集所有研究对象晨起清洁中段尿10 mL,于4 ℃、3000 r/min离心5 min,取上清液5 mL,储于-80 ℃冰箱冻存备用。采用酶联免疫吸附(ELISA)法检测尿肾损伤分子-1(KIM-1)、尿白细胞介素-18(IL-18)、尿转化生长因子-β1(TGF-β1),试剂盒均购自优宁维公司,严格按照试剂盒说明进行操作,正常值参考说明书。

2 结果
2.1 基本临床资料 16例病人中,8例合并2型糖尿病,2例有糖耐量减退,14例有高血压病史;收缩压(126±18)mmHg,舒张压(66±11)mmHg;心率(73±10)次/min;病人的eGFR均>60 mL/min;通过ECT检测GFR水平为(62±12)mL/min。HbA1c水平为(6.02±0.70)%、TSH水平为(3.04±1.50) mIU/L、FT3水平为(3.93±0.72) pmol/L、FT4水平为(16.14±2.65) pmol/L。
2.2 调药前后一般实验室检查结果比较 病人在调整为瑞舒伐他汀治疗后1周,LDL-C水平显著降低(P<0.05),其他实验室一般检查指标变化差异均无统计学意义(P>0.05)。见表1。
2.3 调药前后肾脏相关检查结果比较 经wilcoxon等级检验,病人调药前后肾脏相关检查指标变化差异均无统计学意义(P>0.05)。见表2。
3 讨论
他汀类药物具有减轻肾脏血管动脉粥样硬化、抗炎、改善内皮细胞功能障碍以及延缓肾小管间质纤维化、改善肾脏预后的作用[4-6]。但是,瑞舒伐他汀(80 mg)最初因为显著增加蛋白尿,而未被食品药品监督管理局批准上市。因此,瑞舒伐他汀是否会导致肾脏损害引起了大家的关注。一项将瑞舒伐他汀与安慰剂对肾脏终点事件(AEs)比较的Meta分析、两项与安慰剂比较的研究以及一项40 mg与10 mg瑞舒伐他汀比较的研究均显示,瑞舒伐他汀未改善AEs;且在eGFR<60 mL/min的人群中,瑞舒伐他汀组AEs发生率较安慰剂组有增加的趋势[7]。对合并进展性肾病(eGFR<60 mL/min)的病人进行蛋白尿与GFR的前瞻性研究发现,无论病人是否合并糖尿病,瑞舒伐他汀的治疗均不能改善尿蛋白,同时临床应用大剂量(40 mg)时,eGFR会显著下降。因而提示,在基础肾功能差的人群中,需警惕大剂量瑞舒伐他汀对肾脏功能的影响。
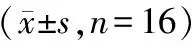
表1 调药前后一般实验室检查结果
注:与调药前比较,*P<0.05

表2 调药前后肾脏相关检查结果
人类从40岁起肾脏的功能开始逐年减退:形态上肾脏体积以每10年平均10%的速度递减,功能上则表现为肾血流量和GFR的下降。Newbold等[1]发现老年人肾脏首先发生皮质肾小球球性硬化,随后引起近髓肾小球肥大和球性硬化,最终所有区域肾小球均发生球性硬化,直接导致肾血流量和GFR的下降。结构的异常使得衰老的肾脏更易受外界因素如循环状态、各种代谢产物及药物的影响。欧洲医药管理局于2012年指出,他汀类药物增加糖尿病的风险为剂量依赖型,并与年龄明显相关,年龄>75岁通常被认为是增加药物不良反应的一个危险因素[8]。因此,我们选择了≥75岁高龄人群作为观察对象,就瑞舒伐他汀对肾脏安全性影响展开研究。
肾脏功能包括肾小球滤过功能与肾小管重吸收功能。临床常用肌酐评估肾小球滤过功能,而研究发现,当GFR降低50%时,血肌酐仍在正常范围内,尤其是在老年人群中,随着年龄的增长,肌肉量减少、蛋白摄入减少,均会使血肌酐水平下降,而不易早期发现肾小球滤过功能的减退[9]。因此,我们选用ECT更精准的评估≥75岁高龄老人的肾小球滤过功能。本次研究发现,根据MDRD简化公式计算eGFR>60 mL/min的老年人群,其ECT-GFR测定值最低可至37.89 mL/min,该结果提示血肌酐水平并不能准确反映≥75岁高龄老年人群的真实肾小球滤过功能。临床常用尿微量白蛋白评估近端肾小管的重吸收功能,NAG是一种重要的细胞内溶酶体酶,在近曲小管上皮细胞中含量较高,是反映肾小管损伤的敏感指标[10]。我们选用尿微量白蛋白滴定联合测定尿NAG来反映肾小管功能。本研究结果表明,在换用瑞舒伐他汀治疗后,病人尿微量白蛋白、尿NAG无明显改变。因每个指标都存在局限性,临床主要靠联合多项指标来提高早期肾脏损伤的检出率,为更完善全面评估瑞舒伐他汀对肾脏安全性的影响,我们应用了可以更早期、更特异性反映肾脏损伤的新型生物标志物KIM-1、IL-18、TGF-β1。KIM-1是由肾脏近曲小管上皮细胞分泌,在肝、肾、脾微量表达,而在损伤后的肾组织中高表达,升高水平与损伤程度相关,尿 KIM-1特异性高,可以早期反映缺血及毒性物质引起的肾脏损害[11]。IL-18是近端肾小管细胞合成和分解的一种促炎因子,发生缺血性肾损害时,IL-18升高明显,而在尿路感染、CKD、肾病综合征、肾前性氮质血症病人上升程度则低得多,引入IL-18反映缺血性肾损害的同时,还可以比较2种他汀类药物对肾小管分泌的促炎因子作用的差异性[12]。TGF-β1表达上调是所有CKD的共同特征,TGF-β是肾间质纤维化的重要调节因子,目前认为TGF-β水平持续升高,是促使CKD进展到终末期肾病的重要因素[13]。本研究发现,在调整为瑞舒伐他汀治疗后,病人LDL-C水平进一步下降(P<0.05),而以上3种肾脏损害指标均无明显变化,说明瑞舒伐他汀短期服用在进一步降低LDL-C水平的同时不会引起肾脏损伤。
综上所述,在年龄≥75岁、平均GFR(62±12)mL/min的人群中,将阿托伐他汀调整为瑞舒伐他汀治疗后1周,肾小管功能与肾脏急性损害标志物变化不明显,提示瑞舒伐他汀短期服用并不影响该类人群肾脏安全性。
