HPLC法同时测定磺胺二甲嘧啶含量和泰乐菌素组分
2018-08-13任玉琴裘丞军吴望君
任玉琴 ,裘丞军,吴望君
(浙江省兽药饲料监察所, 杭州 311199)
泰乐菌素属于大环内酯类抗生素,主要用于敏感菌引起的畜禽各种革兰氏阳性菌、支原体感染,磺胺二甲嘧啶为磺胺类抗菌药,为广谱抑菌剂。泰乐菌素和磺胺二甲嘧啶制成的复方制剂,在作用机理上具有累加作用,主要用于治疗畜禽革兰氏阳性菌和支原体感染,也用于预防猪痢疾[1],市场上应用最早的为“磷酸泰乐菌素、磺胺二甲嘧啶预混剂”[2],被收载于《进口兽药质量标准》1999年版,“酒石酸泰乐菌素、磺胺二甲嘧啶可溶性粉”[3]作为地方标准上升到国家标准,被收载于《兽药国家标准汇编》第一册(兽药地方标准上升国家标准),该产品也是我国兽药企业生产较多的一个品种,兽药国家标准汇编中,泰乐菌素含量采用生物效价法测定、组分采用高效液相色谱(HPLC)法测定,磺胺二甲嘧啶(SM2)含量采用紫外-可见分光光度法测定,方法繁锁。磺胺类结构中均存在共轭双键,在紫外区有吸收,特别是SM2与磺胺嘧啶有相同的官能团,用紫外-可见分光光度法测定含量和最大吸收波长作为鉴别,专属性不强。在动物源性食品中SM2残留测定均采用HPLC或LC/MS-MS法测定[4-6],陶弥峰[7]建立了液相色谱法测定营养品中磺胺类的残留;徐恩民[8]等对氟苯尼考制剂中SM2等测定进行了研究;包洁华[9]等用HPLC法测定酒石酸泰乐菌素有关物质的研究;HPLC法测定磺胺二甲嘧啶和泰乐菌素[10-12]已在各个领域得到应用。为此本文对泰乐菌素组分、磺胺二甲嘧啶含量的测定方法进行研究,建立了用HPLC法同时测定磺胺二甲嘧啶和泰乐菌素组分含量,方法简便、快速,专属性强。
1 材 料
1.1 试剂和药品 市售酒石酸泰乐菌素、磺胺二甲嘧啶可溶性粉,批号:13022501、20140301、14030601;泰乐菌素标准品,中国兽医药品监察所,批号K0161305;磺胺二甲嘧啶对照品,批号:H0371008,含量99.8%,中国兽医药品监察所;磺胺间甲氧嘧啶、磺胺嘧啶、磺胺氯吡嗪钠、磺胺喹噁啉、磺胺甲噁唑对照品来源于中国兽医药品监察所;磺胺氯哒嗪钠、磺胺对甲氧嘧啶、磺胺噻唑、磺胺脒、磺胺甲氧哒嗪对照品均来源于Dr.Ehrenstorfer GmbH公司。
1.2 仪器 Agilent 1100高效液相色谱仪;Agilent 1260高效液相色谱仪;Waters2690高效液相色谱仪;UV-2550紫外分光光度计;Mettler Toledo电子天平。
2 方法和结果
2.1 磺胺二甲嘧啶含量测定方法学建立
2.1.1 液相色谱条件 以ECOSIL C18(4.6 mm×250 mm,5 μm)为色谱柱;流动相:2 mol/L高氯酸钠溶液(用1 mol/L盐酸溶液调pH至2.5±0.1)-乙腈,采用梯度洗脱方法(表1);流速1.0 mL/min;检测波长280 nm;进样量20 μL。

表1 流动相梯度洗脱程序Tab 1 Mobile phase gradient elution program
2.1.2 标准溶液配制 取磺胺二甲嘧啶对照品适量,加0.1 mol/L HCl溶液溶解制成20 μg/mL溶液;取泰乐菌素对照品约35 mg,置100 mL量瓶中,加甲醇10 mL溶解,用水稀释刻度,将磺胺二甲嘧啶与泰乐菌素标准溶液混合,按上述色谱条件测定,结果磺胺二甲嘧啶和泰乐菌素4个组分有较好的分离,泰乐菌素D峰与A峰的分离度≥3.2;泰乐菌素C峰与磺胺二甲嘧啶分离度≥30(图1)。
2.1.3 检测波长筛选 取2.1.2项下的标准溶液,在200~400 nm波长进行扫描,结果磺胺二甲嘧啶在243 nm处有最大吸收、在300 nm处有次吸收,酒石酸泰乐菌素在300 nm波长处有最大吸收,2010版《中国兽药典》[13]酒石酸泰乐菌素组分检测波长为280 nm,美国药典(USP)[14]和欧州药典(EP)[15]标准中泰乐菌素组分检测波长均为290 nm,因此选择280 nm、290 nm进行考察。
按拟定的色谱条件,采用双波长测定,结果磺胺二甲嘧啶在280 nm处的响应值略高于290 nm,泰乐菌素C、B、D、A组分在290 nm的响应值略高于280 nm,因此本方法检测波长选择280 nm,与《中国兽药典》一致。

图1 磺胺二甲嘧啶和酒石酸泰乐菌素混合标准溶液色谱图素Fig 1 Chromatograph of sulfadimidine and tylosin tartrate standard mixture
C2.1.4 磺胺二甲嘧啶定量限和检测限考察 取磺胺二甲嘧啶标准溶液(2.1.2项)适量,用水稀释成不同的上机浓度,按上述色谱条件上机分析,结果上机浓度为0.05 μg/mL ,其S/N=3.9;上机浓度为0.15 μg/mL ,其S/N=13,磺胺二甲嘧啶检出限为0.05 μg/mL:定量限0.15 μg/mL,见图2、图3。
2.1.5 磺胺二甲嘧啶线性考察 取磺胺二甲嘧啶对照品约20 mg,置50 mL量瓶,加0.1 mol/L HCl溶解至刻度,摇匀,精密量取适量,用水稀释成浓度为10、20、40、80、160、200 μg/mL的上机液,按上述色谱条件进行分析,结果线性方程:y=48.618X-63.982,R2=0.9994,在10~200 μg/mL浓度范围内具有良好的线性。

图2 磺胺二甲嘧啶检出限(S/N=3.9)Fig 2 Tylosin limit of detection (S/N=3.9)

图3 磺胺二甲嘧啶定量限(S/N=13)Fig 3 Tylosin limit of quantitation(S/N=13)
2.1.6 磺胺二甲嘧啶准确度与精密度试验 模拟“酒石酸泰乐菌素、磺胺二甲嘧啶可溶性粉”处方:10%酒石酸泰乐菌素+10%磺胺二甲嘧啶+10%无水碳酸钠,用无水葡萄糖加至100%。按处方量的80%、100%、120%添加磺胺二甲嘧啶、酒石酸泰乐菌素,进行加标回收试验。每一浓度制备4~5份,分别置50 mL容量瓶,加水溶解并稀释至刻度,摇匀,精密量取5 mL,置50 mL容量瓶,用水稀释至刻度,摇匀;另称取磺胺二甲嘧啶对照品9.75 mg,置50 mL容量瓶,加0.1 mol/L HCL溶液溶解至刻度,摇匀,精密量取5 mL,置50 mL容量瓶,用水稀释至刻度,摇匀。按上述色谱条件进行分析,精密量取20 μL注入高效液相色谱仪,记录色谱图,按外标法以峰面积计算,试验结果见表2。
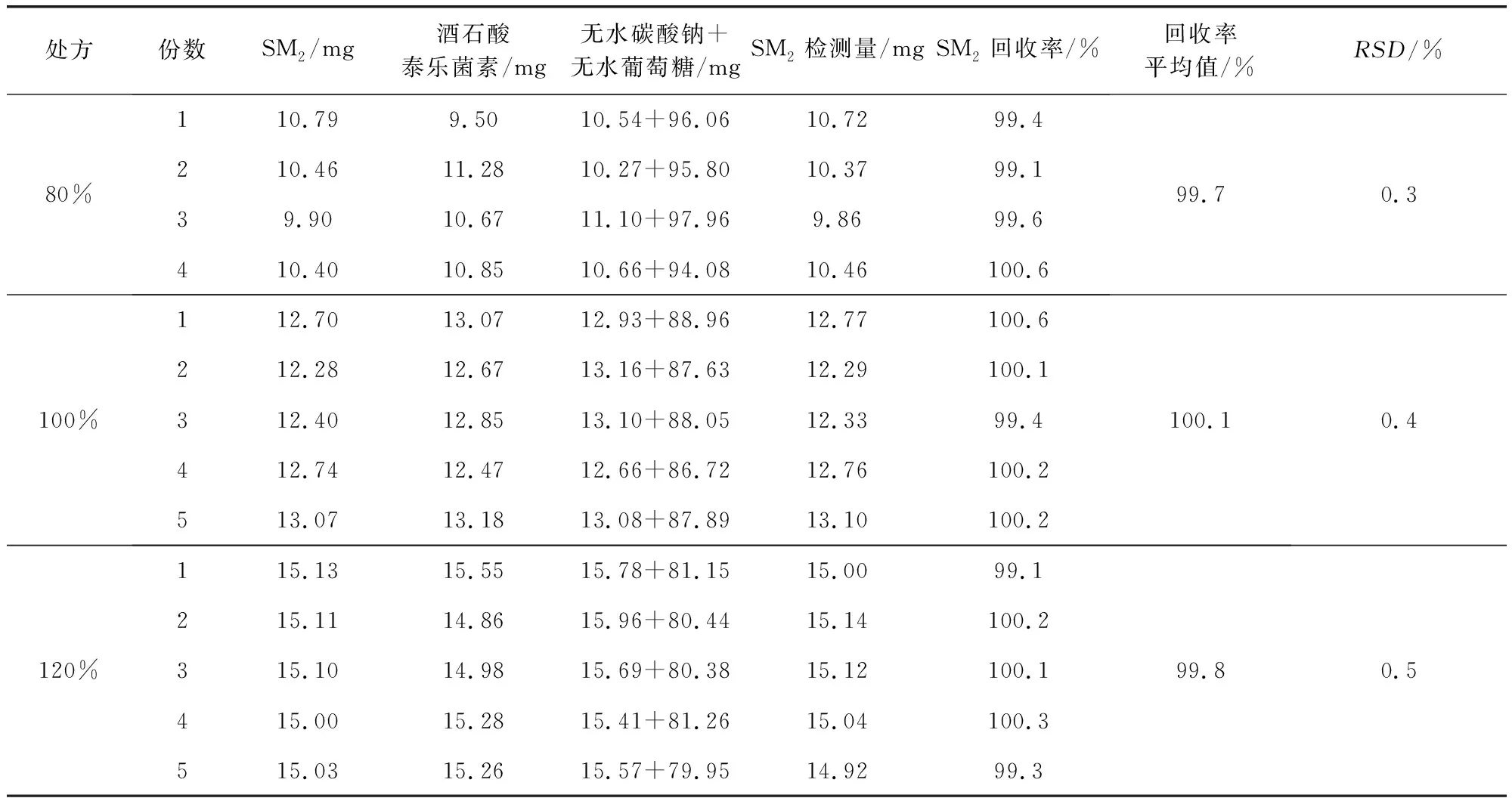
表2 磺胺二甲嘧啶准确度与精密度试验结果Tab 2 Accuracy and precision of tylosin measurements
上述试验结果表明,磺胺二甲嘧啶含量测定平均回收率在99.7%~100.1%间,RSD为0.3%~0.5%,方法的准确度和精密度均满足要求。
2.1.7 磺胺二甲嘧啶含量测定上机液放置稳定性试验 取批号为14030601 、13022501和20140301样品,加0.1 mol/L盐酸溶液溶解并稀释至刻度,摇匀,精密量取适量,用水定量稀释制成每1 mL中约含磺胺二甲嘧啶0.08 mg/mL的溶液,按上述色谱条件,放置不同时间重复测定,结果磺胺二甲嘧啶峰面积变化极小,该方法中溶液非常稳定(表3)。

表3 含量测定溶液放置稳定性试验Tab 3 Sample stability test
2.1.8 方法专属性试验
2.1.8.1 磺胺类产品干扰试验 《中国兽药典》2010年版共收载了磺胺二甲嘧啶、磺胺间甲氧嘧啶、磺胺嘧啶、磺胺氯吡嗪钠、磺胺喹噁啉、磺胺甲噁唑、磺胺氯哒嗪钠、磺胺对甲氧嘧啶、磺胺噻唑、磺胺脒、磺胺甲氧哒嗪11种磺胺类产品,取上述对照品适量,加0.1 mol/L HCl溶液溶解制成20 μg/mL溶液;另取泰乐菌素对照品约35 mg,精密称定,置100 mL量瓶中,加甲醇10 mL溶解,用水稀释刻度。
取混合标准溶液按上述色谱条件测定,结果磺胺二甲嘧啶与另10种磺胺类、泰乐菌素4个组分均能有效分离,见图4。混合标准溶液组分出峰顺序依次为:磺胺脒、磺胺噻唑、磺胺嘧啶、磺胺二甲嘧啶、磺胺甲氧哒嗪+磺胺对甲氧嘧啶、磺胺间甲氧嘧啶、磺胺氯哒嗪、磺胺氯吡嗪、磺胺喹噁啉、泰乐菌素C、泰乐菌素B、泰乐菌素D和泰乐菌素A。

图4 酒石酸泰乐菌素和11种磺胺混合标准溶液色谱图Fig 4 Chromatograph of tylosin tartrate and sulfonamides standard mixture
2.1.8.2 酸降解试验 取酒石酸泰乐菌素与11种磺胺类对照品约15 mg,置25 mL容量瓶,加0.1 mol/L盐酸溶液至刻度,放置2.5 h,用NaOH溶液调pH值至中性,按上述色谱条件上机测定,结果酒石酸泰乐菌素在酸性环境中降解明显,磺胺二甲嘧啶与各降解峰分离良好,见图5。

图5 酸降解后酒石酸泰乐菌素和磺胺类混合标准溶液色谱图Fig 5 Chromatograph of sulfonamides standard mixture and tylosin tartrate after acid hydrolysis
2.1.8.3 碱降解试验 磺胺二甲嘧啶在碱性条件下较稳定,因此本方法仅对酒石酸泰乐菌素进行碱降解试验。取酒石酸泰乐菌素对照品约15 mg,置25 mL容量瓶,加0.1 mol/L氢氧化钠溶液至刻度,放置5 h,用HCL溶液调pH值至中性,按上述色谱条件分析,结果酒石酸泰乐菌素在碱性环境中降解彻底,各降解峰对磺胺二甲嘧啶峰无干扰,见图6。

图6 酒石酸泰乐菌素碱降解色谱图Fig 6 Chromatograph of tylosin tartrate after alkaline hydrolysis
2.1.8.4 氧化破坏试验 取批号为13022501样品约0.2 g,加30%过氧化氢溶液5 mL,放置3 h,加水至25 mL,按上述色谱条件分析,结果酒石酸泰乐菌素主峰全部降解,各降解峰与磺胺二甲嘧啶主峰分离良好(图7、图8)。

图7 批号13022501样品溶液色谱图Fig 7 Chromatograph of Sample 13022501

图8 批号13022501样品氧化破坏色谱图Fig 8 Chromatograph of Sample 13022501 after oxidation
2.1.9 方法耐用性考察 取2.1.2项下的溶液,按上述色谱条件,通过不同品牌的色谱柱,小幅改变流动相比例、柱温及不同液相色谱仪,考察该色谱条件的耐用性,结果磺胺二甲嘧啶与泰乐菌素分离度、峰面积未受影响,该方法有较好的重现性。
2.2 泰乐菌素组分测定
2.2.1 按拟定的方法测定 取样品约0.35g与泰乐菌素对照品约35 mg,精密称定,置100 mL量瓶中,加甲醇10 mL溶解,用水稀释刻度,照2.1.1项下的色谱条件试验,以泰乐菌素标准品溶液中C、B、D、A主组分峰定性供试品溶液的主组分峰,按峰面积归一化法(除磺胺二甲嘧啶峰外)计算,结果泰乐菌素D峰与泰乐菌素A峰的分离度≥3.2;泰乐菌素C峰与磺胺二甲嘧啶分离度R≥30,泰乐菌素A峰拖尾因子0.93;理论板数按泰乐菌素A计算为20507,系统适应性试验均符合要求,样品考察结果该色谱条件有较好的重现性。结果见表4。
2.2.2 按《中国兽药典》方法对泰乐菌素组分定性考察 取泰乐菌素标准品适量,按《中国兽药典》2010年版方法制备上机溶液和测定,结果泰乐菌素C、B、D、A组分的相对保留时间为0.49、0.76、0.82、1,而标准品附带的色谱图中相对保留时间为0.61、0.72、0.8、1, C、B、D组分与《中国兽药典》规定的0.5、0.7、0.8有一定的出入。

表4 泰乐菌素组分检查结果Tab 4 Tylosin component test results
3 讨论与结论
通过酸、碱、氧化破坏、同类产品的干扰试验及方法耐用性考察,结果显示11种磺胺类产品和泰乐菌素组分在该色谱条件中有较好的专属性和重现性。该方法的建立,能同时完成磺胺二甲嘧啶含量和泰乐菌素组分测定,方法简便、准确、专属性强,能有效甄别其他磺胺类成分的非法添加,为产品质量控制提供较好的技术支持。
《中国兽药典》收载了众多的泰乐菌素系列产品,均采用相对保留时间来定位C、B、D、A组分,但在实际操作中,不同品牌、不同规格色谱柱影响组分的相对保留时间,定位有一定难度,给检测结果的准确性带来影响。USP 36版也采用相对保留时间来定位泰乐菌素组分,EP 7.0版采用对照品C、B、D、A组分定性样品中组分,目前泰乐菌素标准品附带含C、B、D、A组分色谱图,用泰乐菌素C、B、D、A组分对照品来定性样品中的组分能有效解决当前组分定性的不准确。
