酒石酸钠标定法测定二氧化硫产品微量水分
2021-07-08郑学根史英俊柴世建鲍志君祝永芳
郑学根,史英俊,柴世建,鲍志君,姚 琴,黄 韵,祝永芳
(浙江巨化股份有限公司硫酸厂,浙江 衢州 324004)
应用GB/T 6283-2008用酒石酸钠(均指Na2C4H4O6·2H2O)作为标定卡尔·费休试剂的水标准物测定产品中微量水分时,由于标准中仅标明酒石酸钠的纯度要求为分析纯,既未说明酒石酸钠的保存条件,也未说明其含水率情况,只在计算公式中使用了酒石酸钠水的质量分数理论量(0.156 6)[1]。这给该方法在日常检测工作中的应用带来了疑惑,一是方法使用者往往需采购基准的酒石酸钠,二是对采购的基准物含水率的稳定性心中无数,既增加了检测费用,又增加了检测者对检测结果准确性的担忧。
为解决上述问题,进行了酒石酸钠保存条件、稳定性、失水温度和含水率方面的实验,建立测定酒石酸钠含水率后标定卡尔·费休试剂水当量来测定二氧化硫产品中微量水分的方法,以有效降低由酒石酸钠含水率变化带来的误差。
1 实验方法
1.1原理
存在于试样中的任何水分(游离水或结晶水)与已知滴定度的卡尔·费休试剂(碘、二氧化硫、吡啶和甲醇组成的溶液)进行定量反应。反应式为:
H2O+I2+SO2+3C5H5N→2C5H5N·HI+C5H5N·SO3,
C5H5N·SO3+ROH→C5H5NH·OSO2OR。
1.2 试剂与仪器
酒石酸钠,分析纯;卡尔·费休试剂,按照GB/T 6283-2008中5.13的方法用甲醇制备;水,符合GB/T 6682的规定的三级水[2]。
烘箱,可调温度(100±2)~(150±2)℃,称量瓶,30 mm×40 mm;分析天平,精度0.1 mg;KF-2型微量水分测定仪;注射器,大小适用,体积经校正。
1.3 保存条件和失水温度
1)活性硅胶干燥器中酒石酸钠不同保存时间下的失水情况。称取适量的酒石酸钠试剂于30 mm×40 mm的称量瓶中,不盖称量瓶盖保存于含活性硅胶的干燥器中,定期取出称量,观察其失水率随保存时间的变化情况。
失水率γ的计算:
γ=(m1-m2)/m1。
式中,m1和m2分别为试样干燥前后的质量。
2)失水温度实验。称取适量的酒石酸钠分别于110、115、120、125、130℃温度下的烘箱中干燥2 h,称量,计算其失水率。
3)实验室正常条件下存放酒石酸钠的稳定性。共存放49 d,期间每隔一段时间测定1次失水率。
4)不同时间采购的酒石酸钠的含水情况。将不同时间采购的酒石酸钠在120℃下干燥2 h,测定其含水率。
1.4 滴定度的标定
用已测定含水率的酒石酸钠标定卡尔·费休试剂的滴定度,然后,用标定后的卡尔·费休试剂滴定产品的水分含量。
称取适量酒石酸钠试剂(m3,精确到0.1 mg),迅速将酒石酸钠加入到滴定容器中,立即塞上胶塞,用待标定的卡尔·费休试剂进行滴定,记录消耗的卡尔·费休试剂的体积。
卡尔·费休试剂的滴定度T的计算:
T=w m3/V1。
式中,w为酒石酸钠的中水的质量分数,m3为酒石酸钠的质量,V1为消耗的卡尔·费休试剂的体积。
1.5 产品测定
通过排泄嘴将滴定容器中的残液放完,用注射器经橡皮塞注入25 mL甲醇,打开电磁搅拌器,为了与存在于甲醇中的微量水反应,由自动滴定管滴加卡尔·费休试剂,直到电量测定装置的显示量突然增加至某一特定的量,并保持1 min不变。
将采样小钢瓶的一头接上已经干燥处理的直角弯管,打开小钢瓶阀门,放出少量液体二氧化硫样品于废液杯中,然后迅速称取约40 g液体二氧化硫(精确至1.0 g)置于已干燥并已恒量(精确至0.1 g)的100 mL锥形瓶中,并将其立即移入到滴定容器中,塞上滴定容器的橡皮塞,由自动滴定管滴加卡尔·费休试剂,直到电量测定装置显示量突然增加至与上次同样的特定量,并保持1 min不变为终点。记录消耗的卡尔·费休试剂的体积(V2)。
产品水的质量分数w的计算:
w=V2T/m。
式中,V2为消耗的卡尔·费休试剂的体积,T为卡尔·费休试剂的滴定度,m为试样的质量。
2 结果与讨论
2.1 干燥器内干燥时间
酒石酸钠在含活性硅胶的干燥器中失水率随干燥时间变化见表1。

表1 酒石酸钠失水率随时间的变化Tab 1 Water loss rate of sodium tartrate with different time
从表1可以看出,酒石酸钠失水率,即含水的稳定性随时间的变化没有规律,将酒石酸钠保存在含活性硅胶的干燥器中的方法,不能完全去除其游离水或完全除去结晶水。
2.2 失水温度
酒石酸钠在不同温度下的干燥数据如表2。
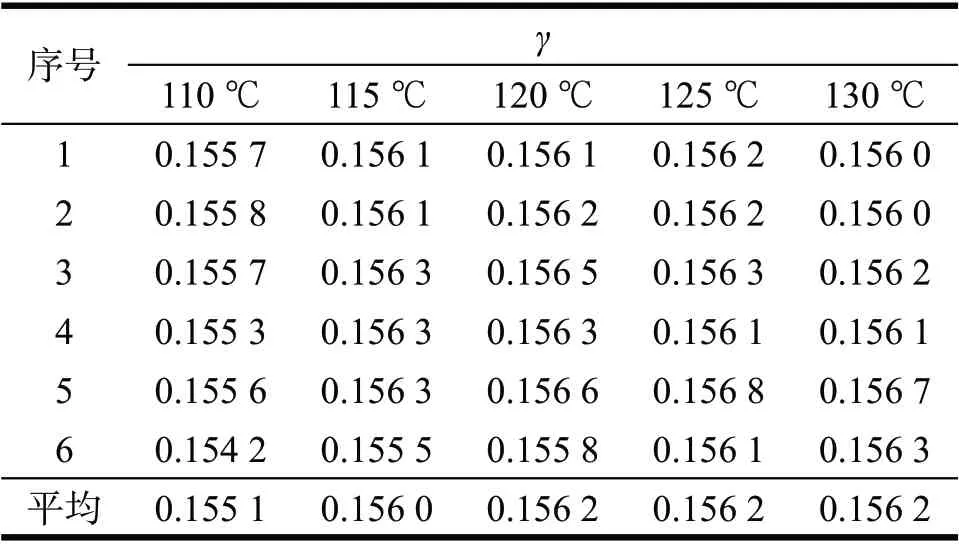
表2 酒石酸钠不同温度下烘干的失水率Tab 2 Water loss rate of sodium tartrate with different temperature
从表2可以看出,酒石酸钠在115~130℃条件下失水率趋于稳定,可以认为其完全失去结晶水,失水率即为酒石酸钠中水的质量分数。
2.3 保存时间的影响
实验室正常存放条件下,酒石酸钠失水率随保存时间的变化如表3。
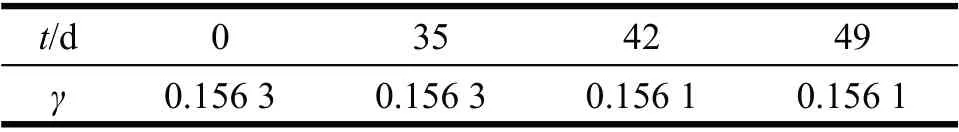
表3 酒石酸钠含水率随保存时间的变化情况Tab 3 Water content of sodiumtartrate with different retention time
从表3可以看出,在正常的实验室环境条件下,保存时间长短对酒石酸钠失水率无明显影响。结合表2的数据进行综合考虑,酒石酸钠试剂在实验室条件下常规保存即可。
2.4 采购时间的影响
不同时间采购的酒石酸钠的失水率见表4。
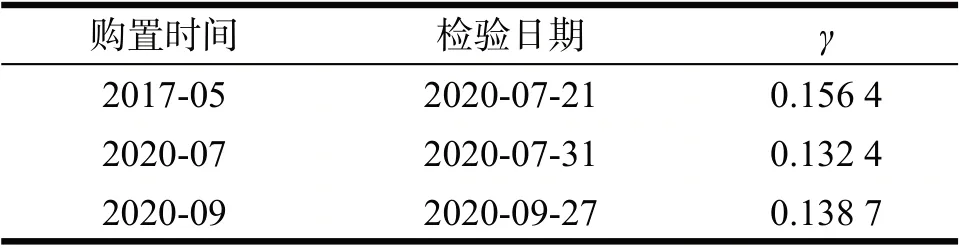
表4 不同时间采购酒石酸钠失水率Tab 4 Water loss rate of sodium tartrate with different purchasing period
从表4可以看出,不同时间采购的酒石酸钠的失水率有较大的差异。若直接采用现购的酒石酸钠标定卡尔·费休试剂的滴定度,使用标准中给出的酒石酸钠水的质量分数的理论量(0.156 6)计算产品中微量水分的含量,由酒石酸钠失水率带来的计算误差将达15%左右。
2.5 滴定度
用已知含水率的酒石酸钠测定卡尔·费休试剂的滴定度的测定结果如表5。

表5 卡尔·费休试剂的滴定度Tab 5 Titration of Karl Fischer reagent
表5的2次测定结果平均为2.365 g/L。
2.5 产品测定
以水和酒石酸钠为标准标定卡尔·费休试剂的滴定度对同一批液体二氧化硫产品水的质量分数的测定结果如表6。
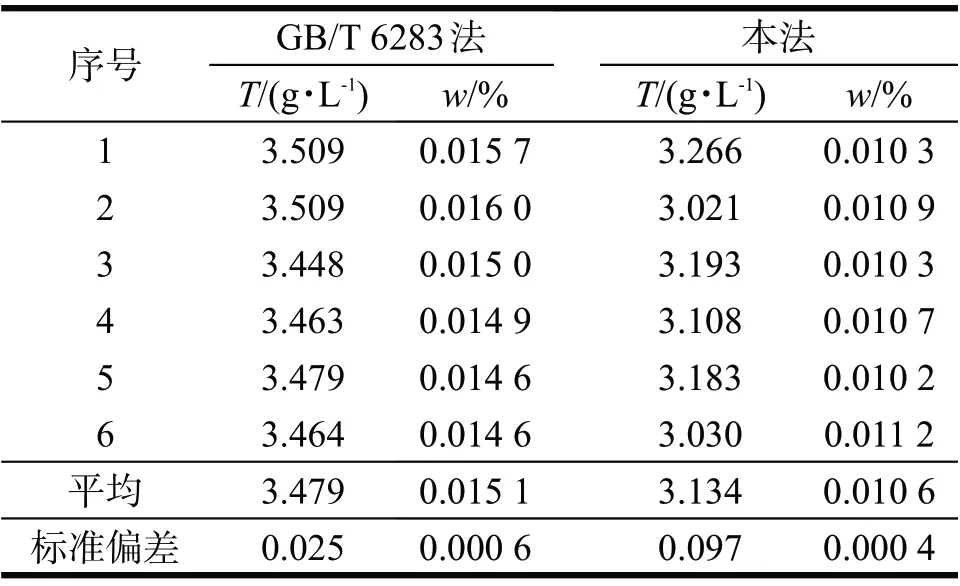
表6 使用不同标准物测定同一批产品中的含水率Tab 6 Water content evaluation with different methods
从表6可以看出,用测定酒石酸钠的含水率标定卡尔·费休试剂滴定度来测定产品中微量水分质量分数的平均结果,低于直接用水标定卡尔·费休试剂滴定度的方法,测定结果更接近于产品中水分真实含量,其测定结果的准确度和精密度可以达到或优于直接用水标定卡尔·费休试剂滴定度的方法,主要原因是环境空气中的水分会不可避免地对卡尔·费休试剂滴定度和测量结果产生影响,且环境空气中的水分带来的影响都是正偏差,直接用水标定卡尔·费休试剂滴定度时,注入水的量小,其计量误差相对较大。
根据酒石酸钠实测失水率γ计算的液体二氧化硫产品水的质量分数w1与用酒石酸钠理论水的质量分数(0.156 6)计算的产品水分含量对比情况如表7。

表7 实测与计算结果对比Tab 7 Comparison of evaluation and theoretical calculation
从表7可以看出,酒石酸钠实测失水率与其理论水的质量分数(0.156 6)相差越多,则产品中水分含量测定结果的误差越大。
3结论
通过实验,明确了酒石酸钠完全失去结晶水的温度和保存条件,酒石酸钠在115~130℃条件下失水率趋于稳定,可以认为其完全失去结晶水。采用先测定酒石酸钠含水率,然后,根据所测得含水率标定卡尔·费休试剂滴定度来测定产品中微量水分的方法可有效提高产品微量水分含量测定结果的准确度(15%以上)。
