复方茵陈保肝口服液的制备与提取工艺研究
2018-08-13陈容李秋萍张泸月李霞辉
陈容,罗 亮,李秋萍,张泸月,曾 杰,李霞辉,舒 刚
(四川农业大学动物医学院,四川成都 610000)
肝脏是动物体具有消化、解毒、免疫等重要功能组织器官。蛋鸡脂肪肝又称脂肪肝综合征或脂肪肝出血性综合征[1],是产蛋鸡常见的一种营养代谢性疾病。主要是脂肪在肝细胞内过分堆积,影响肝脏的正常功能,严重的甚至引起肝细胞破裂,最终导致肝内出血而死亡。患脂肪肝的鸡群很难出现产蛋高峰,产蛋率一般上升到85%左右即开始逐渐下降。而蛋类需求在我国这样畜禽大国较大。中医称脂肪肝为肝癖,在长期的实践中,积累了丰富的治疗脂肪肝的经验[2]。中药口服液是当前中药生产中新兴的,由中药汤剂为基础发展而来的热门剂型。具有起效快、作用明显、方便携带、便于保存等优点[3]。复方茵陈保肝口服液全方由茵陈、党参、柴胡、熟地、淫羊藿、益母草、牛膝七味中药组成,具有清热解毒、活血化淤、滋养肝脏以及强筋补肾、益气养精之功效[4-6]。香豆素[7]是君药茵陈中含有的主要成分,可以抑制肝脏中凝血因子的合成,具有明显保肝作用。后期的动物实验中证明复方的口服液对禽类鹌鹑脂肪肝有防治作用。本研究采用多因素分析与正交试验法,以滨蒿内酯为对照品,通过紫外分光光度法测定口服液中香豆素的含量,以其含量高低作为优选口服液制备工艺的标准。选取料液比、煎煮时间、醇沉时间为多因素,先分别进行单因素试验,优选出每个因素最佳水平后,以最佳水平及其相邻的两个水平进行正交试验法选出口服液最佳提取工艺。口服液制备工艺研究完成后,采用薄层色谱法对口服液中茵陈、党参、淫羊藿进行定性鉴别,并利用高效液相色谱法准确测定口服液中香豆素的含量,以此建立口服液的质量标准。
1 材 料
1.1 主要药品 茵陈、党参、柴胡、熟地、淫羊藿、牛膝、益母草(七种药材均购于四川成都温江惠明路211号惠民大药房)、苯甲酸钠、苯甲酸、蒸馏水、NaOH、乙醇、甲醇、硫酸、乙酸乙酯、乙酸丁酯、乙腈、滨蒿内酯对照品(中国药品生物制品检定所,1511-200001批号)、茵陈对照药材(中国药品生物制品检定所,21555-201101批号)、党参对照药材(中国药品生物制品检定所,10766-20041批号)、淫羊藿苷对照品(中国药品生物制品检定所, 110737-200405批号)
1.2 主要仪器 烧杯、锥形瓶 、玻璃棒 、过滤漏斗、比色皿、UV1100型紫外可见分光光度计(上海天美科学仪器有限公司);BP211S型电子分析天平(北京Sartorius天平有限公司) 、旋转蒸发仪、1XC-110A型超声波清洗器(济宁鑫欣超声电子设备有限公司)、恒温水浴锅(余姚市亚星仪器 仪表有限公司)、紫外分析仪(郑州豫华仪器制造有限公司)、HP1100型高效液相色谱仪(美国惠普公司)、硅胶G薄层板(青岛海洋化工厂)
2 方法与结果
2.1 优选口服液制备工艺
2.1.1 处方 茵陈6 g、党参6 g、柴胡4 g、熟地4 g、淫羊藿4 g、牛膝2 g、益母草2 g。
2.1.2 基本制备工艺 取上述七味中药在1000 mL大烧杯中加10倍的蒸馏水浸泡30 min,煎煮2次,每次煎煮1 h。待药液冷却至室温后,用漏斗滤过,合并两次滤液。随后置于离心机离心10 min,取出上层滤液,弃去残渣,对离心后的滤液进行浓缩,使药液浓缩至相对密度1.02~1.05 g/mL即可。待浓缩液冷却后向其中加入95%的乙醇使其药液里的乙醇浓度达到60%[4],进行醇沉,搅拌均匀后放置5 ℃冰箱静置24 h。取出上清液过滤,用旋转蒸发仪中回收滤液中的乙醇。向回收乙醇后的药液中加入蒸馏水使药液达到28 mL。向药液中加入0.1 g的苯甲酸钠和0.1 g苯甲酸,搅拌均匀,用0.2%NaOH调pH值使药液pH值在5~7之间。最后将所制的28 mL的药液进行分装,灭菌,即可[8]。
2.1.3 含量测定方法 利用滨蒿内酯为对照品,用紫外分光光度法在340 nm处测定口服液中香豆素含量[9]。本研究随机选取料液比为1∶16,煎煮时间为1.5 h,乙醇浓度为60%,按照制备工艺制成的口服液作为样品,对测定方法进行考评,结果表明该方法简单易行,重复性好,可用于本研究的工艺优化。
对照品溶液的制备:精密称取滨蒿内酯6.8 mg,置100 mL量瓶中,加70%乙醇稀释至刻度线,摇匀即得。
供试品溶液的制备:精密量取样品1 mL置100 mL量瓶中,加 70%乙醇稀释至刻度, 摇匀即得。
线性关系的考察:精密量取对照品溶液 1、 2、 3、 4、 5、 6 mL,分别置 25 mL量瓶中,加 70%乙醇稀释至刻度,摇匀[10]。以 70%乙醇为空白,照紫外-可见分光光度法(《中国药典》 2015年版四部通则),在340 nm的波长处测定吸光度,以吸光度(Y)为纵坐标, 浓度(X)为横坐标绘制标准曲线[11]。 得回归方程为Y=0.0597X-0.008,r=0.9998。结果表明,滨蒿内酯在2.72~16.32 μg/mL与吸光度呈良好的线性关系。
精密度试验:取稀释后的对照品溶液(浓度:10.88 μg/mL),在340 nm处连续测定6次吸光度。结果RSD为0.84%,表明仪器精密度良好。
稳定性试验:取供试品溶液, 在340 nm处于0、1、 2、3、4 h测定其吸光度,结果RSD为0.46%,表明供试品在4 h内稳定。
重复性试验:分别取6份口服液,同法制备供试品溶液,在340 nm处测定吸光度,计算样品中香豆素的含量。结果RSD为1.03%,表明方法重复性好。
回收率试验:采用加样回收法,先精密吸取已知含量的样品口服液1 mL共6份,分别加入0.493、0.507、0.613、0.622、0.738、0.745 mg的滨蒿内酯对照品,同法制成供试品溶液,测定它们的吸光度,计算加样回收率。结果香豆素平均回收率为98.64%,RSD为1.07%,表明方法回收率良好。回收率见表1。
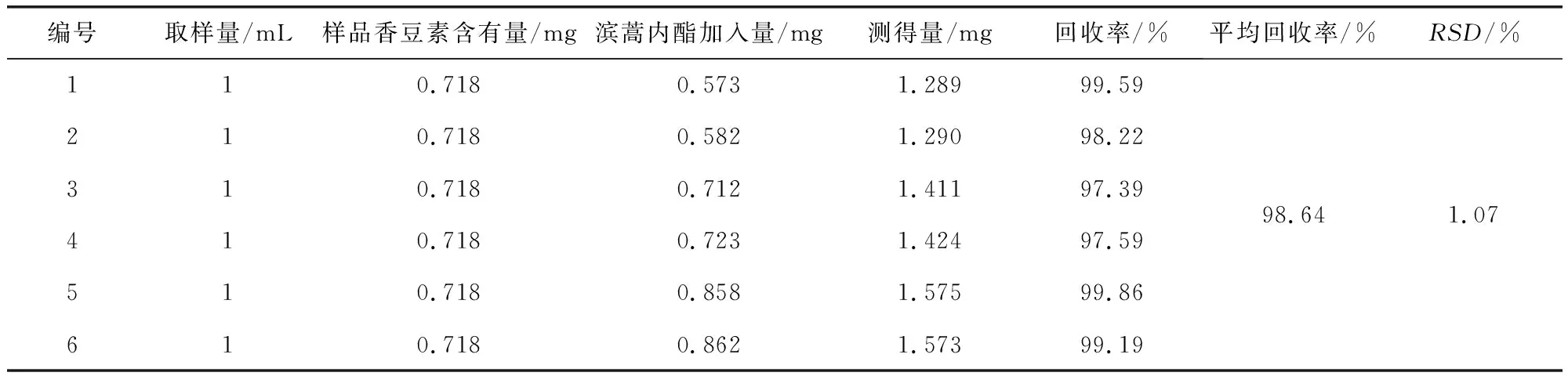
表1 加样回收率结果Tab 1 sample recovery results
样品含量测定:取三份相同制备工艺下制备的口服液同法制成供试品溶液,分别在340 nm处测定其吸光度,计算香豆素含量。结果分别为0.715、0.717、0.723 mg/mL。
2.1.4 单因素水平筛选 上述所示制备工艺中没有明确蒸馏水用量(料液比)、煎煮时间以及乙醇浓度(醇沉体积分数)[11-12]。本实验以这三个因素为考察对象,其中料液比水平见表2,煎煮时间水平见表3,醇沉体积分数水平见表4。

表2 料液比Tab 2 feed ratio

表3 煎煮时间Tab 3 boiling time

表4 乙醇浓度Tab 4 Ethanol concentration
进行单因素水平筛选时,控制其余两个因素不变,其中进行料液比水平筛选时煎煮时间为1.5 h,乙醇浓度为50%;进行煎煮时间水平筛选时,料液比为1∶16,乙醇浓度为50%;进行醇沉体积分数水平筛选时,料液比为1∶16,煎煮时间为1.5 h。其余条件均按照制备工艺制成相应的口服液。每个单因素实验进行三次,按照上述含量测定方法测定各自香豆素含量,以三次实验测得的含量的平均值作为结果。料液比水平浓度曲线见图1,煎煮时间水平浓度曲线见图2,醇沉体积分数水平见图3。
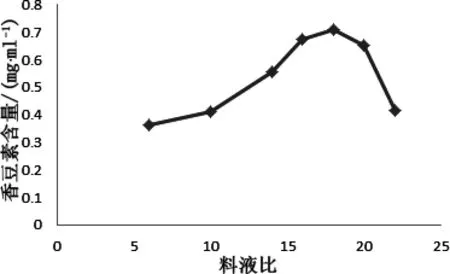
图1 料液比水平含量曲线Fig 1 liquid ratio of the level of content curve
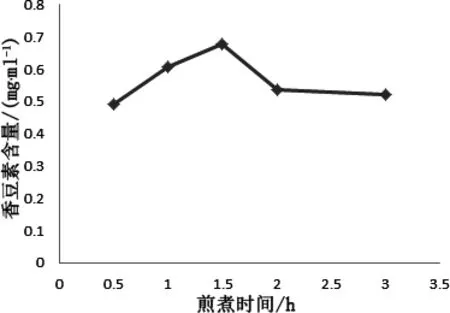
图2 煎煮水平含量曲线Fig 2 boiling horizontal curve
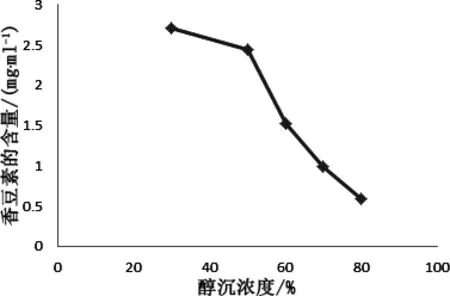
图3 乙醇浓度水平含量曲线Fig 3 ethanol concentration level curve
本品为水溶性,主要成分为蒿属香豆素属于苷类,查中国药典2015版第四部,50%~70%为乙醇浸出苷类的范围。故选择正交醇沉范围为50%~70%。
2.1.5 正交实验优选 经过单因素实验确定最佳料液比为1∶18,最佳煎煮时间为1.5 h,最佳醇沉分数为60%。为了更好地优化制备工艺,需对此三种因素进行正交实验考察[13-15]。正交实验因素水平见表5,正交实验表见表6,依据正交实验表按照上述基本制备工艺熬制口服液样品,每个水平熬制三份,并依法进行香豆素含量测定,以三份测定平均值作为结果。结果见表7。
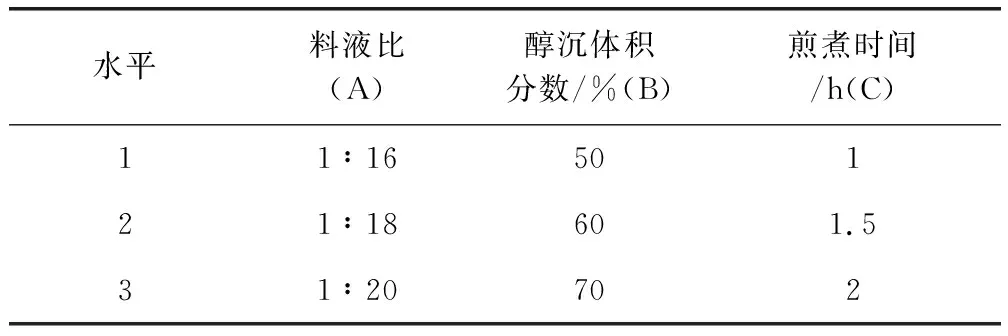
表5 正交实验因素水平Tab 5 Orthogonal experimental factors
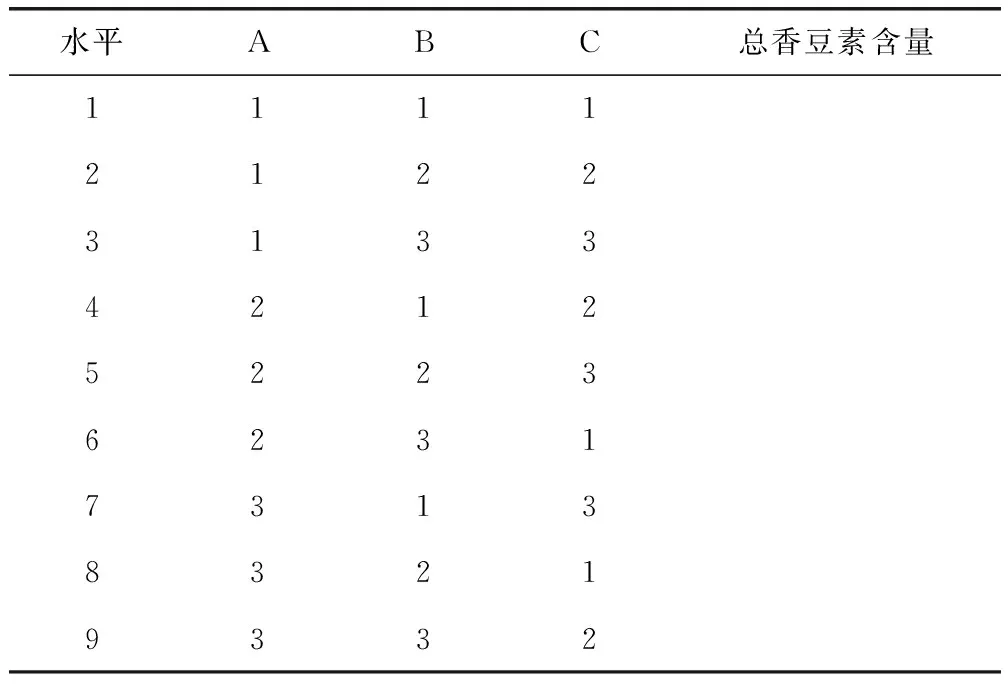
表6 正交实验表格Tab 6 Orthogonal experiment table
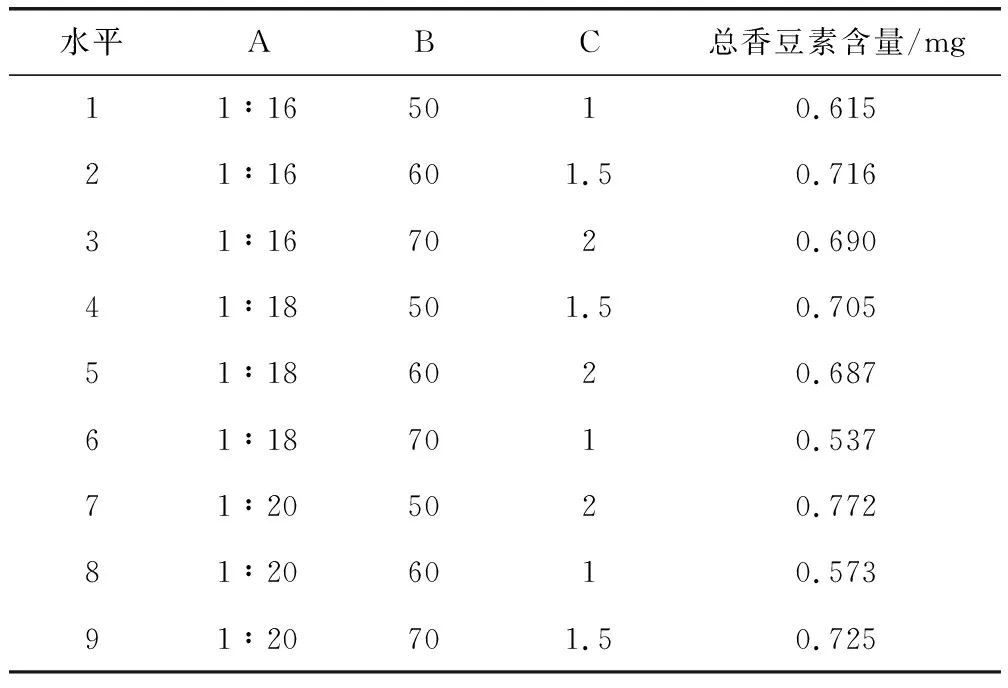
表7 正交实验结果Tab 7 Orthogonal experimental results
经筛选,得出水平7,即料液比1∶20,醇沉体积分数50%,煎煮2 h为最佳制备工艺。
2.1.6 最佳制备工艺 取上述七味中药在1000 mL大烧杯中加至560 mL蒸馏水浸泡30 min,煎煮2次,每次2 h。待药液冷却后,用滤布滤过,合并两次滤液。弃去残渣,对滤液进行浓缩,使药液浓缩至相对密度1.02~1.05 g/mL即可。待浓缩液冷却后向其中加入浓度为50%乙醇进行醇沉,搅拌均匀后放置5 ℃冰箱静置24 h。取出上清液过滤,用旋转蒸发仪中回收滤液中的乙醇。向回收乙醇后的药液中加入蒸馏水使药液达到28 mL。向药液中加入0.1 g的苯甲酸钠和0.1 g苯甲酸,搅拌均匀,用0.2%NaOH调pH值使药液pH值在5~7之间。最后将所制的28 mL的药液进行分装,灭菌,即可。
2.2 口服液质量标准
2.2.1 茵陈的定性鉴别 取口服液10 mL,用乙酸乙酯提取2次,每次15 mL,合并醋酸乙酯提取液,将提取液蒸干,残渣加甲醇1 mL使溶解,作为供试品溶液。取茵陈对照药材1 g,加甲醇20 mL,超声处理30 min,滤过,滤液蒸干,残渣加甲醇1 mL使溶解,作为对照药材溶液。取按照处方工艺制成的不含茵陈的样品,同法制成阴性对照液。按照TLC法(《中国药典》2015版四部通则0502)试验分别吸取上述溶液5~10 μL,分别点同一硅胶G薄层板上,以乙酸丁酯·甲酸-水(7∶2.5∶2.5)为展开剂,展开,取出,晾干。置紫外灯(365 nm)下检视[16-17]。结果见图4。供试品与对照药材在相同位置上显相同颜色的荧光斑点,阴性对照品无干扰。

图4 茵陈定性鉴别图Fig 4 Yin qualitative identification chart
2.2.2 党参的定性鉴别 取口服液10 mL,加水饱和的正丁醇提取2次,每次10 mL,合并两次正丁醇液,将其蒸干,残渣加甲醇1 mL溶解,作为供试品溶液。另取党参对照药材1 g,先加少许水使湿润,再加正丁醇10 mL,超声处理15 min,进行滤过,将滤液蒸干,残渣加甲醇1 mL溶解,作为对照药材溶液。再按处方比例,取按照相同制备工艺制成的缺党参的样品,同法制成阴性对照液。按照(20l5年版《中华人民共和国药典》四部通则0502)试验,吸取上述溶液各5~10 μL,分别点于同一硅胶G薄层板上,以正丁醇-冰醋酸-水(7∶1∶0.5)为展开剂,展开,取出,晾干,随后喷上10%硫酸乙醇溶液,在105 ℃条件下加热,直至斑点显色清晰[18]。结果见图5。供试品与对照药材在相应位置上显相同颜色的斑点,阴性对照无干扰。
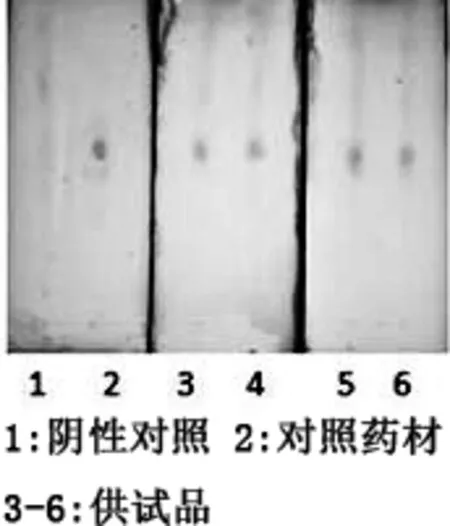
图5 党参定性鉴别图
2.2.3 淫羊藿的定性鉴别 取口服液10 mL,加甲醇20 mL,摇匀后离心,取出上层清液,蒸干,残渣加甲醇1 mL溶解,作为供试品溶液。取同工艺制备的缺淫羊藿的样品口服液,同法制成阴性对照溶液。另取适量淫羊藿苷对照品,加甲醇制成0.5 mg/mL的溶液,作为对照品溶液。吸取上述溶液各5~10 μL,分别点于同一硅胶G薄层板上,以乙酸乙酯-丁酮-甲酸-水(10∶1∶1∶1)为展开剂,展开后取出、晾干,置于紫外光灯(365 nm)下检视[19]。结果见图6。供试品色谱与对照品色谱相应的位置上,显相同颜色的荧光斑点,阴性对照无干扰。

图6 淫羊藿定性鉴别图Fig 6 Epimedium qualitative identification map
2.2.4 高效液相色谱法测香豆素含量 色谱条件:色谱柱:Agilent ZORBAX SB-C18(250 mm×4.6 mm,5 μm);流动相:乙腈-水(34∶66);检测波长:340 nm;流速:1 mL/min;柱温:25 ℃。
对照品溶液的制备:精密称取滨蒿内酯6.8 mg,置100 mL量瓶中,加甲醇60 mL超声溶解30 min,加甲醇至刻度线,摇匀即得对照品溶液。
供试品溶液的制备:精密吸取口服液1 mL,置100 mL量瓶中,加甲醇60 mL超声溶解30 min,随后加甲醇稀释至刻度线,摇匀,经0.45 μm微孔滤膜滤过,即得供试品溶液。
系统适应性实验:精密吸取供试品溶液与对照品溶液各10 μL,按色谱条件进行测定。结果显示,滨蒿内酯主峰保留时间在8.4 min,供试品主峰保留时间与其一致,并且与其他组分分离良好。口服液高效液相色谱图见图7,滨蒿内酯高效液相色谱图见图8。
线性关系考察:精密吸取68 μg/mL滨蒿内酯对照品溶液1、5、10、15、20 μL,按上述色谱条件测定峰面积。以峰面积为纵坐标,绝进样量为横坐标,绘制标准曲线,得回归方程为:Y=6×106X+18263,r=1。结果表明,滨蒿内酯在6.8~136 μg范围内与峰面积有良好的线性关系。
精密度试验:精密吸取68 μg/mL滨蒿内酯对照品溶液10 μL,按照色谱条件,重复进样6次,测定其峰面积,结果RSD为0.58%,表明仪器精密度良好。
稳定性试验:取同一供试品溶液,分别于配制后0、2、、6、24 h进样10 μL,测定峰面积,结果其RSD为0.63%,表明供试品溶液在24 h内稳定。
重复性试验:取同一口服液按上述供试品制备方法制得6份供试品溶液,各进样10 μL,记录峰面积,并计算香豆素含量,结果RSD为1.82%,表明方法重复性良好。
回收率试验:采用加样回收法,精密吸取已知含量的口服液1 mL,共6份,分别精密加入滨蒿内酯对照品0.345、0.351、0.432、0.445、0.518、0.528 mg。按供试品制备方法制成加样回收供试液,分别进行含量测定,计算回收率[20]。结果平均回收率为98.12%,RSD为1.19%。表明方法回收率良好。结果见表8。
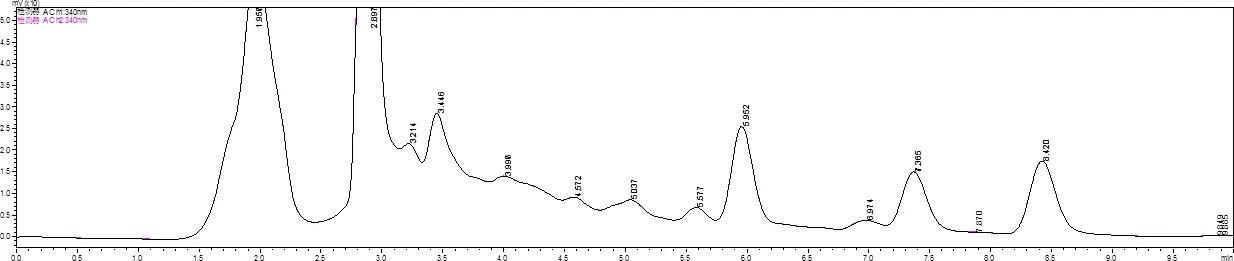
图7 口服液高效液相色谱图Fig 7 Oral liquid high performance liquid chromatography
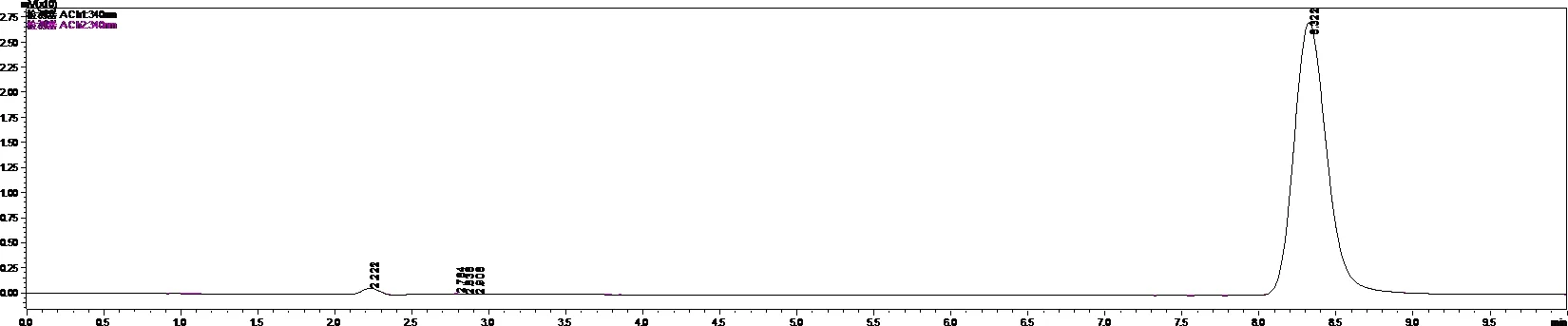
图8 滨蒿内酯高效液相色谱图Fig 8 scopolactone high performance liquid chromatography
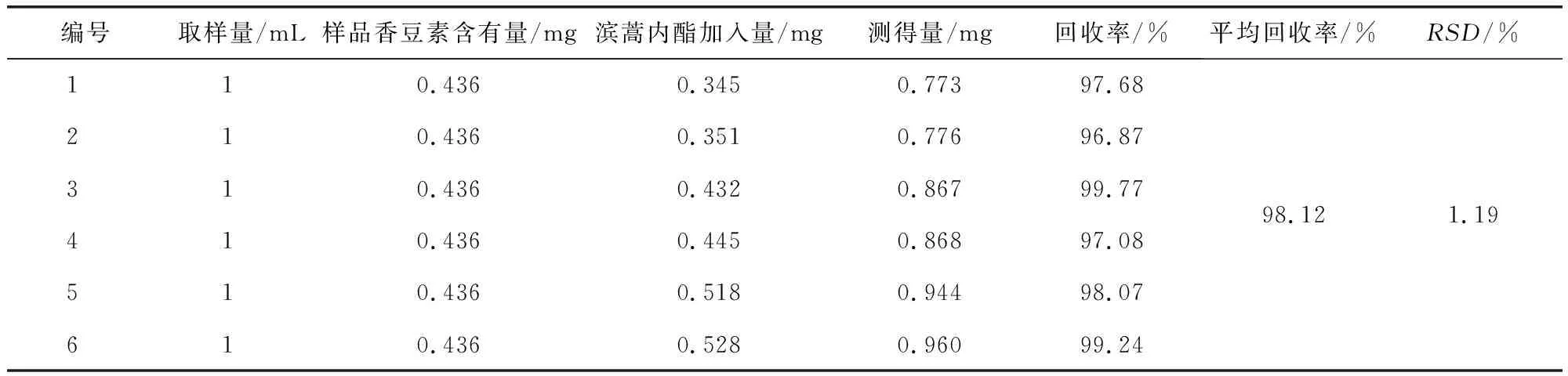
编号取样量/mL样品香豆素含有量/mg滨蒿内酯加入量/mg测得量/mg回收率/%平均回收率/%RSD/%110.4360.3450.77397.68210.4360.3510.77696.87310.4360.4320.86799.77410.4360.4450.86897.08510.4360.5180.94498.07610.4360.5280.96099.2498.121.19
样品测定:取三份口服液按供试品制备方法制成供试品溶液,进样10 μL测定峰面积,每份样品测定2次,以2次测定结果的平均值作为测定值,计算香豆素含量。结果分别为0.435、0.439、0.434 mg/mL。
3 讨 论
3.1 制备工艺优化 本实验在进行口服液制备工艺优化试验前,参考了常明向等[15]瘟必清口服液制备工艺研究(君药茵陈)、黄雄等[16]栀子-茵陈药对提取工艺研究和肖琼等[13]中药醇沉工艺的关键影响因素初步确定了本口服液提取工艺的影响因素:浸泡时间、药液相对密度、煎煮时间、乙醇浓度、料液比,中并通过以上因素进行预试验后发现,料液比、煎煮时间、乙醇浓度三个因素对本口服液制备工艺的影响较大。浓缩药液相对密度在1.02~1.05 g/mL,浸泡时间在30 min适宜。如果药液太浓,会导致进行醇沉时药液凝固较多,最后影响口服液质量。先对料液比、煎煮时间、乙醇浓度进行单因素水平筛选,试验时先用大梯度进行筛选,找出合适范围后,在范围内逐步将梯度缩小,进行制备工艺的优化。单因素筛选完成后,再结合正交试验法,进一步筛选出最佳工艺。综合筛选提取工艺中的主要影响因素,使优选的提取工艺科学合理,并能有效反映该药对药效物质的影响和变化规律,并且通过多次平行试验可以减少误差,更具科学性和参考价值。可以为今后口服液工艺优化提供参考。
3.2 质量标准研究 口服液质量标准的创建一般分为两个部分。第一部分为定性鉴别,第二部分为定量检测。国内外至今有关口服液质量标准创建的研究一般都公认这两个部分可以把控口服液的质量。在薄层色谱中,由于待检样品为口服液,故不能直接按照中国药典上的鉴别方法进行定性测定。应同时结合文献,用相应的方法将口服液样品制成供试品,再进行定性鉴别。本试验参考李建民等[12]在创建清肝利黄口服液质量标准中,对茵陈进行薄层鉴别;张玉杰等[10]在创建参芪苓口服液的薄层色谱鉴别中,对党参进行薄层鉴别;陈林等[11]抗氧化口服液质量标准研究中对淫羊藿进行薄层鉴别,作为定性部分。参考万丽等[7]茵陈中总香豆素的含量测定中对茵陈进行HPLC法测定含量,作为定量部分。因而选择茵陈、党参、淫羊藿作为定性对象。选择香豆素含量作为定量对象。由此创建了本口服液质量标准。经试验后发现,展开剂种类及其比例应尽量以药典为主,这样各试样中的组分可以达到较好的分离。在用HPLC法测定含量过程中,对色谱条件进行了探索,其中流动相在甲醇与水、乙腈与水中进行探索,发现选择流动相为乙腈:水(34∶66),时,可以使本试验中口服液各组分达到良好的分离。通过对单因素进行实验,找出单因素最佳水平,并结合正交实验分析法,筛选出最佳工艺为料液比1∶20,煎煮时间2 h,乙醇浓度50%。用TLC法定性鉴别口服液中茵陈、党参、淫羊藿,均有较好的结果。高液相色谱法中,口服液中主峰与杂峰有较好的分离,滨蒿内酯保留时间适宜。口服液与滨蒿内酯均在8.4 min左右出峰,最后测得口服液中香豆素含量平均为0.436 mg/mL。
