HPLC法同时测定野马追药材中绿原酸、新绿原酸、隐绿原酸的含量
2018-05-22包宜康顾亚琴吴小峰郦红岩
杨 琴,包宜康,顾亚琴,郭 昀,吴小峰,郦红岩
(1.江苏中兴药业有限公司,江苏镇江,212009;2.江苏吉贝尔药业股份有限公司,江苏镇江,212009)
野马追为菊科植物轮叶泽兰Eupatorium lindleyanum DC.的干燥地上部分,味苦,性平,归肺经,具有化痰止咳平喘之功效,常用于治疗痰多咳嗽气喘等症[1]。现代研究表明野马追中主要含有黄酮类、生物碱类、挥发油类、香豆类素、有机酸类及多种微量元素等化学成分[2-4]。目前对野马追的研究主要集中在黄酮、生物碱等大类[5-6],而对有机酸类成分的研究较少,文章在前期研究的基础上,参考相关文献,对野马追药材中绿原酸、新绿原酸、隐绿原酸三种有机酸类成分进行了定量检测,为野马追的质量控制及后续研究开发等奠定实验基础。
1 仪器与材料
1.1 仪器
HPLC(LC-20A系统、SPD-20A检测器,岛津株式会社);N2000色谱工作站(浙大智达);BAS124S电子天平(德国Satorius);HH恒温水浴锅(金坛中大仪器厂)。
1.2 材料
绿原酸对照品(中国食品药品检定研究院,供含量测定用,批号:110753-201415)、新绿原酸、隐绿原酸对照品(上海源叶生物科技有限公司,批号:PA0819RA13、2F0226BA14),色谱级乙腈(德国MERCK),水为公司自制注射用水,其余试剂均为分析纯。
野马追药材原产地江苏盱眙,由亳州吉贝尔现代中药饮片科技有限公司提供,经江苏吉贝尔药业股份有限公司魏福荣高级工程师鉴定为野马追。
2 方法与结果
2.1 色谱条件
Phenomenex C18(250×4.6mm,5μm);流动相:乙腈—0.2%醋酸水溶液(11 ∶89);检测波长:327nm;柱温:30℃;流速:1.0mL/min;进样 20μL,理论板数按绿原酸峰计算应不低于2500。
2.2 溶液的制备
2.2.1 对照品溶液的制备
称取三种对照品适量,精密称定,加流动相制成每1mL分别含新绿原酸0.82mg、绿原酸0.68mg、隐绿原酸 0.58mg 的混合溶液,作储备液备用。
2.2.2 供试品溶液的制备
将野马追药材粉碎,过筛,精密称取1.0g,加50mL石油醚提取以除色素或一些小分子化合物,挥干石油醚,药渣加纯化水20mL,水浴回流2次,每次0.5小时,滤过,合并两次滤液,置50mL量瓶中,加流动相定容至刻度,摇匀即得。
2.3 方法学考察
2.3.1 方法专属性
按“2.1色谱条件”下进样分析,得对照品溶液与供试品溶液的色谱图如图1所示,新绿原酸、绿原酸、隐绿原酸在此条件下分离度良好。
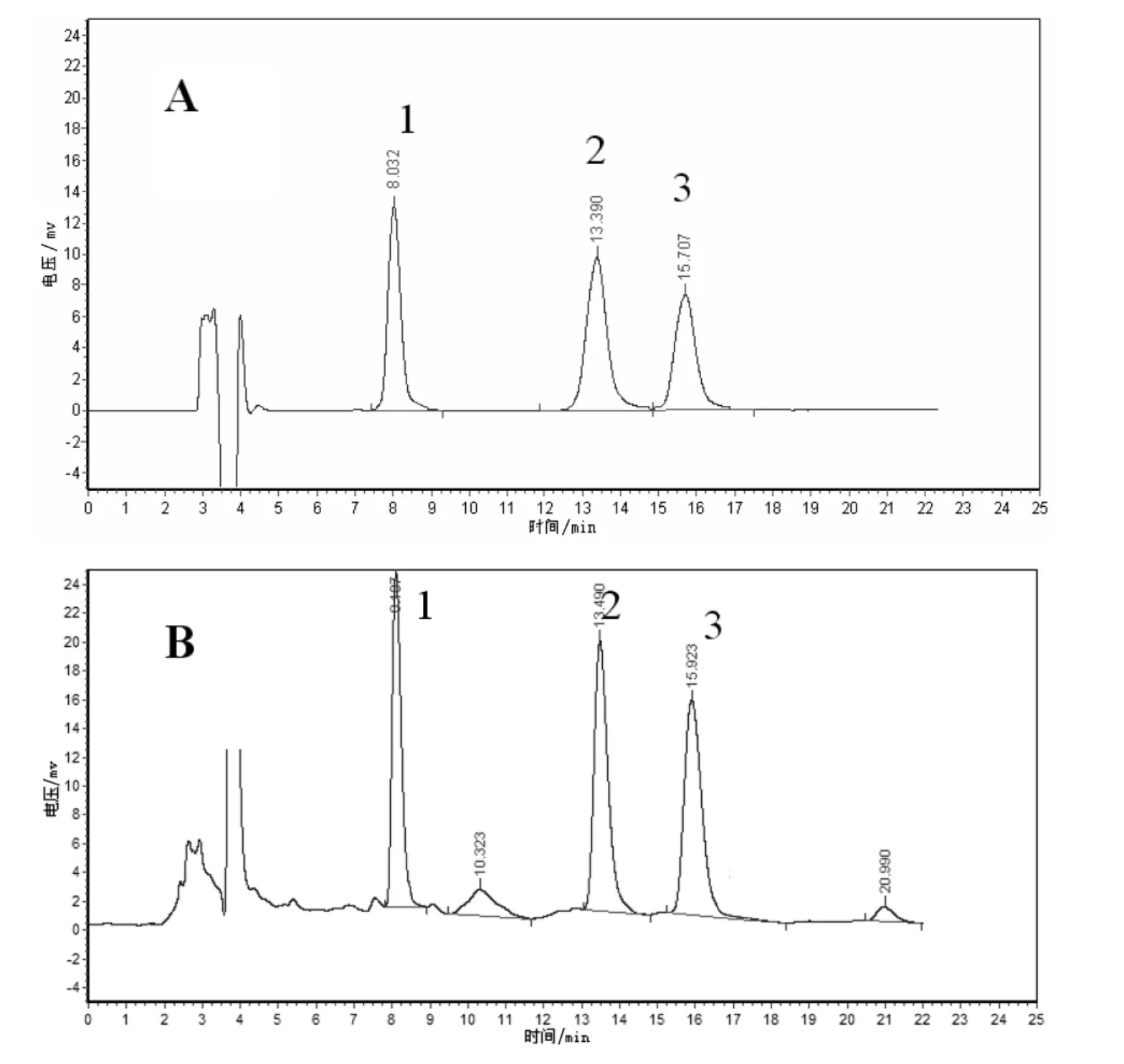
图1 对照品及供试品溶液色谱图(A-对照品溶液;B-供试品溶液;1.新绿原酸2.绿原酸3.隐绿原酸)Fig.1 The chromatogram of the reference solution and the test solution(A-Reference solution;B-Test solution;1.Neochlorogenic acid 2.Chlorogenic acid 3.Cryptochlorogenic acid)
2.3.2 线性关系的考察
分别精密吸取新绿原酸、绿原酸、隐绿原酸的储备对照品溶液0.25、0.5、1、3、5mL至10mL量瓶中,制成新绿原酸、绿原酸、隐绿原酸浓度分级为0.0205、0.041、0.082、0.246、0.41mg/mL,0.017、0.034、0.068、0.204、0.34mg/mL 及 0.0145、0.029、0.058、0.174、0.29mg/mL的系列对照品溶液,按“2.1色谱条件”操作进样分析,以峰面积(Y)对进样量(μg)(X)进行线性回归,得三种成分的回归方程依次分别为 Y=13821X+18.17(r=0.9999),Y=17675X+10.914(r=0.9993),Y=15157X+13.241(r=0.9999),且新绿原酸、绿原酸及隐绿原酸分别在 0.41~8.2μg、0.34~6.8μg、0.29~5.8μg范围内线性关系良好。
2.3.3 精密度试验
精密吸取新绿原酸、绿原酸、隐绿原酸浓度分别为 0.082 mg/mL、0.068 mg/mL、0.058mg/mL的混合对照品溶液20μL,连续进样6次,记录峰面积,结果新绿原酸、绿原酸、隐绿原酸的RSD分别为0.87%、1.15%、1.04%,表明精密度良好。
2.3.4稳定性试验
称取野马追药材适量,按“2.2.2供试品溶液的制备”下制备供试品溶液,分别在0、2、4、6、8、12、24小时测定峰面积,记录峰面积,得新绿原酸、绿原酸、隐绿原酸的峰面积RSD分别为1.36%、0.93%、1.25%,表明供试品在24小时内稳定。
2.3.5 重复性试验
称取野马追药材6份,精密称定,按“2.2.2供试品溶液的制备”项下方法制备供试品溶液,结果得供试品中新绿原酸、绿原酸、隐绿原酸平均含量分别为2.815mg/g、3.381mg/g、2.972mg/g,含量RSD分别为1.21%、1.06%、1.18%。
2.3.6 加样回收率测定
取已知含量的野马追药材6份,每份约0.5g,精密称定,加入2mL重新配制新绿原酸、绿原酸、隐绿原酸对照品溶液的浓度分别为0.7113mg/mL、0.8476mg/mL、0.7511mg/mL的混合对照品溶液,按“2.2.2供试品溶液的制备”项下方法制备供试品溶液,并按“2.1色谱条件”下方法进样分析,得供试品溶液中各成分的回收率如表2所示。
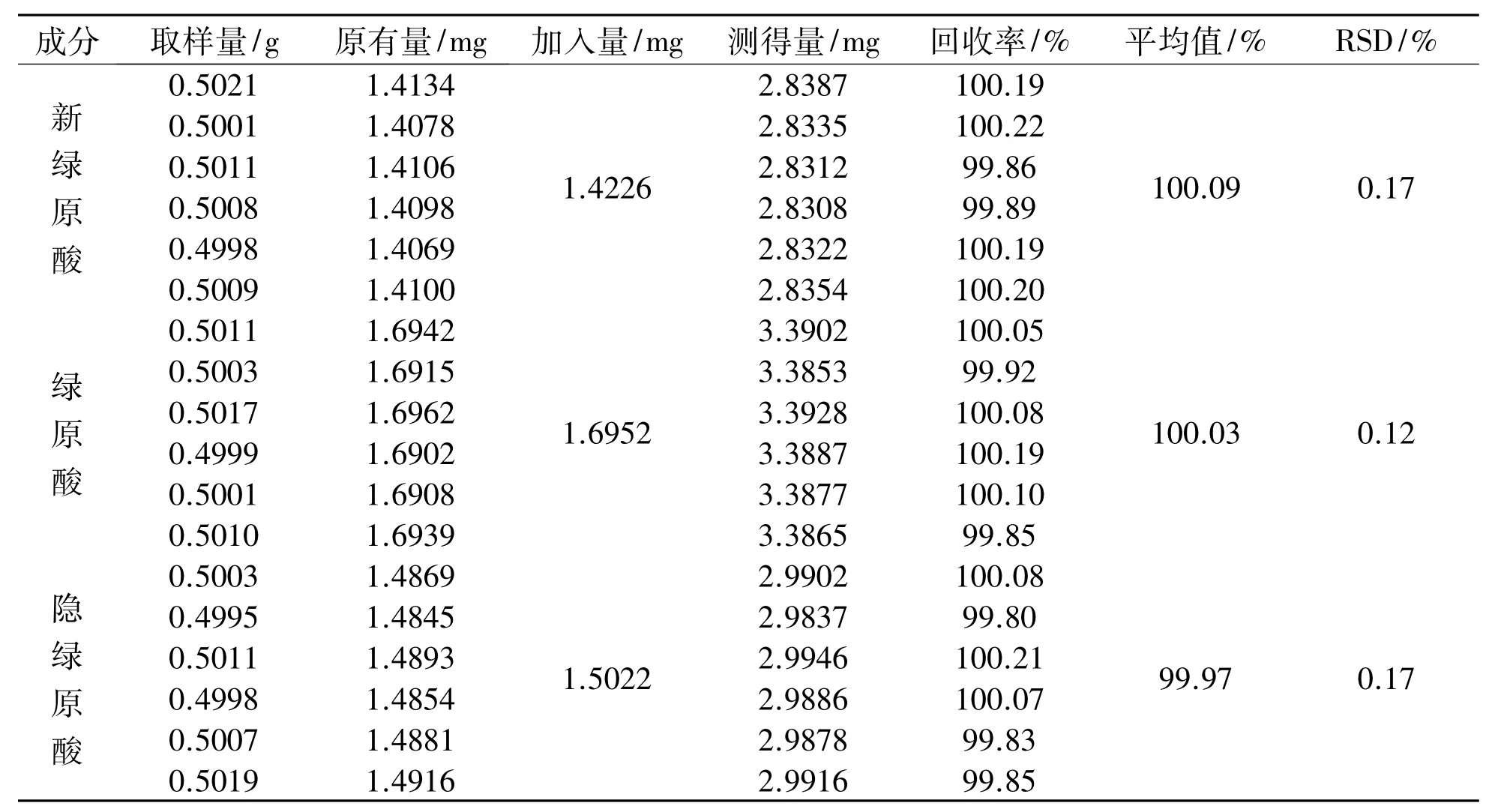
表2 加样回收率试验结果(n=6)Table 2 Results of recovery test(n=6)
2.4 样品测定
分别称取不同批次的野马追药材1g,精密称定,按“2.2.2供试品溶液的制备”项下操作,并按“2.1色谱条件”下方法进样分析,得不同批次的野马追药材中新绿原酸、绿原酸、隐绿原酸的含量数据见表3。
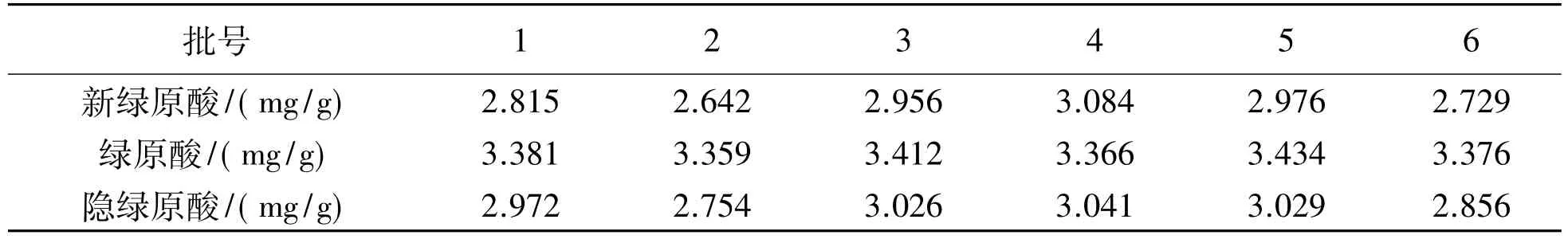
表3 样品含量测定结果Table 3 Determination results of contents in samples
3 讨论
在前期的实验考察中,将绿原酸、新绿原酸和隐绿原酸分别配制一定浓度的对照品溶液进行紫外全波长扫描,结果发现绿原酸、新绿原酸和隐绿原酸均在208nm和327nm左右处有最大吸收峰,而后分别选择208nm和327nm进行绿原酸、新绿原酸和隐绿原酸混合对照品的HPLC检测,发现在208nm波长处检测时,杂峰较多,绿原酸、新绿原酸和隐绿原酸分离度较差,干扰其含量的测定,而在327nm处绿原酸、新绿原酸和隐绿原酸分离度良好,测定无其他成分干扰,故最终选择327nm作为检测波长。
中药材及中药制剂中同时测定的新绿原酸、绿原酸、隐绿原酸含量的报道相对较多[7-10],但大多采用的洗脱方法较为复杂(梯度或分段变波长),笔者通过前期方法考察,筛选乙腈-水系统等度洗脱来进行含量测定,方法具有良好的精密度与稳定性,能够较好地满足实验测定要求。
本研究工作中,初步选择甲醇-水系统和乙腈-水系统分别对野马追供试品溶液进行测定,发现采用乙腈-水系统各成分的分离度及基线的平稳性均优于甲醇-水系统,故初步选择乙腈-水系统作为流动相,同时加入了醋酸进一步调整峰型,最终在乙腈-0.2%醋酸水(11:89)的条件下,各成分分离度、出峰时间及峰型均较好。
笔者在研究过程中分别进行了水、甲醇、乙醇、50%乙醇等不同提取溶剂,加热回流和超声提取等不同的提取方法,以及在0.5、1、1.5h的不同提取时间对提取成分的影响,由于绿原酸类成分的特殊结构,使用甲醇、乙醇、50%乙醇等溶剂提取时,提取出得成分较多,各目标峰之间很难达到基线分离,且相互间有干扰。由于其在热水中的溶解度大于甲醇、乙醇中的溶解度,因此确定先用石油醚脱脂处理,再用纯化水回流提取2次,每次0.5小时,以保证有效成分能提取完全,且避免长时间的高温损坏。
参考文献:
[1]国家药典委员会.中华人民共和国药典一部[S].北京:中国医药科技出版社,2015:313.
[2]吴双庆,孙群,褚纯隽,等.野马追化学成分[J].中国中药杂志,2012,37(07):937-940.
[3]仲欢欢,方诗琦,陈亚军,等.野马追化学成分及其抗炎活性[J].中成药,2017,39(02):329-333.
[4]褚纯隽,任慧玲,吴天威,等.野马追的化学成分及其解热作用研究[J].天然产物研究与开发,2015,27(05):816-821.
[5]李音,吕秀阳.野马追总生物碱提取工艺研究[J].天然产物研究与开发,2010,22:130-133.
[6]田静,夏玉凤,房克慧.HPLC法同时测定苍耳类药材中8种酚酸类成分的含量[J].中药材,2013,36(10):1623-1626.
[7]贺宗毅,梁旭明,张小梅,等.多指标评价技术研究不同产地野马追药材质量[J].中药材,2017,40(07):1647-1650.
[8]陈芳,邓雁如,郭利平.HPLC法同时测定金银花及金芪降糖片中9种成分的含量[J].天津中医药,2014,31(03):168-172.
[9]何兵,杨世艳,张燕,等.HPLC法同时测定青银注射液中8种活性成分的含量药物[J].分析杂志,2012,32(02):224-228.
[10]朱粉霞,张亚丽,汪晶,等.一测多评法测定金银花复方制剂中新绿原酸、绿原酸和隐绿原酸[J].中成药,2013,35(12):2666-2671.
