Box-Behnken Design-响应面法优化绿原酸转化为新绿原酸的工艺研究*
2017-10-26温建辉倪付勇王雪晶宋亚玲王振中
温建辉,倪付勇,王雪晶,李 明,宋亚玲,王振中,萧 伟
(江苏康缘药业股份有限公司 连云港 222000)
Box-Behnken Design-响应面法优化绿原酸转化为新绿原酸的工艺研究*
温建辉,倪付勇,王雪晶,李 明,宋亚玲,王振中,萧 伟**
(江苏康缘药业股份有限公司 连云港 222000)
利用Box-Behnken-响应面法优化绿原酸转化为新绿原酸的工艺条件。在单因素实验基础上,采用Box-Behnken Design实验设计,考察反应温度、反应时间及pH值对新绿原酸产率的影响,优化绿原酸转化为新绿原酸的工艺参数,得到模型预测公式。优化条件为:反应温度107℃,反应时间60 min,pH值为4.72时新绿原酸产率为64.20%,与模型预测值接近,方程拟合良好。采用优选工艺制备新绿原酸并精制纯化,分别运用HPLC、1H-NMR、13C-NMR、ESI-MS等方法对其进行含量测定和结构表征,结果表明纯化后纯度达98.78%,收率为87.37%。
绿原酸 新绿原酸 Box-Behnken Design响应面法 结构鉴定

图2 绿原酸转化为新绿原酸反应式
1 仪器与材料
1.1 仪器
分析液相:Agilent 1260高效液相色谱仪(美国Agilent公司,250 mm×4.6 mm,5 μm),配自动进样器、四元泵、MWD检测器,制备液相:Agilent 1260高效液相色谱仪(美国Agilent公司),四元泵、MWD检测器,制备柱(美国Agilent公司,21.2 mm×250 mm);Bruker-AV-400型核磁共振光谱仪;AE240电子分析天平(瑞士Mettler公司),实验室PH计FE20 Plus(梅特勒-托利多仪器上海有限公司),石英三口烧瓶(广州市精科仪器有限公司)。
1.2 实验材料
绿原酸(自制,批号:130809,纯度为99.14%),新绿原酸(批号MUST-10091501,纯度>98%,成都曼斯特生物科技有限公司提供),甲醇(色谱纯,Oceanpak,瑞典),甲酸、浓盐酸(分析纯,南京化学试剂有限公司),双蒸水(自制)。
2 新绿原酸的测定方法
2.1 对照品溶液的制备
称取新绿原酸对照品适量,精密称定,置棕色容量瓶中,加50%甲醇定容制成新绿原酸浓度为0.2 mg·mL-1的对照品溶液。
2.2 供试品溶液的制备
分别精密称取以下各工序制备的新绿原酸粗品5.0 mg,置于25 mL容量瓶中,用50%甲醇溶解,定容至刻度即得。
2.3 色谱条件
2.3.1 基本条件
色谱柱为Acuity C18(250mm×4.6mm,5μm),流动相甲醇(A)-0.5%甲酸溶液(B),流速1.0 mL·min-1。梯度洗脱条件:0-40 min,15%-50%A;40-52 min,50%-100%A。进样体积10 μL,柱温30℃,检测波长326 nm[18-20]。
2.3.2 线性关系考察
取新绿原酸对照品适量,精密称定,加50%甲醇制成所需浓度的对照品溶液,作为储备液(2.6 mg·mL-1)。取储备液0.25、0.5、1.0、2.0、4.0、8.0 mL,置10 mL量瓶中,分别用50%甲醇稀释至刻度,摇匀,分别进样,测定,以峰面积为纵坐标(Y),对照品浓度(mg·mL-1)为横坐标(X),绘制标准曲线得回归方程为:Y=26.306X+0.395 4(r=1.000 0),新绿原酸在0.065-2.08 mg·mL-1范围内具有良好的线性关系。
2.3.3 精密度试验
精密吸取对照品溶液10 μL,按“2.3.1”项下色谱条件,进样,测定,连续6次。以新绿原酸的峰面积计算,RSD为1.2%,结果表明,仪器精密度良好。
2.3.4 稳定性试验
精密吸取“2.2”项供试品溶液,分别于制备后0、2、4、6、8、10、12、24 h分别进样,按“2.3.1”项色谱条件测定,以新绿原酸峰面积计算,结果RSD为0.84%,结果表明供试品溶液放置24 h稳定。
3 单因素试验
新绿原酸转化的影响因素主要有反应时间、反应温度、pH值、溶剂浓度(甲醇)、绿原酸浓度等,通过预实验,从转化的角度出发,将绿原酸浓度定为0.25 mg·mL-1,溶剂为50%甲醇溶液,结果显示反应时间、反应温度、pH值对新绿原酸含量影响较大。因此,对反应时间、反应温度、pH值进行设计单因素考察,每个单因素实验平行考察三次,取含量均值作为测定结果。
3.1 温度对新绿原酸含量的影响
取20 mg绿原酸用4倍量50%甲醇溶解,考察反应时间为60 min,pH值为5.0条件下,不同的反应温度(90℃,100℃,110℃,120℃,130℃)对新绿原酸含量的影响。以“2.3.1”项下的条件测定当中新绿原酸的含量,含量变化情况见图3。结果表明,随着温度的升高,新绿原酸含量随之增加,当温度超过110℃时,新绿原酸含量反而下降。因此,确定反应温度为110℃。

图3 反应温度单因素考察

图4 反应时间单因素考察

图5 pH值单因素考察
3.2 时间对新绿原酸含量的影响
取20 mg绿原酸用4倍量50%甲醇溶解,考察反应温度为100℃,pH值为5.0条件下,不同反应时间(30、60、90、120、150 min)对新绿原酸含量的影响。以“2.3.1”项下条件测定当中新绿原酸的含量,含量变化情况见图4。结果表明,随着时间的增加,新绿原酸含量随之增加,当反应时间超过60 min时,新绿原酸含量下降。因此,确定反应时间为60 min。

表1 响应面实验设计

表2 Box-Behnken试验设计与结果
3.3 PH值对新绿原酸含量的影响
取20 mg绿原酸用4倍量50%甲醇溶解,考察反应时间为60 min,反应温度110℃,不同的pH(3.0,4.0,5.0,6.0,7.0)对新绿原酸含量影响,以“2.3.1”项下条件测定当中新绿原酸的含量,含量变化情况见图5。结果表明,随着pH值的增大,新绿原酸含量随之增加,当pH大值于5.0时,新绿原酸含量下降。因此,确定pH值为5.0。
3.4 新绿原酸转化工艺优选
在单因素实验的基础上应用响应面法对新绿原酸的转化工艺进行优化,以反应温度(A)、反应时间(B)、pH值(C)为考察因素,根据Box-Behnken设计原理,每因素设3个水平,用代码值-1,0,1表示,因素水平见表1,实验设计及结果见表2。以粗品中新绿原酸的含量为评价指标,采用Design-Exoect V8.0.5软件对综合评分结果进行多元线性回归和二项式方程拟合,得回归方程:含量=62.17-4.54A-1.44B-2.51C+0.27AB+3.80AC-1.82BC-11.26A2-3.57B2-5.76C2,相关系数R2=0.969 6,说明建立的二次项模型与实验拟合较好。由表3响应面二次回归方程方差分析结果所示,模型P<0.01,效应面模型达到极显著水平,影响新绿原酸转化因素的主次顺序为A>C>B,其中因素A反应温度影响极显著(P<0.001),因素C(pH)影响显著(P<0.05),失拟项不显著(P>0.05),因素A和C的交互作用对新绿原酸的转化是显著的,表明二次方程预测值与实际值吻合度较高。方程对应的等高线、三维效应图见图6。

表3 Box-Behnken实验方差分析
3.5 新绿原酸转化工艺验证试验
通过求解回归方程得到最佳转化工艺参数为:反应温度107.49℃,反应时间58.60 min,pH值为4.72,新绿原酸含量预测值为63.19%。结合实际试实际操作,确定反应温度为107℃,反应时间60 min,pH值为4.72,以该参数进行3次验证试验,结果显示,采用该工艺参数进行转化,新绿原酸的含量均值为64.20%,RSD值<2%,与预测值的相对偏差为1.56%,基本与模型预测值一致,适合新绿原酸粗品的制备。新绿原酸粗品A(峰1为新绿原酸)和新绿原酸对照品B色谱图(图7)。
4 新绿原酸的制备
取绿原酸10.0g,以“3.5”项下的优选条件进行反应,最终得到新绿原酸粗品9.12 g,用50%的甲醇溶解,离心取上清液进样,以10%乙腈为流动相,流速20 mL·min-1,进样量 800 μL,柱温为室温,检测波长326 nm,多次进样制备,收集液浓缩、干燥后得到新绿原酸的量为5.12 g,收率为87.37%。
5 新绿原酸质量分数测定
取“4”项下制备的新绿原酸样品,按“2.3.1”项下色谱方法测定,用面积归一化法计算,确定新绿原酸的质量分数为98.78%,新绿原酸样品经ESI-MS分析,m/z:353.090 4[M-H]-,计算相对分子量为354。
6 结构鉴定
新绿原酸,白色粉末,ESI-MSm/z:353[M-H]-。1H-NMR(400 MHz,DMSO-d6)δ:1.86-2.01(4H,m,H-2,H-6),3.78(1H,m,H-4),4.12(1H,m,H-3),5.21(1H,m,H-5),6.26(1H,d,J=16.0 Hz,H-8′),6.77(1H,d,J=8.0 Hz,H-5′),6.95(1H,dd,J=2.0,8.0 Hz,H-6′),7.05(1H,d,J=2.0 Hz,H-2′),7.50(1H,d,J=16.0 Hz,H-7′);13C-NMR(100 MHz,DMSO-d6)δ:35.1(C-2),38.6(C-6),70.3(C-3),70.6(C-4),67.3(C-5),72.6(C-1),114.5(C-2′),114.9(C-8′),115.8(C-5′),121.1(C-6′),125.7(C-1′),144.3(C-3′),144.7(C-7′),145.7(C-4′),166.3(C-9′),175.4(COOH)。以上数据与文献[8]报道的新绿原酸一致。
7 总结与讨论
新绿原酸为热毒宁注射液中有效活性成分之一,是一种咖啡酰奎宁酸类化合物,现代研究表明咖啡酰奎宁酸类化合物在药物、食品、饲料添加剂以及化妆品中具有较高的潜在价值[14]。药理实验也表明它具有抗氧化活性、治疗炎症、抑制微生物和病毒活性、酶抑制作用等多种生物活性[21]。鉴于新绿原酸较好的药理活性,对该化合物研究具有较大的实用价值,因此,本实验采用Box-Behnken Design-响应面法建立一种快速大量制备高纯度的新绿原酸的方法,且通过实验方法验证该工艺稳定可行,为新绿原酸的制备及其下一步药理药效的深入研究提供保障。

图6 自变量A,B,C之间交互作用与应变量R1含量等高线、响应面图

图7 新绿原酸粗品(A)和新绿原酸对照品(B)的HPLC图
1 柴兴云,窦静,贺清辉,等.山银花中酚酸类成分研究.中国天然药物,2004,2(6):339-340.
2 唐陆平,何蓉蓉,李怡芳,等.热毒宁注射液对细菌内毒素性脂多糖致热大鼠的解热作用研究.中国中药杂志,2013,38(14):2374-2377.
3 樊宏伟,李英斌,孙敏,等.金银花中有机酸类成分抗血栓作用研究.中药药理与临床,2007,23(3):34-36.
4 邱葵,刘宇红,孔繁翠,等.金银花体外抗结核活性研究.世界科学技术-中医药现代化,2009,11(6):876-879.
5 汤喜兰,刘建勋,李磊.中药有机酸类成分的药理作用及在心血管疾病的应用.中国实验方剂学,2012,18(5):243-246.
6 李石平,王志鑫,顾睿,等.金银花中抗手足口病HEV71活性成分的虚拟筛选.中药药理与临床,2015,31(3):67-70.
7 宋亚玲,王红梅,倪付勇,等.金银花中酚酸类成分及其抗炎活性研究.中草药,2015,46(4):490-495.
8 倪付勇,刘露,宋亚玲,等.金银花中抗补体活性酚酸类成分的研究.中国中药杂志,2015,40(2):269-274.
9 孙兰,刘艾林,王振中,等.热毒宁注射液及其组分对流感病毒神经氨酶的抑制作用研究.现代药物与临床,2014,29(1):27-31.
10张露,陈豆弟.绿原酸提取工艺研究进展.杭州化工,2012,43(4):4-6.
11闫巧娟,韩鲁佳,江正强,等.金银花中绿原酸提取纯化工艺的优化.中国农业大学学报,2002,7(2):22-26.
12张运典,陈玉海.金银花中绿原酸取工艺研究.中成药,2013,35(7):1564-4566.
13高红宇,金万勤,郭立玮.不同精致工艺对金银花水提液中绿原酸含量的影响.世界科学技术-中医药现代化,2010,12(2):241-244.
14 Dawidowicz A L,Typek R.Thermal stability of 5-O-caffeoylquinic acid in aqueous solutions at different heating conditions.J Agric Food Chem,2010,58(24):12578-12584.
15 Dawidowicz A L,Typek R.The influence of PH on the thermal stability of 5-O-caffeoylquinic acid in aqueous solutions.Eur Food Res Technol,2011,233(2):223-232.
16 Dawidowicz A L,Typek R.Formation of ester and amine derivatives of 5-O-caffeoylquinic acid in the process of its simulated extraction.J Agric Food Chem,2012,60(50):12289-12295.
17 Dawidowicz A L,Typek R.Thermal transformation oftrans-5-O-caffeoylquinic acid(trans-5-CQA)in alcoholic solutions.Food Chem,2015,167:52-60.
18朱粉霞,贾晓斌,李秀峰,等.UPLC法同时测定胆木注射液中原儿茶酸、新绿原酸、绿原酸和隐绿原酸.中草药,2013,44(5):571-573.
19毕宇安,王振中,宋爱华,等.热毒宁注射液高效液相色谱指纹图谱研究及多成分定量分析.世界科学技术-中医药现代化,2010,12(2):298-303.
20倪付勇,宋亚玲,刘露,等.中低压制备色谱制备新绿原酸对照品的研究.世界科学技术-中医药现代化,2015,17(9):1818-1822.
21赵昱,赵军,李湘萍,等.咖啡奎尼酸类化合物研究进展.中国中药杂志,2006,31(11):869-874.
Optimization on Transformation from ChlorogenicAcid to NeochlorogenicAcid by Box-Behnken Design-response Surface Methodology
Wen Jianhui,Ni Fuyong,Wang Xuejing,Li Ming,Song Yaling,Wang Zhenzhong,Xiao Wei
(Jiangsu Kanion Pharmaceutical Co.Ltd.,Lianyungang 222000,China)
Box-Behnken design-response surface methodology was used to optimize the transformation from chlorogenic acid to neochlorogenic acid.Based on single factor experiments,the experiment design were developed by box-benhnhen central composite design with causal factors of the reaction temperature,time and PH to neochlorogenic acid.The optimum transformation conditions were as follow:reaction temperature at 107°C,reaction time of 60 min,the PH of 4.72.Under the optimum extraction technology conditions,the productivity of neochlorogenic acid was 64.20%.Neochlorogenic acid was isolated and purified.The determination and characterization of neochlorogenic acid was detected by HPLC,1H-NMR,13C-NMR and ESI-MS.The results showed that the content of neochlorogenic acid reached to 98.78%and the yield of 87.37%.
Chlorogenic acid,neochlorogenic acid,Box-Behnken design-response surface methodology,structural identification
10.11842/wst.2017.07.026
R284.1
A
新绿原酸为单咖啡酰奎宁酸类化合物,是由咖啡酸的1位和奎宁酸的5位通过酯化反应而形成的天然化合物(结构式见图1),在植物界中分布广泛,为最常见的单咖啡酰奎宁酸类化合物之一。具有抗菌解热[1-2]、抗血栓[3]、体外抗结核活性[4],抗炎、抗氧化、对心血管疾病的作用、抑制血小板聚集[5]等药理作用。现代研究发现,新绿原酸在活性虚拟筛选中与靶蛋白HEV71的结合能为-9.2kcal/mol,具有一定的抑制手足口HEV71病毒活性[6];在抗炎作用方面,新绿原酸对LPS刺激的RAW264.7细胞炎症因子具有一定的抑制作用[7];在抗补体经典途径试验中,新绿原酸的活性要优于阳性药肝素[8];另外,新绿原酸作为热毒宁注射液有机酸的活性成分之一,对H1N1、H3N2、B流感病毒神经氨酸酶表现出良好的抑制作用[9]。
目前,新绿原酸尚无化学合成方法,均从植物中分离纯化得到,但是由于其含量在植物中较低,若要获得大量的高纯度的新绿原酸单体,需要提取大量的药材后利用不同的分离材料对该化合物富集、分离和纯化,工序繁琐,且药材和试剂消耗量大。绿原酸为新绿原酸的同分异构体,在植物中含量高且制备工艺非常成熟[10-13],有研究发现绿原酸在一定条件下可以转化为新绿原酸及其它绿原酸类衍生物[14-17],影响其转化的主要因素有:反应时间、pH值、反应温度。鉴于此,本文拟通过Box-Behnken-响应面法优化绿原酸转化为新绿原酸的最佳条件,为新绿原酸的规模制备提供参考(图2)。
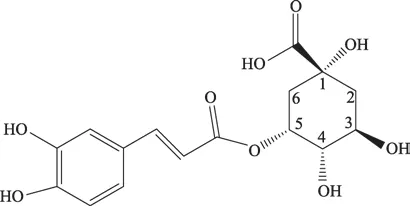
图1 新绿原酸结构式
2015-11-05
修回日期:2016-03-22
* 科学技术部国家“重大新药创制”科技重大专项(2013ZX09402203):现代中药创新集群与数字制药技术平台,负责人:王振中。
** 通讯作者:萧伟,本刊编委,博士,研究员级高级工程师,主要研究方向:中药新药的研究与开发。
(责任编辑:马雅静,责任译审:王 晶)
