鲍恩病27例临床分析
2018-04-28吴晴晴黄春辉肖灿林伟祁强张佩莹刘晓陈卫鑫
吴晴晴, 黄春辉, 肖灿, 林伟, 祁强, 张佩莹, 刘晓, 陈卫鑫
鲍恩病是发生于皮肤或黏膜的早期皮肤原位鳞癌,于1912年由Bowen报道[1]。近年来,鲍恩病发病率有所增加,其诊断和治疗引起了广泛关注,为了进一步掌握本病的特点,提高本病的诊断准确率,现将我们收治的27例鲍恩病资料报道如下。
1 临床资料
1.1 一般资料 2010年6月至2017年6月苏州大学附属第一人民医院收治并经病理活检诊断为鲍恩病患者27例。其中女16例(59.3%),男11例(40.7%),男女比例为1∶1.45;年龄32~89岁,平均年龄63.85岁, 60岁以上占70.4%;病程1~26年。
1.2 临床表现 病灶(皮损)均为单发,其中位于头部5例、躯干部7例、四肢11例,手背、踝部各1例,足部2例。19例皮损较典型,为淡红色或暗红色斑丘疹、斑片或斑块,呈不规则形、圆形、多环形或匍匐形,以角化过度和结痂多见,部分可见白色和淡黄色鳞屑,或棕色、灰色的厚痂,皮损表面平坦、大小不等,直径0.8~11 cm;5例患者皮损表面可见溃疡、糜烂(图1A);2例患者皮损稍高于皮肤表面,呈多环形或不规则形斑块状(图1B);1例患者表现为角化过度性斑块。均伴有瘙痒、7例伴有疼痛。所有患者均未见局部淋巴结及远处转移。

图1 鲍恩病患者病灶表现1A:右小腿内侧4 cm×3.5 cm圆形红色斑块,边界清楚,表面有溃疡,结痂;1B:左下腹部不规则红色斑丘疹,4.5 cm×2.5 cm×2.0 cm,不规则,高出皮面,表面覆有薄层黄色痂皮
1.3 组织病理学表现 镜下见:表皮角化过度或角化不全,颗粒层减少,棘层明显增厚,细胞排列紊乱,全层可见大小不一异形细胞,部分胞核大而深染,有丝分裂象多见,部分散在细胞角化不良,其中2例棘层上部可见空泡细胞,6例可见少许角化不良细胞。基底层完整。真皮浅层有中等密度的淋巴细胞浸润,毛囊、皮脂腺导管及毛囊漏斗部外毛根鞘均有受累。见图2A、2B。
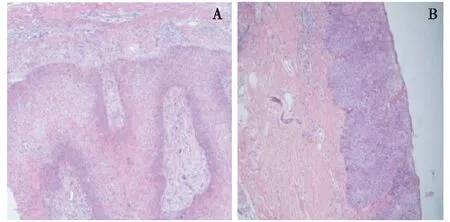
图2 鲍恩病组织病理特征(HE ×100)2A:表皮棘层不良,真皮浅层密集炎症细胞浸润;2B:表皮细胞极性紊乱,细胞异形明显,有角化不良细胞,部分细胞核大深染,核仁明显,可见有丝分裂象,真皮浅层炎症细胞浸润
1.4 误诊情况 27例患者中误诊11例,误诊率为40.7%。其中误诊为湿疹4例(14.8%),银屑病2例(7.4%),基底细胞癌1例(3.7%),Paget病2例(7.4%),脂溢性角化病2例(7.4%)。
1.5 治疗及预后 27例均行手术治疗,切除深度达深筋膜层,切除范围在皮损边缘3~5 cm。随访6~24个月,平均随访时间13个月,仅1例患者复发,行扩大手术切除,随访未见复发。
2 讨论
鲍恩病是一种皮肤肿瘤,病因尚不完全明确。可能与紫外线照射、放射治疗、免疫抑制、遗传等因素有关,过去认为多与砷暴露有关,有种族倾向,白人易发[2]。近年来有研究表明,病毒感染如人乳头状瘤病毒16型[3-4]、梅克尔细胞多瘤病毒[5],或自身免疫性疾病如原发性干燥综合征[6]与该病有关。鲍恩病可能与反复溃疡有关,本组病例中有5例病程较长且反复溃疡。发生机制:一种是微环境学说,反复溃疡可以导致局部组织缺氧。有研究表明,低氧微环境下,可以导致细胞基因组不稳定,抑制细胞凋亡[7]。而基因组不稳定是肿瘤发生发展的重要特征,频繁的缺氧可能导致细胞恶变[8]。另一种是炎症因子及信号通路学说,炎症可以刺激单核巨噬细胞、淋巴细胞、中性粒细胞产生,这些免疫细胞释放大量的肿瘤坏死因子(TNF-α)和白细胞介素-6(IL-6),通过激活一些炎症因子和信号通路,将炎症与肿瘤联系起来[9]。本组病例男∶女为1∶1.45,发病率相近;年龄60岁以上发病率高,占70.4%;均为单发。这些特征与Arlette等[10]报道的相一致。
鲍恩病病灶早期典型表现为淡红或暗红色斑疹、丘疹和(或)小斑片,后逐渐扩大,形成大小不等、形态不一斑块,表面常覆有鳞屑或结痂,痂皮一般不易剥离,若强行去除后可见肉芽状湿润糜烂面或红色颗粒状,少量出血或不出血。临床表现特异性差,误诊率较高,极易与湿疹、银屑病、Paget病、基底细胞癌等疾病相混淆[11]。本组病例患者误诊率为40.7%,可能与病理诊断送检不及时,医师临床经验不足及皮损临床表现不典型等多种因素有关。其中湿疹的误诊率最高,占14.8%,分析可能原因:① 湿疹早期表现为单发或多发粟粒大小的丘疹,基底潮红,后逐渐融合成片,可有点状渗出及小糜烂面,这与鲍恩病早期表现相似,故单从临床表现上较难分辨。② 鲍恩病不常见,临床医生对鲍恩病未引起重视。目前,临床表现结合组织病理学检查是诊断鲍恩病最主要的依据。在临床上,当出现皮损为边界清楚但不规则的红斑,上有溃疡,结痂,渗出,痂皮不易剥离,早期无自觉症状,且病程长,使用糖皮质激素治疗无效时,应高度怀疑本病。此时应及时做组织病理学检查,可确诊为鲍恩病。
鲍恩病虽属原位癌,但它也可突破表皮范围呈侵袭性生长而为鳞状细胞癌,因而一旦确诊应彻底手术切除。切除范围应距离病损边缘3~5 cm,可使皮损完全清除[12],切除深度应达筋膜层,以降低复发。有研究报道,本病手术切除后复发率高达23.1%[13]。本组病例仅1例复发,复发率为3.7%,可能与本组病例深度均切至深筋膜层、切除范围在皮损边缘3~5 cm有关,亦可能与病例数较少及随访时间较短有关。Mohs显微外科手术是一种将特殊冰冻组织切片与皮肤外科技术相结合的手术方法,是1930年由Mohs提出[14]。对复杂或复发皮损,将肿瘤残余边缘逐层切除做病理检查,直至将病变清除干净,可以最大程度的保存正常组织,同时又能最大限度的减少手术缺损面积[15]。但对于老年患者、皮损部位特殊、范围较大及多发的患者,也可以采取冷冻、超脉冲CO2激光、电灼、放射、PDT,或者外涂DHA、5-氟尿嘧啶及咪喹莫特等保守疗法。
综上所述,鲍恩病仅根据临床表现,易发生误诊。应予以重视,仔细观察皮损,尽早行组织病理检查,以便早期诊断,及时治疗。
参考文献:
[1] Lee MM, Wick MM. Bowen’s disease[J]. Clin Dermatol, 1993,11(1):43-46.
[2] Morton CA, Birnie AJ, Eedy DJ. British Association of Dermatologists’ guidelines for the management of squamous cell carcinoma in situ (Bowen’s disease) 2014[J]. Br J Dermatol, 2014,170(2):245-260.
[3] Murao K, Yoshioka R, Kubo Y. Human papillomavirus infection in Bowen disease: negative p53 expression, not p16(INK4a) overexpression, is correlated with human papillomavirus-associated Bowen disease[J]. J Dermatol, 2014,41(10):878-884.
[4] Shimizu A, Tamura A, Abe M, et al. Human papillomavirus type 56-associated Bowen disease[J]. Br J Dermatol, 2012,167(5):1161-1164.
[5] Bellott TR, Baez CF, Almeida SG, et al. Molecular prevalence of Merkel cell polyomavirus in nonmelanoma skin cancer in a Brazilian population[J]. Clin Exp Dermatol, 2017,DOI: 10.1111/ced.13069.
[7] Nelson DA, Tan TT, Rabson AB, et al. Hypoxia and defective apoptosis drive genomic instability and tumorigenesis[J]. Genes Dev, 2004,18(17):2095-2107.
[8] Barnhart BC, Simon MC. Metastasis and stem cell pathways[J]. Cancer Metastasis Rev, 2007,26(2):261-271.
[9] Grivennikov SI, Karin M. Dangerous liaisons: STAT3 and NF-kappaB collaboration and crosstalk in cancer[J]. Cytokine Growth Factor Rev, 2010,21(1):11-19.
[10] Arlette JP, Trotter MJ. Squamous cell carcinoma in situ of the skin: history, presentation, biology and treatment[J]. Australas J Dermatol, 2004,45(1):1-9.
[11] 龙梅, 李东霞. 多发鲍恩病1例[J].中国中西医结合皮肤性病学杂志,2017,16(5):452-454.
[12] Westers-Attema A, van den Heijkant F, Lohman BG, et al. Bowen’s disease: A six-year retrospective study of treatment with emphasis on resection margins[J]. Acta Derm Venereol, 2014,94(4):431-435.
[13] Marchesa P, Fazio VW, Oliart S, et al. Perianal Bowen’s disease: a clinicopathologic study of 47 patients[J]. Dis Colon Rectum, 1997,40(11):1286-1293.
[14] Mohs FE. Chemosurgical treatment of cancer of the skin; a microscopically controlled method of excision[J]. J Am Med Assoc, 1948,138(8):564-569.
[15] Smeets NW, Kuijpers DI, Nelemans P, et al. Mohs’ micrographic surgery for treatment of basal cell carcinoma of the face--results of a retrospective study and review of the literature[J]. Br J Dermatol, 2004,151(1):141-147.
