突破有机物制备实验
2017-07-05河南省鄢陵县第一高级中学高小艳
■河南省鄢陵县第一高级中学 高小艳
突破有机物制备实验
■河南省鄢陵县第一高级中学 高小艳
例题 实验室用乙酸和正丁醇制备乙酸正丁酯。有关物质的相关数据如表1。

表1
(一)乙酸正丁酯的制备。
如图1,在干燥的A中加入13.5mL正丁醇和7.2mL冰醋酸,再加入3~4滴浓硫酸,摇匀,投入1~2粒沸石。然后安装分水器(作用:实验过程中不断分离除去反应生成的水)、温度计及回流冷凝管。
(1)仪器A的名称是____,本实验中选择仪器A的容积为____。
a.50mL b.100mL
c.200mL d.500mL
(2)冷水应该从冷凝管____(填a或b)管口通入。
(3)仪器A中发生反应的化学方程式为____。
(4)沸石的作用是____;如果在沸腾前发现忘记加沸石,应____。
(5)实验中为了提高乙酸正丁酯的产率,采取的措施是____。
(6)有同学拟通过某种方法鉴定所得产物中是否含有杂质,可采用____确定。
图1
a.红外光谱法
b.1H核磁共振谱法
c.质谱法
(7)判断反应终点的依据是____。
(8)反应时加热有利于提高酯的产率,但温度过高酯的产率反而降低,其可能的原因是____。
(二)乙酸正丁酯粗产品的精制。
(Ⅰ)将分水器分出的酯层和反应液合并得粗产品。
(9)用分液漏斗(如图2)可分离有机层与水层,分液完成后,取出有机层的操作是____。
(10)下列关于分液漏斗的使用叙述正确的是____。
A.分液漏斗使用前必须要检漏,只要分液漏斗的活塞处不漏水即可使用

图2
C.萃取振荡操作应如图3所示
D.放出液体时,需将玻璃塞打开或使塞上的凹槽对准漏斗口上的小孔
(11)将乙酸正丁酯粗产品用如下的操作进行精制:①水洗;②蒸馏;③用无水MgSO4干燥;④用10%碳酸钠溶液洗涤。正确的操作步骤是____(填字母)。
A.①②③④ B.③①④②
C.①④①③② D.④①③②③
(12)产品的精制过程中,第一次水洗的目的是____,用饱和Na2CO3溶液洗涤有机层,该步操作的目的是____。
(Ⅱ)将干燥后的乙酸正丁酯滤入50mL烧瓶中,常压蒸馏,收集得11.6g乙酸正丁酯。
(13)将干燥后的产品蒸馏收集乙酸正丁酯产品时,应将温度控制在____左右。
(14)在进行蒸馏操作时,若从118℃开始收集馏分,产率偏____(填“高”或“低”),原因是____。
(15)沸点大于140℃的有机化合物的蒸馏,一般不用上述冷凝管而用空气冷凝管,可能原因是____。
(16)该实验过程中,生成乙酸正丁酯(式量116)的产率是____。

解析:第一步:明确反应原理。
实验室制备乙酸正丁酯的反应原理是:
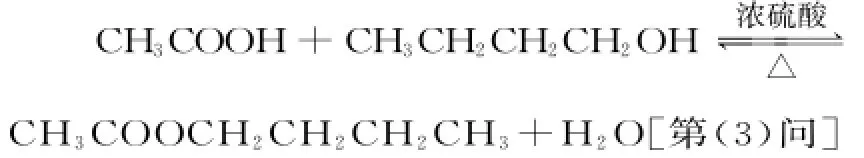
反应中浓硫酸作催化剂,且反应为可逆反应,所以将生成的产物中的水不断从反应体系中移走,促使平衡不断右移,以提高反应的转化率[第(5)问]。当分水器中的水层不再增加时,说明反应达到终点[第(7)问]。反应物酸和醇都是易挥发的,所以温度过高,丁醇与乙酸易挥发,同时副反应也增加[第(8)问]。
红外光谱法可用于测定有机物中的官能团,可通过红外光谱判断所得产物中是否含有杂质[第(6)问]。
第二步:熟知实验仪器。
本实验使用到的主要实验仪器是蛇形冷凝管、三颈烧瓶、温度计等仪器。其中烧瓶加热时所盛液体体积为容积的,本题中液体体积约20.8mL,应选用50mL的烧瓶[第(1)问]。
用水冷凝气体时,冷水要充满整个冷凝管,冷凝管中水从下端口流入,上端口流出。
在烧瓶中加入沸石,防止加热时液体剧烈沸腾,物料喷出;如果在沸腾前发现忘记加沸石,应立即停止加热,冷却后补加[第(4)问]。
分液时应使用梨形分液漏斗,乙酸正丁酯的密度小于水,混合液分层后有机层是上层,所以分液完成后,取出有机层的操作是:将有机层从上口倒入一个干净的烧瓶中[第(9)问]。
分液漏斗使用时注意事项:使用前要检查活塞处和上口处是否漏水;装入分液漏斗内液体的总体积以不要超过分液漏斗容积的为宜,装得太多不利于液体的混合;振荡液体时要倒置分液漏斗,这样有利于液体的混合;分液时,下层液体由下口放出,上层液体从上口倒出。从下口放液体时,将上端玻璃塞的小孔或凹槽对准颈部的小孔使漏斗内外相通,及时关闭活塞,防止上层液体流出[第(10)问]。
沸点大于140℃的有机化合物的蒸馏,一般不用水冷凝管而用空气冷凝管,防止因温差过大,冷凝管炸裂[第(15)问]。
第三步:分析杂质成分。
依据乙酸正丁酯、乙酸、正丁醇、浓硫酸的溶解性判断乙酸正丁酯中混有乙酸、正丁醇、浓硫酸、水等杂质。
第四步:除杂方案设计。

第五步:产率(纯度)计算。
正丁醇的质量为0.8g·mL-1× 13.5mL=10.8g,冰醋酸的质量为1.045g·mL-1×7.2mL=7.524g。根据方程式判断正丁醇过量,以不足量的冰醋酸为标准进行计算。
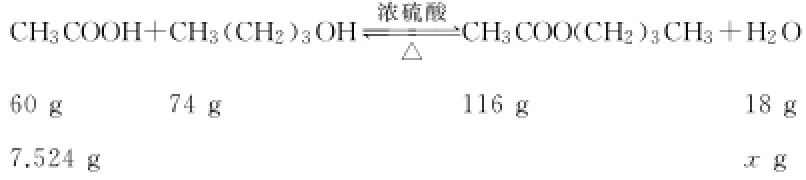

(4)防止暴沸 立即停止加热,冷却后补加
(5)将生成的产物中的水不断从反应体系中移走,促使平衡不断右移,以提高反应的转化率
(6)a
(7)分水器中的水层不再增加时,视为反应的终点
(8)温度过高,丁醇与乙酸易挥发,同时副反应也增加
答案:(1)三颈烧瓶 a
(9)将有机层从上口倒入一个干净的烧瓶中
(10)CD (11)C
(12)除去乙酸、硫酸及少量的正丁醇除去产品中含有的乙酸等酸性杂质
(13)126.1℃
(14)高 会收集到少量未反应的乙酸和正丁醇
(15)防止因温差过大,冷凝管炸裂
(16)80%
练习:
1.乙酸异戊酯是组成蜜蜂信息素的成分之一,具有香蕉的香味。实验室制备乙酸异戊酯的反应、装置示意图(见图4)和有关数据(见表2)如下。

图4


表2
实验步骤:
在A中加入4.4g异戊醇、6.0g乙酸、数滴浓硫酸和2~3片碎瓷片。开始缓慢加热A,回流50min。反应液冷至室温后倒入分液漏斗中,分别用少量水、饱和碳酸氢钠溶液和水洗涤。分出的产物加入少量无水MgSO4固体,静置片刻,过滤除去MgSO4固体,进行蒸馏纯化,收集140℃~143℃馏分,得乙酸异戊酯3.9g。
回答下列问题:
(1)仪器B的名称是____。
(2)在洗涤操作中,第一次水洗的主要目的是____,第二次水洗的主要目的是____。
(3)在洗涤、分液操作中,应充分振荡,然后静置,待分层后____(填标号)。
a.直接将乙酸异戊酯从分液漏斗的上口倒出
b.直接将乙酸异戊酯从分液漏斗的下口放出
c.先将水层从分液漏斗的下口放出,再将乙酸异戊酯从下口放出
d.先将水层从分液漏斗的下口放出,再将乙酸异戊酯从上口倒出
(4)本实验中加入过量乙酸的目的是____。
(5)实验中加入少量无水MgSO4的目的是____。
(6)在蒸馏操作中,仪器选择及安装(见
图5)都正确的是___________(填标号)。

图5
(7)本实验的产率是____(填标号)。
a.30% b.40% c.60% d.90%
(8)在进行蒸馏操作时,若从130℃便开始收集馏分,会使实验的产率偏____(填“高”或“低”),其原因是____。

要的化工原料和医药中间体,实验室合成三苯甲醇的装置如图6所示,合成流程如下。

已知:(Ⅰ)格氏试剂容易水解:

(Ⅱ)相关物质的物理性质如表3。____________________

图6
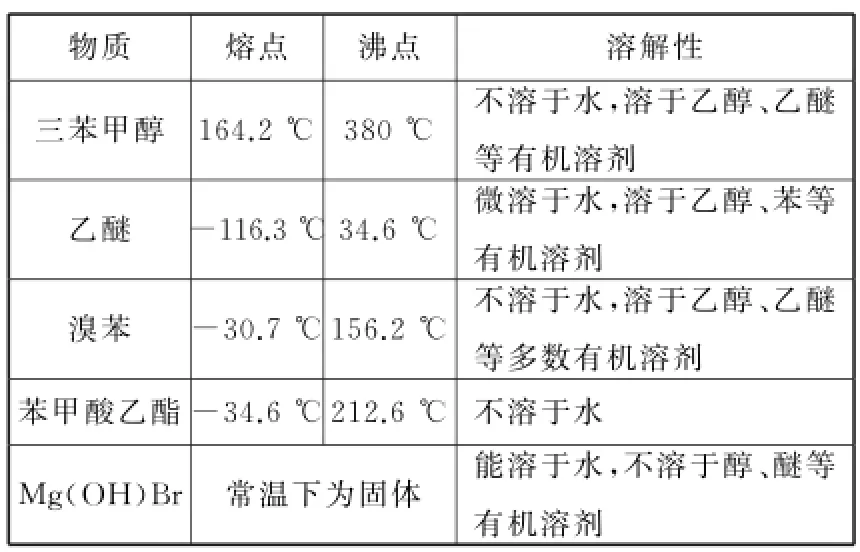
表3
(Ⅲ)三苯甲醇的分子量是260,纯净固体有机物一般都有固定熔点。
(1)图7中玻璃仪器B的名称为____;装有无水CaCl2的仪器A的作用是____。
(2)图7中滴加液体未用普通分液漏斗而用滴液漏斗的作用是____;制取格氏试剂时要保持微沸,可以采用____(方式)加热,优点是____。
(3)制得的三苯甲醇粗产品中,含有乙醚、溴苯、苯甲酸乙酯等有机物和碱式溴化镁等杂质,可以设计如下所示提纯方案。

请填写如下空白:
其中,①操作为____;洗涤液最好选用____(从选项中选)。
A.水 B.乙醚
C.乙醇 D.苯
检验产品已经洗涤干净的操作为____。
(4)纯度测定:称取2.60g产品,配成乙醚溶液,加入足量金属钠(乙醚与钠不会反应),充分反应后,测得生成气体体积为100.80mL(标准状况)。产品中三苯甲醇质量分数为____(保留两位有效数字)。
参考答案:
1.(1)球形冷凝管
(2)洗掉大部分硫酸和乙酸 洗掉碳酸氢钠溶液
(3)d
(4)提高异戊醇的转化率
(5)除去有机层中的少量水,起到干燥作用
(6)b
(7)c
(8)高 收集了少量未反应的异戊醇
2.(1)球形冷凝管 防止空气中水蒸气进入装置,使格氏试剂水解
(2)平衡压强,便于漏斗内试剂滴下 水浴 受热均匀,温度易于控制
(3)蒸馏或分馏 A 取少量最后一次洗涤液于试管中,滴加AgNO3溶液,若无沉淀生成,则已洗涤干净(或“滴加酚酞试液,洗涤液未变色”等)
(4)90%
(责任编辑 谢启刚)
