抑抗灵片质量标准的改进
2016-12-18刘文雅王曙东
刘文雅,王 争,王曙东,汤
(中国人民解放军南京军区南京总医院制剂科,江苏 南京 210002)
抑抗灵片质量标准的改进
(中国人民解放军南京军区南京总医院制剂科,江苏 南京210002)
目的 改进抑抗灵片的质量标准。方法 用薄层色谱(TLC)法定性鉴别制剂中的当归,建立测定淫羊藿中淫羊藿苷含量的方法。结果 薄层色谱斑点清晰,阴性无干扰;含量测定中,淫羊藿苷质量浓度在3.991 86~63.869 76 μg/mL范围内与峰面积线性关系良好(r=0.999 9),平均加样回收率为98.46%,RSD为1.07%(n=9)。结论 该方法简便,准确,灵敏度高,专属性强,重复性好,可作为抑抗灵片的质量控制方法。
抑抗灵片;薄层色谱法;高效液相色谱法;淫羊藿苷
抑抗灵片是由淫羊藿、当归、桃仁、枸杞子等10味中药组方的中药复方制剂,为我院制剂科研发的非标制剂,具有益肾生精的功效,用于抗精子抗体阳性引起的不育症。现行标准仅采用薄层色谱(TLC)法对淫羊藿、枸杞子进行定性鉴别,无指标性成分的定量检测。笔者在原有基础上,增加了当归的TLC定性鉴别,并建立淫羊藿中淫羊藿苷定量检测的高效液相色谱(HPLC)法,旨在为控制其质量提供客观定性定量的评价方法,完善制剂的质量标准。
1 仪器与试药
1.1仪器
高效液相色谱仪(含1525双泵系统、2487紫外检测器、717自动进样器及Empower2色谱工作站,Waters公司);Mettler Toledo AE240型电子天平,KQ2200DB型数控超声波清洗器(昆山市超声仪器有限公司)。
1.2试药
抑抗灵片(南京军区南京总医院制剂科自制);淫羊藿苷对照品(中国食品药品检定研究院,批号为110737-200415,纯度为99.3%);枸杞子对照药材(中国食品药品检定研究院,批号为121072-200505);当归对照药材(中国食品药品检定研究院,批号为120927-200613);硅胶G(供薄层层析用,青岛海洋化工厂);乙腈为色谱纯,水为双蒸水,其余试剂均为分析纯。
2 方法与结果
2.1定性鉴别
2.1.1淫羊藿薄层色谱鉴别[1]
取本品30片,除去包衣,研碎,加乙醇80 mL,加热回流1 h,滤过,蒸干,残渣用石油醚(30~60℃)洗涤3次,每次10 mL,弃去洗涤液,残渣水浴加热挥去石油醚,加2%氢氧化钠溶液30 mL使溶解,用乙酸乙酯振摇提取3次,每次15 mL,合并提取液,蒸干,残渣加甲醇1 mL使溶解,作为供试品溶液。另取淫羊藿对照药材1 g,同法制备对照药材溶液。按处方量1%的量,称取除淫羊藿以外的其余药材,按制剂工艺及供试品溶液制备方法制成阴性对照品溶液。照2015年版《中国药典(一部)》附录ⅥB薄层色谱法试验,吸取上述3种溶液各20 μL,分别点于同一硅胶G薄层板上,以乙酸乙酯-丙酮-甲酸-水(10∶1∶1∶1)为展开剂,展开,取出,晾干,喷以2%三氯化铁乙醇溶液。供试品溶液色谱中,在与对照药材溶液色谱相应位置上显相同颜色的荧光斑点,且阴性对照无干扰,见图1。
2.1.2枸杞子薄层色谱鉴别[2]
取本品20片,除去包衣,研碎,加水100 mL,煎煮15min,滤过,滤液用乙酸乙酯振摇提取3次,每次10mL,合并提取液,蒸干,残渣加甲醇2 mL使溶解,作为供试品溶液。另取枸杞子对照药材1 g,同法制备对照药材溶液。按处方量1%的量,称取除枸杞子以外的其余药材,按制剂工艺及供试品溶液制备方法制备阴性品对照溶液。照2015年版《中国药典(一部)》附录ⅥB薄层色谱法试验,吸取上述3种溶液各20 μL,分别点于同一硅胶G薄层板上,以二氯甲烷-甲醇(9∶1)为展开剂,展开,取出,晾干,置紫外光灯(365 nm)下检视。供试品溶液色谱中,在与对照药材溶液色谱相应位置上显相同颜色的荧光斑点,同时阴性对照无干扰,见图2。

图1 淫羊藿薄层色谱图
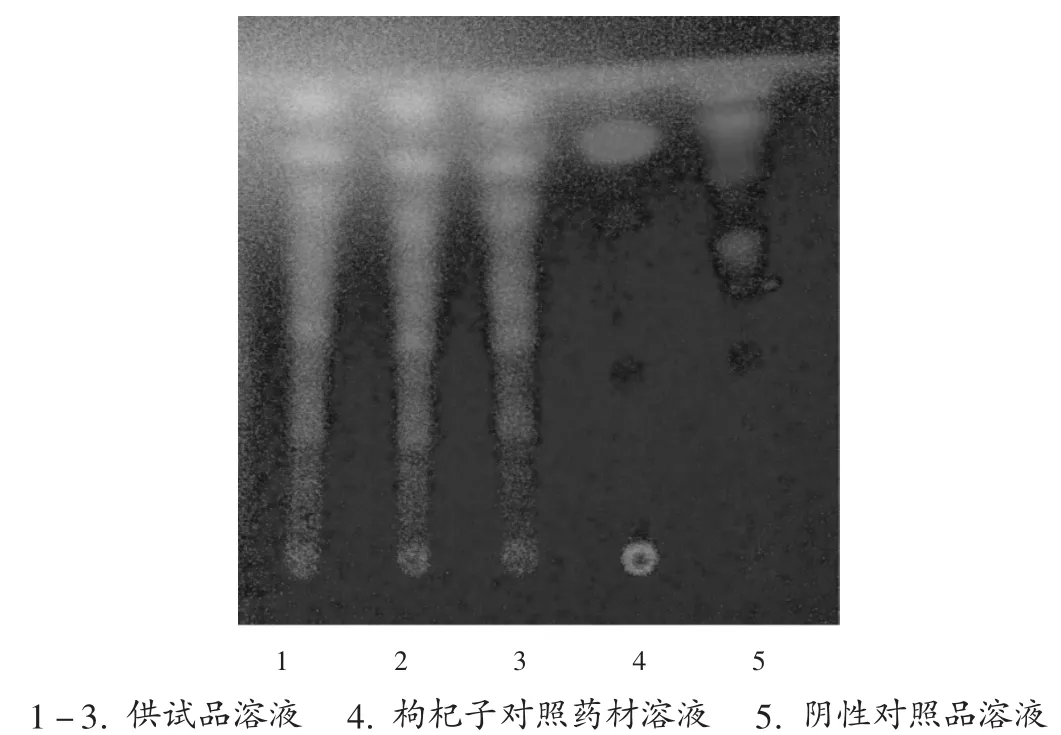
图2 枸杞子薄层色谱图
2.1.3当归薄层色谱鉴别[3-4]
取本品40片,除去包衣,研细,加乙醚30 mL,浸泡4 h以上,滤过,滤液自然挥干,残渣加甲醇1 mL使溶解,作为供试品溶液。另取当归对照药材2 g,同法制备对照药材溶液。按处方量1%的量,称取除当归以外的其余药材按制剂工艺及供试品溶液制备方法制备阴性对照品溶液。照2010年版《中国药典(一部)》附录ⅥB薄层色谱法试验,吸取上述3种溶液各6 μL,分别点于同一硅胶G薄层板上,以正己烷-乙酸乙酯(9∶1)为展开剂,展开,取出,晾干,置紫外光灯(365 nm)下检视。供试品溶液色谱中,在与对照药材溶液色谱相应位置上显相同颜色的荧光斑点,同时阴性对照无干扰,结果见图3。

图3 当归薄层色谱图
2.2淫羊藿苷含量测定[5-6]
2.2.1色谱条件
色谱柱:Hedera-ODS-2 C18柱(250 mm×4.6 mm,5 μm);流动相:乙腈-水(29∶71);检测波长:270 nm;柱温:30℃;流速:1.0 mL/min;进样量:10 μL。理论板数按淫羊藿苷峰计算大于1 500。
2.2.2溶液制备
对照品溶液:称取淫羊藿苷对照品8.04 mg,精密称定,置100 mL容量瓶中,加甲醇至刻度,摇匀,作为贮备液。精密吸取对照品贮备液3 mL,置10 mL容量瓶中,加甲醇至刻度,摇匀,即得。
供试品溶液:取本品粉末约0.5 g,精密称定,置具塞锥形瓶中,精密加入甲醇50 mL,密塞,称定质量,超声处理(功率250 W,频率40 kHz)60 min,放冷,再称定质量,用甲醇补足减失的质量,摇匀,滤过,精密量取续滤液25 mL,蒸干,残渣加水30 mL使溶解,用乙酸乙酯萃取4次,每次30 mL,合并乙酸乙酯液,蒸干,残渣加甲醇适量使溶解,转移至10 mL容量瓶中,并稀释至刻度,摇匀,滤过,取续滤液,即得。
阴性对照品溶液:按处方比例称取除淫羊藿以外的其余药材,按本品制备工艺及供试品溶液制备方法制备阴性对照品溶液。
2.2.3方法学考察
专属性试验:精密吸取上述对照品溶液、供试品溶液与阴性对照品溶液各10 μL,按拟订方法进样测定。供试品溶液色谱中,在与对照品溶液色谱相应保留时间处,有相同色谱峰,而阴性对照品溶液在相应保留时间处则无此峰出现,表明其对样品测定无干扰。结果见图4。
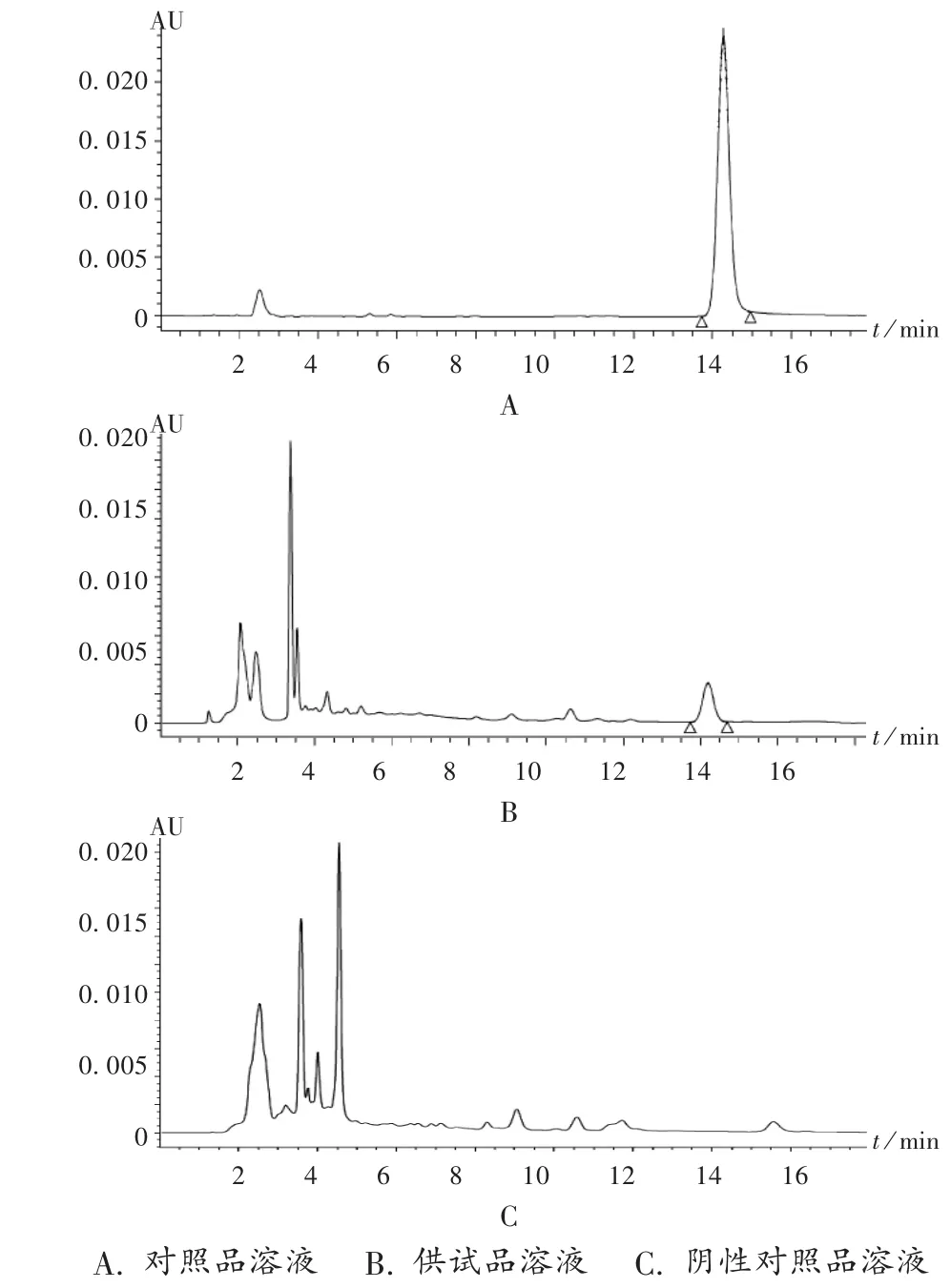
图4 淫羊藿苷高效液相色谱图
线性关系考察:精密吸取淫羊藿苷贮备液0.5,1.5,3.0,5.0,8.0 mL,分别置10 mL容量瓶中,用甲醇稀释至刻度,按拟订色谱条件进样测定,以对照品溶液质量浓度为横坐标(X)、峰面积为纵坐标(Y)进行线性回归,得回归方程 Y=20 729 966 X+1 201,r=0.999 9(n=5)。结果表明,淫羊藿苷质量浓度在3.991 86~63.869 76 μg/mL范围内与峰面积线性关系良好。
精密度试验:取2.2.2项下对照品溶液,按拟订色谱条件连续进样6次。结果淫羊藿苷峰面积的 RSD为0.97%(n=6),表明仪器精密度良好。
稳定性试验:取同一供试品溶液,常温下分别于0,1,2,4,8 h时进样,记录淫羊藿苷峰面积。结果的 RSD为1.83%(n=5),表明供试品溶液在8 h内稳定。
重复性试验:取同一批样品5份,按2.2.2项下方法制备供试品溶液,进样测定。结果峰面积的 RSD为1.72%(n=5),表明方法重复性良好。
加样回收试验:称取已知含量的样品(批号为140519)0.25 g,共 9份,置50 mL锥形瓶中,分别精密加入淫羊藿苷对照品贮备液2.4,3.0,3.6 mL,按2.2.2项下方法制备供试品溶液。精密吸取上述供试品溶液各10 μL注入色谱仪,测定含量,计算回收率。结果见表1。
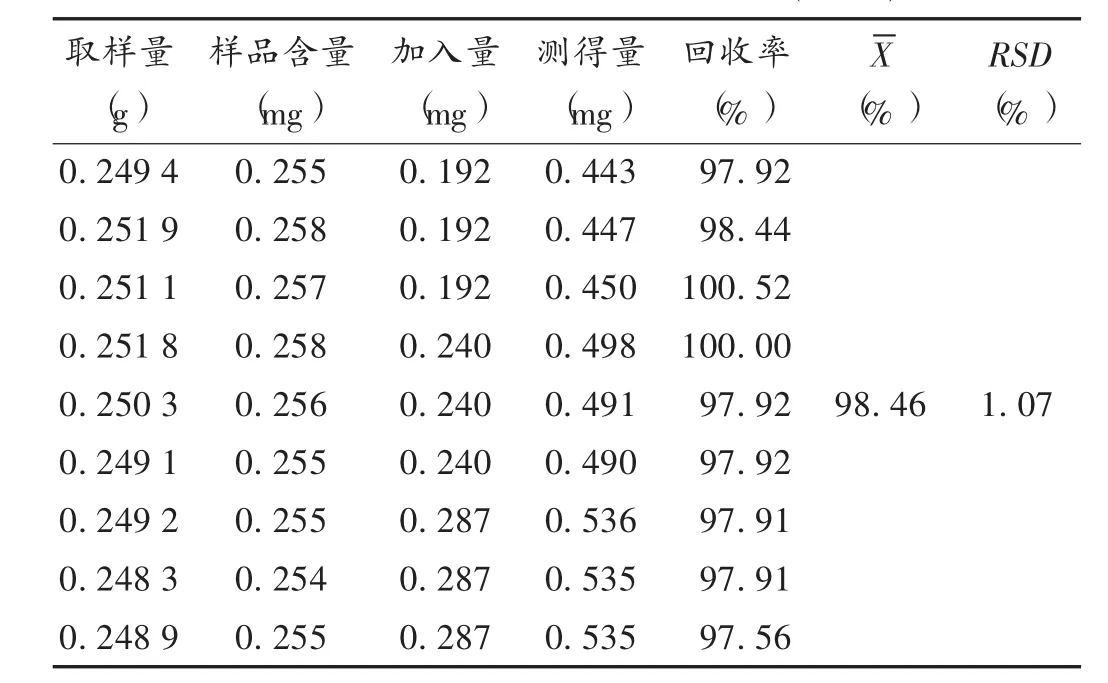
表1 淫羊藿苷加样回收试验结果(n=9)
2.2.4样品含量测定
取3批抑抗灵片,按2.2.2项下方法制备供试品溶液,依法进样测定,结果批号为140422,140519,140612的样品中,淫羊藿苷含量分别为0.93,0.88,0.99mg/g。
3 讨论
抑抗灵片为我院制剂科研发的非标制剂,具有益肾生精的功效,用于抗精子抗体阳性引起的不育症,临床应用多年,效果显著。抑抗灵片原标准仅对淫羊藿、枸杞子进行定性鉴别,不符合制剂质量标准提升要求。本试验曾尝试增加女贞子的定性鉴别,但女贞子的阴性对照存在干扰,故抑抗灵片质量标准中不再选用女贞子作为研究对象。当归有补血活血、润肠通便之功效[7],主治血虚头昏、面色不华、跌打损伤、瘀血肿痛、血脉瘀滞、风湿痹痛、疮疡痈肿、月经不调、痛经闭经、崩漏及产后瘀滞腹痛等病症。其化学成分主要分为挥发油部分和水溶性部分,挥发油部分为主要成分,包括中性、酸性及酚性油三部分。其中,藁苯内酯是当归挥发油部分的主要成分,水溶性成分主要有阿魏酸及多糖等[8]。选择其有效成分作为观察指标进行薄层鉴别,曾采用环己烷-二氯甲烷-乙酸乙酯-甲酸(4∶1∶1∶0.1)为展开剂,经试验,斑点显色不清晰。本试验中采用正己烷-乙酸乙酯(9∶1)为展开剂,晾干后置紫外光灯(365 nm)下检视,薄层色谱结果显示斑点清晰,所建立的方法较简单,阴性无干扰,且分离度和重复性好。
淫羊藿具有补肾壮阳、益精补气等功效,可用于治疗腰膝酸软、风湿痹痛、四肢麻木不仁等病症,为常用的补肾壮阳药物[9]。主要有效成分为黄酮类化合物,还包括酚苷类、多糖类、有机酸等,代表性成分为淫羊藿苷[10],具有体内、外多种生物活性[11],可增强免疫功能、抗肿瘤、改善心脑血管功能、调节内分泌、延缓肾衰竭的进程、增强雄性生殖功能、抗骨质疏松、抗衰老等[12]。本试验中增加了淫羊藿苷指标成分的含量测定,同时删除原标准中“醇浸出物”的含量测定。分别采用甲醇、50%甲醇、乙醇、稀乙醇超声提取30 min,结果显示甲醇超声含量较高,且阴性对照无干扰,故选定甲醇为提取溶剂。同时,对甲醇提取时间进行了考察,结果1 h即可将样品中淫羊藿苷基本提取完全。但采用甲醇超声提取,进样后发现杂质含量较高,淫羊藿苷峰面积相对其他峰较小,后采用甲醇超声后乙酸乙酯萃取以除去部分杂质,并对萃取次数及用量进行了考察。结果表明,萃取4次和5次含量差异不大,故选择乙酸乙酯萃取4次,转移率达98%以上。
综上所述,该方法具有良好的线性关系、精密度、重复性和稳定性,且回收率高,可对抑抗灵片中淫羊藿苷的含量进行准确定量,对产品进行有效的质量控制。作者简介:刘文雅,女,硕士研究生,主管药师,主要从事中药新制剂研究,(电话)025-80863161(电子信箱)aya_a@sina.com;汤,男,硕士研究生,副主任药师,主要从事中药新制剂研究,本文通讯作者,(电话)025-80860343(电子信箱)tanghao@126.com。
[1]蔡杰,赖坤平,温坚,等.藿草壮骨合剂中淫羊藿和熟地黄的薄层色谱鉴别[J].海峡药学,2015,27(3):58-59.
[2]陈宏斌,孟令琨,温瑗源,等.山药益气丸质量标准研究[J].亚太传统医药,2016,12(4):37-38.
[3]耿铮,车慧,苏丹.加味左金丸质量标准提高研究[J].中药材,2014,37(1):137.
[4]任卫琼,万艳群,李珊,等.乳核分散片质量标准的建立[J].中国药师,2014,17(3):395.
[5]刘源,石继伟.高效液相色谱法测定安神补脑片中淫羊藿苷含量[J].中国药业,2014,23(1):14-15.
[6]冯庭平,黄顺旺,陈曼,等.HPLC法测定金马肝泰分散片中淫羊藿苷的含量[J].安徽医药,2014,18(3):453.
[7]Wang Q,Ding F,Zhu N,et al.Determination of the compositions of polysaccharides from Chinese herbs by capillary zone electrophoresis with amperometric detection[J].Biomed Chromatogr,2003,17(7):483-488.
[8]刘医辉,杨世英,马伟林,等.当归药理作用的研究进展[J].中国当代医药,2014,21(22):192-193.
[9]王焕珍,柴艺汇,陈云志,等.淫羊藿化学成分与药理作用研究进展[J].亚太传统医药,2016,12(7):63-65.
[10]王可可,龚其海.淫羊藿化学成分及药理作用的研究进展[J].中国民族民间医药,2015,24(19):16-18.
[11]Cui L,Zhang ZH,Sun E,et al.Effect of β-cyclodextrin complexation on solubility and enzymatic hydrolysis rate of icariin[J].J Nat Sci Biol Med,2013,4(1):201-206.
[12]陈毅平,陈双英,陈文财,等.淫羊藿苷的稳定性及其影响因素[J].中国实验方剂学杂志,2014,20(5):78.
Quality Standard Improvement for Yikangling Tablets
Liu Wenya,Wang Zheng,Wang Shudong,Tang Hao
(Nanjing General Hospital of PLA Nanjing Military Area Command,Nanjing,Jiangsu,China210002)
ObjectiveTo improve the quality standard for Yikangling Tablets.MethodsAngelica sinensis in the Yikangling Tablets was detected qualitatively by TLC.The content of icariin in herba epimedii was determined by HPLC.ResultsThe spots on TLC plates were clear without the interference of negative control.Icariin showed a linear relationship within the concentration range of 3.991 86-63.869 76 μg/mL(r=0.999 9).The average recovery was 98.46%,and the RSD was 1.07%(n=9).ConclusionThe method is simple,accurate,sensitive,specific and reproducible.It can be used for the quality control of Yikangling Tablets.
Yikangling Tablets;TLC;HPLC;icariin
R284.1;R282.71
A
1006-4931(2016)20-0049-04
(2016-06-01)
