氟代苯基异羟肟酸钴的合成及其对乙苯氧化的催化性能
2016-10-25陈小峰吕新宇
陈小峰, 邱 滔, 吕新宇
(常州大学 设计研究院,江苏 常州 213164)
氟代苯基异羟肟酸钴的合成及其对乙苯氧化的催化性能
陈小峰, 邱滔*, 吕新宇
(常州大学 设计研究院,江苏 常州213164)
以全氟碘丁烷为原料,分别与4-碘硝基苯和4-碘苯甲酸反应合成了4-全氟丁基硝基苯(1)和4-全氟丁基苯甲酸(3); 1经还原反应, 3经酰氯化反应,后再缩合反应制得氟代苯基异羟肟酸(5); 5经络合反应合成了氟代苯基异羟肟酸钴(6), 其结构经 UV-Vis,1H NMR, FT-IR和HR-MS(EI)表征。在氟两相中考察了其对乙苯氧化的催化性能。结果表明:在全氟己烷中,6 0.04 mmol,于60 ℃反应6 h,乙苯的转化率为49.2%,苯乙酮的选择性为88.3%。6循环使用5次,选择性保持良好。
氟代苯基异羟肟酸钴; 氟两相催化; 乙苯氧化; 合成; 催化性能
氟两相催化作为一种新型均相催化和分离技术,在1994年Horvath首次使用后便逐渐成为研究热点[1]。氟两相体系由氟相和有机相构成,氟相由全氟溶剂和氟代催化剂构成,氟两相具有升温后有机相和氟相形成均相体系而降温后两相分离的特性,故适合用于催化体系[2-3]。开发合适的氟代催化剂是氟两相催化的关键[4-6]。异羟肟酸结构简单,合成简便,结构可调性大,可作为一种新的金属有机催化剂载体[7-10]。研究表明:在异羟肟酸配体结构上引入基团能增加赤道配体的π-授予性、疏水性,能提高配合物结合氧的能力,从而提高催化氧化性能[11-12]。

Scheme 1
异羟肟酸金属配合物和氟两相体系结合作为催化氧化的报道较少。本文以全氟碘丁烷为原料,分别与4-碘硝基苯和4-碘苯甲酸反应合成了4-全氟丁基硝基苯(1)和4-全氟丁基苯甲酸(3); 1经还原反应,3经酰氯化反应,后经缩合反应制得氟代苯基异羟肟酸(5); 5经络合反应合成氟代苯基异羟肟酸钴(6),其结构经 UV-Vis,1H NMR, FT-IR和HR-MS(EI)表征。在氟两相中考察了其对乙苯氧化的催化性能。
1 实验部分
1.1仪器与试剂
Nicolet 380型傅立叶变换红外光谱仪(KBr压片); Avance 500 MHz型超导傅立叶变换核磁共振仪(CDCl3为溶剂,TMS为内标);Ionspec 4.7 Tesla FTMS型高分辨质谱仪;N2000型气相色谱仪;LC-100型液相色谱仪;QP2010 SE型气相色谱质谱联用仪。
全氟碘丁烷、全氟己烷(质量分数≥99.5 %),百灵威科技有限公司;其余所用试剂均为分析纯。
1.2合成
(1) 1的合成
在反应瓶中依次加入活性铜0.77 g(12 mmol),全氟碘丁烷4.15 g(12 mmol) 和DMSO 4 mL,搅拌下于80 ℃反应0.5 h;加入4-碘硝基苯 1.00 g(4 mmol),反应至终点(TLC检测)。加冰水75 mL,用乙酸乙酯萃取,萃取液蒸干后经硅胶柱层析[洗脱剂:A=V(乙酸乙酯) ∶V(石油醚)=1 ∶7]纯化得黄色固体1 0.89 g,收率65%;1H NMRδ: 8.35(d,J=8.92 Hz, 2H), 7.82(d,J=8.72 Hz, 2H);19F NMRδ: -76.79~-77.30(m, 3F, CF3), -115.06~-118.50(m, 2F, CF2), -128.39~-128.49(m, 2F, CF2), -134.57~-134.96(m, 2F, CF2); GC-MSm/z: 340{[M-H]-}。
(2) 4-全氟丁基苯基羟胺(2)的合成
在反应瓶中加入1 2.00 g(5.8 mmol)和无水乙醇20 mL,搅拌下分批加入锌粉1.00 g(15 mmol),甲酸铵0.60 g(9.5 mmol)和水2 mL,加毕(30 min),反应至终点(TLC检测)。用水淬灭反应,用乙酸乙酯萃取,萃取液旋蒸除溶得黄色晶体2 1.36 g,收率72%;1H NMRδ: 7.55(d,J=8.72 Hz, 2H), 6.77(d,J=8.92 Hz, 2H);19F NMRδ: -76.79~-77.30(m, 3F, CF3), -115.06~-118.50(m, 2F, CF2), -128.39~-128.49(m, 2F, CF2), -134.57~-134.96(m, 2F, CF2); LC-MSm/z: 326.02{[M-H]-}。
(3) 3的合成
在反应瓶中加入活性铜2.00 g(0.03 mol),全氟碘丁烷10.38 g(0.03 mol)和DMSO 4 mL,于80 ℃静置反应0.5 h,加入4-碘苯甲酸1.00 g(4 mmol),搅拌下反应至终点(TLC检测)。加冰水75 mL,过滤,用乙酸乙酯萃取,萃取液蒸除溶剂得固体粗产物。固体粗产品经碱液溶解,盐酸酸化得淡黄色固体3 0.96 g,收率71%; LC-MSm/z: 339{[M-H]-}。
(4) 4-全氟丁基苯甲酰氯(4)的合成
在反应瓶中加入3 0.80 g(1.8 mmol),氯化亚砜8 mL和DMF 1滴,搅拌下于80 ℃反应3 h。蒸除氯化亚砜得黄色油状液体4 0.63 g,收率98%, LC-MSm/z: 357{[M-H]-}。
(5) 5的合成
在反应瓶中加入2 1 .00 g(3 mmol),二氯甲烷30 mL和NaHCO30.18 g,搅拌下于-10~-5 ℃滴加4 1.07 g(3 mmol)的二氯甲烷(20 mL)溶液,滴毕(30 min),于室温反应2~4 h(TLC检测)。过滤,滤饼经柱层析(洗脱剂:A)纯化得黄色晶体5 0.82 g,收率55%;1H NMRδ: 7.82(d,J=8.92 Hz, 2H), 7.73(d,J=8.72 Hz, 2H), 7.49(d,J=8.92 Hz, 2H), 7.44(d,J=8.72 Hz, 2H);19F NMR(470 Hz)δ:-80.949~-80.991(m, 3F, CF3), -111.473~-111.529(m, 2F, CF2), -122.627~-122.667(m, 2F, CF2), -125.515~-125.569(m, 2F, CF2); IRν: 3 188(OH), 1 636(C=O), 1 353(CF3), 1 237, 1 205, 1 135, 1 090(CF2), 1 009(C—F), 908, 745, 735; LC-MSm/z: 648.01{[M-H]-}。
(6) 6的合成
在反应瓶中加入5 1 mmol和无水乙醇10 mL,搅拌下于50 ℃滴加乙酸钴水溶液2 mL,滴毕,反应3 h。于沸水浴加热30 min,过滤,滤饼用热水和95%乙醇洗涤,于100 ℃真空干燥3~4 h得粉红色固体6 0.73 g,收率53%, ICP测试钴含量为3.39%(理论含量为3.3%); IRν: 1 630(C=O), 1 353(CF3), 1 237, 1 205, 1 135, 1 090(CF2), 1 009(C—F), 908, 745, 735; HR-MS(EI)m/z: Calcd for C42H4N2O4F36Co {[M+Na]+}1 355.063, found 1 378.052。
1.3氟两相催化氧化乙苯反应
在反应瓶中依次加入6 0.072 g (0.041 mmol), C6F146 mL (29.6 mmol)和乙苯10 mL (82 mmol),以空气为氧源,于60 ℃持续通入空气反应6 h。冷却至室温,有机相与氟碳溶剂分层,取上层有机相分析产物及含量(气相色谱初始温度50 ℃,终止温度250 ℃,程序升温20 ℃·min-1)。
2 结果与讨论
2.1表征

λ/nm
图1是6的UV-Vis 谱图。由图1可见,在300 nm和550 nm 处有吸收峰,表明其形成了配合物结构[10]。结合HR-MS(EI)谱图,可以说明所得产物为目标化合物。
2.2催化性能研究
以催化氧化乙苯(Scheme 2)为模板反应,考察6在氟两相催化中的性能。分别考察了催化剂用量,反应时间,反应温度和回收次数对乙苯氧化的影响。

Scheme 2
(1) 催化剂用量
以6为催化剂,于60 ℃反应6 h,考察了不同催化剂用量对乙苯催化氧化反应的影响。其结果见表1。

表1 6用量对乙苯氧化的影响
由表1可见,催化剂用量对乙苯转化率影响较大,对苯乙酮选择性影响不大。未加入催化剂时,乙苯的转化率很低;当催化剂用量为0.04 mmol时,乙苯的转化率最大(49.20%)。当催化剂的量进一步加大时,催化剂分子之间会聚集[13],使得活性组分的有效活性面积减小,不利于其与氧气的结合,从而导致催化效率下降。
(2) 反应时间
6 0.04 mmol,反应温度60 ℃,考察了反应时间对乙苯氧化反应的影响,结果见表2。

表2 反应时间对乙苯氧化的影响
由表2可见,随着反应时间增加,乙苯的转化率增大,氧化反应速度明显加快,苯乙酮的选择性变化不大,说明该反应具有明显的诱导期。 反应时间为6 h 时,转化率趋于平缓,同时转化率和选择性都达到最大值,分别为49.20%和88.3%。随着时间的延长,选择性降低明显,这是由于苯乙酮发生深度氧化[14]。

表3 温度对乙苯氧化的影响
(3) 反应温度
6 0.04 mmol,反应时间为6 h,考察温度对乙苯氧化反应的影响,结果见表3。由表3可见,随着温度的升高,乙苯转化率和选择性均有所增加,且反应速率也逐渐提高,但温度达到60 ℃以后,不仅转化率下降,其选择性也下降。故最佳反应温度为60 ℃。导致这种现象可能有两种原因:第一,氧气溶解度下降;第二,升高温度也加速了氧化产物进一步被氧化[15]。
(4) 回收次数对乙苯氧化的影响
根据氟碳溶剂的热力学特性分离回收全氟溶剂及氟代催化剂,再应用于乙苯的催化氧化实验中,回用7次得出的结果见表4。
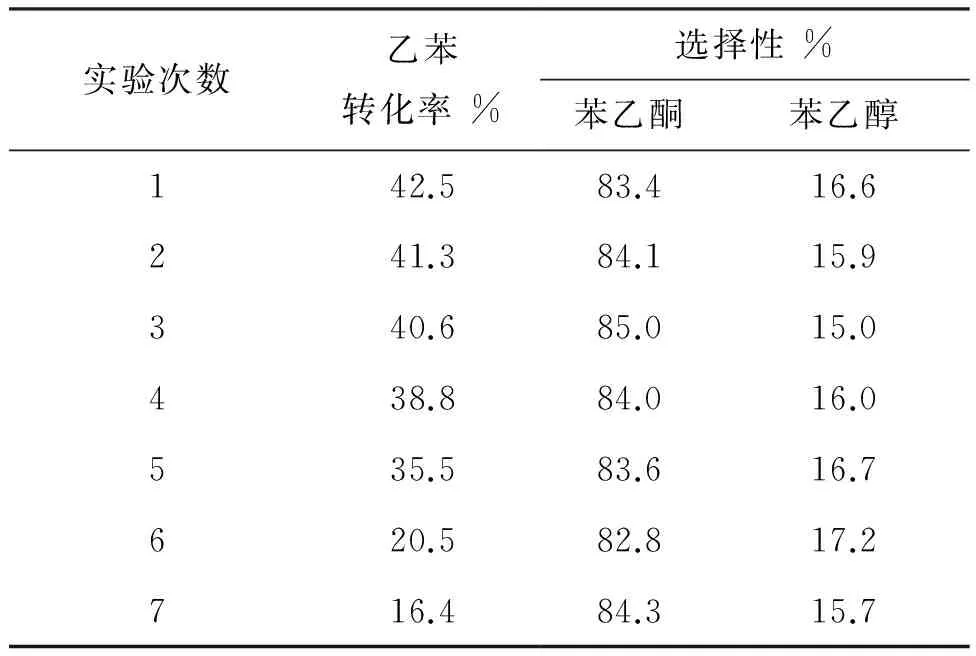
表4 回收次数对乙苯氧化的影响
由表4可以看出,氟碳相重复使用5次后乙苯转化率下降明显,但苯乙酮的选择性保持良好,由此说明6在多次使用后选择性依旧保持良好。
以全氟碘丁烷为原料,分别与4-碘硝基苯和4-碘苯甲酸反应合成了4-全氟丁基硝基苯(1)和4-全氟丁基苯甲酸(3); 1经还原反应,3经酰氯化反应,后经缩合反应制得氟代苯基异羟肟酸(5); 5经络合反应合成氟代苯基异羟肟酸钴(6)。在氟两相中考察了其对乙苯氧化的催化性能。结果表明:在全氟己烷中, 6 0.04 mmol,于60 ℃反应6 h,乙苯的转化率为49.2%,苯乙酮的选择性为88.3%,催化剂循环使用5次,催化剂选择性保持良好。6在氟两相催化中的应用提供了一种绿色环保的催化氧化工艺,对拓展氟两相催化的开发应用具有重要意义。
[1]Horvath I T, Rabai J. Facile catalyst separation without water:Fluorous biphase hydroformylation of olefins[J].Science,1994,266:72-75.
[2]Katarzyna S. Behaviour of the fluorocarbon surfactants in the monolayer at the water-air interface and in the bulk phase[J].Journal of Fluorine Chemistry,2013,150:109-116.
[3]Hongren C. Fluorocarbon and hydrocarbonN-Heterocyclic (C5-C7) imidazole-based liquid crystals[J]. Chem Asian J,2014,9(12):3418-3410.
[4]Xi Z, Dong M H. Fluorous Hydrogenation[J].Top Curr Chem,2012(308):233-246.
[5]Richter B, Spek A L, Van K G,etal. Fluorous versions of wilkinson’s catalyst:Activity in fluorous hydrogenation of 1-alkenes and recycling by fluorous biphasic separation[J].J Am Chem Soc,2000,122:3945-3951.
[6] 卢法冠. 氟代席夫碱体系中C—F键和C—H键的选择性活化和功能化[D].济南:山东大学,2014.
[7]伍新燕,吴成泰. 含氮杂冠醚结构单元的吲哚啉螺苯并吡喃的合成和性质[J].应用化学,1998,15(2):106-108.
[8]张丹,常晓红,张兵,等. 金属酞菁衍生物催化的模拟酶反应研究进展[J].辽宁大学学报自然科学版,2003,30(1):87-97.
[9]付时雨,詹怀宇,余惠生. 苯基羟胺及N-酰基衍生物的合成表征[J].华南理工大学学报,2000,28(5):59-63.
[10]张春春. 杯芳烃异羟肟酸的设计合成及过渡金属配合物的仿酶功能研究[D].成都:四川大学,2003.
[11]吕志凤,李鸿波. 异羟肟酸过渡金属配合物的合成及其催化氧化性能研究[J].四川大学学报,2000,37(3):426-431.
[12]秦川,梁伍. 卤代异羟肟酸钴(II)配合物催化氧化二甲苯的研究[J].分子催化,2009,23(1):62-65.
[13]侯韩鹏,孙霞. 氧化铝负载Co基F-T合成催化剂还原反应[J].分子催化,2011,25(3):238-243.
[14]杜治平,周彬. Cu(phen)Cl2催化甲醇氧化羰基化合成碳酸二甲酯[J].催化学报,2012,33(4):736-742.
[15]王小丽,徐南平,杨刚,等. 枝状钴配合物的合成及其对苯乙烯环氧化的催化性能[J].南京工业大学学报(自然科学版),2014,36(1):23-27.
Synthesis of Fluoro-phenyl Hydroxamic Acid Cobalt and Its Catalytic Activity for the Oxidation of Ethylbenzene
CHEN Xiao-feng,QIU Tao*,LÜ Xin-yu
(Institute of Design and Research, Changzhou University, Changzhou 213164, China)
p-Perfluorohexyl nitrobenzene(1) andp-perfluorohexyl acid(3) were synthesized by reaction of perfluorobutyl iodide with 4-iodonitrobenzene and 4-iodobenzoic acid respectively. Fluoro-phenyl hydroxamic acid (5) was prepared by condensation reaction of the reduction product of 1 with acyl chloride product of 3. The hydroxamic aic-containing cobalt perfluorohexyl chain complexes(6) was synthesized by complexation reaction of 5. The structure was characterized by UV-Vis,1H NMR, FT-IR and HR-MS(EI). Its catalytic activity for the oxidation of ethylbenzeneIt was investgated. The results indicated that the amount of catalyst was 0.04 mmol and the reaction was carried out at 60 ℃ for 6 h, the conversion of ethyl benzene was up to 49.2% and the selection of acetophenone was 88.3% under the conditions of perfluorohexane as solvent. The selectivity of catalyst can maintain good after recycling for five times.
fluoro-phenyl hydroxamic acid cobalt; fluorocarbon catalysis; oxidation of ethyl benzene; synthesis; catalytic activity
2015-11-12;
2016-06-16
国家自然科学基金资助项目(21276030)
陈小峰(1990-),男,汉族,江苏淮安人,硕士研究生,主要从事精细化工的研究。E-mail: xfchen2009@163.com
邱滔,研究员, Tel. 0519-86330181, E-mail: qiutao@cczu.edu.cn
O641.4; O621.3
ADOI: 10.15952/j.cnki.cjsc.1005-1511.2016.09.15376
