微波辅助法合成Hantzsch酯
2016-10-25尹晓刚吴小云陈治明
尹晓刚, 吴小云, 王 野, 陈治明, 陈 卓
(贵州师范大学 化学与材料科学学院 贵州省功能材料化学重点实验室,贵州 贵阳 550001)
微波辅助法合成Hantzsch酯
尹晓刚, 吴小云, 王野, 陈治明, 陈卓*
(贵州师范大学 化学与材料科学学院贵州省功能材料化学重点实验室,贵州 贵阳550001)
以芳香醛、乙酰丙酮及碳酸氢铵为原料,固载路易斯酸蒙脱土为催化剂,通过微波辅助法催化合成了5个Hantzsch酯类化合物,其结构经1H NMR和IR确证。考察了催化剂、溶剂、温度、时间和氮源对产率的影响。结果表明:反应温度60 ℃,微波辐照时间10 min,n(芳香醛) ∶n(乙酰乙酸乙酯) ∶n(碳酸氢铵)=2.0 ∶2.0 ∶1.0,氯化镍固载蒙脱土为催化剂(10%),产率高达97.8%。
微波辅助法; 固载路易斯酸蒙脱土; 合成; Hantzsch酯
Hantzsch酯具有抗菌、抗癌、抗肿瘤、抗氧化、抑制糖尿病和钙拮抗剂等多种生理活性,可以作为氢源,完成C=C、C=N、C=O的氢转移反应[1-2]。最早由芳醛、5,5-二甲基-1,3-环己二酮、氨水及乙酰乙酸乙酯在乙醇中回流制得,反应时间较长,产率不高。近年来,其合成受到广泛关注。路军[3]等使用三氯化铁作催化剂,醛、乙酰乙酸乙酯和碳酸氢铵为原料加热回流合成多种Hantzsch酯,用时0.5~1 h。史达清[4]等以醋酸铵为氮源,水溶液中氯化三乙基苄基铵催化合成1,4-二氢吡啶衍生物,于90 ℃反应4~8 h。以醛、乙酰乙酸乙酯和醋酸铵为原料,当用三甲基氯硅烷和碘化钠作催化剂时,室温下反应6~8 h,产率中等[5]。现有合成方法仍存在反应时间长、催化剂腐蚀性较大且不易回收、产物后处理步骤复杂等问题[6-10]。

Scheme 1
1986年,Richard Gedye等在苯胺酸性水解反应中首次引入微波辐照[11]。微波反应可以提供非常特殊的物理环境,有效缩短反应时间,降低能耗并提高反应产率。微波辐射法具有如下优势[12]: (1) 微波的穿透作用使其不受反应容器的限制,热效应均匀迅速,具有良好的加热效率;(2) 微波可以减少反应时间从而降低能耗,符合“绿色化学”的要求。我们通过微波辅助法完成了KP550,季鏻盐及芦竹碱等多种化合物的合成[13-15]。
本文以芳香醛、乙酰丙酮及碳酸氢铵为原料,蒙脱土负载路易斯酸为催化剂,通过微波辅助法一锅合成5个Hantzsch酯类化合物(4a~4e, Scheme 1),其结构经1H NMR和IR确证。并考察了催化剂、溶剂、温度、时间和氮源对收率的影响。
1 实验部分
1.1仪器与试剂
X-6型显微熔点仪;ZF-I型三用紫外分析仪;AVANCEIII 400MHz型核磁共振仪(CDCl3为溶剂); IS5型傅立叶变换红外光谱仪(KBr压片);Nova型单模微波合成仪。
固载蒙脱土/路易斯酸参考文献[16]方法制备;水为蒸馏水; 其余所用试剂均为分析纯。
1.2合成
(1) 4a~4e的合成(以4a为例)
在反应瓶中依次加入苯甲醛(1a)51.0 μL(0.5 mmol)、乙酰丙酮(2) 123.2 μL(1.2 mmol)、碳酸氢铵39.5 mg(0.5 mmol),蒸馏水0.5 mL,于60 ℃微波辐射10 min。冷却至室温,经乙酸乙酯(3×10 mL)萃取,合并萃取液,用无水硫酸钠干燥,经硅胶柱层析(洗脱剂: A=V乙酸乙酯∶V石油醚=1 ∶7)纯化得白色固体4a 91.3 mg,产率67.9%。
用类似方法合成4b~4e。
4a: 产率67.9%, m.p.179~181 ℃(180~182 ℃[17]);1H NMRδ: 7.25(dd,J=8.8 Hz, 2.4 Hz, 2H), 7.15~7.10(m, 3H), 5.60(br s, 1H), 5.01(s, 1H), 2.37(s, 6H), 2.23(s, 6H); IRν: 3 321(N—H), 3 065(=C—H), 2 931(C—H), 1 671(C=O), 1 600, 1 470(C=C), 1 375(C—C=O), 1 302(C—C—C), 1 021(C—N), 791, 727(芳香环一元取代) cm-1。
4b: 产率97.8%, m.p.151~153 ℃(152~153 ℃[17]);1H NMRδ: 7.25(s, 1H), 6.20(m, 1H), 5.98(d,J=3.6 Hz, 1H), 5.64(br s, 1H), 5.18(s, 1H), 4.16(q,J=8.2 Hz, 4H), 4.10(q,J=7.1 Hz, 4H), 2.33(s, 6H), 1.25(t,J=7.2 Hz, 6H); IRν: 3 347(N—H), 3 091(C—H), 2 987(CH3), 1 695(C=O), 1 651, 1 490(C=C), 746, 727 cm-1。
4c: 产率83.1%, m.p.135~137 ℃(136~138 ℃[4]);1H NMRδ: 7.16(d,J=7.2 Hz, 2H), 7.00(d,J=7.2 Hz, 2H), 5.72(br s, 1H), 4.91(s, 1H), 4.10(q,J=7.2 Hz, 4H), 2.30(s, 6H), 2.29(s, 3H), 1.21(t,J=7.2 Hz, 6H); IRν: 3 352(N—H), 2 991(CH3), 1 702(C=O), 1 652, 1 491(C=C), 1 100, 1 093, 821(芳香环对二元取代) cm-1。
4d: 产率89.0%, m.p.158~160 ℃(158~159 ℃[4]);1H NMRδ: 7.21(d,J=8.0 Hz, 2H), 6.73(d,J=8.0 Hz, 2H), 5.70(br s, 1H), 4.90(s, 1H), 4.11(q,J=7.2 Hz, 4H), 3.77(s, 3H), 2.31(s, 6H), 1.21(t,J=7.2 Hz, 6H); IRν: 3 352(N—H), 2 992(C—H), 1 702(C=O), 1 651, 1 503(C=C), 1 385(C—N), 1 300(C—O—C), 1 211, 806(芳香环对二元取代) cm-1。
4e: 产率95.8%, m.p.160~161 ℃(162~163 ℃[4]),1H NMRδ: 8.13(s, 1H), 8.00(d,J=8.0 Hz, 1H), 7.66(1H), 7.36(t,J=8.0 Hz, 1H), 5.77(br s, 1H), 5.10(s, 1H), 4.12(q,J=7.2 Hz,4H), 2.35(s, 6H), 1.21(t,J=7.2 Hz,6H); IRν: 3 331(N—H), 2 993(C—H), 1 701(C=O), 1 635, 1 511, 1 478(C=C), 1 346, 1 208(C—N), 753, 701(芳香环间二元取代) cm-1。
2 结果与讨论
2.1反应条件优化
为进一步优化4的合成条件,以4a的合成为例,研究了催化剂、溶剂、温度、时间和氮源对收率的影响。
(1) 氮源
考察氮源对产率的影响,结果见表1。由表1可见,碳酸氢铵为氮源时产率最高(61.8%),碳酸铵为氮源时产率稍低(54.9%),可能因为碳酸铵溶液在70 ℃时开始分解,而碳酸氢铵溶液在60 ℃时就可完全分解,有利于氮参与反应;浓氨水为氮源时产率为37.4%,推测是氨水中含大量的水导致体系浓度降低,产率下降;醋酸铵和氯化铵为氮源时产率分别为35.2%和13.4%,推测原因是这两种铵盐分解温度较高,且氯化铵要在137.8 ℃时才完全分解出氨气,导致氮不能被有效利用,影响反应收率。因此选碳酸氢铵为氮源。

表1 不同氮源对产率的影响*
*n(苯甲醛) ∶n(乙酰丙酮) ∶n(氮源)=1 ∶2 ∶1, MMT/NiCl2(10%)为催化剂,水为溶剂,于80 ℃微波5 min。
(2) 催化剂及溶剂
溶剂对1,4-二氢吡啶产率的影响见表2。由表2可见, MMT/NiCl2作催化剂时产率最高(61.8%);因此,选用MMT/NiCl2为催化剂。以 MMT/NiCl2为催化剂,考察溶剂对产率的影响。结果表明:用水做溶剂时产率最高(61.8%);可见质子性溶剂有利于反应产率的提高,碳酸氢铵在水溶液中溶解度好,利于其分解为氨参与反应。值得注意的是:该反应体系不需相转移催化剂,推测反应可能在固载催化剂表面进行。
(3) 反应时间、温度及原料比
以反应温度、时间,苯甲醛、乙酰丙酮及碳酸氢铵的用量为5因素,设计L16(4)5正交实验。以MMT/NiCl2为催化剂,水作溶剂,考察反应温度、时间及原料摩尔比对产率的影响。得出最佳合成条件为MMT/NiCl2(10% mol)为催化剂,水作溶剂,反应温度为60 ℃、时间10 min,n(苯甲醛) ∶n(乙酰丙酮) ∶n(乙酰乙酸乙酯)=1.0 ∶2.4 ∶1.0,此时产率为67.9%。
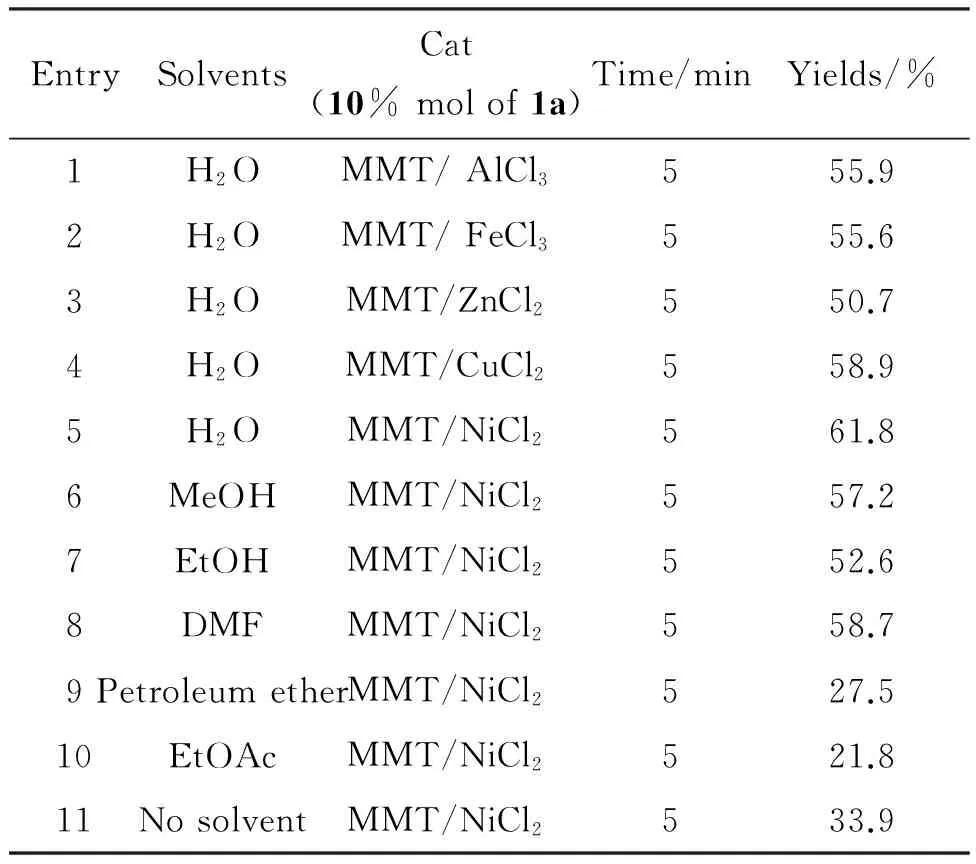
表2 催化剂及溶剂对产率的影响*
*苯甲醛0.5 mmol、乙酰丙酮1.0 mmol、碳酸氢铵0.5 mmol,于80 ℃微波5 min,催化剂用量为(10%)。
(4) 催化剂循环使用次数
回收催化剂继续催化该反应,以考察催化剂的循环使用能力(表3)。结果表明:催化剂回收3次后产率为71.1%;回收2次后产率为64.0%,回收1次后产率为66.0%。催化效率基本稳定,催化剂具有良好的循环使用能力。

表3 催化剂回收次数对产率的影响*
*1a 51.0 μL(0.5 mmol),n(苯甲醛) ∶n(乙酰丙酮) ∶n(碳酸氢铵)=1.0 ∶2.4 ∶1.0, MMT/NiCl2作催化剂(10%醛摩尔比),水作溶剂,于60 ℃微波10 min。
综上所述,最佳反应条件为反应温度60 ℃,微波辐照时间10 min,n(芳香醛) ∶n(乙酰乙酸乙酯) ∶n(碳酸氢铵)=2.0 ∶2.0 ∶1.0,氯化镍固载蒙脱土为催化剂(10%)。
2.2底物适应性考察
在最优条件下,考察不同醛与1,3-二羰基化合物及碳酸氢铵的反应(Scheme 1)。实验结果表明:1,3-二羰基化合物为乙酰乙酸乙酯时,呋喃甲醛的产率最高(97.8%, 4b);可见杂环化合物对该反应有良好的适应性;当苯环被吸电子基取代时,有利于此反应的进行。以乙酰丙酮为原料时,苯甲醛的产率为67.9%(4a)。可见R2为酯基时有利于1,3-二羰基化合物参加反应,空间位阻对产率也会产生影响。
采用微波辅助法水相合成了5个1,4-二氢吡啶衍生物,最佳反应条件为:n(醛) ∶n(乙酰乙酸乙酯) ∶n(碳酸氢铵)=1.0 ∶2.4 ∶1.0, MMT/NiCl2(10%)为催化剂,微波辐射10 min、温度60 ℃,产率最高达97.8%, 催化剂有一定的循环使用能力。该方法具有反应时间短、产率高、能耗低的优点,符合“绿色化学”的时代要求。
[1]Stoud D M, Meyers A I.Recent advances in the chemistry of dihydropyridines[J].Chem Rev,1982,82(2):223-243.
[2]Wang D H, Liu Q, Chen B,etal. Photooxidation of Hantzschhantzsch esters by molecular oxygen[J].Chinese Sci Bull,2010,55:2855-2858.
[3]路军,白银娟,杨秉勤,等. 1,4二氢吡啶衍生物合成方法的改进和芳构化研究[J].有机化学,2000,20(4):514-51.
[4]史达清,牟杰,庄启亚,等. 水溶液中4-芳基-1,4-二氢吡啶衍生物的一步合成法[J].有机化学,2004,24(9):1042-1044.
[5]Sabitha G, Reddy G S K K, Reddy C S,etal. A novel TMSI-Mediated synthesis of Hantzsch 1,4-dihydropyridines at ambient temperature[J].Tetrahedron Letters,2003,44(21):4129-4131.
[6]赵炳筠,朱晓晴,何家淇,等. 1,4-二氢Hantzsch吡啶衍生物的合成及其1H NMR和荧光光谱研究[J]高等学校化学学报,1999,20(11):1733-1737.
[7]陈翠,谭丽泉,邱会华. 乙酰乙酰芳胺类化合物导向的五取代1,4-二氢吡啶衍生物的合成[J].有机化学,2014,34:1673-1676.
[8]王道林,吴健莹,董哲,等. 3,3′-芳基(烷基)二(4-氨基香豆素)和1,4-二氢吡啶并[3,2-c][5,6-c]双香豆素类衍生物的有效合成[J].有机化学,2015,35:200-206.
[9]赵兴华,牟书勇,赵莉. 无溶剂微波辐射下硝酸镱高效催化合成1,4-二氢吡啶衍生物[J].高等学校化学学报,2012,33(5):954-957.
[10]Javad S, Sayed H B, Shiva D K. Cobalt nanoparticles promoted highly efficient one pot four-component synthesis of Hantzsch esters under solvent-free conditions[J].Chinese Journal Cat,2011,32(12):1850-1855.
[11]Gedye R, Smith F, Westaway K,etal. The structures of spirasine V and pirasine VI[J].Tetrahedron Lett,1986,27(3):279-292.
[12]Kremsner J M, Kappe C O. Microwave-assisted organic synthesis innear-criti[J].Polym Prepr,2008,49:951-981.
[13]尹晓刚,张林,赵正容,等. 微波辅助法合成KP550[J].工业水处理,2013,30(12):56-58.
[14]尹晓刚,赵正容,肖维军,等. 微波辅助法合成季鏻盐[J].日用化学工业,2014,44(1):15-18.
[15]吴伟,吴小云,吴江,等. 负载型蒙脱土催化芦竹碱的微波合成[J].合成化学,2015,23(6):543-546.
[16]李记太,蔺志平. 蒙脱土K10-ZnCl2催化下研磨法合成二吲哚甲烷衍生物[J].有机化学,2008,28(7):1238-1242.
[17]蔡小华,张国林. 无溶剂一锅法合成1,4-二氢吡啶[J].有机化学,2005,25(8):930-933.
Preparation of Hantzsch Ester Derivatives under Microwave Conditions
YIN Xiao-gang,WU Xiao-yun,WANG Ye,CHEN Zhi-ming,CHEN Zhuo*
(Key Laboratory of Functional Materials Chemistry of Guizhou Province, School of Chemistry and Materials Science, Guizhou Normal University, Guiyang 550001, China)
Five Hantzsch ester derivatives were synthesized using aromatic aldehydes, acetacetic ester and ammonium bicarbonate as starting materials with immobilized montmorillonite/Lewis acid as catalyst under microwave conditions. The effects of the reaction temperature, reaction time, solvent, catalyst and nitrogen source on the yield were investigated. The optimal conditions were as followed: the reaction temperature was 60 ℃, microwave irradiation for 10 min, the molar ratio of aromatic aldehyde, ethyl acetoacetate and ammonium bicarbonate was 2.0 ∶2.0 ∶1.0, nickel chloride immobilized montmorillonite as catalyst, the yield was up to 97.8%.
microwave assisted method; imobilized montmorillonite/Lewis acid; synthesis; Hantzsch ester
2016-01-04
国家自然科学基金资助项目(21362006); 贵州省科学技术基金资助项目(黔科合J字[2014]2129号)
尹晓刚(1976-),男,汉族,浙江嘉兴人,博士,主要从事有机合成方法学研究。 E-mail: m13885115516@163.com
陈卓,硕士,教授, Tel. 0851-86700050, E-mail: chenzhuo19@163.com
O629.32
ADOI: 10.15952/j.cnki.cjsc.1005-1511.2016.09.16004
