呋喃西林片2015年版微生物限度检查标准及探索性研究
2016-10-10李俨姜丽
李 俨 姜 丽
呋喃西林片2015年版微生物限度检查标准及探索性研究
李 俨 姜 丽
目的 为了适应《中国药典》2015年版的出版,新版药典中微生物限度检查法中对部分培养基和试验菌株进行了改动,需要对呋喃西林片重新建立微生物限度检查方法。方法 采用薄膜过滤法作为需氧菌总数测定及霉菌和酵母菌总数的测定(总冲洗量均为1 000 ml);薄膜过滤法作为控制菌检查方法。结果 需氧菌总数测定可采用薄膜过滤法,霉菌和酵母菌总数的测定可采用薄膜过滤法,控制菌检查金黄色葡萄球菌可采用薄膜过滤法(总冲洗量为1 000 ml)、铜绿假单胞菌可采用培养基稀释法(总冲洗量为1 000 ml)。结论 经多次试验方法准确精密度强、重复性好,可用于该制剂的微生物限度检查。
2015年版药典;薄膜过滤法;呋喃西林片;抑菌;菌液;回收率
呋喃西林片是由呋喃西林、10%淀粉浆、硬脂酸镁、滑石粉混合制成,具有消毒防腐。用于皮肤、粘膜、肠道的消毒。为了人民群众的用药安全和保证药品质量,进行微生物限度检查方法验证试验,采用最适宜的方法,尽可能的检出不合格产品。
1 仪器、培养基与菌种
1.1 仪器
SPX-150B-Z型生化培养箱;GHB-9162型电热恒温培养箱;GZX-9070型电热干燥箱;LMQ·C型高压锅;JA5003型电子天平(d=0.01 g)。
1.2 培养基
胰酪大豆胨琼脂培养基、沙氏葡萄糖琼脂培养基、沙氏葡萄糖液体培养基、胰酪大豆胨液体培养基、肠道菌增菌液体培养基、麦康凯液体培养基、RV沙门增菌液体培养基、木糖赖氨酸脱氧胆酸盐琼脂培养基、溴化十六烷基三甲铵琼脂培养基、甘露醇氯化钠琼脂培养基、pH 7.0无菌氯化钠-蛋白胨缓冲液、0.9%无菌氯化钠溶液均符合《中国药典》2015年版四部的要求[1]。以上培养基均由中国食品药品检定研究院提供。
1.3 菌种
金黄色葡萄球菌、铜绿假单胞菌、枯草芽孢杆菌、白色念珠菌、黑曲霉均符合《中国药典》2015年版四部的要求。
1.4 供试品
呋喃西林片,解放军空军某医院,批号20160202、20160210、20160204
2 方法与结果
2.1 需氧菌、霉菌和酵母菌计数方法的验证
2.1.1 供试液制备 取供试品10 g,加入45℃ pH7.0无菌氯化钠-蛋白胨缓冲液至100 ml,振荡混匀,取上清液作为1:10供试液。
2.1.2 计数方法适用性试验 试验组:
(1)培养基稀释法(0.1 ml):取1:10供试液10 ml,加入试验菌0.1 ml,混匀,分别吸取2 ml注入2个平皿中,立即倾注胰酪大豆胨琼脂培养基,置35℃温度培养3~5 d逐日观察结果,按平皿法测定其菌数。
(2)薄膜过滤法:取1:10供试液1 ml,滤膜孔径为0.45 µm,直径为50 mm,每张滤膜每次冲洗量为100 ml,总冲洗量为700 ml。
(3)薄膜过滤法:取1:10供试液1 ml,滤膜孔径为0.45 µm,直径为50 mm,每张滤膜每次冲洗量为100 ml,总冲洗量为1 000 ml。
供试品对照组:取1:10供试液,以稀释液代替菌液同试验组操作。
菌液对照组:用pH7.0无菌氯化钠-蛋白胨缓冲液代替供试液,按试验组操作加入试验菌液并进行微生物回收试验。
2.1.3 结果 详见表1~3。
以上5种菌的回收率薄膜过滤法比值均在0.5~2。
2.2 控制菌检查方法的验证
2.2.1 取供试品10 ml,加入45℃ pH7.0无菌氯化钠-蛋白胨缓冲液至100 ml,振荡混匀,作为1:10供试液。
2.2.2 金黄色葡萄球菌 阳性对照试验组:
薄膜过滤法:取1:10供试液上清液10 ml,用45℃ pH7.0无菌氯化钠-蛋白胨缓冲液冲洗,过滤,共10次,在最后一次冲洗液中加入10~100 cfu金黄色葡萄球菌试验菌液1 ml,总冲洗量为1 000 ml,冲洗后取出滤膜接入100 ml胰酪大豆胨液体培养基中,置规定温度培养48 h,取上述培养物,划线接种于甘露醇氯化钠琼脂培养基的平板上,培养72 h,观察结果。
阴性对照组:取稀释液10 ml,用100 ml 45℃ pH7.0无菌氯化钠-蛋白胨缓冲液冲洗,取出滤膜接入100 ml营养肉汤培养基中,置规定温度培养48 h,取上述培养物,划线接种于甘露醇氯化钠琼脂培养基的平板上,培养72 h,观察结果。
结果:薄膜过滤法总冲洗量为1 000 ml,检出。
2.2.3 铜绿假单胞菌 阳性对照试验组:
薄膜过滤法:取1:10供试液上清液10 ml,用45℃ pH7.0无菌氯化钠-蛋白胨缓冲液冲洗,过滤,共10次,在最后一次冲洗液中加入10~100 cfu金黄色葡萄球菌试验菌液1 ml,总冲洗量为1 000 ml,冲洗后取出滤膜接入100 ml胰酪大豆胨液体培养基中,置规定温度培养48 h,取上述培养物,划线接种于溴化十六烷基三甲铵琼脂培养基的平板上,培养72 h,观察结果。
阴性对照组:取稀释液10 ml加入100 ml胰酪大豆胨液体培养基中,35℃培养24 h后按照薄膜过滤法方法观察结果。
结果:薄膜过滤法总冲洗量为1 000 ml,检出。
3 结论
我们按照《中国药典》2015年版四部微生物限度检查法计数方法适用性试验中以上5种菌的比值均在0.5~2。符合药典规定;MPN法的精确度和准确度不及平皿计数,故没采用。按照《中国药典》2015版四部微生物限度检查法控制菌的方法学验证试验,金黄色葡萄球菌可采用培养基稀释法(取1:10供试液10 ml加入1 000 ml胰酪大豆胨液体培养基中)、铜绿假单胞菌可采用培养基稀释法(取1:10供试液10 ml加入1 000 ml胰酪大豆胨液体培养基中)时,阳性对照试验组检出,阴性对照组未检出,表明该控制菌检查方法的专属性好,适用于呋喃西林片的控制菌检查[3]。

表1 菌液组(菌落计数结果,单位:cfu/ml)
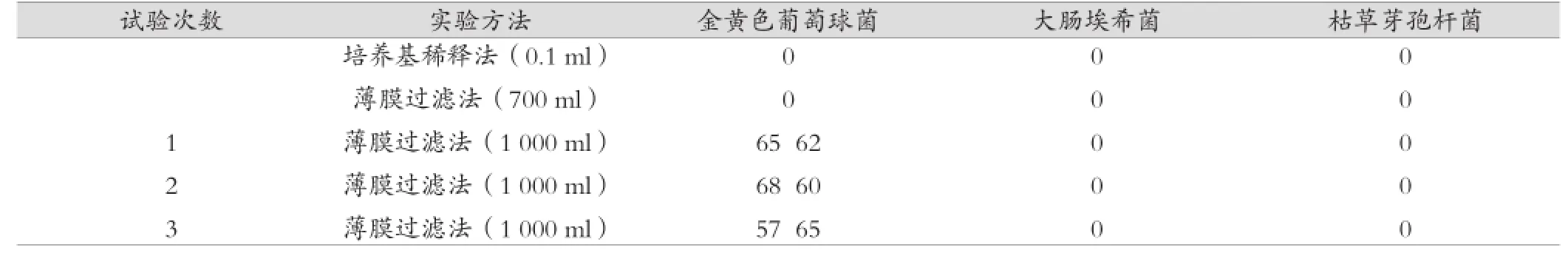
表2 试验组

表3 试验组
[1] 国家药典委员会. 中华人民共和国药典[M]. 北京:中国医药科技出版社,2015:140-148.
[2] 中国药品生物制品检定所,中国药品检验总所. 中国药品检验标准操作规范[M]. 北京:中国医药科技出版社,2010:351.
[3] 李霞,董卫红,韩曼雪,等. 新清宁片微生物限度检查方法研究[J]. 中国中医基础医学杂志,2010(16):825-826.
Inspection Standard and Exploratory Research of Microbial Limit in 2015 With Nitrofurazone
LI Yan JIANG Li Antibiotics Office,Food and Drug Inspection of Jilin City,Jilin Jilin 132001,China
【Abstract】
Objective In order to adapt to the chinese pharmacopoeia 2015 edition of the publication,the new pharmacopoeia in microbial limit test on the part of the culture medium and test strains in the changes,need of nitrofurazone piece to establish microbial limit inspection method. Methods The membrane filtration method is adopted as the determination of the total number of aerobe and determination of the total number of mold and yeast(always flush volumes are 1 000 ml). Membrane filtration method as the control bacteria checking method. Results Determination of the total number of aerobe membrane filtration method can be used,the total number of mold and yeast can be used for determination of the membrane filtration method,control check bacteria staphylococcus aureus can use membrane filtration method(total capacity of 1 000 ml)flushing、pseudomonas aeruginosa culture medium dilution method can be used(total capacity of 1 000 ml)flushing. Conclusion After repeated strong test method for accurate precision,good repeatability,can be used for the preparation of microbial limit examination.
2015 edition pharmacopoeia,Culture medium dilution method,Nitrofurazone,Bacteriostatic,Bacteria liquid,Recovery rate
R97
A
1674-9316(2016)15-0121-03
10.3969/j.issn.1674-9316.2016.15.071
吉林市食品药品检验所抗生素室,吉林 吉林 132001
