辛苍颗粒中药材的定性鉴别和黄芩苷的含量测定*
2016-06-27陈华于波涛范开华金伟华蒲志强王诗华谢秋
陈华 于波涛 范开华 金伟华 蒲志强 王诗华 谢秋
(解放军成都军区总医院药剂科, 四川 成都 610083)
·论著·
辛苍颗粒中药材的定性鉴别和黄芩苷的含量测定*
陈华于波涛范开华金伟华蒲志强王诗华谢秋
(解放军成都军区总医院药剂科, 四川 成都 610083)
【摘要】目的建立辛苍颗粒质量控制标准。方法采用薄层色谱法(TLC)对辛苍颗粒处方中的黄芩、甘草、黄芪进行定性鉴别;采用高效液相色谱法(HPLC)对处方中的黄芩苷进行含量测定,色谱柱为Agilent HC-C18(4.6mm ×250mm,5μm),流动相为甲醇-0.1%磷酸(40∶60),流速为1.0ml/min,检测波长为280nm,柱温为34℃。结果TLC斑点清晰,分离度较好,专属性强,阴性对照无干扰;黄芩苷在1.92~61.44μg/ml范围内浓度与峰面积呈良好的线性关系(r=0.9999),平均回收率为100.30%,RSD=1.82%(n=9)。结论该研究方法准确可靠,重复性好,且简便可行,可用于辛苍颗粒的质量控制。
【关键词】辛苍颗粒;质量标准;黄芩苷;薄层色谱法;高效液相色谱法
辛苍颗粒是由白芷、川芎、苍耳子、黄芪、栀子等11味中药材经提取精制而成的医院制剂,批准文号为成制字(2011)F02010号,具有清热、解毒、祛风、通窍等功效,主治鼻塞、流鼻涕、感冒等。经过多年的临床应用,已成为疗效确切的验方,原质量控制标准方法较为简单。为适应国家对医疗机构制剂室进行GPP管理和军队医疗机构制剂标准提高计划要求,有效控制该制剂质量标准,保证临床用药安全有效,本研究结合现有技术条件,采用薄层色谱法(TLC)对处方中黄芩、甘草、黄芪进行定性鉴别,采用高效液相色谱法(HPLC)对处方中黄芩苷含量进行测定,现将结果报告如下。
1仪器与试药
1.1仪器HP 1100高效液相色谱仪[G1311A Quat Pump泵,G1315A DAD 紫外检测器,Agilent HC-C18(4.6 mm×250 mm,5μm)分析柱,美国Agilent公司];AB135-S型精密电子天平(梅特勒-托利多仪器公司,精度:0.01mg);AE-200S型电子天秤(梅特勒-托利多仪器公司,精度:0.1mg);VGT-1990QTD型超声仪(苏州江东精密仪器有限公司);TGL-18G-C型高速台式离心机(上海安亭科学仪器厂);DU730型紫外分光光度计(美国贝克曼仪器公司);HHS11-Ni2电热恒温水浴锅(北京长安永创科学仪器有限公司);SZ-97型自动三重纯水蒸馏器(上海亚荣生化仪器厂)。
1.2药品与试剂辛苍颗粒样品(成都军区总医院,规格:5g/袋,批号:150120、150121、150122),甘草对照药材(批号:120904-201318),黄芪对照药材(批号:121462-201304),均由中国食品药品检定研究院提供;黄芩苷对照品(批号:110715-201117,纯度:97.0%)由中国食品药品检定研究院提供;阴性样品均为自制;甲醇为色谱纯,其它试剂均为分析纯;水为三重蒸馏水;硅胶G薄层板(青岛海洋化工厂)。
2方法与结果
2.1 TLC鉴别
2.1.1黄芩的TLC鉴别[2,3]取供试品10g,研细,加甲醇30ml,加热回流30min,滤过,滤液蒸干,残渣加甲醇2ml溶解,离心,取上清液,作为供试品溶液。另取黄芩苷对照品适量,加甲醇制成1.0mg/ml的照品溶液。取缺黄芩阴性样品10g,同供试品溶液制备方法制成阴性对照溶液。参照2010年版《中国药典》一部中TLC法[1],分别吸取黄芩苷对照品溶液2μl,供试品溶液和阴性对照品溶液各3μl,点于同一含4%醋酸钠的羧甲基纤维素钠为黏合剂的硅胶G薄层板上,以乙酸乙酯-丁酮-甲酸-水(5∶3∶1∶1)为展开剂,预饱和15min,展开,取出,晾干,喷以1%三氯化铁乙醇溶液,晾干至斑点显色清晰。结果显示,在供试品色谱中,与对照品色谱相应位置上显相同颜色的斑点,阴性对照无干扰,见图1。
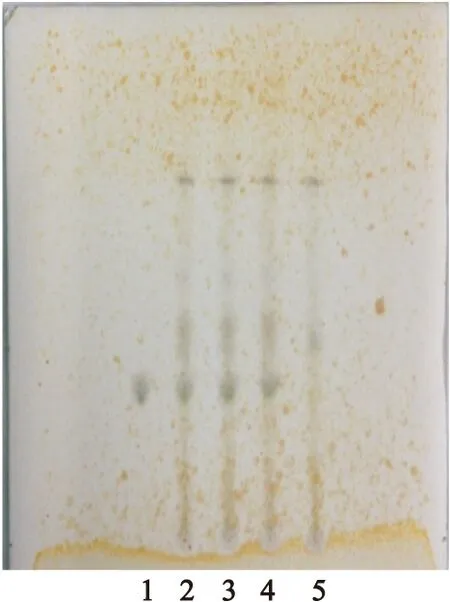
图1黄芩TLC图
Figure 1TLC of Radix Scutellariae
注:1.黄芩苷对照品;2~4.供试品;5.阴性对照
2.1.2甘草的TLC鉴别[4,5]取供试品10g,研细,加三氯甲烷25ml,加热回流1小时,滤过,弃去三氯甲烷液,药渣挥干溶剂,加水5ml搅拌湿润,加水饱和正丁醇50ml,超声处理30min,滤过,取正丁醇液蒸干,残渣加甲醇2ml使溶解,作为供试品溶液。另取甘草对照药材1g和缺甘草的阴性样品10g,同法分别制成对照药材溶液和阴性对照溶液。参照2010年版《中国药典》一部中TLC法[1],分别吸取对照药材溶液6μl、供试品溶液和阴性对照溶液各15μl,点于同一硅胶G薄层板上,以乙酸乙酯-甲酸-冰醋酸-水(15∶1∶1∶2)为展开剂,预饱和15min,展开,取出,晾干,喷以10%硫酸乙醇溶液,在105℃加热至斑点显色清晰并置紫外光灯(365nm)下检视。结果显示,在供试品色谱中,与对照药材色谱相应位置上显相同颜色的斑点,阴性对照无干扰,见图2。

图2甘草TLC图
Figure 2TLC of Radix et Rhizoma Glycyrrhizae
注:1.甘草对照药材;2~4.供试品;5.阴性对照
2.1.3黄芪的TLC鉴别[6,7]取供试品10g,研细,加甲醇10ml,超声处理30min,滤过,滤液蒸干,残渣加水20ml溶解,用水饱和正丁醇振摇提取2次,每次20ml,合并正丁醇液,用氨试液洗涤2次,每次20ml,弃去氨试液,正丁醇液蒸干,残渣加甲醇1ml使溶解,作为供试品溶液。另取黄芪对照药材1g和缺黄芪阴性样品10g,同法制成对照药材溶液和阴性对照品溶液。参照2010年版《中国药典》一部中TLC法[1],分别吸取对照药材溶液8μl、供试品溶液和阴性对照溶液10μl,点于同一硅胶G薄层板上,以乙酸乙酯-丁酮-甲酸-水(5∶3∶1∶1)为展开剂,预饱和15min,展开,取出,晾干,喷以10%硫酸乙醇溶液,在105℃加热至斑点显色清晰后置紫外光灯(365nm) 下检视。结果显示,在供试品色谱中,在与对照药材色谱相应位置上显相同颜色的斑点,阴性对照无干扰,见图3。
2.2黄芩苷的含量测定[8-10]
2.2.1色谱条件与系统适用性试验 色谱柱:Agilent HC-C18(4.6mm×250mm,5 μm);流动相:甲醇-0.1%磷酸(40∶60);流速:1ml/min;检测波长:280nm;柱温:34℃;进样量:10μl,理论板数按黄芩苷峰计算应不低于3000。
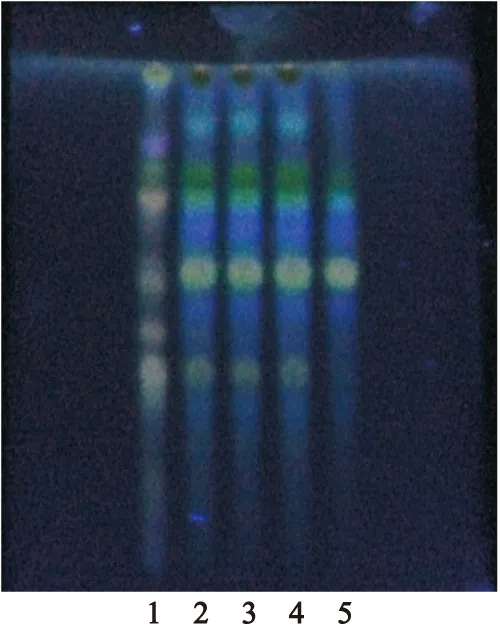
图3黄芪TLC图
Figure 3TLC of Astragali Radix
注:1.黄芪对照药材;2~4.供试品;5.阴性对照
2.2.2对照品溶液的制备精密称取干燥至恒重的黄芩苷对照品适量,加甲醇制成50μg/ml的溶液,即得。
2.2.3供试品溶液的制备取装量差异下的供试品适量,研细,取约0.5g,精密称定,置具塞锥形瓶中,精密加入50%甲醇75 ml,密塞,称定重量,超声处理20min,放冷,称定重量,用50%甲醇补足减失的重量,摇匀,离心,滤过,取续滤液,即得。
2.2.4阴性对照溶液的制备取缺黄芩的阴性样品适量,按“2.2.3”项下方法制备阴性对照溶液,即得。
2.2.5专属性试验精密吸取上述黄芩苷对照品溶液、供试品溶液、阴性对照溶液各10μl, 按上述色谱条件进样测定,记录色谱图。结果显示,阴性对照溶液在与黄芩苷对照品溶液相应的出峰处未见吸收峰,表明阴性对照溶液无干扰,见图4。
2.2.6线性关系考察精密称取黄芩苷对照品适量,加甲醇溶液制成76.8μg/ml的对照品储备溶液。再分别取适量对照品储备溶液,精密量取,加甲醇适量,分别制成每1ml含1.92、3.84、7.68、15.36、30.72、61.44μg的对照品溶液。分别精密吸取上述对照品溶液10μl,按上述色谱条件进样测定,记录色谱图。以对照品的测定浓度(x,mg/ml)为横坐标,峰面积积分值(y)为纵坐标,进行线性回归,得回归方程为:y=23.939x-5.5149(r=0.9999)。结果显示,黄芩苷在1.92~61.44μg范围内浓度与峰面积积分值呈良好的线性关系。
2.2.7精密度试验精密吸取 “2.2.6”项下61.44μg/ml黄芩苷对照品溶液10μl,注入液相色谱仪,按上述色谱条件测定,连续进样6次,记录色谱图。结果显示,计算RSD=0.16%(n=6),表明仪器精密度良好。
图4高效液相色谱图
Figure 4HPLC chromatograms
注:A. 黄芩苷对照品;B. 供试液品;C. 阴性对照品;1.黄芩苷
2.2.8稳定性试验取同一批样品,按“2.2.3”项下方法制备供试品溶液,在室温下放置,分别于0、2、4、8、12,24小时各进样1次,按上述色谱条件测定,记录峰面积。结果显示, RSD=0.54%(n=6),表明供试品溶液在24小时内稳定性良好。
2.2.9重复性试验分别取同一批号样品6份约0.5g,精密称定,按“2.2.3”项下方法制备供试品溶液,进样6次,按上述色谱条件测定,记录峰面积。结果显示, RSD=1.0%(n=6),表明本法重复性良好。
2.2.10加样回收率试验取已知含量的样品9份,约0.25g,精密称定,按3份为1组,每组中分别按样品中黄芩苷含量的80%、100%、120%精密加入对照品溶液,按照“2.2.3”项下方法制备供试液,进样9次,按上述色谱条件测定,计算加样回收率,见表1。
2.2.11样品含量测定取3批供试品各适量,分别按 “2.2.3”项下方法制备供试品溶液,按上述色谱条件测定,记录峰面积,计算样品中黄芩苷的含量,见表2。
3讨论
辛苍颗粒为中药复方制剂,成分较多,彼此干扰,在供试品的前处理过程中,通过提取、分离、纯化,使溶液成分由复杂变简单,减少干扰。在甘草TLC鉴别中,以三氯甲烷为提取溶剂,提取后弃去三氯甲烷液,可减少脂溶性成分干扰。在黄芩TLC鉴别时,参考《中国药典》2010版一部方法,黄芩鉴别使用的薄层板为聚酰胺薄膜,经实验后修订采用含4%醋酸钠的羧甲基纤维素钠为黏合剂的硅胶G薄层板,系临用前自制的薄层板;展开剂筛选过程中,以乙酸乙酯-丁酮-甲酸-水(5∶3∶1∶1)为展开剂,展开后斑点清晰易观察,Rf值适中,斑点清晰匀称,阴性无干扰,重现性好。

表1 加样回收率试验结果(n=9)
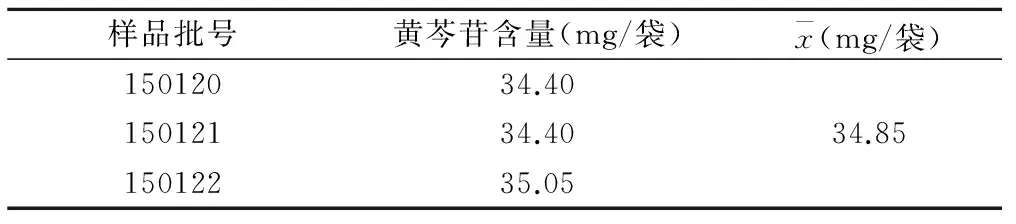
表2 样品中黄芩苷的含量
在黄芩苷含量测定项下流动相的选择中, 参照《中国药典》2010 年版及有关文献,试用多种流动相体系, 甲醇-水-磷酸 (47∶53∶0.2) 、甲醇-0.1%磷酸 (40∶60) 、甲醇-0.3%磷酸 (20∶80)、 甲醇-冰醋酸-水 (40∶1∶60)进行试验, 结果表明,用甲醇-0.1%磷酸溶液 (40∶60)作为流动相,样品分离度较好,峰型佳,保留时间稳定,无杂质峰干扰。
目前,《中国人民解放军医疗机构制剂规范》(以下简称《军规》)虽然经历了多次修订,但随着医药检验技术的发展和安全监管要求的提高,与现行版《中国药典》等国家药品标准相比差距较大,突出表现在以下几个方面。①部分制剂处方工艺不合理。②检验项目设置不够齐全。③检测方法落后,当前通用的技术和设备应用较少。④质控指标偏低,难以控制制剂质量。⑤凡例通则项明显落后于现版《中国药典》,难以保证药品安全、有效和质量可控。⑥非标准制剂审批把握尺度宽严不一,批准后未再进行系统评价和验证,其执行标准中存在的问题比标准制剂更为严重[11]。军队医疗机构制剂标准提高计划是以确保人民群众与官兵用药安全为根本目的,以提高药品标准和药品质量为工作重心,完善监管体制,创新监管机制,依法科学实施监管。通过本次制剂标准提高计划,能够对制剂质量标准有个整体的推进,并初步建立制剂的准入和退出标准,同时完善标准提高的长效机制,将加快《军规》向《中国药典》等国家标准看齐的步伐,更加完善军队医疗制剂的监管制度,全面保障军民用药安全有效。
此次启动“军队制剂标准提高计划”对军队医疗机构制剂的发展是一种强有力的引导,尤其会对军队医疗机构制剂滑坡现状起到推动作用[12],引导配制单位争取各种资金,加大研发投入,引导医院制剂向着重视研发的良性道路发展。
4结论
本研究建立的辛苍颗粒定性鉴别方法,特征斑点明显,分离度佳,阴性对照无干扰;建立的定量方法,精密度、重复性、稳定性均符合要求,所建标准可用于辛苍颗粒质量控制。
【参考文献】
[1]国家药典委员会.中华人民共和国药典一部[S]. 2010年版.北京:中国医药科技出版社,2010 :282.
[2]付延伟,纪松岗,李明春,等.复方茵陈颗粒的质量标准研究[J].解放军药学学报,2015,31(1):53-56.
[3]胡北,马宏达,张朝绅,等. 和肝利胆颗粒的质量标准研究[J].中国药房,2014,25(39):3679-3681.
[4]王辉,袁海铭,陈梅荣.羚羊感冒片薄层临别研究[J].江西中医药,2008,39(2):45-46.
[5]黄可婧,王丽娟.附子理中片的质量标准研究[J].天津药学,2014,26(5):16-20.
[6]农毅清,蒋林,谭安蔷.癌痛消颗粒质量标准研究[J].中国药师,2014,17(11):1859-1832.
[7]尹华,章建华,张春霞,等.芪参健骨颗粒的薄层鉴别研究[J].浙江中医药大学学报,2011,35(1):79-81.
[8]邵红燕,张和明.高效液相色谱法测定肩周炎痛贴中黄芩苷的含量[J].中国药师,2009,12(10):1498-1499.
[9]马一明,刘淑媛.高效液相色谱法测定祛斑膏中黄芩苷的含量[J],中国医院药学杂志, 2010,30(13):1167-1168.
[10] 邵礼梅,王云龙,李延雪.高效液相色谱法测定蒲地蓝消炎片中黄芩苷与黄芩素含量[J].中国药业,2012,21(4):37-38.
[11] 陈征宇,孔爱英. 军队医疗机构制剂标准提高计划实施构想[J].中国药事,2013,27(11):1157-1160.
[12] 文娟,张珂良,汪丽,等.对我国医疗机构制剂管理现状的思考[J].中国药事,2012,26 (4):321-323.
Qualitative identification of Xincang Granules and determination of Baicalin in Xincang Granules
CHEN Hua,YU Botao,FAN Kaihua,et al
(DepartmentofPharmacy,GeneralHospitalofChengduMilitaryCommand,Chengdu610083,China)
【Abstract】ObjectiveTo establish the quality standard of Xincang Granules. MethodsThe TLC method was used to qualitatively identify Radix Scutellariae, licorice and Astragali Radix. HPLC method was adopted to determine the content article of baicalin.The determination was performed on Agilent HC-C18(4.6mm ×250mm,5μm) column with mobile phase consisted on methyl alcohol-0.1% phosphoric acid(40∶60) at the flow rate of 1.0ml/min,the column temparature was 34℃ and the detection wavelength was set at 280nm.ResultsThe spots of TLC were fairly clear with the good separation. The negative samples showed no interference. The linear range of baicalin was 1.92~61.44μg/m1(r=0.9999).The average recovery rate was 100.30%. The RSD was 1.82%(n=9).ConclusionThe simple, rapid and reliable method can be used for the quality control of Xincang Granules.
【Key words】Xincang Granules;Quality standard;Baicalin; TLC;HPLC
基金项目:总后卫生部军队医疗机构制剂标准提高科研专项课题(14ZJZ18-2)
通信作者:范开华,主任药师,硕士研究生导师。E-mail:fankeyi@sohu.com
【中图分类号】R 914
【文献标志码】A
doi:10.3969/j.issn.1672-3511.2016.06.026
(收稿日期:2015-12-02; 编辑: 母存培)
