有机化学中的大-电子云分析法
2015-12-06黄池宝胡明华曾启华曾伯平
黄池宝,胡明华,曾启华,曾伯平
(1.遵义师范学院化学化工学院,贵州遵义563002;2.韶关学院农业科学与工程学院,广东韶关512005)
黄池宝1,2,胡明华1,曾启华1,曾伯平1
(1.遵义师范学院化学化工学院,贵州遵义563002;2.韶关学院农业科学与工程学院,广东韶关512005)
作者通过系统阐述苯及其衍生物、吡啶及呋喃、噻吩、吡咯的大 -电子云分析法,揭示了大 -电子云分析法不仅是把握化合物性质与反应特性的便捷办法,而且是解答有机化学问题的一把钥匙。用大 -电子云分析法来理解与掌握有机化学理论体系可以收到高屋建瓴、事半功倍的效果,是一种优良的教学方法,值得大力推广应用。
大 -电子云;有机化学;分析法;教学效果
芳香化合物与芳香杂环化合物,都属于共轭化合物,共轭p-电子数比较多,-电子云密度一般也比较大。这些共轭化合物性质比较复杂,反应特性千差万别,学起来比较费劲,难度也比较大。有机化学几乎离不开这些共轭化合物,虽然脂肪烃与脂环烃不属于这类化合物,但它们在有机化学中所占比重很小,考试与实验研究很少遇到纯粹的脂肪烃与脂环烃,至多是共轭体系中带有这些结构单元。
因此,学好共轭化合物对学好有机化学至关重要。单纯的熟记知识点与多做练习固然重要,但更为重要的是要采用便捷的学习方法与技巧来指导自己的学习,这样才能学起来轻松,且能收到事半功倍的效果。教师在讲授共轭体系化合物时也应注意方法的引导,使学生一点便通,既可以提高教学效果与学习效率,还可以减轻施教者与受教者双方共同的负担,从而显著提高学生的学习成绩。
电子云分析法正是满足这些要求的一种比较稳妥可靠的有机化学学习与教授之法。笔者对大-电子云分析法在有机化学教学中的运用作了系统阐述,以期为学习该门课程的学生提供借鉴,促进这一
教学法的推广与应用,同时也为有机化学的教学起到抛砖引玉的作用。
1 大?-电子云分析法
当原子之间有一对以上电子时,所对应的化学键称为重键。最常见的重键是由一个键和一个或数个p―p键或p―p大键组成的。键是成健原子的p轨道电子云“肩并肩”进行重叠而形成的共价键。一般来说,健不能独立存在,总是和键一起形成双键或叁键。键的特点是重叠的电子云分布在两核连线的上下两方,受原子核束缚力小,电子云重叠程度要比键小得多,所以键不如键牢固。但是键电子云受原子束缚力小,离核较远,能级较高,电子的能量较高,易活动,其化学性质较键活泼。键绕键轴(两轴连线)旋转后会发生断裂。
2 大?-电子云分析法的三种方式
苯及其衍生物、稠环化合物、吡啶、吡咯、呋喃和噻吩均含有大-电子云,有的是六元环(如苯),有的则为五元环(如呋喃)。不论环的大小,-电子数均必须符合4n+2才能形成稳定的芳香结构。大-电子云分析法包括苯及其衍生物的大-电子云、吡啶的大-电子云和呋喃、噻吩、吡咯的大-电子云三种方式。
苯分子中的碳是sp2杂化,每个碳原子的两个sp2杂化轨道与相邻的两个碳原子形成两根键,同时第三个sp2杂化轨道与氢原子形成一根键,每个碳原子各拿出一个p电子从六元环的侧面交盖,形成一个六中心六电子的6大键,6个电子的离域形
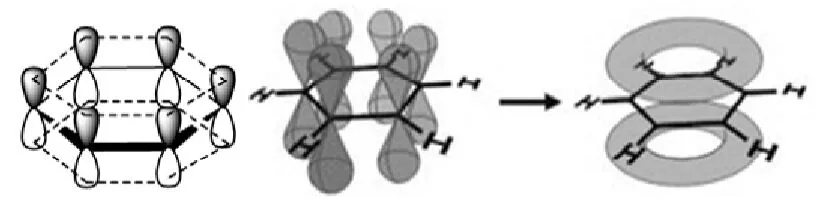
图1 苯分子的大 -电子云示意图
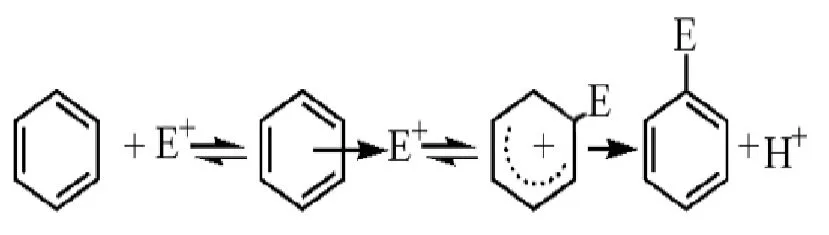
图2 苯环上的亲电取代反应
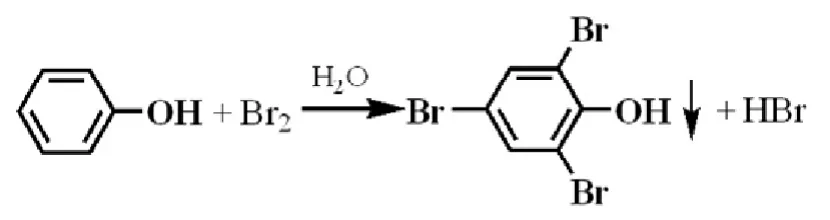
图3 苯酚的溴代反应
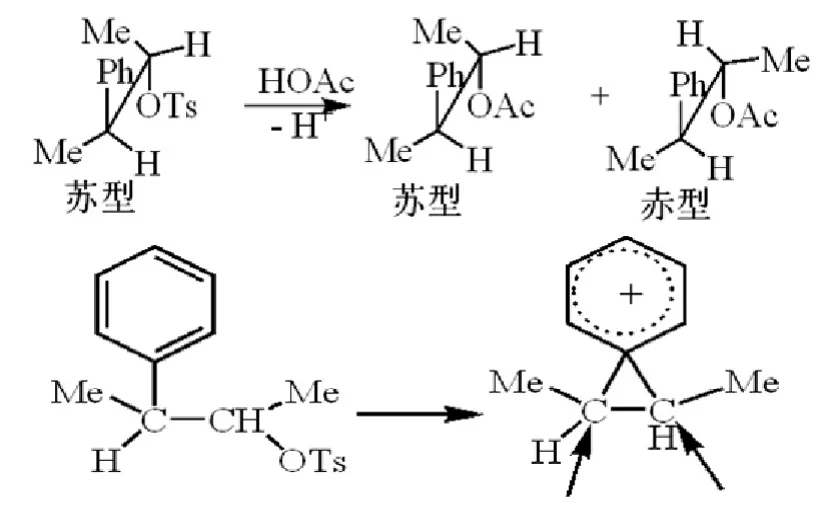
图4 大 -电子云的邻基参与效应
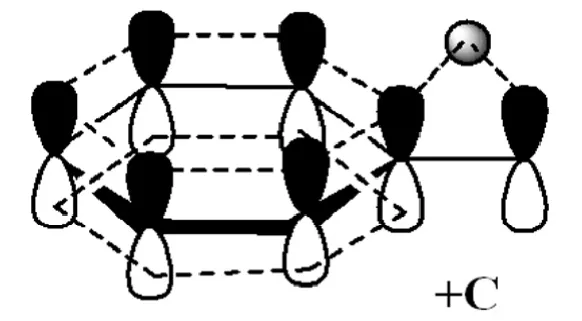
图5 甲基的共轭效应示意图
苄基正离子(C6H5CH2+)中的亚甲基碳原子上的空轨道p与苯环的66-电子云交盖,形成p-66共轭,共轭导致电荷平均化,使碳正离子上的正电荷向苯环转移,降低了亚甲基碳原子上的正电荷密度,能量降低,更稳定(图6)。除了苄基正离子外,还有苄基负离子(C6H5CH2-)和苄基自由基(C6H5CH2·),都由于p-66共轭而增加了其稳定性。
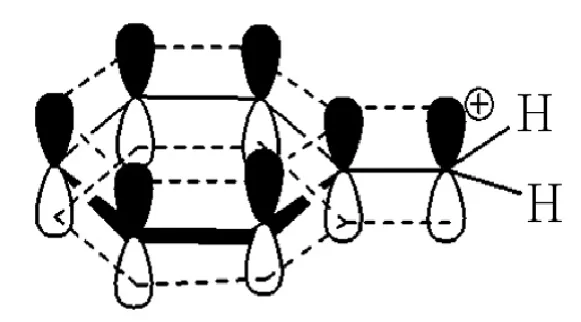
图6 苄基的共轭效应示意图
苯乙烯(C6H5CH═CH2)中乙烯基的-电子云与苯环上的66-电子云交盖,形成-66共轭,此时乙烯基的键受到了削弱,在与苯环碳相连的乙烯基碳和苯环碳之间形成了部分的键,具有双键的部分性质,比如键长缩短,键更牢固,整个体系比较稳定。在这里,由于共轭,苯环上的66-电子云密度略有增大。这是因为共轭体系中的乙烯基-电子云可以微弱地向苯环66-电子云上转移,66体系较体系更能稳定较多的电荷(图7)。这个-66共轭效应可以作为卤代烃消除取向的判据,如3-甲基-1-苯基-2-氯丁烷的消除反应生成3-甲基-1-苯基-1-丁烯,而非生成3-甲基-1-苯基-2-丁烯(图8)。
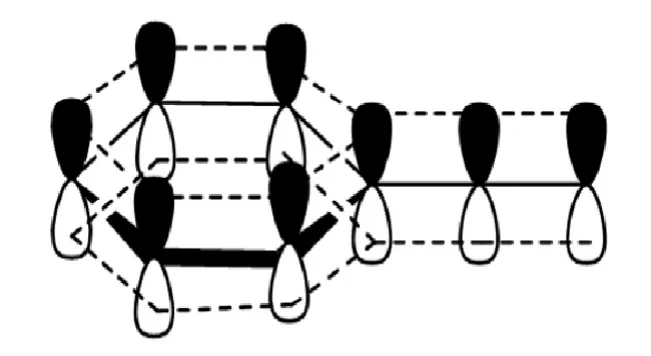
图7 C6H5CH═CH2的共轭效应示意图
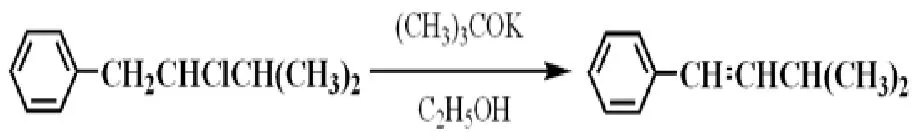
图8 3-甲基-1-苯基-2-氯丁烷的消除反应
攻苯环而生成的负离子中间体所带的负电荷,使负电荷密度降低,能量减低,中间体更稳定,有利于反应的进行,所以带有强吸电子基团的苯环亲核取代反应活性更高。
芳环上的亲核取代反应一般有三种历程:一是加成-消除历程(图9),二是消去-加成历程(图11),三是单分子亲核取代反应SNAr1(图12)[1]。

图9 芳环上的加成-消除历程
如图10所示,1-正丙氧基-2,4-二硝基苯由于两个硝基的强吸电子作用,使苯环上的大-电子云密度显著降低,因而能接受亲核试剂苯胺氮原子的进攻,形成-络合物,环中的5个碳原子共享6个p电子,带一个单位负电荷,然后氨基氮原子上的氢转移至正丙氧基的氧原子上,再脱去一个正丙醇生成目标产物。这是一个典型的加成-消除实例。
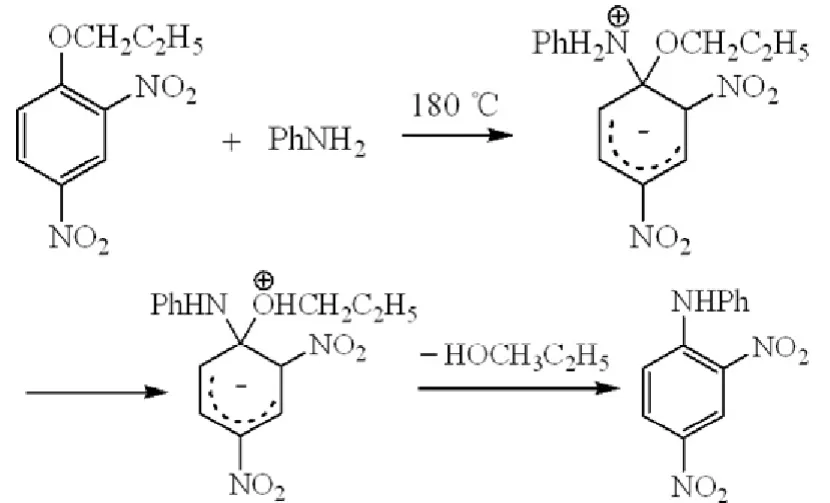
图10 芳环上的加成-消除实例
芳环上的加成-消除历程,形成了负离子活性中间体,强吸电子基团能使中间体的大-电子云密度降低,从而使负离子活性中间体的负电荷密度降低,因而起到稳定中间体的作用,有利于反应的进行(图11)。
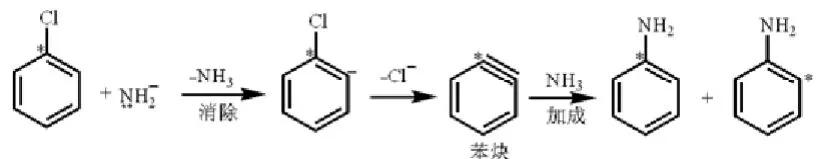
图11 芳环上的消去-加成历程
但在单分子亲核取代反应SNAr1中,生成的是正离子中间体,而非负离子中间体,芳环上供电子基团的存在使大-电子云密度增大,可以部分抵销正电荷的吸电子效应,即使正电荷得到分散,从而显著降低正电荷密度,稳定中间体,促使反应进行。但吸电子基团的存在不利于反应的发生,因为会使正离子中间体的正电荷密度进一步增强(图12)。
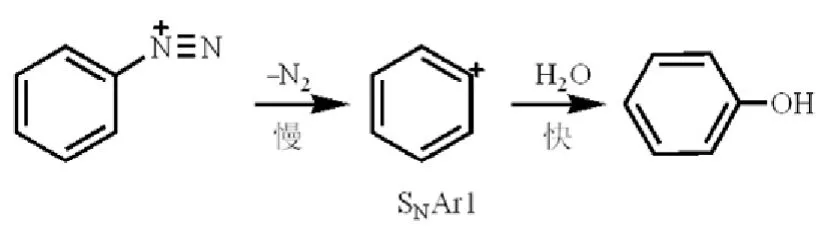
图12 芳环上的单分子亲核取代反应SNAr1
吡啶环上的碳原子和氮原子均以sp2杂化轨道相互重叠形成键,构成一个平面六元环。每个原子上有一个p轨道垂直于环平面,每个p轨道中有一个电子,这些p轨道侧面重叠形成一个封闭的大键,-电子数目为6,符合4n+2规则(图13),与苯环类似。因此,吡啶具有芳香性。氮原子上还有一个sp2杂化轨道没有参与成键,被一对孤对电子所占据,使吡啶具有碱性。吡啶环上的氮原子的电负性较大,对环上电子云密度分布有很大影响,使-电子云向氮原子上偏移,在氮原子周围电子云密度高,而环的其他部分电子云密度降低,尤其是邻、对位上降低显著。所以吡啶的芳香性比苯差[2]。
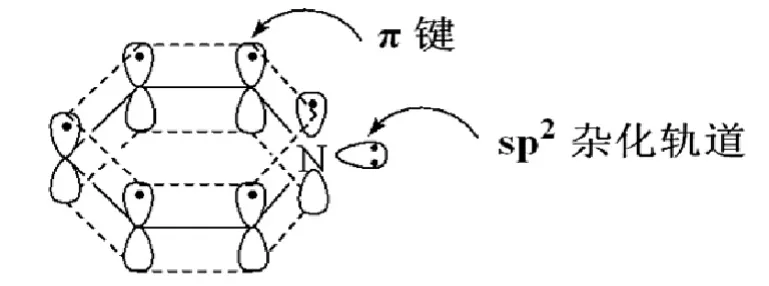
图13 吡啶的大-电子云示意图
由于氮原子的吸电子作用,中间体正离子都不如苯取代的相应中间体稳定,所以,吡啶的亲电取代反应比苯难。比较亲电试剂进攻的位置可以看出,当进攻2()位和4()位时,形成的中间体有一个共振极限式是正电荷在电负性较大的氮原子上,这种极限式极不稳定,而3位取代的中间体没有这个极不稳定的极限式存在,其中间体要比进攻2位和4位的中间体稳定。所以,3位的取代产物容易生成(图14)。
张培林告诉记者,医疗机构成本管理的难点在于技术难度与社会学难点两个方面,技术难度涉及样本量大、统一核算归类、成本分摊、信息化支撑等方面;社会学难点是指医学的伦理学与卫生经济学的相关性,现行体制中由于市场性与公益性的界定不清晰,医院发展难免存在“逐利与医者仁心的人道主义”形成的悖论纠结。
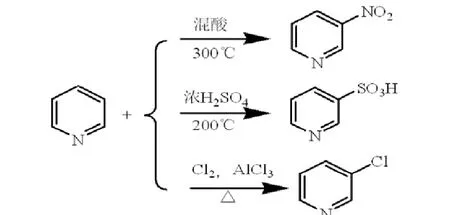
图14 吡啶的亲电取代反应
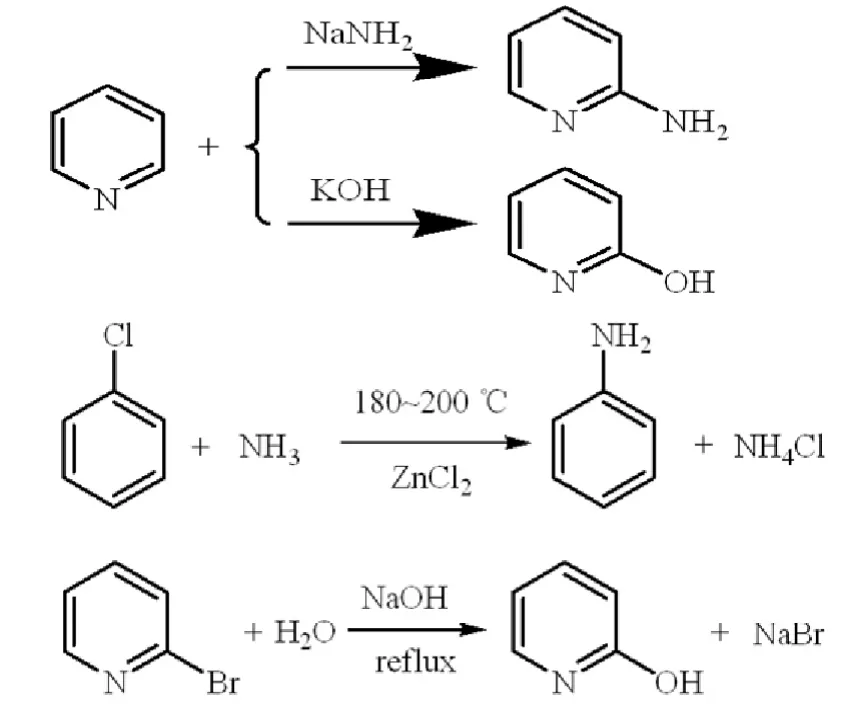
图15 吡啶的亲核取代反应
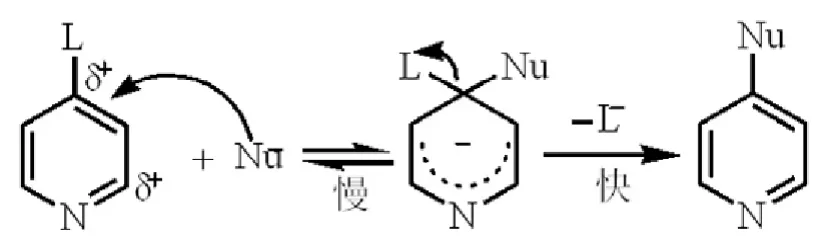
图16 吡啶的亲核取代反应机理
呋喃、噻吩与吡咯结构相似,都是由一个杂原子和四个碳原子结合构成的化合物。从结构上它们可以看作是由O、S、NH分别取代了1,3-环戊二烯(也称为茂)分子中的CH2后得到的化合物。但从化学性质上看,它们与环戊二烯并无多少相似之处,倒是与苯非常类似。例如,呋喃、噻吩、吡咯这三个化合物都非常容易在环上发生亲电取代反应,而不太容易发生加成反应。
按照杂化理论的观点,呋喃、噻吩、吡咯分子中四个碳原子和一个杂原子间都以sp2杂化轨道形成键,并处于同一平面上,每一个原子都剩一个未参与杂化的p轨道(其中碳原子的p轨道上各有一个电子,杂原子的p轨道上有两个电子)。这五个p轨道彼此平行,并相互侧面重叠形成一个五轨道六电子的环状共轭大键,-电子云分布于环平面的上方与下方(图17),其-电子数符合休克尔的4n+2规则。这三个化合物所形成的共轭体系与苯非常相似,所以它们都具有类似的芳香性。但是,这三个化合物所形成的共轭体系与苯并不完全一样,主要表现在以下两处。
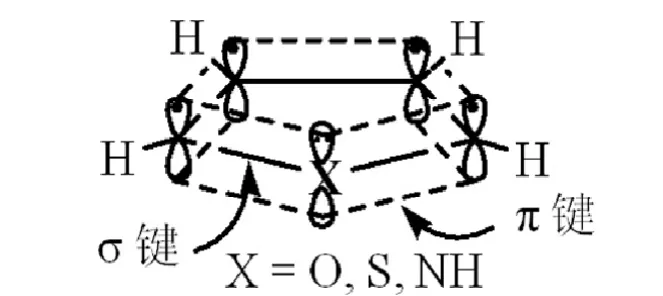
图17 呋喃、噻吩与吡咯的大 -电子云示意图
一是键长平均化程度不一样。苯的成环原子种类相同,电负性一样,键长完全平均化(六个碳碳键的键长均为140 pm),其电子离域程度大,-电子在环上的分布也是完全均匀的。这三个化合物都有杂原子参与成环,由于成环原子电负性的差异,使得它们分子键长平均化的程度不如苯,电子离域的程度也比苯小,-电子在各杂环上的分布也不是很均匀,所以呋喃、噻吩、吡咯的芳香性都比苯弱。三种杂环分子中共价键的长度如图18[3]。
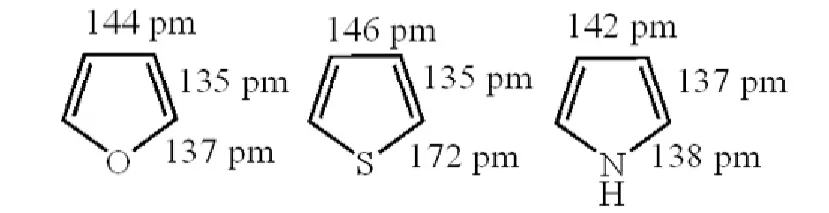
图18 三种杂环分子中共价键的长度
它们的偶极矩相差也很大(图19)。
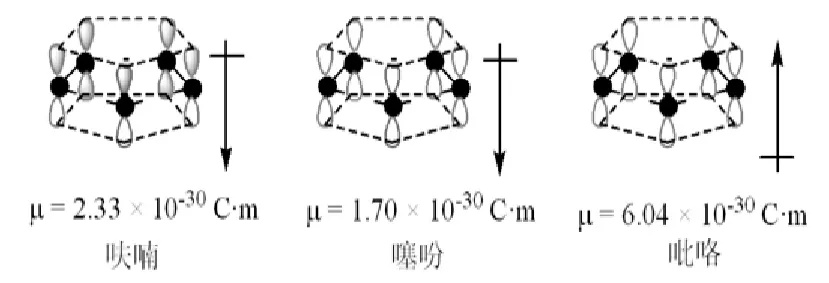
图19 三种杂环分子的偶极矩

图20 三种杂环分子的芳香性顺序
2.3.1 呋喃、噻吩、吡咯的亲电取代反应活性强弱
但是,噻吩中的硫原子与碳原子不属于同周期,p轨道能级相差较大,4个碳原子的4个p轨道与硫原子的1个p轨道由于能阶不一样,肩并肩重叠程度就要大打折扣,所以56共轭效应没有呋喃和吡咯强,对大-电子云的贡献就要小很多,虽然硫原子的-I诱导效应没有呋喃和吡咯强,但这个诱导效应是次要因素,不足以扭转共轭效应弱的颓势,因此,噻吩的亲电取代反应活性比呋喃和吡咯都要小。由此可得总的活性顺序是:吡咯〉呋喃〉噻吩。
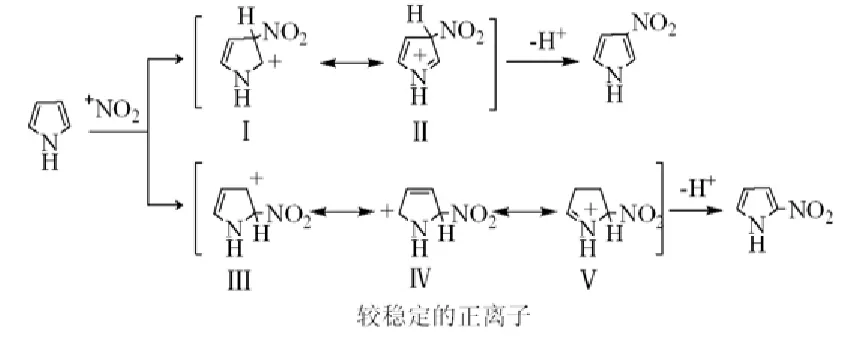
图21 吡咯的亲电取代定位效应机制
呋喃、吡咯还可作为双烯体,与亲双烯体,如丁烯二酸酐,发生Diels-Alder反应,生成相应的产物,噻吩不能发生这一反应,这足以证明噻吩共轭效应弱且大-电子云密度低(图22)。
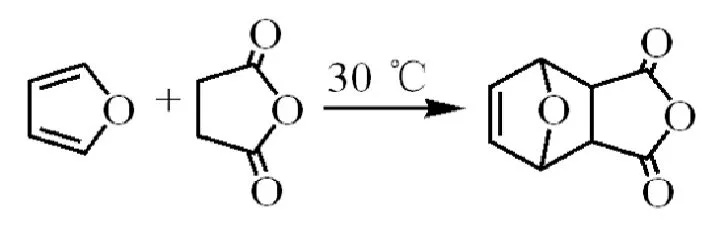
图22 呋喃的Diels-Alder反应
2.3.2 呋喃、噻吩、吡咯的水溶性
呋喃、噻吩、吡咯分子中杂原子的未共用电子对因参与组成环状大-共轭体系56,失去或减弱了与水分子形成氢键的可能性,致使它们都较难溶于水。但吡咯由于氮原子上的一对p电子参与构成大-共轭体系,致使仲氨基电子云密度显著降低,亦即氮原子上的电子云严重偏向大-环,所以其碱性严重减弱,逆转为呈现酸性,可与水形成氢键,故水溶性稍大。三者水溶性顺序为:吡咯(1:17)〉呋喃(1:35)〉噻吩(1:700)。
2.3.3 呋喃、噻吩、吡咯对酸的稳定性
噻吩对酸比较稳定,吡咯与浓酸作用可聚合成树脂状物,呋喃对酸很不稳定,稀酸就可使环破坏,生成不稳定的二醛,并聚合成树脂状物。这是因为杂原子参与环系共轭的电子对能不同程度地与质子结合,从而部分地破坏了环状大键,导致环的稳定性下降。
2.3.4 呋喃、噻吩、吡咯的酸碱性
酸碱性。三个化合物中,噻吩和呋喃既无酸性,也无碱性;吡咯从结构上看是一个仲胺,应具有碱性,但由于氮上的未共用电子对参与构成环状大键,削弱了它与质子的结合能力,因此吡咯的碱性极弱比一般脂肪仲胺(的碱性弱得多,它不能与酸形成稳定的盐,可以认为无碱性。另外由于氮原子上的未共用电子对参与环系的大ffffea共轭,致使其电子云密度相对减小,氮原子上的氢能以质子的形式离解,所以吡咯显弱酸性它可以看成是一种比苯酚酸性更弱的弱酸,能与固体氢氧化钾作用生成盐,即吡咯钾(图23)。
HUANG Chi-bao1,2,HU Ming-hua1,ZENG Qi-hua1,ZENG Bo-ping1
(1.Chemistry and Chemical Engineering College,Zunyi Normal University,Zunyi 563002,China;2.Department of Agricultural Engineering,Yingdong Bioengineering College,Shaoguang University,Shaoguan 512005,China)
The author of this paper systematically expounds the large-electron cloud analysis method including the large-electron cloud of benzene and its derivative,the large-electron cloud of pyridine,and the large-electron cloud of furan,thiophene and pyrrole, revealing that the large -electron cloud analysis is not only the key to the laws of the reactions and transformations of substances,but is one true way to be thoroughly familiar with the theoretical system of organic chemistry as well,pointing out that,by large-electron cloud analysis,to understand and grasp the theoretical system can receive the effect of pouring water off a steep roof and gaining twice the result with half.The large-electron cloud analysis method is an excellent teaching method,worth promoting applications.
large-Electron clouds;organic chemistry;analysis;teaching effect
G642.41
A
1009-3583(2015)-0093-06
2014-11-10
中国博士后科学基金资助项目(20100471224);广东省自然科学基金资助项目(s2011040000536);湖南省科技计划资助项目(2011RS4020);深圳大学省、部重点实验室开放基金资助项目(201202);韶关市科技计划资助项目(2011CX/K19)
黄池宝,男,湖南汨罗人,遵义师范学院化学化工学院教授,博士,博士后,主要从事双光子荧光探针及其显微成像研究。
