多波长HPLC梯度洗脱法同时测定保安万灵丹中升麻素苷、5-O-甲基维斯阿米醇苷、茅术醇、β-桉叶醇和苍术素的含量
2015-02-10杨雪梅班小军杨海红范潇予
杨雪梅,班小军, 杨海红, 范潇予
(1.甘肃省金昌市药品检验检测中心,甘肃 金昌 737100;2.甘肃省张掖市食品药品检验检测中心,甘肃 张掖 734000;3.沈阳药科大学中药学院,辽宁 沈阳 110013)
·药学研究·
PHARMACEUTICAL RESEARCH
多波长HPLC梯度洗脱法同时测定保安万灵丹中升麻素苷、5-O-甲基维斯阿米醇苷、茅术醇、β-桉叶醇和苍术素的含量
杨雪梅1,班小军2*, 杨海红1, 范潇予3
(1.甘肃省金昌市药品检验检测中心,甘肃 金昌 737100;2.甘肃省张掖市食品药品检验检测中心,甘肃 张掖 734000;3.沈阳药科大学中药学院,辽宁 沈阳 110013)

目的:建立同时测定保安万灵丹中升麻素苷、5-O-甲基维斯阿米醇苷、茅术醇、β-桉叶醇和苍术素含量的方法。方法:采用多波长HPLC梯度洗脱法:色谱柱为C18柱(200 mm×4.6 mm,5 µm);流动相A为甲醇-乙腈(2∶ 1),流动相B为0.1%磷酸水溶液,流速为1.0 mL · min-1;进样量为20 μL;检测波长分别为254 nm(用于升麻素苷和5-O-甲基维斯阿米醇苷)、203 nm(用于茅术醇和β-桉叶醇)和340 nm(用于苍术素)。结果:升麻素苷、5-O-甲基维斯阿米醇苷、茅术醇、β-桉叶醇和苍术素的线性范围分别为4.30~86.00 mg · L-1(r=0.999 4)、5.85~117.00 mg · L-1(r=0.999 7)、16.42~328.40 mg · L-1(r=0.999 3)、15.16~303.20 mg · L-1(r=0.999 9)和12.78~255.60 mg · L-1(r=0.999 5);精密度、重复性及稳定性试验中所测各目标组分峰面积的RSD均小于2.0%;升麻素苷、5-O-甲基维斯阿米醇苷、茅术醇、β-桉叶醇和苍术素的平均加样回收率/RSD(n=6)分别为97.49%/1.45%、96.81%/0.94%、98.60%/1.65%、97.96%/1.38%和99.22%/1.24%。结论:本法操作简便、结果准确、重复性好,可用作保安万灵丹的质量控制方法。
保安万灵丹;升麻素苷;5-O-甲基维斯阿米醇苷;茅术醇;β-桉叶醇;苍术素;含量测定
保安万灵丹收载于《国家药品标准中药成方制剂:第7册》中[1],由防风、苍术、荆芥、羌活、麻黄、细辛、川芎、制川乌、制草乌、天麻、当归、甘草、石斛、制何首、全蝎、雄黄、朱砂等17味中药组成,具有解毒消痈、舒筋活血、祛风止痛等作用,临床上用于治疗痈疽发背、深部脓疡、风寒湿痹、肢体瘫痪、偏正头痛、疝坠痛等症状。防风和苍术为方中的主要药物,而升麻素苷和5-O-甲基维斯阿米醇苷为防风的主要成分,茅术醇、β-桉叶醇和苍术素则为苍术的主要成分[2]。保安万灵丹的原部颁标准未要求对方中的任何药物进行定性或定量测定,这样难以保证对产品质量和疗效的有效控制。鉴于此,笔者参考相关文献,采用多波长HPLC梯度洗脱法同时对保安万灵丹中防风所含升麻素苷和5-O-甲基维斯阿米醇苷以及苍术所含茅术醇、β-桉叶醇和苍术素等组分进行含量测定,为该药品的质量控制提供科学依据。
1 仪器与试药
Agilent 1200 型高效液相色谱仪,包括G1311A四元泵、G1330B自动进样器、恒温器、G1322A脱气机、G1315B可变波长检测器以及Chemstation色谱工作站;VS-100UE恒温超声波提取机(无锡沃信仪器有限公司)。
保安万灵丹样品(每丸质量:7.5 g,北京同仁堂股份有限公司同仁堂制药厂,批号:4015311、3015814、3015770)。升麻素苷对照品(纯度:95.0%,批号:111522-201310),5-O-甲基维斯阿米醇苷对照品(纯度:96.4%,批号:111523-201208),苍术素(纯度:99.7 %,批号:111924-201404),均购于中国食品药品检定研究院;茅术醇(纯度:98.0%,批号:23811-08-7),β-桉叶醇(纯度:98.0%,批号:51317-08-9),均购于上海士锋生物科技有限公司。甲醇、乙腈均为色谱纯,磷酸为分析纯,水为超纯水。
2 方法与结果
2.1 色谱条件
色谱柱为依利特C18柱(200 mm×4.6 mm,5 µm);流动相A为甲醇-乙腈(2∶ 1),流动相B为0.1%磷酸水溶液,梯度洗脱(0~10 min,30.0%流动相A;10~20 min,30.0%→38.0%流动相A;20~40 min,38.0% → 60.0% 流 动 相 A;40~ 44 min,60.0%→30.0%流动相A)[3-5],流速为1.0 mL·min-1;进样量为20 µL。依据文献报道和预试验,升麻素苷和5-O-甲基维斯阿米醇苷的保留时间为0~20 min,检测波长为254 nm[6-10];茅术醇和β-桉叶醇的保留时间为20~34 min,检测波长为203 nm[11-12];苍术素的保留时间为34~44 min,检测波长为340 nm[5]。
2.2 溶液制备
2.2.1 混合对照品溶液的制备分别精密称定升麻素苷、5-O-甲基维斯阿米醇苷、茅术醇、β-桉叶醇和苍术素对照品适量,加入甲醇溶解并稀释,依次制成质量浓度为0.430、0.585、1.642、1.516和1.278 g·L-1的对照品储备液;然后,依次量取各对照品储备液1.5、1.0、5.0、7.5和5.0 mL,置50 mL量瓶中,加甲醇稀释至刻度,摇匀,即得混合对照品溶液,其中升麻素苷、5-O-甲基维斯阿米醇苷、茅术醇、β-桉叶醇和苍术素的质量浓度依次为0.0129、0.0117、0.1642、0.2274和0.1278 g·L-1。
2.2.2 供试品溶液的制备取保安万灵丹样品适量,剪碎,取5.0 g,精密称定,置50 mL具塞锥形瓶中,精密加入50 mL甲醇[6,8-9,13],密塞,称定质量,超声处理(200 W,20 kHz)1 h,放冷至室温,再称定质量,用甲醇补足减失的质量,摇匀,滤过,即得供试品溶液。
2.2.3 阴性样品对照溶液的制备按照保安万灵丹处方工艺分别制备不含防风的防风阴性样品和不含苍术的苍术阴性样品,再按“2.2.2”项下方法分别制得防风阴性样品对照溶液和苍术阴性样品对照溶液。
2.3 色谱系统专属性考察
按“2.1”项下色谱条件,将混合对照品溶液、供试品溶液、防风阴性样品对照溶液和苍术阴性样品对照溶液分别进样,记录色谱图。结果显示,升麻素苷、5-O-甲基维斯阿米醇苷、茅术醇、β-桉叶醇和苍术素等各
组分间及与样品中其他成分或杂质间的分离效果良好,即其他成分或杂质对各目标组分的测定无干扰;理论塔板数按5-O-甲基维斯阿米醇苷计算不低于2 500,各组分间分离度均大于1.5(色谱图见图1)。
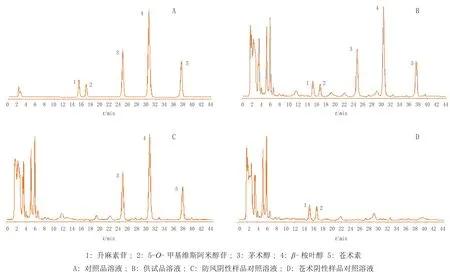
图1 色谱系统专属性实验色谱图Figure 1 Chromatograms from specificity test of the chromatographic system
2.4 线性关系考察
精密量取“2.2.1”项下制备的每个对照品储备液0.1、0.2、0.5、1.0、2.0 mL,分别置于5个10 mL的量瓶中,加甲醇稀释至刻度,摇匀,按“2.1”项下色谱条件,进样,记录色谱图。以峰面积(A)为纵坐标,对照品质量浓度(C)为横坐标,进行线性回归,回归方程和线性范围见表1。
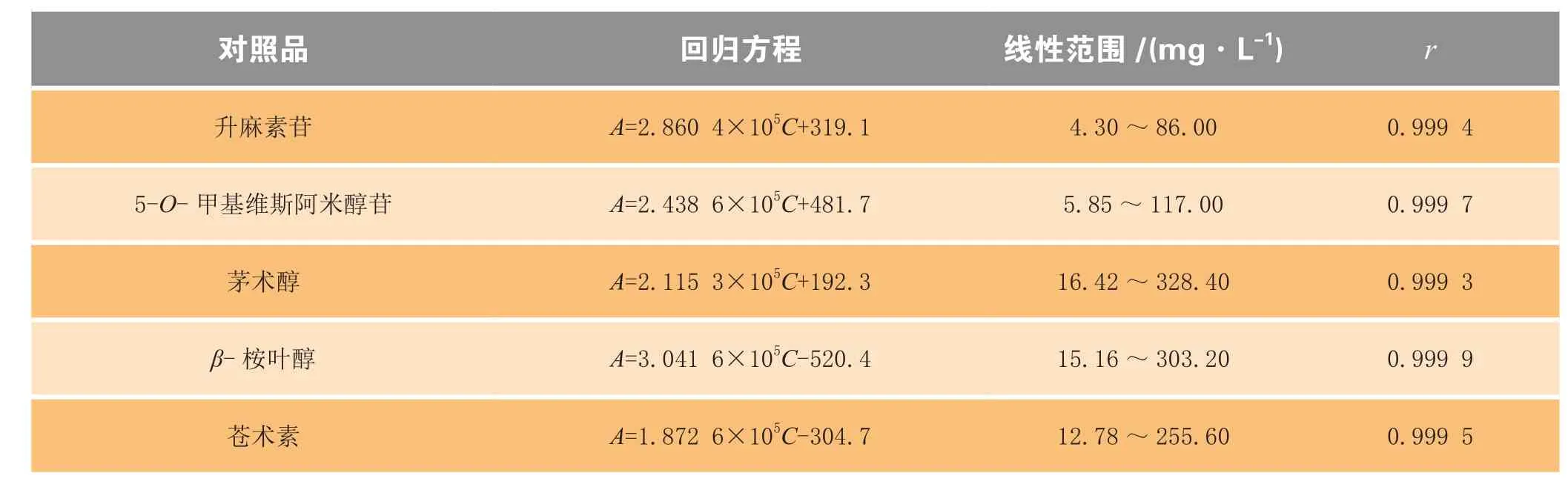
表1 各对照品的回归方程和线性范围Table1 Regression equations and linear ranges of various reference substances
由表1可见,各对照品的质量浓度在线性范围内与峰面积线性关系良好。
2.5 精密度试验
取“2.2.1”项下制备的混合对照品溶液,按“2.1”
项下色谱条件,连续进样6次,记录色谱图。结果测得,升麻素苷、5-O-甲基维斯阿米醇苷、茅术醇、β-桉叶醇和苍术素的峰面积RSD分别为1.39%、1.57%、0.54%、0.44%和0.85%(n=6),表明方法精密度良好。
2.6 重复性试验
称取同一批号样品,按“2.2.2”项下方法制备供试品溶液6份,按“2.1”项下色谱条件,进样,记录色谱图。结果测得,升麻素苷、5-O-甲基维斯阿米醇苷、茅术醇、β-桉叶醇和苍术素的峰面积RSD分别为1.52%、1.32%、0.72%、0.35%和0.59%(n=6),表明方法重复性良好。
2.7 稳定性试验
按“2.2.2”项下方法制备一供试品溶液,分别在室温下放置0、2、4、6、8、12 h后,按“2.1”项下色谱条件,进样,记录色谱图。结果测得,升麻素苷、5-O-甲基维斯阿米醇苷、茅术醇、β-桉叶醇和苍术素的峰面积RSD分别为1.07%、1.26%、0.77%、0.54%和0.89%(n=6),证明供试品溶液在12 h内稳定性良好。
2.8 加样回收试验
称取已知各组分含量的保安万灵丹(升麻素苷、5-O-甲基维斯阿米醇苷、茅术醇、β-桉叶醇和苍术素的含量分别为0.136、0.109、1.653、2.281和1.268 mg·g-1)适量,剪碎,取2.5 g,精密称定,置50 mL具塞锥形瓶中,精密加入混合对照品溶液25 mL,甲醇稀释至刻度,称定质量,超声处理(200 W,20 kHz)1 h,放冷,再称定质量,用甲醇补足减失的质量,摇匀,滤过,作为加样供试品试液,按“2.1”项下色谱条件,进样,记录色谱图。重复以上操作6次。结果测得,升麻素苷、5-O-甲基维斯阿米醇苷、茅术醇、β-桉叶醇和苍术素的平均加样回收率/RSD(n=6)分别为97.49%/1.45%、96.81%/0.94%、98.60%/1.65%、97.96%/1.38%和99.22%/1.24%。
2.9 样品测定
取3个批号的样品各3份,按照“2.2.2”项下方法分别制备供试品溶液,按“2.1”项下色谱条件,进样,记录色谱图。各批号样品的含量测定结果见表2。
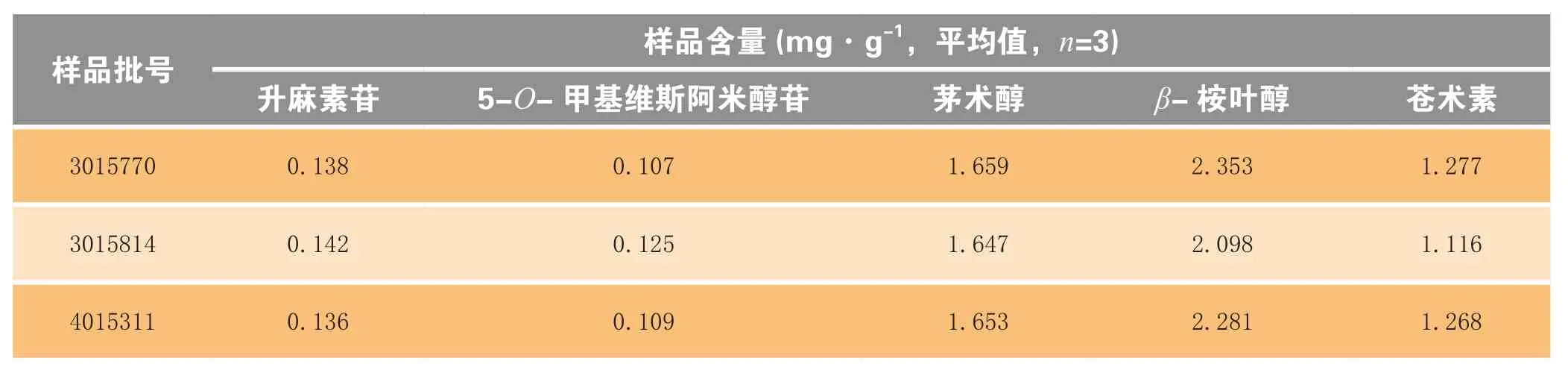
表2 样品含量测定结果Table2 Results of content determination for samples
3 讨论
在预实验中,笔者分别选用50%甲醇、75%甲醇和色谱纯甲醇对样品进行超声(200 W,20 kHz)提取1 h,并对提取效果进行比较,结果显示,色谱纯甲醇超声提取效果最佳,所提取各目标组分的含量均高于50%甲醇和75%甲醇提取组。且分别用色谱纯甲醇对样品进行超声(200 W,20 kHz)提取0.5、1 和1.5 h,以考察超声提取时间对提取效率的影响,结果表明,超声提取1 h的效果与超声提取1.5 h的差异不大,但明显高于超声提取0.5 h。故最终本文选用色谱纯甲醇对样品进行超声(200 W,20 kHz)提取1 h,制备供试品溶液。
本文所建立同时测定保安万灵丹中升麻素苷、5-O-甲基维斯阿米醇苷、茅术醇、β-桉叶醇和苍术素含量的多波长HPLC梯度洗脱法,操作简便,结果准确,重复性好,可用作保安万灵丹的质量控制方法。
[1]国家药典委员会.国家药品标准中药成方制剂: 第7册[M].北京: 人民卫生出版社, 2004: 130.
[2]国家药典委员会.中华人民共和国药典: 一部[M].北京: 中国医药科技出版社, 2010: 140, 150-151, 附录30, 附录36.
[3]牛德斌.HPLC测定防风通圣丸中2个色原酮苷类成分含量[J].中国实验方剂学杂志, 2012, 18(16): 113-115.
[4]张贝贝, 方婧, 许海玉, 等.HPLC测定道地产地和主产地茅苍术中β-桉叶醇及其他成分的含量[J].中国实验方剂学杂志, 2011, 17(8): 116-118.
[5]陈佳, 刘欣, 刘合刚.湖北英山茅苍术药材最佳采收期的研究[J].湖北中医药大学学报, 2012, 14(4): 32-33.
[6]邵留英, 喻志斌, 瞿发林, 等.不同产地防风饮片中有效成分含量比较[J].海峡药学, 2013, 25(2): 52-54.
[7]于春月, 张特立, 白玉华, 等.大庆市不同产地防风中有效成分含量比较[J].中国医药导报, 2011, 8(34): 39-41.
[8]刘婵, 张水寒, 黄惠勇, 等.Box-Behnken设计-效应面法优选防风炮制工艺[J].中国实验方剂学杂志, 2014, 20(5): 18-21.
[9]李悦悦, 王慧, 陈俊, 等.HPLC法测定防风中升麻苷、升麻素、5-O-甲基维斯阿米醇苷和亥茅酚苷的含量[J].药学实践杂志, 2010, 28(6):445-447, 474.
[10]赵博, 杨鑫宝, 杨秀伟, 等.HPLC法同时测定防风中6个主要成分的含量[J].药物分析杂志, 2013, 33(3): 382-387.
[11]谢小霞, 陈佳, 刘合刚.高效液相色谱法测定不同产地茅苍术中β-桉叶醇的含量[J].湖北中医药大学学报, 2014, 16(1): 41-43.
[12]朱爱兰, 潘扬, 张弦.二妙丸、三妙丸、四妙丸中β-桉叶醇和茅术醇的含量测定[J].南京中医药大学学报, 1999, 15(1): 30-32.
[13]姚佳, 刘玉强, 才谦, 等.GC法测定不同来源苍术饮片中茅术醇和β-桉叶醇的含量[J].中国药房, 2014, 25(3): 246-248.
Simultaneous Determination of Prim-O-glucosylcimifugin, 5-O-methylvisammioside, Hinesol,β-eudesmol and Atractylodin in Bao'an Wanling Dan by Multiwavelength HPLC Gradient Elution Method
YANG Xuemei1, BAN Xiaojun2, YANG Haihong1, FAN Xiaoyu3
(1.Gansu Jinchang Drug Inspection Testing Center, Jinchang 737100, China; 2.Gansu Zhangye Food and Drug Inspection Testing Center, Zhangye 734000, China; 3.School of Pharmacy, Shenyang Pharmaceutical University, Shenyang 110013, China)
Objective: To establish a method for simultaneous determination of prim-O-glucosylcimifugin, 5-O-methylvisammioside, hinesol,β-eudesmol and atractylodin in Bao'an Wanling Dan.Methods:A multiwavelength HPLC gradient elution method was adopted with the chromatographic conditions including a C18column(200 mm×4.6 mm, 5 µm), methanol-acetonitrile(2:1) as mobile phase A, 0.1% phosphoric acid solution as mobile phase B, a fow rate of 1.0 mL · min-1, an injection volume of 20 μL and the detection wavelengths of 254 nm(for prim-O-glucosylcimifugin and 5-O-methylvisammioside), 203 nm(for hinesol andβ-eudesmol) and 340 nm(for atractylodin).Results: The linear ranges of prim-O-glucosylcimifugin, 5-O-methylvisammioside, hinesol,β-eudesmol and atractylodin were 4.30-86.00 mg · L-1(r=0.999 4), 5.85-117.00 mg · L-1(r=0.999 7), 16.42-328.40 mg · L-1(r=0.999 3), 15.16-303.20 mg · L-1(r=0.999 9) and 12.78-255.60 mg · L-1(r=0.999 5) respectively.The RSDs of the peak areas of each target component detected in precision, reproducibility and stability tests were less than 2.0%.The average recoveries/ RSDs(n=6) of prim-O-glucosylcimifugin, 5-O-methylvisammioside, hinesol,β-eudesmol and atractylodin were 97.49%/1.45%, 96.81%/0.94%,
Bao'an Wanling Dan; prim-O-glucosylcimifugin; 5-O-methylvisammioside; hinesol;β-eudesmol; atractylodin; content determination
R286.0
A
1001-5094(2015)05-0384-05
接受日期:2015-04-03
*通讯作者:班小军,主管药师;研究方向:药品检验及天然药物有效成分研究;Tel:0936-8312120; E-mail:496108658@qq.com
98.60%/1.65%, 97.96%/1.38% and 99.22%/1.24% respectively.Conclusion:The method is simple, accurate and reproducible, thus it could be used as the approach for the quality control of Bao'an Wanling Dan.
