内分泌相关高钙血症的临床对策
2014-11-26解放军总医院内分泌科谷伟军
解放军总医院内分泌科 谷伟军
高钙血症是临床常见的内分泌代谢紊乱之一,临床表现差异很大,轻者可以无症状,仅常规筛查中发现血钙水平升高,重者可导致昏迷、甚至危及生命。成人血清钙正常值2.25~2.75mmo1/L,高于2.75mmol/L即为高钙血症(hypercalcemia)。按血钙升高水平可将高钙血症分为轻、中和重度,轻度高血钙为血总钙值2.75~3mmol/L;中度为3~3.5mmol/L;重度时>3.5mmol/L,同时可导致一系列严重的临床征象,即称高钙危象,可危及生命,是内科急症之一[1]。
高钙血症的病因及发病机制
生理情况下,体内钙稳态主要由甲状旁腺激素(PTH)、降钙素、1,25(OH)2-D这三种激素共同调节,参与调节的器官包括骨骼、肠道和肾脏,期间任何一个环节发生异常均可导致高钙血症[2]。病因不同,其发病机制亦不相同,归结起来,主要有骨质再吸收增加;肠钙吸收增加;尿钙重吸收增加;血液浓缩等四个方面。其中,骨质再吸收增加是其主要发病机制。在诸多病因中,最常见的是原发性甲状旁腺功能亢进症(PHPT)和恶性肿瘤,占总致病因素的90%以上。筛查出的无症状患者高血钙原因多为甲旁亢,而住院患者的高血钙往往由肿瘤所致。恶性肿瘤引起高钙血症的主要途径有:①乳腺癌等恶性肿瘤骨转移所致的局限性溶骨性骨破坏;②多发性骨髓瘤和其他累及骨髓的血液系统恶性肿瘤,以及发生于肺、肾、泌尿生殖系的恶性肿瘤合成、分泌一些细胞因子和肿瘤相关激素,如IL-1、IL-6、TNFα、甲状旁腺激素相关蛋白(PTHrP)等导致体液性高钙血症;③肉芽肿性疾病:包括结节病、结核、麻风病、球孢子菌病、组织胞浆菌病等,由于产生过多的活性维生素D,使得肠道及肾脏对钙的回吸收过多而升高血钙水平。根据甲状旁腺细胞功能是否紊乱分为两大类,即甲状旁腺激素依赖性高钙血症和非甲状旁腺激素依赖性高钙血症(见表1)。

表1 高钙血症的病因分类[1,3,4]
高血钙的临床表现
一般而言,当患者血清钙超过3.0mmol/L便会有明显的多系统症状。
1. 胃肠道
高血钙可引起厌食、胃肠道蠕动减弱、恶心、呕吐、腹胀、便秘、吞咽困难等。
2. 泌尿系统
口干、多饮、多尿、夜尿增多。高水平的尿钙、磷易形成尿路结石或肾实质钙盐沉着。本病所致尿路结石的特点是双侧性和多发性,表现为肾绞痛、血尿或继发尿路感染,反复发作可引起肾功能损害,导致肾功能衰竭。
3. 骨骼系统
早期仅有疼痛,局部压痛,长期患病可出现椎体压缩、骨骼畸形,易发生病理性骨折。
4. 神经肌肉系统
高血钙可引起乏力、倦怠、健忘、注意力不集中、忧郁和精神疾病等症状。
5. 心血管系统
可发生高血压和各种心律失常心电图表现有Q-T问期缩短,ST-T段改变,若未及时治疗,可发生致命性心律失常。
6. 肿瘤相关性高钙血症
许多症状缺乏特异性,因此常被误认为原发疾病进展所致或与肿瘤治疗有关。
高钙血症的诊断及鉴别诊断流程
临床上,一般将高钙血症的诊断分为两步,首先明确有无血钙升高,然后明确高血钙的病因。需要多次重复测定血钙以除外实验室误差及止血带绑扎时间过长等人为因素造成的高血钙,还需注意患者有无脱水及血浆蛋白浓度升高等。粗略估计血清蛋白每增加约10g/L,血清钙约增加0.2mmol/L。另外,有报道在原发性血小板增多症时,大量异常活化的血小板在体外释放钙,可引起假性高钙血症。临床上,通常计算校正钙,计算公式为:校正钙=实测钙+(40-实测白蛋白)×0.02,钙浓度单位用mmol/L,白蛋白单位用g/L,此公式有助于排除假性高钙血症[5]。此外,离子钙的测定也有助于假性高钙血症的鉴别。
高钙血症诊断一经确立,即应从病因角度进行鉴别诊断。需要综合分析患者的病史,包括症状、体征、实验室的相关检查、影像学等特殊检查结果。家族史、用药史亦是诊断中不可缺少的资料。由于90%以上都是PHPT和恶性肿瘤,因此二者鉴别非常重要。一般恶性肿瘤并发高钙血症时病情已相当严重,原发病灶通常易于发现或可见转移病灶,原发性甲旁亢病情通常较轻,病程较长。因此临床表现为无症状或慢性过程者很可能为甲旁亢;而高血钙通常是恶性疾病病情恶化的表现,如果临床表现为重症、急性者,很可能是恶性肿瘤。之后再结合血PTH测定结果来考虑:①若PTH测定值高,则诊断为原发性甲旁亢,尽管非常罕见,仍需注意除外恶性肿瘤异位分泌PTH;②若PTH测定值正常,还要警惕家族性低尿钙高血钙综合征(FHH),该病的尿钙与肌酐清除率之比<0.01;③若PTH测定值低,则需根据病史、体征、各种实验室检查以及影像学检查仔细筛查恶性肿瘤,确定是否为结节病或维生素D中毒等其他少见原因导致的高钙血症,若均为阴性结果,则筛查可引起高钙血症的其他内分泌疾病[6],例如甲状腺功能亢进、嗜铬细胞瘤、肾上腺皮质功能减退、血管活性肠肽分泌瘤(VIP瘤)以及肢端肥大症等。鉴别诊断流程见图1。

图1 高钙血症鉴别诊断流程[7]
高钙血症的治疗
治疗高钙血症最根本有效的办法是查明病因和去除病因,如手术、化疗、放疗等,控制原发病、立即停止使用导致高血钙的药物、制动患者尽可能增加负重锻炼等。由于高钙血症造成的各系统功能紊乱会影响病因治疗,严重时高钙危象可危及生命,因此,降低血钙缓解急性症状、延长生命往往成为当务之急。短期治疗通常能有效缓解急性症状、避免高钙危象造成的死亡,争取时间确定和去除病因。对高钙血症的治疗取决于血钙水平和临床症状。通常对轻度高血钙,无临床症状的患者,一般不积极采取控制血钙的措施;对有症状、体征的中度高血钙患者,需立即进行治疗。然而,对于无症状的中度高血钙,需要根据病因决定是否治疗和采取何种治疗。
在高钙血症的病因分类中,原发性甲旁亢占据很大比重。在某些人群,其患病率达到5%,而且近年来随着自动生化分析仪的使用,检出率也有很大幅度升高[8,9]。很多无症状患者被检出。通常有症状患者采取手术治疗,无症状患者手术治疗指征如表2、表3,对于不愿意采取手术治疗或是不能手术治疗的患者,可以选择药物治疗。

表2 无症状性PHPT患者的手术治疗指征[10]
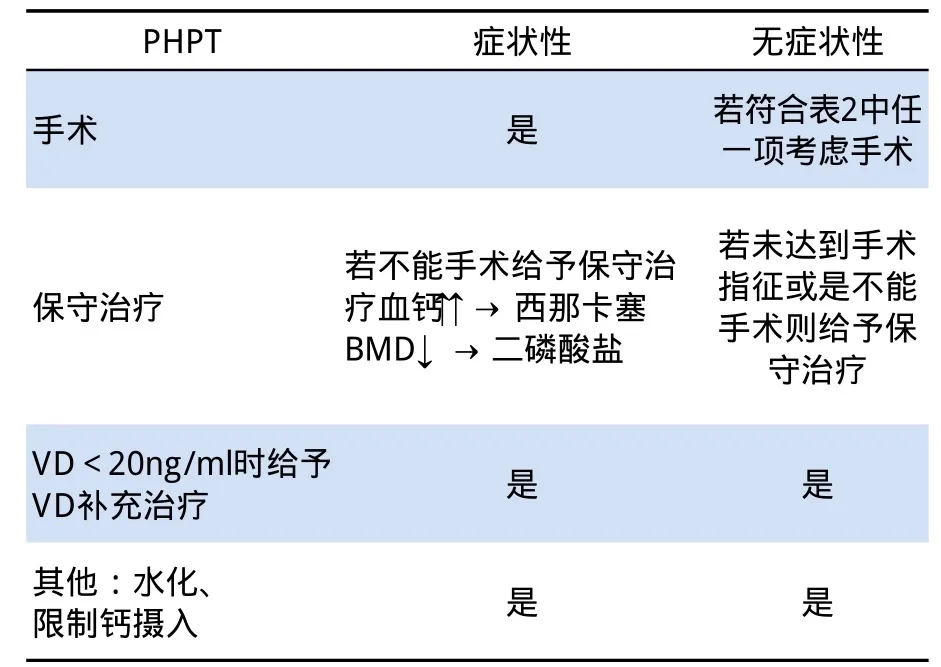
表3 PHPT患者的管理[11]
1. 扩容、促进尿钙排泄
1.1 生理盐水 高钙血症时由于恶心、呕吐、多尿往往导致机体脱水,因此均需首先使用生理盐水补充细胞外液容量。开始24~48h每日持续静脉滴注3000~4000ml,可使血钙降低10~30mg/L。生理盐水补充一是纠正脱水,而是通过增加肾小球钙的滤过率以及降低肾脏近、远曲小管对钠和钙的重吸收,使尿钙排泄增多。但老年患者及心肾功能不全的患者应慎重。心功能不全的患者可同时从胃肠道补充盐水。不过,单纯使用盐水往往不能使血钙降至正常,还必须采取其他治疗措施。
1.2 利尿 细胞外液容量补足后可使用呋塞米(速尿)。呋塞米和依他尼酸可作用于肾小管髓袢升支粗段,抑制钠和钙的重吸收,促进尿钙排泄,同时防止细胞外液容量补充过多。速尿应用剂量为20~40mg静脉注射;当给予大剂量速尿加强治疗(每2~3h 80~120mg)时,需注意补充水和电解质,尽可能监测中心静脉压、血及尿电解质以防止发生水、电解质紊乱。目前,利尿剂常与抗骨吸收药物一同使用,一般仅用1~3d,在抗骨吸收药物起效后即可停用。由于噻嗪类利尿剂可减少肾脏钙的排泄进而加重高血钙,因此绝对禁忌。
2. 应用抑制骨吸收药物
由于破骨细胞骨吸收的增加是绝大多数高钙血症患者最常见和重要的发病机制,因此,目前经常使用阻断破骨细胞骨吸收的药物来降低血钙。此类药物的早期使用还可以避免长期大量使用生理盐水和利尿剂造成的水及电解质代谢紊乱。主要有以下药物:
2.1 二磷酸盐 静脉使用二磷酸盐是迄今为止最有效的治疗方法。高钙血症已经诊断明确,必须尽早开始使用,因为二磷酸盐起效需2~4d,达到最大效果需4~7d,60%~70%患者血钙能降至正常水平,效果可持续1~3周。二磷酸盐胃肠道吸收率很低,因此治疗高钙血症时常采用静脉滴注给药。将一定剂量的二磷酸盐溶解于500ml以上溶液中静点,维持4h以上,以防二磷酸盐和钙的复合物沉积造成肾损害。其不良反应主要为肾脏损害及抑制矿化,少数可引起下颌骨坏死[12],其他极少见的不良事件包括结膜炎、葡萄膜炎、巩膜炎、眼睑浮肿、眼眶感染和颅神经麻痹等,发生率低于0.05%。常用药物及用药方法见表4。
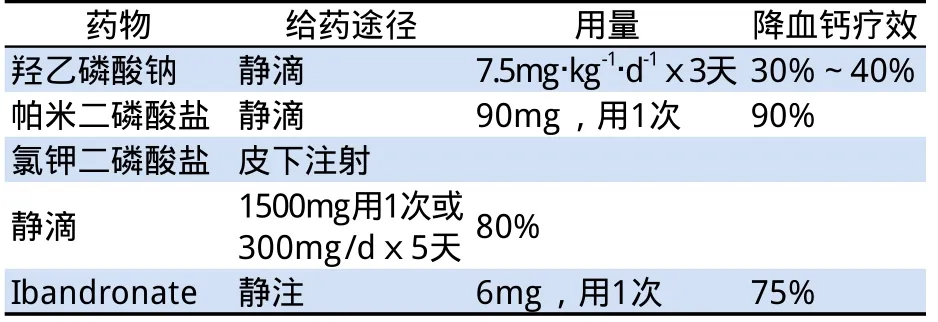
表4 常用二磷酸盐制剂用法及疗效
帕米磷酸钠是临床上广泛应用的二磷酸盐类药物。它可以抑制破骨细胞活性,抑制骨钙动员,多数患者于用药后3~7d血钙可降至正常,作用持续数周,目前应用二磷酸盐后,临床上已不再使用光辉霉素[13]。解放军总医院巴建明等[14]研究评价了8例PHPT患者使用帕米磷酸钠治疗高钙血症的疗效及安全性,结果显示:用药后第1天内即起效,降低血钙最佳最用时间为5~7d,血钙最大降幅为40%。在临床研究中,大约有10%的患者在帕米磷酸钠治疗过程中出现肾功能损伤。多数血清肌酐的升高是轻中度和短暂的,停药后可恢复至正常。但少数患者可发展为急性或慢性肾功能衰竭,且肾损害的发生与药物呈剂量依赖性[15]。综合看来,帕米磷酸钠治疗高钙血症起效快,持续时间长、不良反应轻微。
2.2 降钙素 其作用为直接抑制破骨细胞骨吸收,同时能减少肾小管钙的重吸收,增加尿钙排泄。起效快,但效果不及二磷酸盐显著。使用降钙素2~6h内血钙可平均下降0.5mmol/L,但不能使大多数患者的血钙水平降至正常。治疗剂量:鲑鱼降钙素2~8IU/kg,鳗鱼降钙素0.4~1.6IU/kg,每6小时1次,肌肉或皮下注射,每6~12小时重复注射,停药后24h内血钙回升。重复注射同一剂量的降钙素不能达到首次注射的降血钙效果,即多次注射,作用减弱,不适于长期用药。这种降钙素“脱逸”现象可能与破骨细胞上降钙素受体的快速降调节有关,据报道可被同时使用糖皮质激素减弱。与糖皮质激素或普卡霉素合用可产生协同作用,与二磷酸盐联合使用能够更迅速和大幅度地降低血钙水平。不良反应主要为恶心、呕吐、腹痛、面色潮红、皮疹等,一般均可耐受。
2.3 光辉霉素(普卡霉素)和硝酸镓 二者均为治疗肿瘤的药物,可以抑制骨吸收而具有降低血钙的作用,但是由于其严重的不良反应(肾脏毒性、骨髓抑制),不适合用于慢性高钙血症的长期治疗,目前临床上已很少应用此类药物。
狄诺塞麦与西那卡塞:很多HMM患者用二磷酸盐治疗效果不佳,因为二磷酸盐并不能阻断所有PTHrP的作用,并且降钙时间较短暂,而PTHrP的水平并没有被降低,还能够继续发挥破骨作用[16]。骨转移时,肿瘤细胞可以分泌细胞因子以及生长因子促进细胞核因子κB受体活化因子配基(RANK-RANKL)通路活化,该通路是破骨细胞分化及激活的中心环节,狄诺塞麦是RANKL配体的单克隆抗体,可以干扰RANK-RANKL通路活化,目前国外已批准治疗骨质疏松以及骨转移[17]。而它对恶性肿瘤相关的高钙血症的作用也处于临床研究阶段[18]。钙敏感受体(CaSR)在生理状态以及肿瘤细胞中对于调节PTHrP分泌过程均起着重要作用,具体的机制尚不明确。西那卡塞是一种拟钙剂,作用于CaSR。Bech等[16]在1例对二磷酸盐抵抗的HMM患者中应用西那卡塞,发现其可以快速降低PTHrP和血钙水平。
3. 糖皮质激素
糖皮质激素通过多种途径降低血钙,如抑制肠道吸收、增加尿钙排泄等;有研究报道糖皮质激素还能使产生1,25-(OH)2-D3的肉芽肿病患者血中的1,25-(OH)2-D3水平降至正常。可用于治疗由于血液系统恶性肿瘤如淋巴瘤和多发性骨髓瘤导致的高钙血症,也可用于治疗维生素D和维生素A中毒或肉芽肿病导致的血钙升高。对于实性肿瘤或原发性甲旁亢所致的高钙血症无效。常用剂量为氢化可的松200~300mg每日静脉滴注,共用3~5d。
4. 其他
4.1 透析 使用低钙或无钙透析液进行腹透或血透,治疗顽固性或肾功能不全的高钙危象,可以达到迅速降低血钙的目的。
4.2 活动 卧床的患者应尽早活动,以避免和缓解长期卧床造成的高钙血症。
综上,对于高钙血症患者,应尽可能明确其病因,根据病因给予恰当治疗。在高钙危象阶段,首先必须用生理盐水扩容,在补足血容量的基础上使用速尿,在此阶段需密切监测水、电解质水平;同时可联合使用二磷酸盐和降钙素,降钙素起效迅速,但由于作用时间缓和以及脱逸现象,降钙效果和持续时间有限;二磷酸盐虽然起效缓慢,但降钙作用显著且持续时间长久;狄诺塞麦和西那卡塞对高钙血症的治疗仍处于探索阶段。
[1] 邢小平.高钙血症//陈家伦.临床内分泌学[M].上海:上海科学技术出版社, 2011: 1385-1392.
[2] 邢小平,孔晶,王鸥.高钙危象的诊治[J].临床内科杂志, 2012, 29: 590-592.
[3] Endres DB. Investigation of hypercalcemia[J]. Clinical Biochenistry,2012, 45: 954-963.
[4] 颜湘.钙磷代谢失常综合征//廖二元.内分泌代谢病学[M].北京:人民卫生出版社, 2012: 1854-1862.
[5] Al-Azem H, Khan A. Primary hyperparathyroidism[J].CMAJ, 2011,183: E685-E689.
[6] Carroll MF, Schade DS. A practical approach to hypercalcemia.Am Fam Physician[J]. 2003, 67: 1959-1966.
[7] Patrick R, Antonello P, Mitchell H, et al. Approach to Diagnosis and Treatment of Hypercalcemia in a Patient With Malignancy[J]. Am J Kidney Dis, 2013.
[8] Marcocci C, Cetain F. Clinical practice Primary hyperparathyroidism[J].NEJM, 2011, 365: 2389-2397.
[9] Bollerslev J, Marcocci C, Sosa M, et al. Current evidence for recommendation of surgery, medical treatment and vitamin D repletion in mild primary hyperparathyroidism[J]. European Journal Endocrinology, 2011, 165: 851-864.
[10] Udelsman R, Pasieka JL, Sturgeon C, et al. Surgery for asymptomatic primary hyperparathyroidism: proceedings of the third international workshop[J]. Journal of Clinical Endocrinology and Metabolism, 2009, 94: 366-372.
[11] Rachel K, Crowley, Neil J. et al. When would I use medical therapies for the treatment of primary hyperparathyroidism?[J]. Clinical Endocrinology, 2013, 79: 770-773.
[12] Migliorati CA, Siegel MA, Elting LS. Bisphosphonate-associated osteonecrosis: a long-term complication of bisphosphonate treatment[J].Lancet Oncol, 2006, 7: 508-514.
[13] Kearney T, Dang C. Diabetic and endocrine emergencies[J]. Postgrad Med J, 2007, 83: 79-86.
[14] 苏俊平,巴建明,谷伟军,等.帕米磷酸钠治疗甲状旁腺机能亢进高钙血症的疗效及安全性(附8例报告)[J].军医进修学院学报, 2011, 32: 1096-1098.
[15] Nagahama M, Sica DA. Pamidronate-induced kidney injury in a patient with metastatic breast cancer[J]. Am J Med Sci, 2009, 338: 225-228.
[16] Bech A, Smolders K, Telting D, et al. Cinacalect for hypercalcemia caused by pulmonary squamous cell carcinoma producing parathyroid hormone-related Peptide[J]. Case Rep Oncol, 2012, 5: 1-8.
[17] Stopeck AT, Lipton A, Body JJ, et al. Denosumab compared with zoledronic acid for the treatment of bone metastases in patients with advanced breast cancer: a randomized, double-blind study[J]. J Clin Oncol, 2010, 28: 5132-5139.
[18] Clines GA. Mechanisms and treatment of hypercalcemia of malignancy[J]. Curr Opin Endocrinol Diabetes Obes, 2011, 18: 339-346.
