NH4 Cl薄层液膜下X70钢腐蚀的电化学研究
2014-11-09邓祖宇
邓祖宇
(四川幼儿师范高等专科学校学前教育二系,四川江油621709)
大气腐蚀其实质为金属处于薄层电解质液膜下的一种电化学过程,因此,电化学原理,测量技术和数据处理方法原则上都可以应用,但它又与完全浸在电解液中的腐蚀过程有所区别.20世纪50年代后期,Tomashow和Sereda等人提出了基于电偶腐蚀原理的大气腐蚀电化学研究方法(EACM);1976年 Mansfeld等人[1]提出采用大气腐蚀监测仪(ACM)进行薄层液膜下的腐蚀电化学测试;近年来前(后)置微距参比电极技术的应用[2-3],都为研究金属的大气腐蚀提供了比较多的方法,但由于要设计出能很好模拟实际情况并且重现性较好的电化学腐蚀电池有一定的难度,使得金属在薄层液膜下的研究远远落后于金属在全浸状态下的研究.X70是一种管线钢,主要用于石油、天然气的长距离输送,如国家的西气东输项目.关于X70钢土壤、溶液中的腐蚀行为已被广泛研究[4-7],而对于它在薄层液膜下的研究报道不多[8-9].本文采用电化学阻抗法和阴极极化曲线法研究了液膜厚度和NH4Cl浓度对X70钢在薄层液膜下电化学行为的影响.
1 实验方法
1.1 仪器及药品
CHI618B电化学分析仪(上海辰华仪器公司).所用药品NH4Cl(AR级).
1.2 电极制备
基材为 X70钢,其化学组成(质量分数):0.100%C,0.220%Si,1.450%Mn,0.024%P,0.015%Nb,0.015%V,余量 Fe.将 X70 钢基材用环氧树脂涂封制成工作电极,工作面积为0.422 cm2,经280#~1 600#金相砂纸逐级打磨,Al2O3抛光,再分别用丙酮、二次蒸馏水冲洗干净,冷风吹干,放入干燥器中备用.
1.3 三电极电化学电解池的设计
三电极电化学电解池见文献[9-10],如图1所示.饱和甘汞电极为参比电极,Pt电极为辅助电极,X70钢电极工作面向上,固定在三电极电解池中,用石蜡密封.将电池置于可调节水平性的水平台上,当水平台调节至水平后,工作电极上的液膜厚度将保持均匀.
1.4 实验溶液的制备
实验溶液为NH4Cl溶液,用二次蒸馏水将不同质量的NH4Cl固体定容于2 000 mL的容量瓶中,即可以得到不同浓度的NH4Cl溶液.
1.5 薄层液膜厚度的测量
测量装置,见图1.该测量装置,可精确测量液膜厚度到10μm.
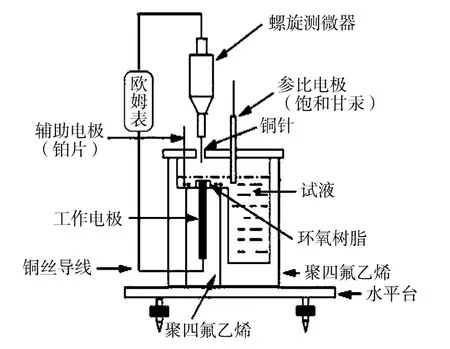
图1 测量金属在薄层液膜下腐蚀的三电极电化学电解电池
1.6 电化学行为测定
分别测试X70钢在不同液膜厚度,含不同浓度NH4Cl的薄层液膜下的阴极极化曲线和电化学阻抗谱.测试在三电极体系中进行.电化学阻抗频率范围为100 kHz~10 mHz,电化学阻抗激励信号幅值为5 mV;阴极极化曲线扫描速度为1 mV·s-1,动电位扫描区间为 -1.0 ~0.0 V(相对于Ecorr),实验温度为20±2℃.
2 结果与讨论
2.1 薄层液膜厚度对X70钢阴极极化曲线的影响
图2 为X70 钢在0.1 mol·L-1NH4Cl不同液膜厚度下浸泡30 min后的阴极极化曲线.
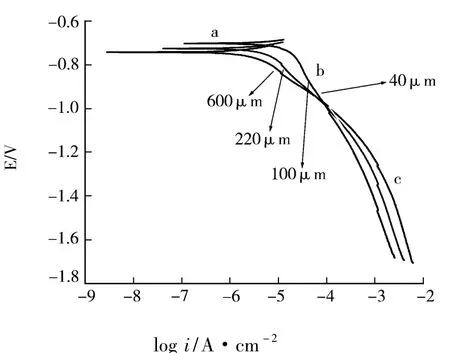
图2 X70钢在不同液膜厚度下的阴极极化曲线
当液膜厚度大于1 000μm时,金属的腐蚀与其在溶液中相似,因此,在本研究中,液膜厚度变化的范围为1 000~20μm.从图2可知,在不同液膜厚度下,阴极极化曲线均分为3个区域:(a)自腐蚀电位附近,电流密度较低,发生吸氧腐蚀,O2+2H2O+4e-4OH-,为弱极化区;(b)氧气从空气中进入溶液并迁移到阴极表面发生还原反应的阴极扩散区;(c)强极化区,该区域发生析氢反应,2H2O+2e→—-H2↑+2OH-,电流密度迅速升高.
图3为阴极极限扩散电流(电势为-0.90 V(SCE)的电流)与液膜厚度d关系.
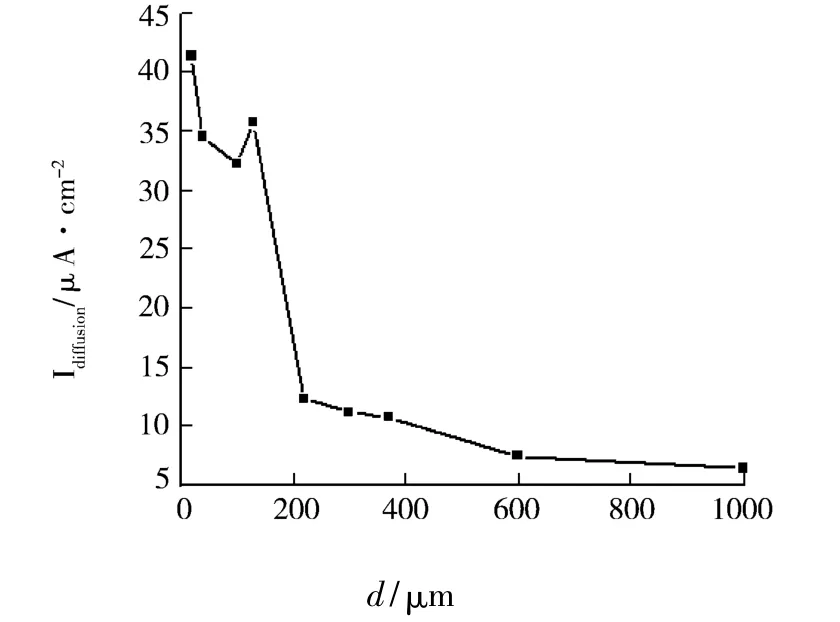
图3 阴极极限扩散电流(电势为-0.90 V(SCE))与液膜厚度d的关系
从图3可知,液膜厚度的变化对阴极极限扩散电流的影响很大.液膜厚度减薄,阴极极限扩散电流增大.液膜厚度约为130μm时,阴极极限扩散电流出现峰值.液膜厚度在130~100μm之间时,阴极极限扩散电流反而减小;厚度进一步减薄,阴极极限扩散电流又增加.根据能斯特-菲克扩散定律:
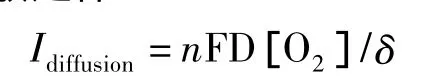
式中Idiffusion为扩散电流密度,D和[O2]分别为液膜中溶解氧的扩散系数和浓度,δ为扩散层厚度,n为反应电子转移数,F为法拉第常数.溶液中,溶液层分为对流层和扩散层.液膜比较厚时,液膜厚度的变化主要影响对流层的传质流量,此时idiff变化不大.液膜厚度减薄,由于δ的降低,O2更容易扩散到电极表面,idiff迅速增大,在130μm时阴极极限扩散电流达到峰值.液膜厚度进一步减小,腐蚀产物沉积于电极表面上,将影响O2的扩散与传输,从而使得O2在电极表面上的浓度减小,因此当液膜厚度在130~100μm之间时,极限扩散电流反而减小;另外,虽然腐蚀产物在电极表面富集会降低阴极极限扩散电流,但当液膜厚度减小的一定值后,氧的扩散与对流变得更加的容易,氧易从与电极表面垂直的方向穿过水膜,极化过程中消耗的氧气容易得到及时的补给,这使得电化学过程中的氧去极化过程容易进行,所以液膜厚度小于100μm时阴极极限扩散电流又升高,加快X70钢的腐蚀.
C区为强极化区,该区域发生析氢反应,2H2O+2e→—-H2↑+2OH-,随着阴极极化电势增加,阴极电流密度增大.液膜厚度减小,E(H2O/H2)负移动,根据Nernst方程:
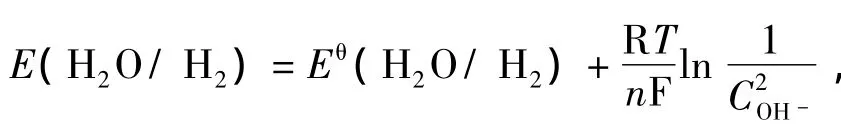
式中Eθ为标准电极电动势,R为气体常数,T为温度,n为电极反应中电子转移数,F为法拉第常数,COH-为电解液中OH-的浓度.薄层液膜下,液膜厚度越薄,OH-更容易扩散到溶液中,OH-浓度越大,E(H2O/H2)减小[11].
2.2 NH4 Cl浓度对X70钢阴极极化曲线的影响
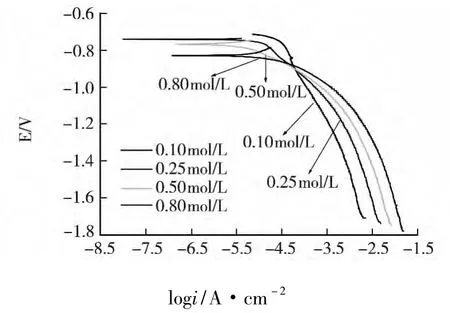
图4 X70钢在不同浓度NH4 Cl薄层液膜下的阴极极化曲线
图4为X70钢在液膜厚度为300μm不同浓度NH4Cl薄层液膜下的阴极极化曲线.
从图4可以看出,在薄层液膜下,随着NH4Cl浓度的增大,阴极极限扩散电流减小,其原因主要是:在薄层液膜下,阴极发生吸氧腐蚀,随着NH4Cl浓度的增大,薄层液膜中溶解O2含量减少,从而降低了液膜中O2浓度[12-13],使得阴极过程变得困难,从而阴极极限扩散电流减小.
2.3 薄层液膜厚度对X70钢腐蚀电位的影响
图5为薄层液膜厚度对X70钢腐蚀电位的影响.从图5可知,液膜厚度减薄,X70钢腐蚀电位增大.其原因为:薄层液膜下,阴极发生吸氧腐蚀:O2+2H2O+4e→—-4OH-,阳极反应为:Fe(s)-2 e→—-Fe2+,生成的Fe2++2OH→—-Fe(OH)2↓,Fe(OH)2+O2+H2→—O Fe(OH)3,液膜厚度减薄,氧的扩散和对流受到的阻碍变小,加剧了阴极反应,腐蚀电位将升高;此外,薄层液膜厚度减薄,腐蚀产物的扩散与传递变得困难,阳极过程受到抑制,也会使腐蚀电位升高[14].
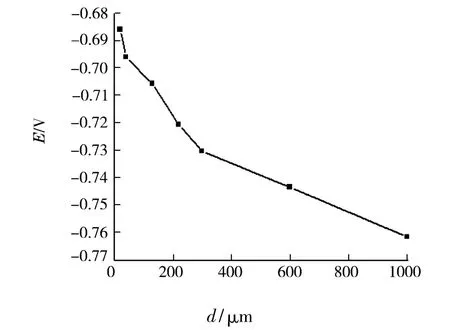
图5 液膜厚度与腐蚀电位的关系
2.4 薄层液膜厚度对X70钢电化学阻抗谱的影响
图6 为X70 钢在0.1 mol·L-1的NH4Cl薄层液膜下浸泡30 min后的电化学阻抗谱图.
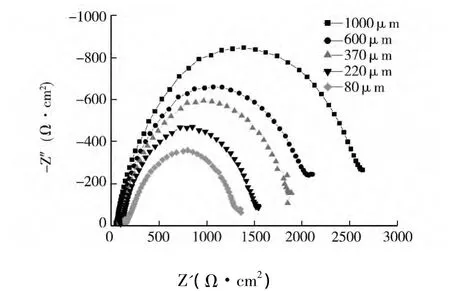
图6 X70钢在不同液膜厚度下浸泡30 min后的电化学阻抗谱图
从谱图可看出,液膜厚度为1 000~80μm时,阻抗谱图均由一个高频容抗弧组成,表现为一个时间常数.高频容抗弧象征着电极表面和液膜间的双电层弛豫过程.液膜厚度的减薄,高频容抗弧的直径减小,电荷传递电阻(R ct)与高频容抗弧的直径相关,而R ct-1与腐蚀速率是成正比,薄层液膜下,O2更容易扩散到电极表面,从而加速X70钢的腐蚀.拟合结果见表1,从表1可知,液膜厚度减小,高频容抗弧的直径逐渐减小,R ct减小,R ct-1增大,X70钢的腐蚀速率加快.

表1 液膜厚度与电荷传递电阻的关系
2.5 NH4 Cl浓度对X70钢电化学阻抗谱的影响
图7为X70钢在液膜厚度为300μm不同浓度NH4Cl薄层液膜下电化学阻抗谱图.
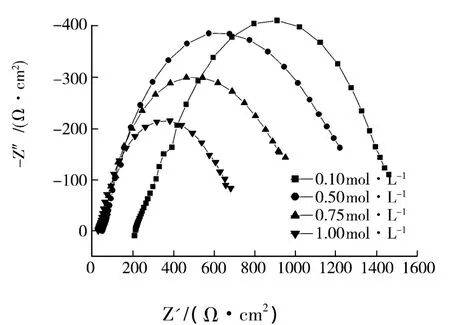
图7 X70钢在不同浓度NH4 Cl薄层液膜下的电化学阻抗谱图
从谱图可看出,液膜厚度为300μm,浓度范围为0.10 ~1.00 mol·L-1时,X70 钢腐蚀的电化学阻抗谱由一个高频容抗弧组成,表现为一个时间常数,呈现为圆心向下的圆弧,这是固体电极固有的特征.随着NH4Cl浓度增大,溶液电阻Rs减小,高频容抗弧直径减小.拟合结果见表2,从表2,结合图4,在 NH4Cl浓度(0.10 ~1.00 mol·L-1)范围内,浓度增大,阴极极限扩散电流减小,对阴极过程有一定的抑制作用;浓度升高,电荷传递电阻变小,电荷传递电阻的倒数R ct-1正比于腐蚀速率,说明NH4Cl浓度增大,加速了X70钢的腐蚀速率.金属的腐蚀受阴极过程和阳极过程共同影响,通过分析可知,浓度增大,抑制了阴极过程,而X70钢腐蚀速度增大,显然,浓度的升高,对阳极过程有一定的促进作用.

表2 NH4 Cl浓度与电荷传递电阻的关系
3 结 论
(1)0.1 mol·L-1的 NH4Cl薄层液膜下,液膜厚度减薄,阴极极限扩散电流增大.液膜厚度约为130μm时,阴极极限扩散电流达最大值.液膜厚度为130~100μm时,阴极极限扩散电流反而降低.液膜厚度小于100μm,阴极极限扩散电流又增大.
(2)NH4Cl浓度增大,阴极极限扩散电流减小,抑制了阴极过程.
(3)液膜厚度减薄,X70钢腐蚀电位正移.
(4)NH4Cl浓度增大,对阳极过程有一定的促进作用,加速了X70钢的腐蚀速率.
[1] F Mansfeld,J.V Kenkel.Electrochemical monitoring of atmospheric corrosion phenomena[J].Corrosion Science,1976,16(3):113-122.
[2] A.Cox,S.B.Lyon.An electrochemical study of the atmospheric corrosion of mild steel-I.Experimental method[J].Corrosion Science,1994,36(7):1167-1176.
[3] 张学元,柯克,杜元龙.金属在薄层液膜下电化学腐蚀电池的设计[J].中国腐蚀与防护学报,2001,21(2):117.
[4] 王文杰,邱于兵,金名惠,等.X70钢在库尔勒土中腐蚀初期的电化学阻抗谱特征[J].材料保护,2007,40(12):18-21.
[5] 郭红,何晓英,伍远辉.H2S对X70钢在弱酸性溶液中的腐蚀行为的影响[J].腐蚀科学与防护技术,2006,18(4):258.
[6] L.J.Zhang,Z.Zhang,F.H.Cao,et al.Study of the X70 pipeline steel corrosion in 3.0%NaCl solution using electrochemical impedance spectroscopy technique[J].金属学报:中文版,2004,17(6):907.
[7] 邓海英,何晓英,王红云,等.X70钢在饱和CO2的HAc-NaAc溶液中的腐蚀行为[J].中国腐蚀与防护学报,2007,27(4):224-227.
[8] 邓祖宇,廖钫,何晓英,等.NaCl薄层液膜下X70钢腐蚀的电化学研究[J].西华师范大学学报:然科学版,2008,29(1):89-92.
[9] 何晓英,邓祖宇,邓海英.(NH4)2SO4薄层液膜下X70钢腐蚀的电化学研究[J].腐蚀科学与防护技术,2008,20(3):213-215.
[10] L Cheng,ZZhang,F H Cao,et al.A study of the corrosion of aluminumalloy 2024-T3 under thin electrolyte layers[J].Corrosion Science.2004,46:1649.
[11] A.Nishikata,Y.Ichihara,Y.Hayashi,et al.Influence of electrolyte layer thickness and pH on the initial stage of the atmospheric corrosion of iron[J].J.Electrochem.Soc.,1997(144):1244-1252.
[12] Werner lang,Rolf zander.Salting-Out of oxygen from A-queous Electrolyte Solutions:Prediction and measurement[J].Ind.Eng.Chem.Fundam,1986,25(4):775-782.
[13] Groisman,A,SH,Khomutov,N,E.Solubility of oxygen in electrolyte solutions[J].Russian Chemical Reviews,1990,59(8):707-727.
[14] Gamal Ahmed El-Mahdy,A Nishikata,Tooru Tsuru.AC impedance study on corrosion of 55%Al-Zn alloycoated steel under thin electrolyte layers[J].Corrosion Science,2000,41:1509.
