术前希罗达化疗对结直肠癌患者外周血循环CK20mRNA的影响*
2014-09-14秦锴贺长林刘峰
秦锴 贺长林 刘峰
(都江堰市人民医院 四川都江堰 611830)
临床流行病学资料显示,早期可手术治疗的结直肠癌患者预后较好,但仍有部分患者术后发生肿瘤复发和远处转移,因此,术前探寻早期结直肠癌患者微转移的标志物及如何降低患者术前微转移的发生成为了研究热点[1]。本研究采用实时荧光定量PCR的方法检测结直肠癌患者术前外周血CK20mRNA的水平并判断术前口服希罗达是否对患者外周血CK20mRNA的相对含量产生影响,从而推测术前口服希罗达化疗是否能降低患者术后远处转移和复发风险[2]。
1 资料与方法
1.1 一般资料 四川都江堰市人民医院2011年10月至2013年10月收治的结直肠癌患者75例,随机分为试验组38例和对照组37例。试验组男23例,女15例,平均年龄(45.5±10.6)岁,术后病理类型:中高分化腺癌13例,中分化15例,低分化10例;对照组男20例,女17例,年龄(42.3±11.1岁),术后病理类型高分化15例,中分化14例,低分化8例。经统计学处理两组患者的年龄、性别、肿瘤分期等差异无统计学意义(P>0.05),组间具有可比性。
1.2 仪器试剂
1.2.1 仪器 ABI PRISM7000real-time PCR 反应仪(购自美国ABI公司);恒温水浴锅(购自美国GRANT公司);普通离心机(购自美国Beckman公司。
1.2.2 试剂材料 RNA提取试剂盒(购自TAGENG公司);CK20mRNA荧光定量PCR试剂盒(上海久盛医疗用品有限公司)。CK20mRNA上游引物:5′-CAGGCACACGGT-GAACTATGG-3′,下 游: 5′-GATCAGCTTCCACTGTTAGCG-3′。cDNA反转录采用oligoDT方法对全基因组mRNA进行反转录成Cdna,所有引物序列由TAKARA大连宝生物有限公司合成。
1.3 方法
1.3.1 给药方法 试验组术前每天希罗达2500 mg/m2,两次口服,共1周,对照组为进行术前辅助化疗。于患者术晨抽取外周静脉血10mL进行检测血浆循环采CK20mRNA。
1.3.2 RNA提取剂real-time PCR 根据全基组RNA提取试剂盒操作说明,提取两组患者外周血总RNA,然后根据TAKARA反转录试剂盒操作说明,将总RNA反转录为cDNA并检测cDNA浓度。根据real-timePCR荧光定量试剂盒操作说明,对上述两组患者cDNA中的CK20mRNA进行检测,并根据荧光强度判断CK20mRNA相对含量及阳性率(图1)。
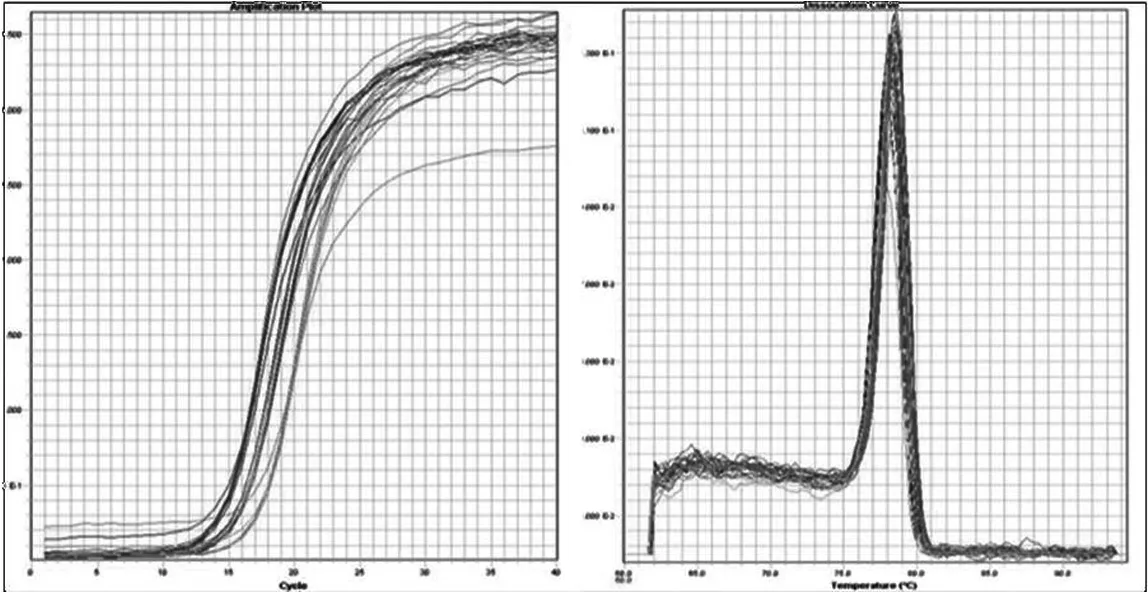
图1 CK20mRN实时荧光定量PCR扩增及溶解曲线
1.4 统计学方法 SPSS15.0统计学软件进行数据分析,计量资料采用()表示,组间比较采用t检验,计数资料采用率表示,组间比较采用χ2或fisher确切概率法比较,P<0.05为差异有统计学意义。
2 结 果
2.1 两组患者外周CK20mRNA阳性率比较 试验组38例患者希罗达口服1周后外周血CK20mRNA检测阳性21例(55%),对照组CK20mRNA检测阳性35例(95%),试验组CK20mRNA阳性率显著低于对照组(P<0.05)。
2.2 两组阳性患者CK20mRNA相对含量比较试验组CK20mRNA阳性患者其CK20mRNA相对换量为0.13±0.08,显著低于对照组0.78±0.22(P<0.05)图2。

图2 两组患者CK20mRNA相对含量比较
3 讨 论
结直肠癌是我国常见消化道肿瘤,临床上较为常见,早期接受手术治疗患者预后较好,但晚期发生转移患者预后较差,5年生存率较低[3]。但临床流行病学资料显示,部分早期患者术后仍然发生肿瘤复发和远处转移,因此提示临床分期为早期的结直肠癌患者在进行手术时可能已经发生了微转移[4、5]。术前或术中发生微转移是导致结直肠癌患者术后预后不良的重要原因之一。因此,术前探寻早期结直肠癌患者微转移的标志物成为了研究热点。CK源于上皮细胞,包括至少20种相关基因多肽家族,是上皮细胞分化的标记物,临床研究显示,发生远处转移的晚期结直肠癌患者血清CK20的水平显著升高,被认为是检测癌细胞循环的敏感标记物。CK20是一种新发现的多肽,局限在胃肠上皮细胞具有严格组织特异性,几乎在所有大肠癌中都明显表达。我们推测,用编码CK20蛋白的CK20mRNA作为CK20蛋白的上游表达产物,应与CK20在预测结直肠癌微转移方面具有同样效果,且其为CK20的编码基因转录产物,应在判断的敏感性和特异性方面更优于 CK20[6,5]。因此,本研究采用real-timePCR的方法对我院收治的75例早期接受手术的结直肠癌患者进外周血CK20mRNA水平检测,并根据是否术前应用希罗达口服化疗分为试验组和对照组,判断希罗达术前口服化疗对患者外周血CK20mRNA表达水平的影响。研究结果发现,试验组CK20mRNA阳性率显著低于对照组(P<0.05);试验组 CK20mRNA 阳性患者其CK20mRNA相含量显著低于对照组(P<0.05)。结果提示,结直肠癌患者术前口服希罗达可显著降低患者外周血CK20mRNA阳性率及拷贝数。
本研究中采用术前希罗达口服化疗,降低了患者外周血CK20mRNA的表达水平,因而可能在一定程度上减低患者术后肿瘤复发风险,但由该研究部分数据尚未获得,无法对两组患者术后转移复发及生存率进行完整统计,因而希罗达术前口服化疗是否降低肿瘤复发风险及延长患者生存时间有待进一步研究。
[1]Ricardi U,Racca P,Franco P,et al.Prospective phase II trial of neoadjuvant chemo-radiotherapy with Oxaliplatin and Capecitabine in locally advanced rectal cancer(XELOXART)[J].Medical oncology,2013,30(2):581.
[2]Al-Gahmi AM,Kerr IG,Zekri JM,et al.Capecitabine-induced terminal ileitis[J].Ann Saudi Med,2012,32(6):661-662.
[3]张健.希罗达与奥沙利铂治疗中晚期结肠癌的疗效分析与评价[J].临床合理用药杂志,2011,04(36):53.
[4]Matsuda C,Tamagawa H,Nishikawa K,et al.Study of tolerability of capecitabine in postoperative adjuvant chemotherapy in colon cancer[J].Cancer &chemotherapy,2013,40(3):327-330.
[5]Schmiegel W,Reinacher-Schick A,Arnold D,et al.Capecitabine/irinotecan or capecitabine/oxaliplatin in combination with bevacizumab is effective and safe as first-line therapy for metastatic colorectal cancer:a randomized phase II study of the AIO colorectal study group[J].Annals of oncology:official journal of the European Society for Medical Oncology/ESMO,2013,24(6):1580-1587.
[6]Kim KP,Kim HS,Sym SJ,et al.A UGT1A1*28 and *6genotype-directed phase I dose-escalation trial of irinotecan with fixed-dose capecitabine in Korean patients with metastatic colorectal cancer[J].Cancer Chemother Pharmacol,2013,71(6):1609-1617.
