大米过氧化氢酶活性的2种测定方法比较
2014-06-11朱银硕
郎 杰 朱银硕
(河北经贸大学生物科学与工程学院,石家庄 050061)
大米在储藏过程中会由于自身陈化作用而劣变,降低大米品质,大米的储藏保鲜问题一直倍受重视。检测大米等谷物的陈化程度或新鲜度有很多指标[1],酶活性检测也是其中之一,例如在粮油检验中的过氧化氢酶(CAT)活动度检验。
大米储藏中的代谢会产生少量过氧化氢使大米脂质等成分氧化而品质下降。大米中的过氧化氢酶可将产生的过氧化氢分解减轻氧化作用,大米中的过氧化氢酶活性与大米储藏品质有密切关系[2]。
过氧化氢酶的测定方法有十几种[3],例如气量法、滴定法、分光光度法、荧光法、电化学法等。粮油检验的国家标准一直使用高锰酸钾滴定法[4-5]。滴定法优点是所用设备简单,不需贵重仪器,缺点是测定中凭肉眼观测滴定终点,不可避免地存在较大的人为判断误差,以及操作中滴定液流量的控制误差。以钼酸铵作为反应终止剂和显色剂对过氧化氢酶进行分光光度法测定,已广泛用于动物血清测定及临床检验,但在粮谷类测定中尚未采用。本试验应用钼酸铵比色法与高锰酸钾滴定法一同测定大米中过氧化氢酶活性,以探讨钼酸铵法用于粮谷检验的可行性。同时也选择不同产地大米测定其过氧化氢酶活性是否存在差异。
1 材料与方法
1.1 供试材料
选择6种市售商品大米,分别产自黑龙江的佳木斯和哈尔滨地区、辽宁盘锦地区、河北唐山地区、安徽阜阳地区和广东佛山地区(品种略去),依次标号为Ⅰ、Ⅱ、Ⅲ、Ⅳ、Ⅴ、Ⅵ。各称取100 g测定水分,将其余大米放置冰箱预冷(-15 ℃)24 h,粉碎过100目筛(150 μm孔径)后仍置冰箱备用。
1.2 主要试剂和仪器
过氧化氢(H2O2含量30%)、高锰酸钾和钼酸铵等试剂均为分析纯。草酸钠基准试剂购自阿拉丁试剂有限公司。
UV-752型可见紫外分光光度计:上海光谱分析仪器厂; Avanti J-25型高速冷冻离心机:美国贝克曼库尔特公司。
1.3 过氧化氢酶提取与测定
1.3.1 高锰酸钾滴定法(国标法)
过氧化氢酶提取及活性测定参照文献[5]进行,包括试剂配制和标定。
称取5.00 g(已扣除水分)过筛后的大米粉,加入50.0 mL pH 7.8 PBS(磷酸盐缓冲液),研磨振荡混合后置冰箱预冷1 h,在冷冻离心机中6 000 r/min离心15 min,收集上清液得到过氧化氢酶粗提液。提取的粗酶液立即按文献描述方法进行测定并按文献[5]公式进行计算。每样本(大米)分为6组测定,分2批由2人分别进行,每组测定设3次重复。同时用标定的过氧化氢配制0.01%~2.00%的一系列标准液滴定做高锰酸钾滴曲线,以检验不同浓度与滴定液体积的线性关系。
1.3.2 钼酸铵比色法(钼酸铵法)
过氧化氢酶提取与前项相同。测定方法参照文献[6]略作改动。底物溶液为60 mmol/LH2O2(用高锰酸钾标定),PBS为60 mmol/L的Na2HPO4和NaH2PO4(pH 7.8)。
3组试管分别标记为空白管1、空白管2和测试管,均加入5 mL 60 mmol/L过氧化氢溶液,再向空白管1中加入5 mL 50 mmol/L钼酸铵溶液和3 mL煮沸的提取酶液;空白管2中加入5 mL 50 mmol/L钼酸铵溶液和3 mL PBS;测试管中加入3 mL 提取酶液,摇匀后在30 ℃下水浴15 min,然后立即加入5 mL 50 mmol/L钼酸铵溶液摇匀。与前2管一起用分光光度计在410 nm处测定吸光度。以每分钟分解1 μmol过氧化氢为1个酶活单位(U),参照文献[6]中公式计算酶活性。然后换算为酶活动度(mgH2O2/g)。
式中:分子项60为反应液H2O2浓度/μmol,5为反应液量/mL,50为提取酶液量/mL;分母项中3为待测酶液量/mL,5为大米样品质量/g,15为反应时间/min。
每样本(大米)分为6组测定,每组测定设3次重复。再由不同试验者重复测定1次。同时用标定的过氧化氢配制0.01%~2.00%的一系列标准液再按空白管2方法做钼酸铵吸光曲线,以检验不同浓度与吸光度的线性关系。
1.4 数据处理
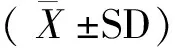
2 结果与分析
2.1标定过氢化氢的高锰酸钾滴定曲线和钼酸铵吸光曲线比较
用标定的不同质量分数的过氧化氢(0.01%、0.05%、0.10%、0.25%、0.50%、0.75%、1.00%、1.50%、2.00%)分别进行高锰酸钾滴定和钼酸铵比色做标准曲线(图1),2条曲线几乎完全平行,高锰酸钾滴定体积与过氧化氢浓度的相关性为R2=0.999(r=0.999**,P<0.01),钼酸铵比色的吸光度与过氧化氢浓度的相关性为R2=0.998 6(r=0.999**,P<0.01),都达到极显著相关,表明二者在测定过氧化氢的线性关系和浓度适应范围上几乎是相同的。
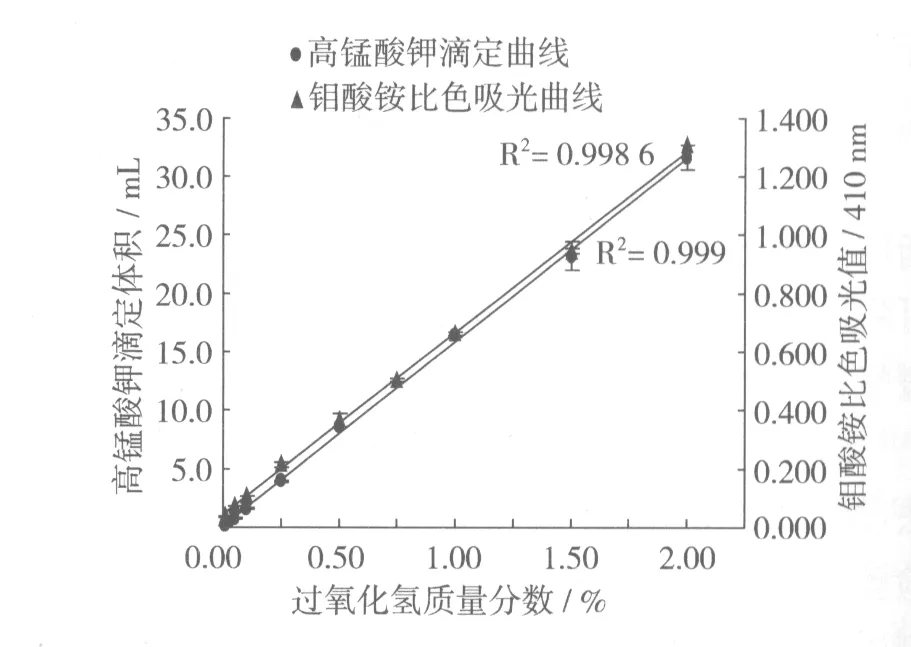
图1 标定过氧化氢的高锰酸钾滴定曲线和钼酸吸光曲线比较

表1 高锰酸钾滴定法测定6个产地大米过氧化氢酶活动度(mgH2O2/g)分析
2.2高锰酸钾滴定法对6个产地大米过氧化氢酶活动度的测定及分析
高锰酸钾滴定法测定6个产地大米中过氧化氢酶活动度平均10.22 mgH2O2/g,活动度变化约在8.05~12.02 mgH2O2/g间,产地偏北方地区样本相对略高于偏南方地区样本。2批测定的均值差与均数之比未超过文献[5]的国标误差限度,符合测定要求。2批测定结果为显著相关(表2)。但从方差分析表中可以看出,误差一项明显较高,使产地因素差异不够显著。
2.3钼酸铵比色法对6个产地大米过氧化氢酶活动的测定及分析
钼酸铵法测定结果表明,6个产地大米过氧化氢酶活动度平均为11.66,活动度变化在9.05~13.88 mgH2O2/g 之间,大米产地活动度趋势与高锰酸钾法测定一致,但各样本测定值均略高于高锰酸钾法。2批测定的均值差与均数之比小于高锰酸法测定法,同样未超过文献[5]的国标误差限度,符合测定要求。2批测定结果为极显著相关。从方差分析表中可以看出,误差一项的变异远小于产地因素变异,略大于测定组因素。与高锰酸钾法相比,用钼酸铵法测定产地因素差异较为显著。
2.4 2种方法测定6个产地大米过氧化氢酶活性的比较分析
为比较2种测定方法的差异,将2种方法的测定结果列于表5。

表2 高锰酸钾滴定法测定6个产地大米过氧化氢酶方差分析表
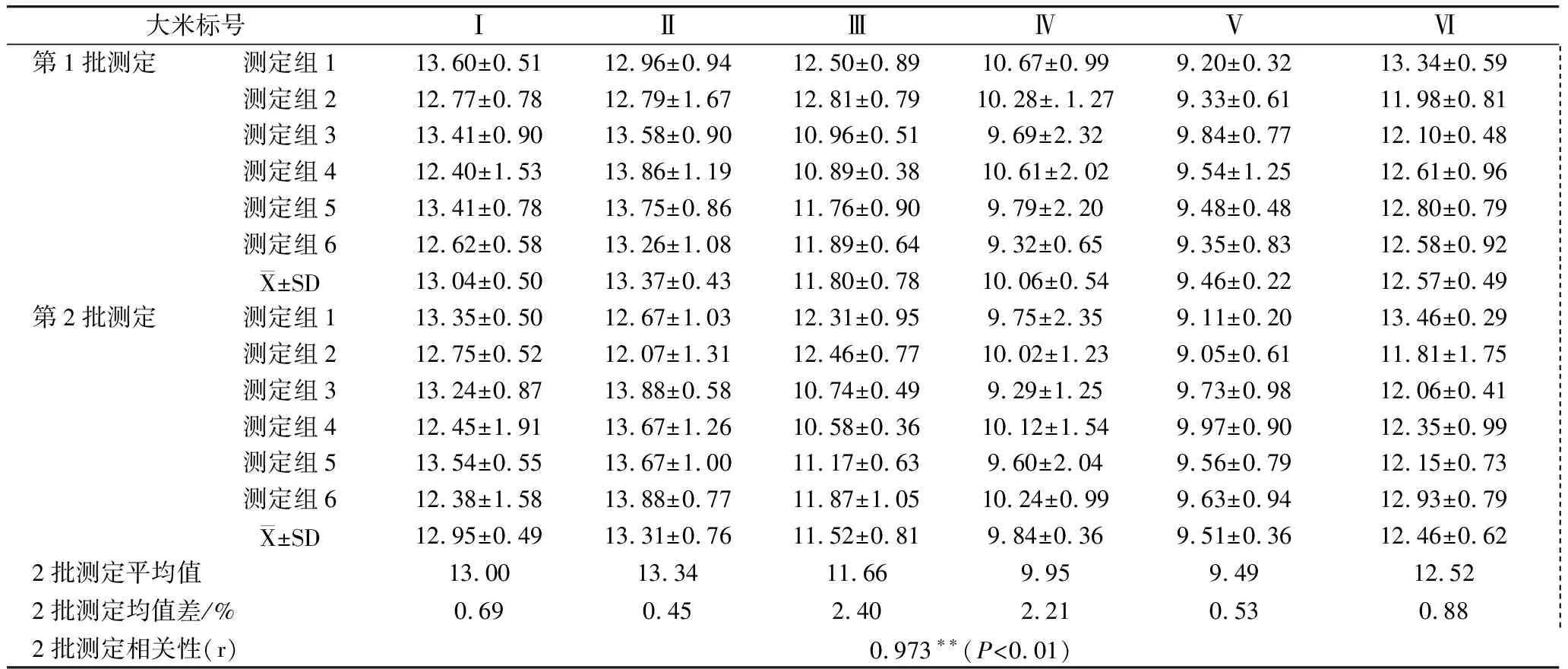
表3 钼酸铵比色法测定6个产地大米过氧化氢酶活动度(mgH2O2/g)分析

表4 钼酸铵法测定6个产地大米过氧化氢酶方差分析表
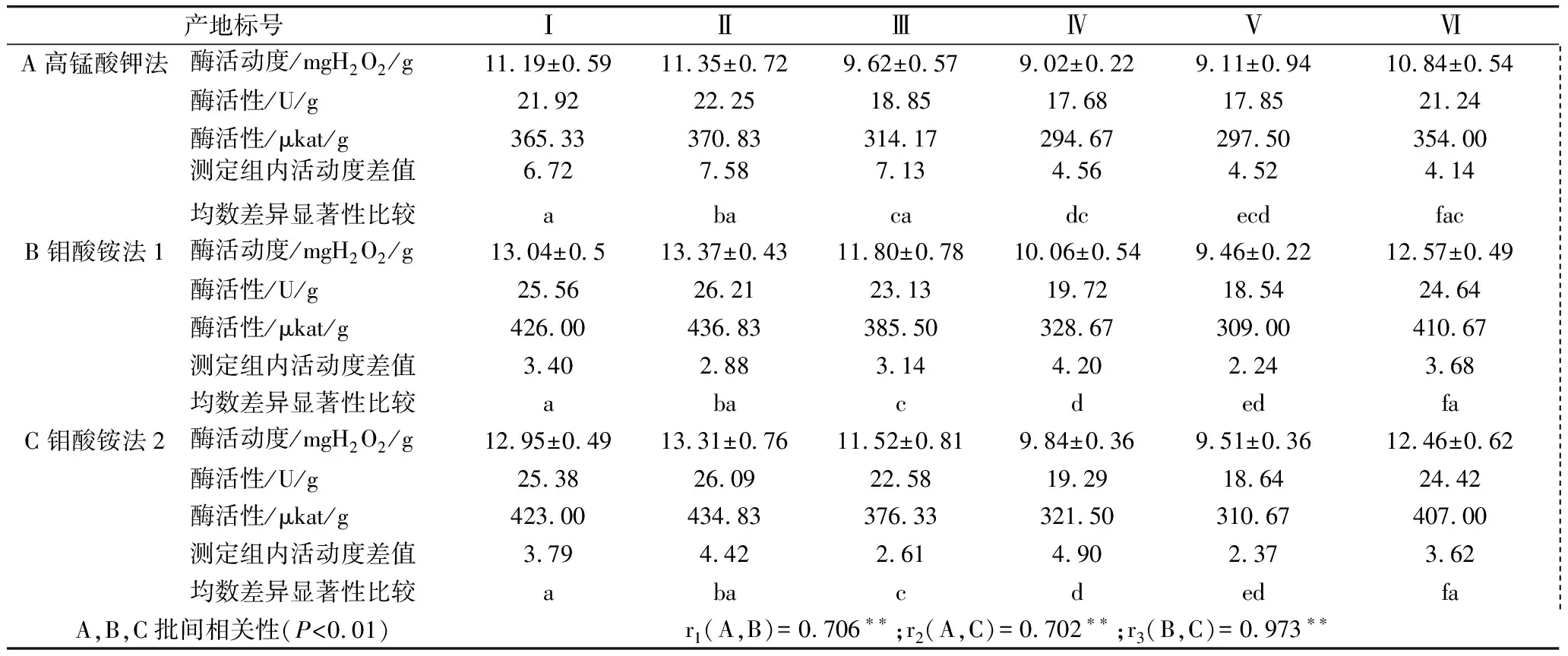
表5 2种方法测定6个产地大米过氧化氢酶活性比较
注:酶活动度均数为6次测定平均值;测定组内活动度差值为同一样本在不同测定组中的最小值与最大值差;表5中均数差异显著比较为LSD(P<0.05),字母不重复者间为差异显著;钼酸铵法1和2表示2批重复性测定。
从过氧化氢酶活动度的测定结果看,钼酸铵法测定的6个产地样本平均数高于高锰酸钾滴定法1.44个活动度。从测定的稳定性方面,钼酸铵法明显好于高锰酸钾法,高锰酸钾法测定组内平均差值为5.78,钼酸铵法为3.44,虽然二者都存在波动,但钼酸铵法的波动相对较小。由前面的方差分析表中也可以看到,高锰酸钾法的误差大于钼酸铵法。由此,2种方法对多个样本测定结果的差异显著性比较时,钼酸铵法更能反映不同样本间的差异。如表5中的不同产地样本过氧化氢酶活动度差异显著性的成对比较中,高锰酸钾法只出现5对差异显著,钼酸铵法则出现11对差异显著。对于比较不同样本的过氧化氢酶活动度,钼酸铵法更为适合。钼酸铵法对6个产地样品的过氧化氢酶活动度的2批测定(表5中的B和C)与高锰酸钾法测定(表5中的A)的相关性为极显著。
3 讨论
钼酸铵法目前多用于测定动物血清中过氧化氢酶。用高锰酸钾滴定法测定大米过氧化氢酶活动度只限于粮油检验报告中,在专业性学术刊物中鲜见报道。本试验应用2种方法对大米过氧化氢酶进行测定比较,测定数据表明钼酸铵法明显优于目前国家标准中的高锰酸钾滴定法。高锰酸钾法测定数据波动相对较大,原因主要是操作中滴定液的流量凭手感控制以及终点颜色变化凭肉眼观察,容易导致误差产生。其次,高锰酸钾滴定虽是等当量反应,但受反应液酸度影响很大也会引起误差。与高锰酸钾滴定法相比较,钼酸铵法稳定性较好,操作相对较为简单,可大批量测定,由此认为粮谷类过氧化氢酶检验采用钼酸铵法取代国家标准中的高锰酸钾滴定较为可行。但钼酸铵比色法要作为标准方法用于粮谷检测,许多操作细节及各项反应条件设置还有待于进一步优化或改进。
至于本试验测定中钼酸铵法测定值略高于高锰酸钾滴定法,推测其原因可能在于酶提取液中的微量淀粉等物质在保温反应中颗粒膨大增加少量光吸收,尤其是作为空白的煮沸酶液,这可尝试通过减少酶提取液用量,以及对酶提取液严格过滤解决。或也可能还有其他原因,这有待于进一步研究。
本试验也尝试了用直接紫外分光光度法和重铬酸钾比色法测定大米的过氧化氢酶(数据未列出),但其稳定性和适用性均不强于高锰酸钾滴定法。还有一些利用过氧化氢与喹啉、鲁米诺、联苯胺等发色物质反应生成有色物质进行比色测定的方法,例如联吡啶或喹啉等可与H2O2反应产生荧光,过氧化氢酶可分解H2O2减少荧光产生,由此检测过氧化氢酶活性[7];鲁米诺可受过氧化氢酶催化H2O2分解时产生的氧自由基激发而发光,测定发光值的增加可反映CAT活性[8]。这类方法虽反应灵敏,但对测定条件及反应时间要求严格,控制不当则稳定性明显降低,测定过程较难掌握。
过氧化氢酶活性在国标GB/T 5522—2008中用过氧化氢酶活动度表示有待商榷。从过氧化氢酶活动度的单位mgH2O2/g来看,是表示每克样品中能催化过氧化氢分解的质量(mg),实际仍是表达的酶活性大小的概念。国际生物化学联合会(IUB,现名为国际生物化学与分子生物学联盟 IUBMB)酶学委员会曾于1961年规定每分钟催化1 μmol底物转化为产物所需的酶量为1个国际单位(IU或U),虽已广泛使用但并未被国际计量委员会(CIPM)承认为SI单位。国际纯粹与应用化学联合会(IUPAC)与国际临床化学联合会(IFCC)推荐使用的酶活性单位katal(符号kat)于1999年被国际计量大会(CGPM)批准,也尚未获得国际计量委员会承认,但其成为新的国际单位制(SI)基本已成事实。所以酶的活性单位倾向于使用kat(1 kat=1 mol/s)[9-10]。质量催化活性单位应为kat/kg或其分数单位[11]。kat和U的关系为:1U=16.67×10-9kat =16.67×10-6mkat =16.67×10-3μkat =16.67 nkat。
尽管酶的活动度、酶的活性单位U (IU)及kat都未纳入我国的国际单位制标准GB 3100—1993中,但从3个单位的比较看,kat单位相对更规范一些。我国在某些出版行业已要求酶的活性单位使用kat[12]。因此建议过氧化氢酶检验标准中改用kat较好,更便于与其他研究结果进行比较。
4 结论
通过试验中钼酸铵法和高锰酸钾滴定法对不同产地大米样本过氧化氢酶活动度测定的比较和分析,认为钼酸铵法在测定粮谷过氧化氢酶方面优于现行国家标准中的高锰酸钾滴定法,其优点在于测定中体现出较好的稳定性,重复测定间波动性明显低于高锰酸钾法,因此在比较不同样本过氧化氢酶活性差异具有相对较高的分辨力;由于钼酸铵法比色测定较为简单,可进行大批量样本测定。另外由于钼酸铵法所需试剂少,操作简便,容易掌握,而高锰酸钾法配制试剂时间长而麻烦,滴定操作也不便于大批量样本测定,所以钼酸铵法适用性更强。通过以上分析认为钼酸铵法更适用于粮油检验中的过氧化氢酶检测。
[1]祁明霞,林艳,解彬.大米新鲜度及其影响因素的研究[J].啤酒科技,2007(9):23-29
[2]宋伟,陈瑞,刘璐.不同储藏条件下糙米中过氧化氢酶活动度的变化规律[J].粮食储藏,2010,39 (6):28-33
[3]朱星晔,韩育梅.过氧化氢酶的检测方法及其在大米贮藏中的应用[J].农产品加工·学刊,2010(8):103-105
[6]程鲁京,孟泽.钼酸铵显色法测定血清过氧化氢酶[J].临床检验杂志,1994,12(1):6-8
[7]薛细平,陈荣,赵一兵,等.过氧化氢酶的荧光法测定及其在海洋环境污染评估中的应用[J].厦门大学学报:自然科学版,2003,42(1):83-86
[8]谭亚芳,孙树秦,赖炳森.一种优化的测定过氧化氢酶活性的方法[J].生物技术,2001,11(5):39-41
[9]秦社彩.生物农医领域中的酶活性单位[J].科技与出版,1999(2):24-25
[10]钟传欣.酶活力的量和单位的用法探讨[J].贵州教育学院学报:自然科学版,2008,19(12):73-74
[11]何扬举,董邦权,潘伯荣.kat是酶活性的SI单位[J].编辑学报,2004,16(1):30
[12]中国高等学校自然科学学报研究会编.中国高等学校自然科学学报编排规范[M].北京:北京工业大学出版社,1993:54.
