单核细胞增生李斯特菌三种检测方法的比较
2013-04-11张烜榕颜军李文龙侯敏蒋玉佳卜舒李桂满
张烜榕,颜军,李文龙,侯敏,蒋玉佳,卜舒,李桂满
(昆明市疾病预防控制中心,昆明650228)
单核细胞增生李斯特菌三种检测方法的比较
张烜榕,颜军,李文龙,侯敏,蒋玉佳,卜舒,李桂满
(昆明市疾病预防控制中心,昆明650228)
目的:通过比较国标法、real-time PCR法和LAMP方法,得到适合基层实验室快速检测单核细胞增生李斯特菌的方法。方法:分别用国标法、real-time PCR法和环介导的等温扩增(loop-mediated isothermal amplification,LAMP)法检测李斯特菌,并进行方法比较。结果:三种方法对单增李斯特菌的检测结果一致.国标法整个检测过程需5~7 d;real-time PCR法实验条件要求高,成本高,检测需1.5~2.5 d;LAMP法实验条件低,成本低,检测时限与real-time PCR相同。结论:LAMP法检测单增李斯特菌灵敏度高、特异性强、快速高效和低成本,适合基层实验室应急检测和现场监测使用。
国标法;LAMP;PCR;单核细胞增生李斯特菌检测
单核细胞增生李斯特菌(Listeria monocytogenes,LM)是一类兼性细胞内生长的革兰阳性杆菌,致病力较强,可引起人畜李斯特病,临床表现为败血症、脑膜炎、单核细胞增多和胃肠炎,主要通过污染的肉类、乳制品和蔬菜等引起李斯特菌感染。国内外对单增李斯特菌高度重视,1986年WHO已将其列为食品四大致病菌之一,2000年在WHO食品安全工作计划中,已将该菌列为重点检测的食源性致病菌之一〔1〕。最近,美国从2011年7月31日出现首例李斯特病病例报告至同年12月8日,共报告病例146例,死亡30例,这是10多年来美国最严重的一起食源性疾病暴发事件〔2〕。所以及时有效的控制食品中LM的污染是食品安全的重要保障之一。
LM的鉴定方法有国标的分离鉴定法、免疫学鉴定法、PCR法等。分离培养鉴定法较简单,但操作繁琐,鉴定过程需要5~7 d,检出限较低,费时费力,难以满足突发事件的快速检测要求。免疫学鉴定法由于菌体及鞭毛抗原交叉反应的存在,难以进行李斯特菌种间的特异性鉴别〔3〕。PCR法具有特异性强、灵敏度高和反应速度快的优点,但需要昂贵的PCR仪,且检测成本高,不适宜基层实验室使用。由Notomi等〔4〕在2000年设计的LAMP法是一种恒温核酸扩增方法,该方法是通过4条特异性引物识别靶基因的6个区域和具有链置换活性的Bst(Bacillusstearothermophilus)DNA聚合酶作用,在65℃的恒温条件下扩增。与PCR不同,LAMP不需要精密的PCR仪和昂贵的试剂〔5〕,尤其适合在缺乏设备支持的基层实验室和突发现场开展检测工作。本实验通过同时应用国标的分离鉴定法,PCR法和LAMP法检测鉴定LM来比较LAMP方法在LM检测中的高效性、准确性和可靠性。
1 材料与方法
1.1 菌株实验室保存的李斯特菌11株。
1.2 主要试剂和仪器设备单增李斯特菌检测试剂盒(荧光PCR法)购自深圳易瑞生物技术有限公司;单核细胞增生李斯特氏菌核酸检测试剂盒(环介导恒温扩增法)购自广州华峰生物科技有限公司;琼脂购自基因公司;10000×SYBR GreenI购自北京优尼康生物科技有限公司;全自动微生物生化鉴定仪(VITEK32);上海一恒恒温水浴锅;BIO-RAD凝胶成像系统;北京八一六厂电泳仪。
1.3 方法
1.3.1 国标法根据食品安全国家标准《食品微生物学检验单核细胞增生李斯特氏菌检验》GB4789.30-2010分离鉴定菌株。李氏增菌肉汤LB1 30℃培养24 h,转种李氏增菌肉汤LB2 30℃培养24 h,接种于PALCAM平板和李斯特氏显色培养基36℃培养24 h,取菌落分别接种在木糖和鼠李糖发酵管36℃培养24 h,同时在TSA-YE上纯化30℃培养24 h,选择木糖阴性、鼠李糖阳性的菌继续进行全自动生化鉴定6~7 h,并依次进行动力试验、生化鉴定和溶血试验。
1.3.2 real-time PCR法取培养24 h的LB2增菌液1 mL,10 000 r/min离心2 min,弃上清,加入80 μL DNA提取液混匀煮沸裂解10 min,置冰上10 min,10 000 r/min离心2 min,上清即为模板。按试剂盒说明书准备反应体系,分别取5 μL阴性、阳性质控品和提取的DNA加入反应体系中。循环参数:预变性95℃10 min,1次循环;变性95℃10 s,退火、延伸及检测荧光58℃45 s,40次循环。
1.3.3 LAMP法菌株DNA提取参见real-time PCR法。根据试剂盒说明书分别取2.5 μL阴性、阳性质控品和提取的DNA加入反应体系中,置65℃60 min。
1.4 结果判定
1.4.1 国标法VITEK32直接判读结果后,进行后续的生化试验鉴定。所用李斯特菌株生化反应特征,见表1。
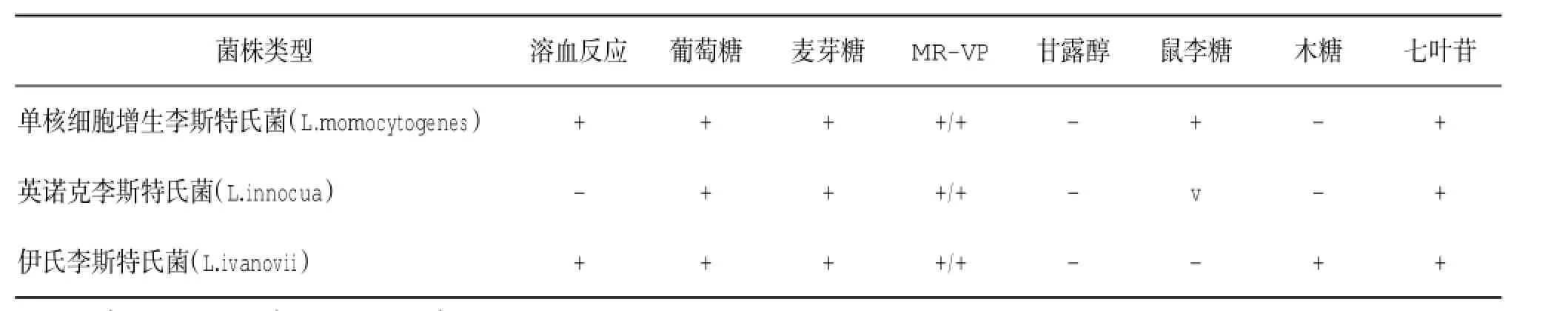
表1 单核细胞增生李斯特氏菌生化特征与其他李斯特氏菌的区别
1.4.2 real-time PCR法阳性结果呈现典型的S型扩增曲线。Ct值≥38或undet为阴性结果,Ct值<35为阳性结果,35≤Ct值<38为检测灰区,重复测定两次,两次测定Ct值≥38为阴性结果,其中一次Ct值<38为阳性结果。
1.4.3 LAMP法肉眼观察产物颜色变化,出现绿色判定为阳性,橙色为阴性。扩增产物在1.5%琼脂糖凝胶上进行电泳,有不同大小的梯形条带为阳性结果,不产生条带为阴性结果。
2 实验结果
2.1 国标法检测11株李斯特菌中7株为LM,3株为英诺克李斯特菌,1株为伊氏李斯特氏菌,见表2。11株李斯特菌4株从速冻熟制米面制品中分离,3株从熟肉制品中分离,2株从即食非发酵性豆制品中分离,1株为省疾控下发质控,1株为国家临检中心下发考核样。其中,检出7株LM中除1株为省疾控下发质控样外,其余为2株从速冻熟制米面制品中分离,2株从熟肉制品中分离,2株从即食非发酵性豆制品中分离;3株英诺克李斯特菌中1株从熟肉制品中分离,2株从速冻熟制米面制品中分离;1株伊氏李斯特菌是国家临检中心下发考核样,见表2。说明李斯特菌对环境要求和营养要求都不高,可污染不同的食物,特别是加工后即食的食品。
2.2 real-time PCR法采用针对目标菌为LM的荧光PCR法分别对11株实验菌株核酸进行扩增,其中有7株菌株PCR扩增呈现典型S型扩增曲线,Ct值均<35,检测结果为LM,其它4株李斯特菌为阴性,检测结果与国标法一致,见表3。

表2 国标法检测结果

表3 三种方法检测单增李斯特菌结果比较
2.3 LAMP法恒温扩增实验菌株核酸,目测扩增产物,11株李斯特菌中有7株绿色为LM,其余橙色为其它李斯特菌,结果见图1。扩增产物经琼脂糖凝胶电泳后,7株LM菌株与阳性质控菌株一样有相同的明亮的梯形条带,4株非单增李斯特菌没有典型的LAMP扩增条带,见图2。其LM检测结果与国标法和real-time PCR法检测一致,见表3。

图1 LAMP法检测单增李斯特菌目测结果
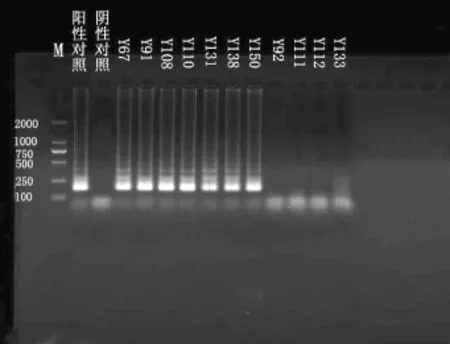
图2 LAMP法检测单增李斯特菌琼脂糖电泳图
3 讨论
LM广泛存在于自然界中,生存条件要求不高,在极端环境中仍可生长。该菌在5~45℃均可生长,经58~59℃10 min可杀死,在5℃低温生长是典型特征之一,在-20℃可存活一年,能在冰箱冷藏室内较长时间生长繁殖,不易被冻融,耐碱不耐酸,在pH 9.6中仍能生长,在10%NaCl中可生长,在4℃的20%NaCl中仍可存活8周。该菌引起致病的物质为李斯特菌溶素O,此溶素须细菌被吞噬后在细胞内生长时释放。几乎所有被诊断为单增李斯特菌感染的患者均有侵袭性感染症状(即细菌从胃肠道扩散到血液或其他部分),突出的临床表现为败血症、脑膜炎、脑脊髓炎、发热,有时可引起心内膜炎。
随着社会经济的快速发展,生活节奏越来越快,人们对即食食品、冷藏和速冻食品的需求量迅速增加,这也同时增加了LM对人们的威胁,因此对LM进行快速、灵敏、准确的检测能有效的保证食品安全卫生。本实验选取的11株李斯特菌有分离于速冻熟制米面制品、熟肉制品和即食非发酵性豆制品,说明LM在我们周围是普遍存在的,其生存条件要求不高,生存耐受力很强,在冰箱冷藏室内仍可生长繁殖的生存能力使其具有极高的感染人畜的潜在危险机率。本实验通过用三种方法对LM检测结果进行比较,获得一种较为简便易行的检测方法。国标法是对分离培养后的可疑菌落通过生化试验、动力试验和溶血试验等进行鉴定,检验过程需要5~7 d,耗时耗力、且操作复杂,不能达到迅速为食物中毒等食品安全突发事件提供病原学依据的要求。Real-time PCR法特异性强、灵敏度高,省时省力,其检验过程需要1.5~2.5 d,但需要昂贵的PCR仪,而且对试验环境要求和操作人员技术的要求都很高,在一定程度上限制了其发展和应用。近年来的研究〔6-9〕表明LAMP法在检测各种食源性致病菌方面具有很多优势。本实验应用LAMP法检测了11株李斯特菌株,结果对其中7株LM的核酸均有扩增,对其余4株其它李斯特菌的核酸均无扩增,其结果与国标法和realtime PCR法一致,检验过程需1.5~2.5 d,显示出该方法对LM的检测的特异性、灵敏性和准确性不亚于PCR法,且对试剂要求简单,仪器要求不高,只需要提供恒定温度的设备即可,产物鉴定简便易行,视觉观察产物变绿的是LM,橙色是非单增李斯特菌,因而能在短时间内、简单的实验条件和要求不高的实验环境下为食品安全突发事件提供快速的病原学的初步检测依据。
综上所述,通过对三种检测鉴定方法的结果比较可知LAMP法检测LM是三种检测法中较简便和快速的方法,与其它核酸扩增技术相比,具有实验操作简单、快速、成本低、对设备条件要求低等方面的优势。其特异性强、灵敏度高、快速高效和产物鉴定简便的优点,适合县区级疾病预防控制中心快速检测和现场监测等应用。
〔1〕严剑波,王虹玲,朱水荣,等.单增李斯特菌LMAP方法的建立〔J〕.中国卫生检验杂志,2009,19(9):2048-2050.
〔2〕Multistate Outbreak of Listeriosis Linked to Whole Cantaloupes from Jensen Farms,Colorado〔EB/OL〕.〔2011-11-08〕.http://www.cdc.gov/listeria/outbreaks/ cantaloupes-jensen-farms/index.html.
〔3〕巢国祥,周晓辉,焦新安.单核细胞增生性李斯特菌PCR快速检测方法的建立及应用〔J〕.中国人兽共患病杂志,2004,20(9):797-800.
〔4〕Notomi T,Okayama H,Masubuchi H,et al.Loop-mediated isothermal amplification of DNA〔J〕.Nucleic Acids Res,2000,28(12):E63.
〔5〕肖斌,朱永红,邹全明.简便敏感的环介导等温扩增基因诊断新技术〔J〕.中华检验医学杂志,2005,28(7):761-763.
〔6〕Maruyama F,Kenzaka T,Yamaguchi N,et al.Detection of Bacteria Carrying the stx2 Gene by In Situ Loop-Mediated Isothermal Amplication〔J〕.App1 Environ Microbiol,2003,69(8):5023-5028.
〔7〕Song T,Toma C,Nakasone N,et al.Sensitive and rapid detection of Shigella and enteroin vasive Escherichia coli by a loop-mediated isothermal amplification method〔J〕. FEMS Micribiol Lett,2005,243(1):259-263.
〔8〕Yukiko H K,Nemoto J,Ohtsuka K,et al.Sensitive and rapid detection of Vero toxin-producing Escherichia coil using loop-mediated isothermal amplification〔J〕.Journal of Medical Microbiology,2007,56:398-406.
〔9〕侯敏,颜军,张烜榕,等.环介导等温扩增技术检测技术检测志贺氏菌的研究〔J〕.云南预防医学杂志,2012,17(2):28-31.
(责任编辑 李杨)
Comparison of Three Methods of Listeria monocytogenes Detection
ZHANG Xuanrong,YAN Jun,LI Wenlong,HOU Min,JIANG Yujia,BU Shu,LI Guiman
(Disease Control and Prevention Center of Kunming,Kunming 650228,China)
Objective:To find a suitable method for rapid detection of Listeria monocytogenes(LM)in grassroots labs.Methods: GB law,real-time PCR and LAMP were adopted to detect LM,then,the results were evaluated.Results:The results of the three mothods were quite consistent.The detection process of GB law took 5 to 7 days.While the real-time PCR requiring high experimental conditions and cost took 2.5 days.LAMP method,requiring low experimental conditions and cost,took the same time as the real-time PCR.Conclusion:The LAMP assay was a sensitive,specific,rapid and economical method for the detection of LM, which could be widely used by grassroots labs.
GB law;LAMP;PCR;detection of Listeria monocytogenes
R155.5
A
1672-2345(2013)06-0038-05
10.3969/j.issn.1672-2345.2013.06.011
2012-09-16
2012-10-16
张烜榕,初级检验师,主要从事病原生物检验研究.
