清开灵注射剂致82例不良反应/不良事件文献分析
2013-03-17李曼王忠荆志伟
李曼王忠荆志伟
(1沈阳药科大学工商管理学院,辽宁沈阳110016;2中国中医科学院,北京100700)
清开灵注射剂致82例不良反应/不良事件文献分析
李曼1王忠2荆志伟2
(1沈阳药科大学工商管理学院,辽宁沈阳110016;2中国中医科学院,北京100700)
目的:搜集清开灵注射剂临床使用中的药品不良反应/事件(ADR/ADE)文献报道,分析导致ADR/ADE的风险因素,为临床安全用药提供依据。方法:检索中国期刊全文数据库(CNKI)(1979-2010)、万方数据库(1982-2010),以“清开灵and(注射液or注射剂or粉针剂or冻干粉)and(不良反应or不良事件or病例报告)”为检索式,共收录来自35种期刊的82篇文献。结果:清开灵注射剂ADR/ADE可累及多个器官和系统,以过敏性休克导致的呼吸系统损害最为常见,其次是皮肤及其附件损害和全身性损害;以速发型为主,兼有迟发型,严重者可致死亡。结论:应加强清开灵注射剂的ADR/ADE监测,促进临床合理用药。
清开灵注射剂;不良反应;不良事件;文献分析
清开灵注射剂是由牛黄、水牛角、珍珠母、黄芩、金银花、栀子、板蓝根等提取物制备的中药制剂,有清热解毒、化痰通络、醒神开窍的功效。主要用于热病神昏、中风偏瘫、神志不清,亦可用于急、慢性肝炎,上呼吸道感染,肺炎,高热以及脑血栓形成、脑出血见上述证候者。
1992年12月,国家中医药管理局将清开灵注射液列入《全国中医医院急诊科(室)首批必备中成药目录》[1],广泛应用于临床。2001年,国家药品不良反应(ADR)监测中心首次通报了清开灵注射液引起的过敏反应,其ADR/药品不良事件(ADE)开始受到人们的广泛关注。2009年国家ADR监测中心再次对清开灵注射液ADR/ADE进行报道,其安全性问题引起更加广泛的关注。本研究对文献报道的清开灵注射剂ADR/ADE进行分析,旨在为清开灵注射剂的安全应用提供参考。
1 数据来源及检索条件
以“清开灵 and(注射液 or注射剂 or粉针剂or冻干粉)and(不良反应 or不良事件 or病例报告)”为检索式,在中国期刊全文数据库(CNKI)(1979-2010)及万方数据库(1982-2010)中检索,共检索到358篇相关文献。
2 排除标准
2.1 文献筛选结果
共有来自35种期刊的82例清开灵注射剂ADR/ADE详细病案入选。
2.2 数据整理
2.2.1 确定研究变量 具体字段信息见表1。

表1 变量采集
2.2.2 数据采集 通读文献,在文献中标注需要采集的信息;然后根据采集的患者信息及用药信息对照原始文献,判断ADR/ADE的严重程度、是否有中医证候信息、用法是否正确;采用EpiData软件进行双份录入,经逻辑检验后导入SPSS软件进行统计分析。
2.3 统计方法
采用SPSS 18.0软件进行数据处理,计量资料的描述采用±s,计数资料的描述如采样率、构成比及次序,采用χ2检验对计数数据进行组间差异性分析。
2.4 统计结果
2.4.1 ADR/ADE个案报道发表情况 见图1。

图1 ADR/ADE个案报道发表年限分布
从图1可以看出2000-2002年个案报道数量呈上升趋势,但是由于国家ADR监测中心2001年发布的第1期《药品不良反应信息通报》涉及到清开灵注射液过敏反应的问题,通报公布后受到医疗机构的重视,其后ADR/ADE报告数量有一定下降。个案报道在2006年出现了一个高峰,其他年份略有起伏,总体差异不大。由于纳入的文献量较少,该图仅描述本研究清开灵注射液ADR/ADE报告的年限分布情况。
2.4.2 患者性别、年龄分布 82例患者中男46例,女36例;最小22个月,最大82岁,平均年龄为(33.38±21.48)岁,见表2。其中30~岁组所占比例最大(20.73%)。男女患者的年龄分布差异无统计学意义(P=0.747)。

表2 82例患者年龄分布
2.4.3 过敏史 82例中仅有26例对患者过敏史进行了描述,其余过敏史不详,见表3。其中有2例有过敏史者分别对花草过敏和对阿司匹林、甲硝唑过敏。

表3 82例患者过敏史描述情况
2.4.4 合并用药 82例中合并用药记载不详者6例(7.32%);54例患者没有合并用药记录(65.85%);22例记载有合并用药信息(26.82%)。合并1种其他药物7例,合并2种其他药物8例,合并3种以上其他药物7例。其中合并使用抗生素者14例,占合并用药患者的63.64%。合并用药排在前10位的药物见表4。其中1例对阿司匹林、甲硝唑过敏的患者,合并使用病毒唑。
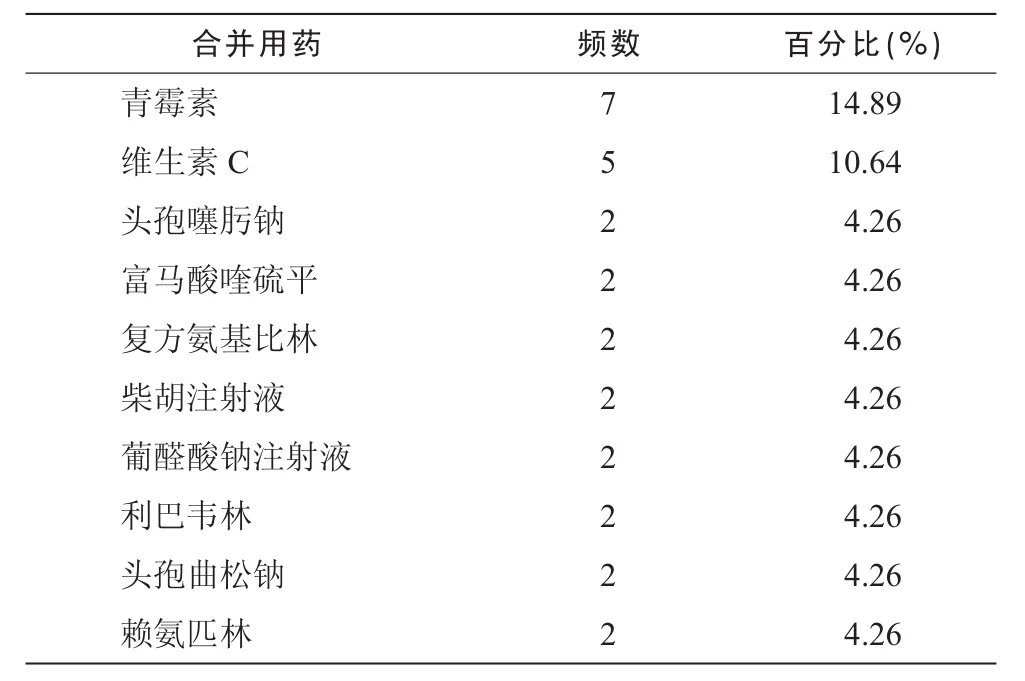
表4 清开灵注射剂合并用药前10位
2.4.5 ADR/ADE发生时间 82例报告中有63例(76.83%)记录了患者从用药到发生ADR/ADE的时间。其中,有52例(82.54%)患者的ADR/ADE发生于用药后30 min内,57例 (90.48%)发生在1 h内,60例(95.24%)发生在用药后2 h内。需要说明的是有2例患者的ADR/ADE分别发生在用药后的第3和7 d。63例ADR/ADE发生时间分布见图2。

图2 63例ADR/ADE发生时间分布
2.4.6 ADR/ADE严重程度 ADR/ADE严重程度分为3类(一般ADR/ADE、严重ADR/ADE、死亡)。82例患者中发生一般ADR/ADE者67例(81.71%);严重ADR/ADE者10例(12.19%);5例死亡。合并用药组ADR/ADE严重程度构成与无合并用药组无显著差别(P=0.706)。
82例中只有26例对过敏史进行了描述,严重ADR/ADE组和死亡组分别只有1例,例数未达到统计分析的要求,根据需要将ADR/ADE类型合并为2组,即ADR/ADE组与死亡组,进行统计分析,合并结果见表6,有过敏史组ADR/ADE严重程度与无过敏史组差别无统计学意义(P=0.768)。

表5 清开灵注射剂ADR/ADE类型与合并用药的关系

表6 清开灵注射剂ADR/ADE类型与过敏史的关系
2.4.7 药物剂量与滴速 82例ADR/ADE报告中77例使用清开灵注射液,其余5例剂型不详。82例患者中最小用量1 mL,最大用量达到60 mL,平均剂量为25.62 mL。由于缺乏患者的体重信息,无法判断患者的药物浓度是否恰当。
82例患者中,仅有 22例患者有详细的滴速信息,平均滴速(48.50±15.38)滴/min。有5例儿童患者(年龄≤12 a),平均滴速为(48.00±30.33)滴/min,其余17例患者平均滴速(48.65± 8.97)滴/min。清开灵注射液药品说明书中规定儿童滴速在20~40滴/min,成人滴速正常与否与ADR/ADE构成情况见表7,滴速正常组的ADR/ADE类型构成与滴速不正常组的ADR/ADE类型构成差异无统计学意义(P=0.421)。
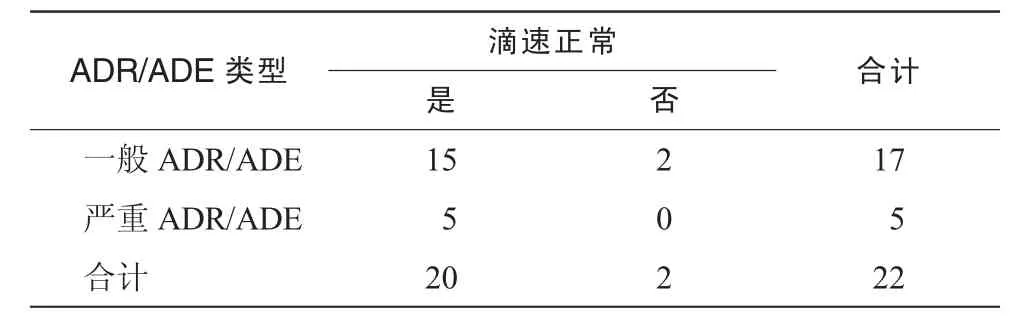
表7 滴速正常与否与ADR/ADE构成情况
2.4.8 ADR/ADE临床表现及累及系统器官分类82例患者涉及98种ADR/ADE症状,出现最多的是 “胸闷”(28.05%),ADR/ADE临床表现排前10位者见表8,按累及系统器官分类,居前3位的分别是呼吸系统损害,皮肤及其附件损害及全身性损害。
3 讨论
3.1 ADR/ADE的特点及类型分析
3.1.1 ADR/ADE出现时间 由图2可知,清开灵注射剂引起的ADR/ADE以速发型为主,兼具迟发型。因而在使用清开灵注射剂的30 min内,医护人员应加强对患者的观察[2]。
3.1.2 ADR/ADE类型描述 清开灵注射剂ADR/ ADE以过敏性休克导致的呼吸系统损害最多,其次是皮肤及其附件损害和全身性损害。呼吸系统损害按照其损害程度不同有以下几种表现,胸闷、皮疹、呼吸困难、面色苍白、瘙痒、汗出、心悸、口唇发绀、烦躁、面色潮红、气促等症状组成,也可作为引起的过敏性休克的表现,在输液的前期(30 min内)对以上症状进行密切观察。皮肤及其附件系统损害排名第二,主要表现为皮疹、皮肤瘙痒。此外还可引起呼吸困难、心悸等循环系统损害及头晕、头疼等血管神经系统损害。
3.2 清开灵注射剂使用中的不合理因素分析
3.2.1 合并用药与ADR/ADE[2-10]82例患者中有14例合并使用抗生素,另外说明书明确标明清开灵注射剂不能与青霉素配伍,仍有7例患者合并使用青霉素,且青霉素的合并使用居所有合并用药的首位。在82例患者中有65.85%的患者ADR/ ADE报告中对有无合并用药未进行描述。建议清开灵注射剂与抗生素合用时,注意间隔用药[3]。
3.2.2 滴速与 ADE[2-10]82例患者中有2名儿童的滴速达到80滴/min,比说明书中规定的成人最高滴速还要高。滴速过高导致的患者产生ADE值得医护人员的高度关注,在注射液的使用过程中要尽量避免由滴速过快而导致的药害事件。
3.2.3 剂量使用与ADE[2-10]82例患者中有2例用量为50 mL,3例用量达60 mL,都超出了说明书规定的对于重症患者每日滴注20~40 mL的剂量,其中1例死亡,尽管不能说明过量使用与清开灵注射剂ADE严重程度有直接的关系,提示临床应按照说明书的规定用量谨慎使用,以防因使用不当而导致ADE的发生。
82例患者中有21例患者存在不合理用药的情况,使用中存在药物配伍禁忌、滴速过快、过量使用等情况。56例患者无过敏史的记录,报告中对相当一部分患者的滴速、用药量、合并用药情况、年龄及出现ADR/ADE的时间都未进行描述。提示文献报道要求低,未进行报道质量控制,医务人员对说明书掌握程度不够,未按照说明书的适应证、禁忌证、注意事项等规定进行操作,这些都为ADE埋下隐患。提示医务工作者及相关从业人员要加强对药品说明书的学习,避免因用药不当而导致的ADE的发生。
3.3 本研究的不足
本研究旨在为临床使用提供参考,为企业开展临床安全性集中监测提供指导,但由于纳入病例只来源于医学期刊检索的部分文献,不包括各级ADR监测中心的ADR报告;源文献未对患者过敏史、清开灵注射剂使用时的滴速等信息详细描述,ADR报告质量有待提高,对本研究结果造成一定程度的影响,有待进一步探讨。
[1] 国家中医药管理局医政司.全国中医医院急诊科(室)首批必备中成药应用指南[M].北京:中国医药出版社,1993:28-37.
[2] 郝园,孔翔瑜,吴泰相.277篇1486例清开灵注射液不良反应 /不良事件系统评价[J].中国循证医学杂志,2010,10(2):162-175.
[3] 唐春燕,曾立威,董静,等.301例清开灵注射液不良反应/事件分析[J].中国药物警戒杂志,2009,8(6):478-481.
[4] 史霞.罕见的清开灵不良反应1例报告[J].职业与健康杂志,2007,23(16):1469.
[5] 陈萍.静滴清开灵引起变态反应 1例[J].中国当代医药杂志,2010,17(30):125.
[6] 施振国,尹红.55例清开灵注射液不良反应文献分析[J].中国药物应用与监测杂志,2009,6(6):361-363.
[7] 贾歆.清开灵的不良反应[J].中国误诊学杂志,2005,5(10):1986-1987.
[8] 周春玲,钟宪澎.静脉滴注清开灵注射液致迟发性过敏反应2例报告[J].吉林医学杂志,2006,27(5):558.
[9] 邱建永.1例清开灵注射液药物不良反应分析及文献复习[J].国际医药卫生导报,2009,12(12):72.
[10] 郭颖.静滴清开灵致面部皮丘疹 1例[J].中国煤炭工业医学杂志,2007,10(11):1325.
Literature Analysis of 82 Cases of Adverse Reactions/Events Caused by Qingkailing Injection
Li Man1,Wang Zhong2,Jing Zhiwei2
(1 School of Business Administration of Shenyang Pharmaceutical University,Liaoning Shenyang 110016,China;2 China Academy of Chinese Medical Sciences,Beijing 100700)
Objective:To investigate the situation of adverse drug reactions/events(ADRs/ADEs)in the clinical application of qingkailing injection and analyze the risk factors leading to the ADRs/ADEs so as to provide a reference for the safety of clinical medication.Methods:About 82 literatures of 35 journals were retrieved from CNKI(1979-2010)and Wanfang Database(1982-2010)by taking “qingkailing and (injection or powder-injection or freeze-dried powder)and(adverse reaction or adverse event or case-reporting)”as the retrieval strategy.Results:The adverse drug reactions/events caused by qingkailing injection may implicate multiple organ systems.Respiratory damage caused by anaphylactic shock was the most common,followed by the skin and its appendages and systemic damages,mainly occurred as the rapid reaction and sometime as the late onset and severe cases can cause death.Conclusion:The monitoring of ADRs/ADEs caused by qingkailing injection should be strengthened so as to promote the rational drug use.
Qingkailing Injection;Adverse Reaction;Adverse Event;Literature Analysis
10.3969/j.issn.1672-5433.2013.03.001
2012-04-13)
国家自然科学基金(81001596)
李曼,女,硕士。研究方向:药品监管。E-mail:limanyida1986@163.com
荆志伟,男,博士,副研究员。研究方向:中药安全性评价方法学。通讯作者E-mail:jzwgll@sina.com
