H PLC测定大鼠血浆中缬沙坦浓度及其药代动力学研究
2013-03-17许金红宋建国李永霞
许金红宋建国李永霞
(1中国人民解放军海军安庆医院药剂科,安徽安庆246003;2皖南医学院药理教研室,安徽芜湖241002)
H PLC测定大鼠血浆中缬沙坦浓度及其药代动力学研究
许金红1宋建国2李永霞1
(1中国人民解放军海军安庆医院药剂科,安徽安庆246003;2皖南医学院药理教研室,安徽芜湖241002)
目的:建立高效液相色谱法(HPLC)测定大鼠血浆中缬沙坦浓度的方法,并考察其药代动力学特征,为临床合理用药提供参考。方法:12只SD雄性大鼠随机分成2组,于8:00及20:00分别灌胃给予缬沙坦(16 mg/kg),于给药前及给药后0.33、0.67、1、2、4、8、12及24 h眼内眦静脉取血,HPLC紫外法测定大鼠血浆缬沙坦浓度。结果:缬沙坦在大鼠体内浓度(C)-时间(t)曲线呈一室模型,给药后2 h达血药峰值,8:00用药t1/2(6.45±1.74)h。20:00用药的Cmax显著下降(P<0.05),平均驻留时间(MRT)及t1/2延长(P<0.05或P<0.01)。结论:本方法测定血浆中缬沙坦浓度准确、简便,适用于缬沙坦药代动力学研究。大鼠8:00用药,血药浓度较高,而t1/2较短;20:00用药,血药浓度偏低,t1/2延长。缬沙坦昼夜不同时间用药对其药代动力学有一定影响。
高效液相色谱法;缬沙坦;血药浓度;昼夜节律;药代动力学;实验研究
缬沙坦可用于各种类型高血压,对心脑肾有较好的保护作用,并可选择性阻断AT1受体,而基本不影响AT2受体介导的血管扩张及细胞修复、凋亡作用[1-2]。本品降压具有强效、平稳、长效的特点,降压谷/峰比(T/P)值高,服药后可24 h持续降压且对清晨血压降低作用优于他药[3-4]。本品以原形经胆汁(约70%)及尿液排泄(约30%),肝、肾功能无严重障碍者用药不受限制。参考相关文献资料[5-7],本研究建立了简单准确的高效液相色谱法(HPLC)测定缬沙坦血药浓度,可用于缬沙坦药代动力学(药动学)研究,为临床合理用药提供参考。
1 材料
1.1 仪器
Waters高效液相色谱仪(515泵、717plus自动进样器、474FLD荧光检测器、996PDAD检测器、柱温箱、Breeze色谱工作站),美国 Waters公司;XW-80A旋涡混合器,上海精科实业有限公司;TGL-16G高速离心机,上海安亭科学仪器厂;DL系列溶剂过滤器,天津市东康科技有限公司;DN系列氮吹干仪,天津市东康科技有限公司;IKA-Werke TypVX2E型摇床,德国仪科公司;TG-322A微量分析天平,上海精密科学仪器有限公司;Sartorius BS124S型电子天平,德国赛多利斯公司;PHS-2F型酸度计,上海精科实业有限公司。
1.2 实验药品与试剂
1.2.1 标准品 缬沙坦(原中国药品生物制品检定所,批号 100651-200902,含量> 98%);厄贝沙坦(原中国药品生物制品检定所,批号 100607-200301,含量>98%)。
1.2.2 药物 缬沙坦胶囊(80 mg/粒,北京诺华制药有限公司,批号X1076)。
1.2.3 化学试剂 甲醇(色谱纯,Merck公司);乙腈(色谱纯,Merck公司);磷酸(分析纯,无锡市亚盛化工有限公司);三乙胺(分析纯,上海精化科技研究所)。
2 实验动物
SPF级SD大鼠,体质量180~220 g,雄性,购自上海市西普尔-必凯实验动物有限公司,合格证:2008001612491。动物置于明、暗周期下饲养(明暗各12 h,明期08:00-20:00),维持室温20~25℃,相对湿度(60±10)%,自由进食、进水。给药前禁食12 h,禁水2 h。
3 方法
3.1 色谱条件
色谱柱:Phecda C18(250 mm×4.6 mm,5μm)。流动相:取3.5 mL三乙胺,加水稀释至500 mL,磷酸调pH至(3.0±0.1)。取上述溶液500 mL,加乙腈350 mL,甲醇150 mL,0.22 μm尼龙滤膜过滤,超声脱气。流速1.4 mL/min,柱温30℃,检测波长237 nm。
3.2 溶液配制
3.2.1 缬沙坦标准溶液配制 精密称取缬沙坦10 mg,置100 mL量瓶中,加入适量甲醇溶解并稀释至刻度,得100 μg/mL标准液。精密吸取标准液适量,用甲醇稀释定容,配制成浓度为100、50、20、10、5、2、1、0.5 μg/mL的标准溶液,-70℃冰箱贮存备用。
3.2.2 内标溶液配制 精密称取厄贝沙坦10 mg,置10 mL量瓶中,加入适量甲醇溶解并稀释至刻度,得1 000 μg/mL的内标液,4℃避光保存备用。取上述内标液1 mL,置10 mL量瓶中,加入适量甲醇溶解并稀释至刻度,得100 μg/mL内标溶液。
3.3 给药方案及血浆样本采集
SD大鼠12只,随机分为2组,每组6只,分别于8:00和20:00灌胃给予缬沙坦。以0.5%羧甲基纤维素钠(CMC-Na)配成含缬沙坦1.6 mg/mL混悬液,给药体积10 mL/kg。于给药前及给药后0.33、0.67、1、2、4、8、12、24 h由眼内眦静脉采血0.5 mL,置1.5 mL抗凝离心管中,12 000 r/min离心 10 min,取上层血浆,-70℃冰箱保存备用,HPLC测定血浆缬沙坦浓度。
3.4 血浆样本处理
精密吸取内标溶液40 μL,置2 mL离心管中,氮气吹干。加入血浆(空白或含药血浆)200 μL,乙腈600 μL,振荡3 min,12 000 r/min离心10 min。取上清液200 μL,12 000 r/min离心10 min,取上清液30 μL进样分析。
3.5 统计方法
采用Drug And Statistics of Windows 2.1(DAS2.1)软件一室开放模型及统计矩法分析药动学特征并求算参数;采用SPSS Statistics17.0软件进行统计分析。计量资料数据用±s表示,组间均数比较采用t检验进行显著性检验,P<0.05为有统计学差异。
4 结果
4.1 专属性
取 6份不同来源大鼠血浆,按 3.4项下方法处理,所得色谱图(图1)显示缬沙坦保留时间约17.87 min,内标保留时间约13.03 min。缬沙坦与内标分离完全,峰形良好,血浆内源性物质不干扰测定。证明方法专属性高,测得结果为缬沙坦实际浓度。

图1 缬沙坦血浆浓度的HPLC图A:空白血浆;B:缬沙坦及内标血浆;C:缬沙坦用药血浆
4.2 标准曲线
精密吸取不同浓度的缬沙坦标准溶液,加入内标和空白血浆,配制成 80、40、16、8、4、1.6、0.8和0.4 μg/mL的血浆标准溶液,按3.4项下方法操作,进行色谱分析。以缬沙坦对照品峰面积与内标峰面积比(Y)对浓度(C,μg/mL)作线性计算,得方程

线性范围0.4~80 μg/mL。血浆缬沙坦最低定量限为0.5 μg/mL。
4.3 回收率
取浓度为0.8、8和40 μg/mL的缬沙坦标准溶液加入空白血浆中,制成浓度为0.8、8和40 μg/mL的标准缬沙坦含药血浆溶液,每浓度各5份,按3.4项下方法操作,取30 μL进样分析。分别记录血浆样本及标准溶液的缬沙坦色谱峰面积A1及A2,以A1/A2×100%计算回收率为(70.29±5.09)%、(75.90±1.60)%及(68.13±2.12)%,见表1。

表1 血浆缬沙坦提取回收率(n=5)
4.4 精密度与准确度
配制低、中、高三个浓度为0.8、8和40 μg/mL的缬沙坦含药血浆并绘制相应随行曲线,每批每浓度各5份及1条随行曲线,3.4项下方法操作后进行色谱分析,考察缬沙坦的日内、日间精密度和方法回收率(表2)。
表2 血浆缬沙坦测定的精密度与准确度(±s,n=5)
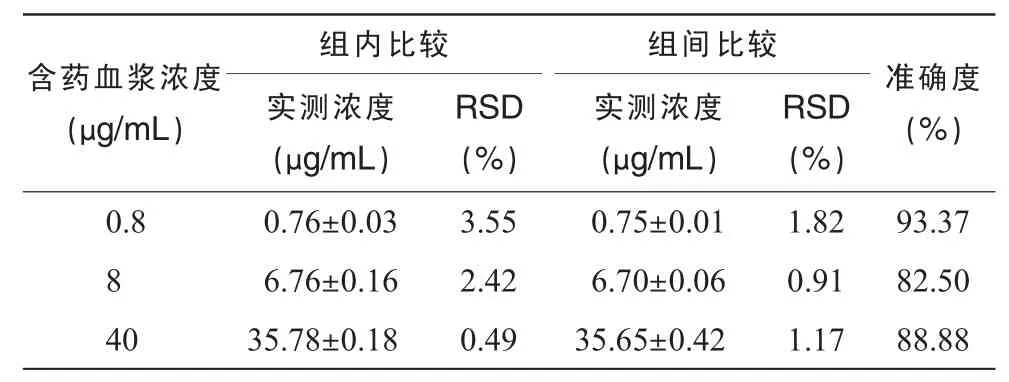
表2 血浆缬沙坦测定的精密度与准确度(±s,n=5)
组内比较 组间比较含药血浆浓度(μg/mL)RSD(%)0.8 0.76±0.03 0.75±0.01 1.82 93.37 8 6.76±0.16 6.70±0.06 0.91 82.50 40 35.78±0.18 35.65±0.42 1.17 88.88实测浓度(μg/mL)RSD(%)3.55 2.42 0.49实测浓度(μg/mL)准确度(%)
4.5 定量下限
取缬沙坦浓度为 0.4 μg/mL的空白血浆(缬沙坦含药血浆),平行5份测定,由随行曲线求算缬沙坦浓度为(0.32±0.01)μg/mL,见表3。

表3 血浆缬沙坦定量下限(n=5)
4.6 稳定性
取0.8、8和40 μg/mL的缬沙坦含药血浆,分别置室温12 h、进样器内8 h,-70℃冰箱冻融3次,各条件同一浓度平行处理3份测定,由随行曲线测得准确度为80.9%~95.3%,说明样本稳定,符合生物样本分析要求(表4)。
表4 血浆缬沙坦稳定性(±s,n=5)
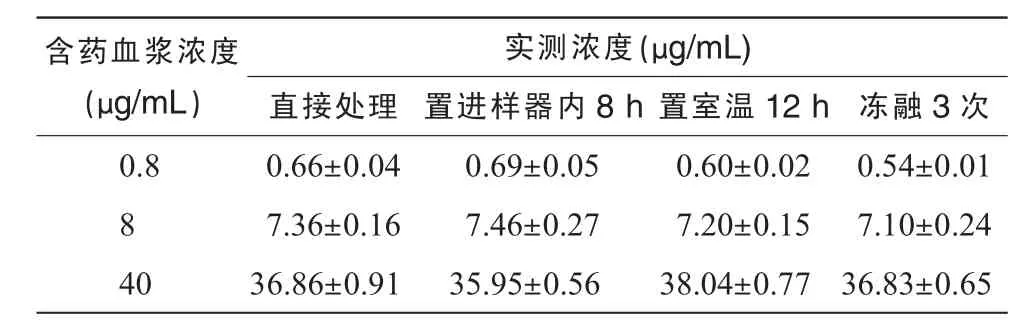
表4 血浆缬沙坦稳定性(±s,n=5)
含药血浆浓度(μg/mL)实测浓度(μg/mL)直接处理 置进样器内8 h置室温12 h 冻融3次0.8 0.66±0.04 0.69±0.05 0.60±0.02 0.54±0.01 8 7.36±0.16 7.46±0.27 7.20±0.15 7.10±0.24 40 36.86±0.91 35.95±0.56 38.04±0.77 36.83±0.65
4.7 药动学研究
昼(8:00)、夜(20:00)不同时间,单剂量灌胃给予缬沙坦(16 mg/kg)后,缬沙坦在大鼠体内血药浓度有较大差异(P<0.05),见图2、表5。提示用药时间不同对缬沙坦在大鼠体内的药动学有一定影响。白昼用药的 Cmax显著升高(P< 0.05)但药物-时间曲线下面积(AUC)差异无显著统计学意义(图2)。
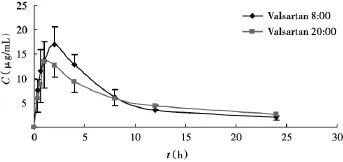
图2 用药时间对缬沙坦浓度(C)-时间(t)曲线影响(±s,n=6)
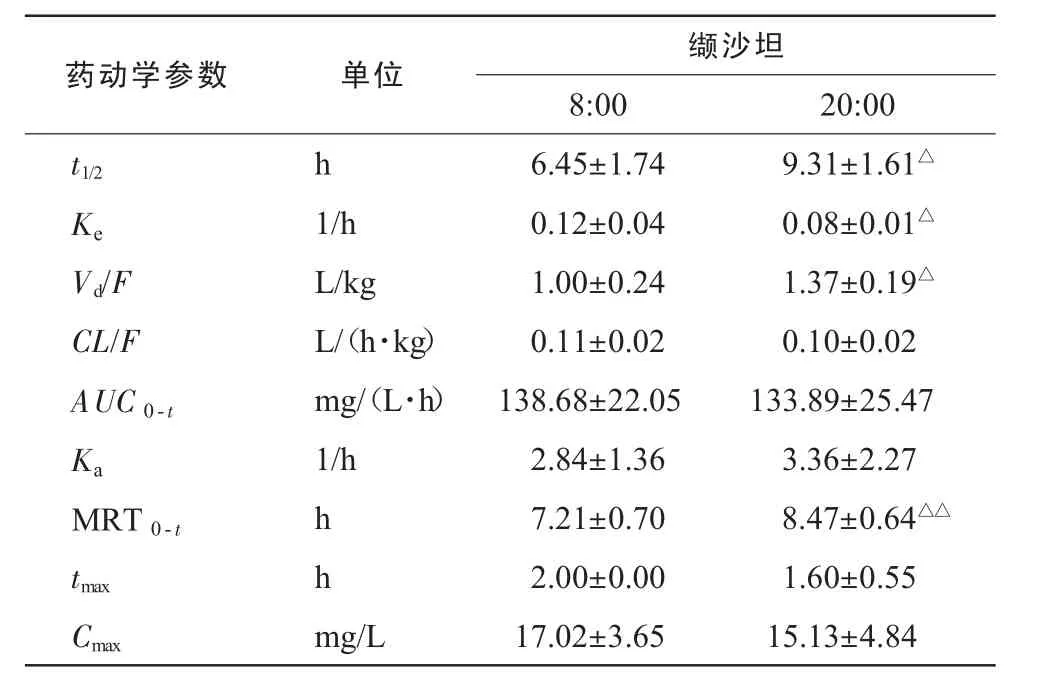
表5 缬沙坦在大鼠体内的药动学参数(x±s,n=6)
各组动物的药动学主要参数见表5。结果表明,用药时间不同,对缬沙坦的药动学也有很大影响。20:00用药较8:00用药使得缬沙坦平均滞留时间(MRT)及 t1/2延长(P< 0.05或 P< 0.01),而表观分布容积(Vd)显著增大(P<0.05)。
5 讨论
5.1 血药浓度测定方法
本研究采用文献[8-9]报道的 HPLC紫外分析法,检测缬沙坦血药浓度,并对该方法作了一定优化改进。预实验证实,流动相取乙腈与甲醇比例为7∶3时,样本和内标的保留时间更为适宜,检测波长定为237 nm,可获得良好的吸收峰。血浆样本预处理中的蛋白沉淀,一般采用加入高氯酸、三氟乙酸等方法。鉴于此类物质具强氧化性,可能会导致缬沙坦和内标氧化破坏,且强酸性可能损伤色谱柱。本研究在比较多种蛋白沉淀方法后证实,以加入3倍体积乙腈的方法,蛋白沉淀最为完全,提取回收率高,重现性好,血浆中杂质不干扰药物测定。表明该方法符合生物样本的分析要求,可以用于血浆缬沙坦浓度测定及临床药动学研究。
5.2 择时用药对缬沙坦药动学的影响
缬沙坦单剂量(16 mg/kg)灌胃给药,大鼠体内C-t曲线呈一室模型。以8:00用药组为例,用药后约 2 h Cmax达(17.02± 3.65)mg/L,t1/2(6.45± 1.74)h,结果与文献[10]报告值相似。昼夜不同时间用药,尚可影响缬沙坦的其他药动学参数。20:00用药组可使缬沙坦t1/2及MRT显著延长 (P<0.05或P<0.01)。已知缬沙坦主要以原形经胆汁及尿液排泄[11],时间生物学研究证实,人及大鼠肾排泄功能呈昼夜波动,在活动期肾功能较高,尿量较多[12-13],大鼠为夜行性动物,夜间肾功能高于白昼,且大鼠于夜间的摄食、饮水量约占全天摄入量的80%以上[14]。大鼠肾功能、尿量及胆汁分泌的昼夜差异可能是引起缬沙坦排泄昼夜差异的主要原因。对8:00用药组,在进行血药浓度监测的24 h内,前半段为动物休息期,此时血浆蛋白水平较低、药物排泄较慢,因此血药浓度较高;而后半段消除相为动物活动期,此时血浆蛋白水平较高,药物排泄较快,t1/2较短。20:00用药组情况则恰好相反,呈血药浓度较低,t1/2较长的趋势。结果表明昼夜不同时间用药对大鼠缬沙坦药动学有一定影响,本研究为临床择时使用缬沙坦提供参考,临床应选择何时用药尚需进一步研究。
[1] 黎春辉.抗高血压药物治疗中不合理用药案例分析[J].中国执业药师,2010,7(1):6-8.
[2] 杨赴云.ACEI和ARB治疗原发性高血压的疗效比较[J].中国执业药师,2009,6(6):42-44.
[3] Nishimura T,Hashimoto J,Ohkubo T,et al.Efficacy and duration of action of the four selective angiotensinⅡ subtype 1 receptor blockers,losartan,candesartan,valsartan and telmisartan,in patients with essential hypertension determined by home blood pressure measurements[J].Clin Exp Hypertens,2005,27(6):477-489.
[4] 刘晓云,宋建国.抗高血压单片复方制剂缬沙坦/氨氯地平临床药理学研究进展[J].中国执业药师,2011,8(1):31-36.
[5] 何宝时.缬沙坦在人体的药物动力学分析[J].中国现代药物应用,2010,4(11):149-150.
[6] Kaneshiro Y,Ichihara A,Sakoda M,et al.Add-on benefits of amLodipine and thiazide in nondiabetic chronic kidney disease stage1/2patientstreatedwithvalsartan[J].KidneyBloodPressRes,2009,32(1):51-58.
[7] 霍强,杨敏,吴华璞,等.缬沙坦分散片人体生物等效性研究[J].蚌埠医学院学报,2008,33(3):347-349.
[8] 李扬,陈今扬,王德志,等.高效液相色谱法测定人血浆中缬沙坦、氢氯噻嗪浓度[J].中国新药杂志,2005,14(11):1335-1338.
[9] 国家药典委员会.中华人民共和国药典(2005版)二部[M].北京:化学工业出版社,2005:附录152-156.
[10] Asmar R,Gosse P,Queré S,et al.Efficacy of morning and evening dosing of amlodipine/valsartan combination in hypertensive patients uncontrolled by 5 mg of amlodipine[J].Blood Presse Monit,2011,16(2):80-86.
[11] 许金红,刘晓云,宋建国.高血压的时间治疗用药方案[J].实用药物与临床,2012,15(1):54-56.
[12] 周天禄.生理机能的时间节律.时间药理学与时间治疗学[M].天津:天津科学技术出版社,1994:48.
[13] 赵玉玲,戴伦,李国臣,等.抑制血压晨峰的方法[J].中华高血压杂志,2009(2):104-106.
[14] Ofili EO,Oparil S,Giles T,et al.Moderate versus intensive treatment of hypertension using amlodipine/valsartan and with the addition of hydrochlorothiazide for patients uncontrolled on angiotensin receptor blocker monotherapy:results in racial/ethnic subgroups[J].J Am Soc Hypertens,2011,5(4):249-258.
Concentration Determination of Valsartan in Rat Plasma by HPLC and its Pharmacokinetics Study
Xu Jinhong1,Song Jianguo2,Li Yongxia1
(1 Pharmacy Department of the PLA Navy Anqing Hospital,Anhui Anqing 246003,China;2 Department of Pharmacology of Wannan Medical College,Anhui Wuhu 241002)
Objective:To establish an method for the determination of the concentration of valsartan in rats plasma by HPLC and to study its pharmacokinetics so as to provide useful information for clinical practice.Methods:Twelve male SD rats were divided into two groups randomly,and a single dose of valsartan (16 mg/kg)was administered intragastrically at either 8:00 or 20:00 respectively.Plasma samples were collected at 0,0.33,0.67,1,2,4,8,12 and 24 h after the drug administration.A HPLC with UV detection method was developed to determine the concentration of valsartan in rats plasma.Results:The results showed that valsartan plasma concentration-time(C-t)curves in rats were fitted by one-compartment model with tmax=2 h and t1/2=(6.45±1.74)h(dosing at 8:00).There were lower Cmax(P<0.05),longer t1/2(P<0.05)and mean retention time (MRT) (P<0.01)in rats when administrated at 20:00 compared with those of dosing at 8:00. Conclusion:This method is simple with high sensitivity and good precision and is proved to be suitable for the pharmacokinetic study of valsartan.The blood concentration of valsartan was higher and t1/2was shorter when dosing at 8:00 than those at 20:00.The administration of valsartan at different times of a day showed a certain effect on the pharmacokinetics of valsartan.
HPLC;Valsartan;Blood Concentration;Circadian Rhythm;Pharmacokinetics;Experimental Research
10.3969/j.issn.1672-5433.2013.03.005
2012-08-16)
许金红,女,硕士,药师。研究方向:临床药学和定量药理学。E-mail:xujinhon_2006@126.com
宋建国,男,博士,硕士生导师。研究方向:定量药理学和时间药理学。通讯作者E-mail:sjg68755356@163.com
