14种中成药微生物限度检查方法研究
2013-03-17黄英
黄英
(丽江市食品药品检验所,云南丽江674100)
14种中成药微生物限度检查方法研究
黄英
(丽江市食品药品检验所,云南丽江674100)
目的:建立14种中成药的微生物限度检查方法。方法:按照《中国药典》(2010年版)微生物限度检查法的规定,采用常规法、培养基稀释法及薄膜过滤法对各品种细菌、霉菌和酵母菌数进行回收率测定,通过回收率试验测定药物的抑菌性;采用直接接种法对各品种控制菌进行测定。结果:6种供试品(抗宫炎片、克咳胶囊、保济丸、夏桑菊颗粒、妇炎康复胶囊、小儿咽扁颗粒)无抑菌作用,细菌回收率均大于70%,可采用常规法对细菌数测定;4种供试品(藿香清胃片、护肝宁片、橘红丸、黄芩片)对细菌抑菌作用较强,可采用培养基稀释法(0.2 mL/皿)进行细菌数测定;4种供试品(清热解毒片、鼻渊丸、冠心丹参胶囊、清喉利咽颗粒)对金黄色葡萄球菌和枯草芽孢杆菌有很强的抑菌作用,需采用薄膜过滤法测定细菌数;上述各品种的霉菌和酵母菌及各种必检控制菌均可采用常规法检查。结论:经验证的微生物限度检查方法适用于以上中成药的微生物限度检查,可有效控制其质量。
中成药;微生物限度检查;方法验证
中成药虽不像抗生素有明显的抗菌谱,但对不同菌种其抑菌作用不同。为保证微生物限度检查法的准确性,根据《中国药典》(2010年版)一部附录的规定,在进行药品的微生物限度检查时,必须采用方法学验证试验说明方法的有效性[1]。现行《中国药典》收载的各中成药品种检查项下,很少规定具体的微生物限度检查方法,为确保用药的安全与有效,本研究按《中国药典》(2010年版)、《中国药品检验标准操作规范》[2]、《药品微生物学检验技术》[3]及有关文献[4-11],探索并建立藿香清胃片等14种中成药的微生物限度检查方法。
1 仪器与材料
1.1 仪器
HTY-2000(A)型集菌仪,杭州高得医疗器械有限公司;GSP-9270MBE隔水式电热恒温培养箱,上海博讯实业有限公司医疗设备厂;SPX-150生化培养箱,上海金慧科电子有限公司;LDZM-6KCS立式压力蒸汽灭菌器,上海申安医疗器械厂。
1.2 菌种
枯草芽孢杆菌[CMCC(B)63501]、金黄色葡萄球菌[CMCC(B)26003]、大肠埃希菌[CMCC(B)44102]、白色念珠菌[CMCC(F)98001]、黑曲霉[CMCC(F)98003]均由云南省食品药品检验所提供。
1.3 培养基
营养琼脂(批号 101104)、玫瑰红钠琼脂(批号 1102232)、营养肉汤(批号 101124)、改良马丁琼脂(批号 101104)、麦康凯琼脂(批号 101018)、胆盐乳糖(批号 1012012)、乳糖胆盐发酵培养基(批号080214)均为北京三药科技开发公司产品。按规定进行的适用性检查结果合格。稀释剂为pH7.0无菌氯化钠-蛋白胨缓冲液。
1.4 样品
藿香清胃片(吉林省俊宏药业有限公司,薄膜衣0.31 g/片);护肝宁片(通化斯威药业股份有限公司,0.3 g/片);橘红丸(云南腾药制药股份有限公司,6 g/丸);黄芩片(葵花药业集团(佳木斯)有限公司,0.26 g/片);清热解毒片(陕西盘龙制药集团有限公司,糖衣片);鼻渊丸(李时珍医药集团有限公司,每10粒重2 g);冠心丹参胶囊(长春远大国奥制药有限公司,0.3 g/粒);清喉利咽颗粒(桂龙药业(安徽)有限公司,5 g/袋);抗宫炎片(江西天施康中药股份有限公司,0.25 g/片);克咳胶囊(贵州益佰制药股份有限公司,0.3 g/粒);保济丸(广州王老吉药业股份有限公司,3.7 g/粒);夏桑菊颗粒(四川蜀中制药有限公司,10 g/袋);妇炎康复胶囊(江西杏林白马药业有限公司,0.38 g/粒);小儿咽扁颗粒(黄石三九药业有限公司,8 g/袋)。
2 方法与结果
按《中国药典》(2010年版)一部附录微生物限度检查法进行验证。
2.1 菌液制备
2.1.1 金黄色葡萄球菌、枯草芽孢杆菌、大肠埃希菌取经30~35℃培养18~24 h的金黄色葡萄球菌、枯草芽孢杆菌、大肠埃希菌的营养肉汤培养物1mL,用0.9%无菌氯化钠溶液10倍递增稀释至10-5~10-7,使成50~100 cfu/mL,经活菌计数后备用。
2.1.2 白色念珠菌 取经23~28℃ 培养24~48 h的白色念珠菌的改良马丁液体培养物1 mL,用0.9%无菌氯化钠溶液10倍递增稀释至10-5~10-6,使成50~100 cfu/mL,经活菌计数后备用。
2.1.3 黑曲霉 取经23~28℃培养1周的黑曲霉改良马丁琼脂斜面培养物,用5 mL含0.05%(V/V)聚山梨酯80的0.9%无菌氯化钠溶液洗下黑曲霉孢子,吸出孢子悬液 1 mL至无菌试管内,用含0.05%(V/V)聚山梨酯80的0.9%无菌氯化钠溶液制成每1 mL含孢子数50~100 cfu的孢子悬液。
2.2 供试液制备
称样品10 g,加pH7.0无菌氯化钠-蛋白胨缓冲液至100 mL,摇匀,得1∶10供试液。
2.3 验证试验
细菌、霉菌与酵母菌计数方法的验证,若试验组的菌回收率均不低于70%,可按该供试液制备方法和计数方法测定供试品的细菌、霉菌与酵母菌数;若任一次平行试验中试验组的菌回收率低于70%,应建立新的方法,并重新验证。
2.3.1 常规法 取供试液(1∶10)1 mL入皿,然后每皿加营养琼脂或玫瑰红钠琼脂培养基15~20 mL,摇匀,按《中国药典》(2010年版)一部附录微生物限度检验方法进行。用常规法测定各品种对5株试验菌的回收率,以确定其抑菌程度,结果见表1。
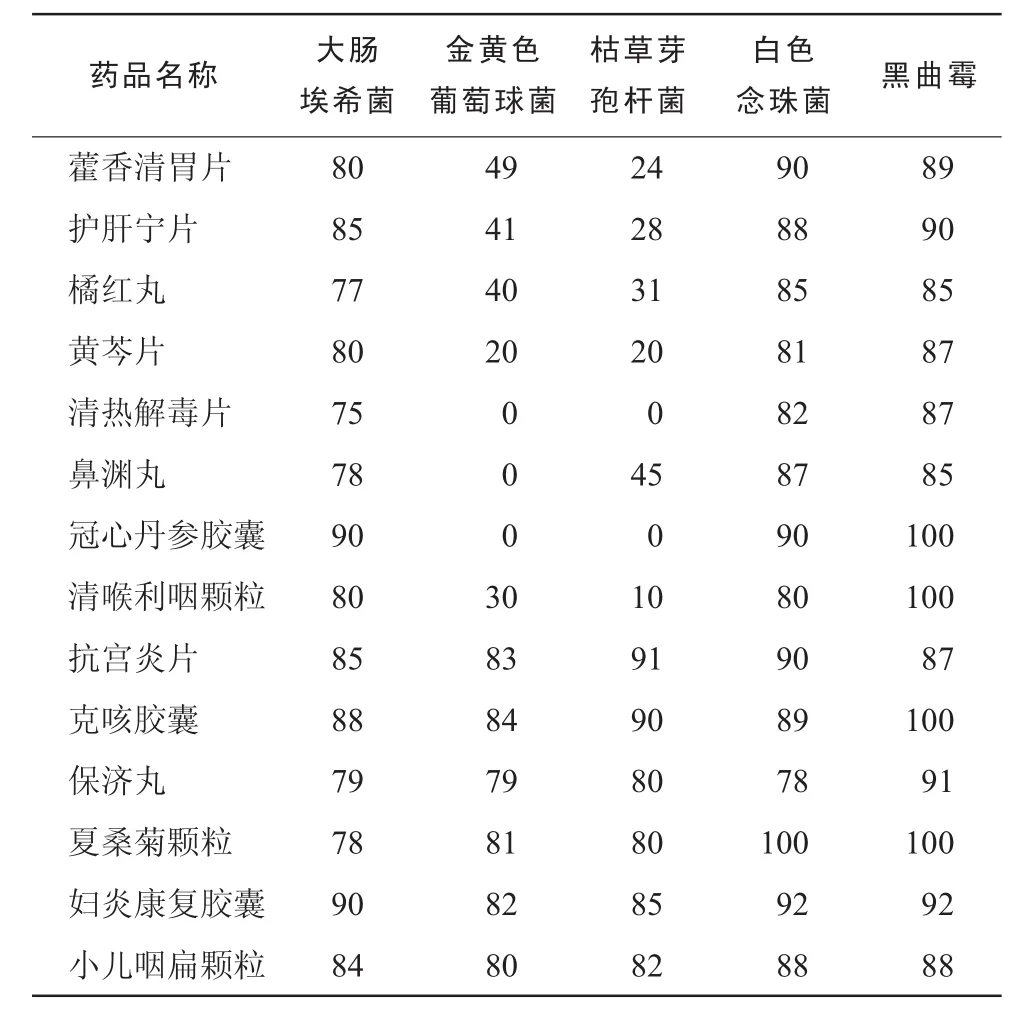
表1 14种中成药常规法(1 mL/皿)不同试验菌回收率(%)
由表 1可知,抗宫炎片、克咳胶囊、保济丸、夏桑菊颗粒、妇炎康复胶囊、小儿咽扁颗粒6个品种对5株试验菌的回收率均高于 70%,证明无抑菌作用。藿香清胃片、护肝宁片、橘红丸、黄芩片4个品种对金黄色葡萄球菌或枯草芽孢杆菌有一定的抑菌作用;清热解毒片、鼻渊丸、冠心丹参胶囊、清喉利咽颗粒抑菌作用很强,改用培养基稀释法或薄膜过滤法重新验证。各品种对大肠埃希菌、白色念珠菌及黑曲霉均无抑制作用,回收率均达到70%以上,可采用常规法测定。
2.3.2 培养基稀释法 取上述供试液(1∶10)1 mL,注入5个平皿中(每平皿0.2 mL),然后每皿加营养琼脂培养基15~20 mL,摇匀,按《中国药典》(2010年版)一部附录微生物限度检验方法进行。用培养基稀释法测定上述有抑菌作用品种对各抑菌菌株的回收率,结果见表2。可知,经培养基稀释(每平皿0.2 mL),藿香清胃片、护肝宁片、橘红丸、黄芩片对金黄色葡萄球菌或枯草芽孢杆菌已无明显抑菌能力,回收率均大于70%,而对清热解毒片、鼻渊丸、冠心丹参胶囊、清喉利咽颗粒,由于抑菌作用很强,采用培养基稀释法(0.2 mL/皿)不能完全消除其抑菌作用。

表2 培养基稀释法(0.2 mL/皿)和薄膜过滤法回收率(%)
2.3.3 薄膜过滤法 取上述供试液(1∶10)1 mL,加入置有100 mL冲洗液的滤器中,经减压抽滤干净后,用pH7.0无菌氯化钠-蛋白胨缓冲液冲洗,每次约100 mL,共冲洗400 mL/膜,在最后一次冲洗液中加入50~100 cfu。滤干后取膜,菌面向上贴于营养琼脂平板,经35℃培养3 d后,点计菌落数。测定结果见表2。由表1、2可知,清热解毒片、鼻渊丸、冠心丹参胶囊、清喉利咽颗粒常规法和培养基稀释法(0.2 mL/皿)检验时对金黄色葡萄球菌或枯草芽孢杆菌有很强的抑菌作用,回收率低于70%,采用薄膜过滤法,回收率均大于70%,因此,薄膜过滤法可用于上述4种中成药的细菌计数检查。
2.4 控制菌检查方法验证
2.4.1 大肠埃希菌 取1∶10试验组供试液 10 mL及1 mL(50~ 100 cfu/mL)大肠埃希菌液,加入到胆盐乳糖增菌培养基100 mL中,依据大肠埃希菌检查法进行试验。
取1∶10样品组供试液10 mL,加入到胆盐乳糖增菌培养基100 mL中,依据大肠埃希菌检查法进行试验。
2.4.2 大肠菌群 取1∶10试验组供试液1 mL及1 mL(50~100 cfu/mL)大肠埃希菌液,加入到乳糖胆盐发酵培养基10 mL中,依据大肠菌群检查法进行试验。
取1∶10样品组供试液1 mL,加入到乳糖胆盐发酵培养基10 mL中,依据大肠菌群检查法进行试验。
2.4.3 本研究14个品种均为口服制剂,按《中国药典》(2010年版)一部附录微生物限度检查法的规定,每 1 g不得检出大肠埃希菌;有原药材粉末投料的应检大肠菌群,每1 g不得超过100个。本研究试验组检出试验菌(大肠埃希菌),样品组未检出控制菌(大肠埃希菌、大肠菌群)。因此该试验方法成立。
3 微生物限度检查方法的建立
3.1 细菌计数检查法
当大肠埃希菌、金黄色葡萄球菌和枯草芽孢杆菌3种试验菌株的回收率均达到70%以上时,说明样品中污染的各类细菌均能顺利检出,可用该法检查本品的细菌数。因此本研究中14个品种的细菌计数检查法为抗宫炎片、克咳胶囊、保济丸、夏桑菊颗粒、妇炎康复胶囊、小儿咽扁颗粒可用常规法检查;藿香清胃片、护肝宁片、橘红丸、黄芩片可用培养基稀释法(0.2 mL/皿)检查;清热解毒片、鼻渊丸、冠心丹参胶囊、清喉利咽颗粒可用薄膜过滤法检查。
3.2 霉菌和酵母菌计数检查法
上述各品种的霉菌和酵母菌,均可用常规法检查。
3.3 控制菌检查法
各必检控制菌均可用常规法检查。
4 讨论
4.1 本研究所涉及的14种中成药进行细菌、霉菌和酵母菌计数方法验证时,试验菌株仅选用金黄色葡萄球菌和枯草芽孢杆菌2株菌即可,这样即可保证检验方法的有效性,又节省了大量的人力和物力。
4.2 如中成药含有较强的抑菌成分,由于抑菌成分的干扰,采用常规法进行微生物限度检查,结果不能真实反映其污染的微生物的状况。因此,使用适当的方法(通过对供试品作相应的处理,采取离心、培养基稀释法、薄膜过滤法等或几种方法联用)消除其抑菌成分的干扰,才能提高中成药中污染微生物的检出率。对具有抑菌作用的中成药,因其抑菌作用的强弱不同,进行微生物限度检查时,要消除其抑菌活性所采用的方法也有所区别。
[1] 国家药典委员会.中华人民共和国药典(2010年版)一部[S].北京:中国医药科技出版社,2010:附录79-88.
[2] 中国药品生物制品检定所,中国药品检验总所.中国药品检验标准操作规范 2010年版[M].北京:中国医药科技出版社,2010:351-407.
[3] 苏德模,马绪荣.药品微生物学检验技术[M].北京:华龄出版社,2007:221-227.
[4] 林丽英,湛文青,陆广欣.银翘解毒颗粒等中成药微生物限度检查法的建立[J].中成药,2006,28(12):1845-1847.
[5] 向东,张赟华,钱文璟.益心舒微丸微生物限度检查法及有效性验证试验研究[J].药物分析杂志,2007,27(5):730-732.
[6] 刘鹏,马仕洪,戴翚,等.加替沙星微生物限度检查方法的建立[J].药物分析杂志,2007,27(6):881-884.
[7] 杨静.药品微生物限度检查法的影响因素分析[J].中国药事,2008,22(12):1095-1096.
[8] 潘强.六种中药微生物限度检查方法验证[J].中国药品标准,2010,11(1):44-47.
[9] 王翠蓉,丁艳霞.速效止泻胶囊微生物限度检查方法的建立和验证[J].中国药品标准,2010,11(1):47-50.
[10] 宋勤,杜平华.中成药微生物限度检查方法的探讨[J].中国药事,2006,20(1):46-48.
[11] 许华玉,杜芸,钱文静,等.药品微生物限度检查法中细菌和真菌计数方法的验证试验[J].中国中药杂志,2005,30(24):1918-1920.
Study on the Microbial Limit Test Method for 14 Kinds of Chinese Patent Medicines
Huang Ying
(Lijiang Institute for Food and Drug Control,Yunnan Lijiang 674100,China)
Objective:To establish a method of microbial limit test for 14 kinds of Chinese patent medicines.Methods: According to the microbial limit test method set forth in the Chinese Pharmacopoeia of 2010 edition,the conventional method,medium dilution method and membrane filtration method were used for the recovery determination of the varieties of bacteria,mould and yeast,the antibacterial property of drugs was tested through the recovery determination,and the different control bacteria were determined by the direct inoculation method.Results:Six testing samples(kanggongyan tablets,keke capsules,baoji pills,xiasangju granules,fuyankangfu capsules,and xiaoeryanbian granules)showed no bacteriostasis and their bacterial recovery rates were more than 70%,which showed that the conventional method can be used to determine the bacterial count.The testing samples of huoxiangqingwei tablets,huganning tablets,juhong pills and huangqin tablets showed strong bacteriostasis,and the culture medium dilution method (0.2 mL/plate)can be used for the bacterial count determination.The testing samples of qingre jiedu tablets,biyuan pills,guanxin danshen capsules and qinghou liyan granules presented very strong bacteriostasis on Staphylococcus aureus and Bacillus subtilis,and membrane filtration method should be used for the bacterial counting test.The conventional method can be used for the testing of mould and yeast and various control bacteria of above mentioned testing samples.Conclusion:The method of microbial limit test was verified suitable for the above mentioned Chinese patent drugs and the method was proved effective in the quality control of the drugs.
Chinese Patent Medicine;Microbial Limit Test;Method Validation
10.3969/j.issn.1672-5433.2013.03.007
2012-08-31)
黄英,女,副主任药师。研究方向:药品检验。E-mail:huangyinglj11@163.com
