海泡石用于调湿涂料的吸湿性能改性研究
2013-01-19王汉青杨荣郭王正祥康良麒周慧文
王汉青 杨荣郭 王正祥 康良麒 周慧文
1湖南工业大学土木工程学院
2湖南工业大学包装与材料工程学院
0 引言
人的一生有90%的时间在室内度过[1],室内空气质量与人们的身体健康密切相关。空气湿度是一个与人们生活和生产有密切关系的重要环境参数,湿度对人体舒适度、室内空气质量、家具、图书及文物的养护都有重要意义[2]。按是否消耗人工能源,可将湿度控制调节方法分为主动式方法和被动式方法[3]。主动式方法主要是现有的空调技术,是目前湿度控制普遍采用的方法。被动式湿度控制调节即利用可再生能源或材料的吸放湿特性控制调节湿度。相对于主动式调湿方法,调湿材料作为调节室内相对湿度的手段,具有不消耗人工能源,利用自身的吸放湿性能调节室内空气湿度的优势。研究调湿材料,在不消耗任何外界能量的情况下,自动调节居住环境或物品保持环境湿度,必然将成为今后的发展趋势。
海泡石属斜房晶系粘土矿物,理论分子式为Si12O30Mg8(OH)4·8H2O[4],理论化学成分:SiO2,55.56%;MgO,24.89%;H2O+,8.34%;H2O-,11.12%。一般海泡石含杂质较多,产地不同,海泡石所含氧化物成分也不相同。海泡石是链式结构的镁硅酸盐,其结构是由滑石状板条与两个硅氧四面体单元片组成。海泡石的特殊结构决定了它拥有包括贯穿整个结构的沸石水通道和孔洞以及极大的表面积[5],说明海泡石具有一定的吸湿性能。本文简单分析了海泡石的表面特征,重点研究了海泡石作为调湿材料的吸放湿性能及调湿性能的改性研究。
1 实验部分
1.1 原料与试剂
海泡石(编号B):工业品,粒度200目,纯度70%,购自湖南浏阳某海泡石加工厂;海泡石(编号C):工业品,粒度200目,纯度60%,购自湖南湘潭某海泡石科技有限公司;NaOH:分析纯;CaCl2:分析纯;H2SO4:分析纯。
1.2 实验仪器
JA2003型电子天平;HH-WO型水浴锅;D971型电动搅拌器;SHB-Ⅲ型抽滤机;101-1AB型鼓风干燥箱;DZF-6090型真空干燥箱;HT402型恒温恒湿箱;自动比表面积分析仪:QUADRASORBSI型,美国某公司产;扫描电子显微镜:6360LV型,日本某公司产。
1.3 改性样品的制备
1.3.1 海泡石碱化处理
称取一定量的B、C样品,分别加入到浓度为3%的NaOH水溶液的烧瓶中(海泡石的含量大约在20%),在常温并在电磁搅拌下浸泡10h,所得样品抽滤干燥,得到碱化处理样品,样品分别命名为B1、C1,贮于干燥塔中备用。
1.3.2 海泡石酸化改性
称取一定量的样品B1分别加入到含不同浓度的硫酸溶液(10%,15%,20%,固液比按1:2计)的三口瓶中,在80℃下进行搅拌3h,然后将悬浮物抽滤,洗涤并于100℃下烘干至恒重,取出,粉碎,得到酸化改性样品,分别命名为B11、B12、B13;按同样的操作,对样品C1 酸化改性,得到样品 C11、C12、C13。
为便于比较,对样品C(即没经碱化处理的海泡石样品)直接进行酸化改性,处理方法同样品C1,所得样品分别命名为 C01、C02、C03。
1.3.3 海泡石氯化钙改性
称取一定量的无水氯化钙加入到带搅拌装置的三口烧瓶中并加入蒸馏水配制成50%溶液,按海泡石与无水氯化钙质量比分别为1:0.5、1:1、1:2、1:4进行原料配比,得到四份相同溶度不同量的CaCl2溶液,称取四份一定量的样品B1(约20g),分别加入到相同溶度不同量的CaCl2溶液中,在常温下搅拌0.5h,然后静置2h后,抽滤,得到滤饼,再干燥,得到氯化钙改性样品,分别命名为 B14、B15、B16、B17。
将样品C1在100℃下烘干至恒重备用,称取四份20g 样品 B1,分别称取 10g、20g、40g、80g 无水氯化钙(使海泡石与无水氯化钙质量比分别为1:0.5、1:1、1:2、1:4),加水配置不同溶度的 CaCl2溶液,将4份B1样品分别加入相同量不同溶度的CaCl2溶液中,在常温下搅拌0.5h,静置2h后,再进行抽滤,得到滤饼,干燥,得到样品分别命名为 C14、C15、C16、C17。
为了验证碱化处理对氯化钙改性的影响,现做一对比组,对样品B直接进行氯化钙改性,改性方法同B1,设置的对照组为三份,三份海泡石与无水氯化钙质量比分别为1:0.5、1:1、1:2,得到样品分别命名为B04、B05、B06。
1.4 测试与表征
样品的比表面积采用QUADRASORBSI型自动比表面积分析仪进行常规测定;样品的表面形貌在6360LV型扫描电子显微镜上测定。
样品的吸湿性能测试采用常规方法,具体测定如下:将原样及改性所得所有样品用100目的分子筛进行筛选,称取5~10g分别用培养皿盛放,测试各个样品的原重,再放在真空干燥箱中真空干燥6~8h,每隔2h称重一次,直到样品干燥达到恒重。将干燥后的所有样品放入恒温恒湿箱中进行吸湿,恒温恒湿箱的参数设置为:温度为25℃,湿度设置为95%,每隔一段时间称取各个样品的重量,算出各个样品的吸湿量及吸湿率。假设样品原重为W1,吸湿若干小时后重量为W2,则样品吸湿量为W2-W1,样品吸湿率为[(W2-W1)/W1]×100%。本实验测试样品的时间点为 2.5h、15h、27h、50h。
2 结果与讨论
2.1 比表面积及电镜扫描
2.1.1 海泡石原样的比表面积测试
海泡石样品B和C的比表面积测试结果见表1,从表格可以看出,海泡石样品B的比表面积比样品C的大30%,本实验采用的海泡石样品比表面积都在100m2/g以下,说明不同产地的海泡石的比表面积存在差异,但相差不是很大。

表1 海泡石原样的比表面积
2.1.2 海泡石原样的电镜SEM分析
对海泡石样品B和样品C进行扫面电镜分析,放大倍数为2000倍及20000倍,样品的微观形貌见图1至图4。

图1 样品B放大2000倍的扫描电镜图

图2 样品B放大20000倍的扫描电镜图

图3 样品C放大2000倍的扫描电镜图

图4 样品C放大20000倍的扫描电镜图
图1 和图2是海泡石样品B的2000倍和20000倍的扫描电镜图,图3和图4是样品C的2000倍和20000倍的扫描电镜图。从图1和图3可以看出,海泡石粉末主要以不规则颗粒状形式存在,并且海泡石粒径存在较大的变化范围,大粒径颗粒海泡石附近存在很多粒度不同的小颗粒;从图2可知,海泡石样品B的表面呈片麟状,而从图4中可知,海泡石样品C的表面呈纤维状,并以松散的束状形式存在。从图中可知,海泡石存在大量空隙,表明海泡石有一定的吸湿能力。
2.2 样品吸湿性能测试
测出所有样品在不同时间点的吸湿量,算出所有样品在不同时刻的吸湿率,最后结果见表2。将不同样品的吸湿率进行对比,绘制成吸湿率随时间变化关系图,所得结果如图5至图10所示。

表2 不同海泡石样品在不同时间点的吸湿率

图5 样品 B、B1、B11、B12、B13 吸湿率
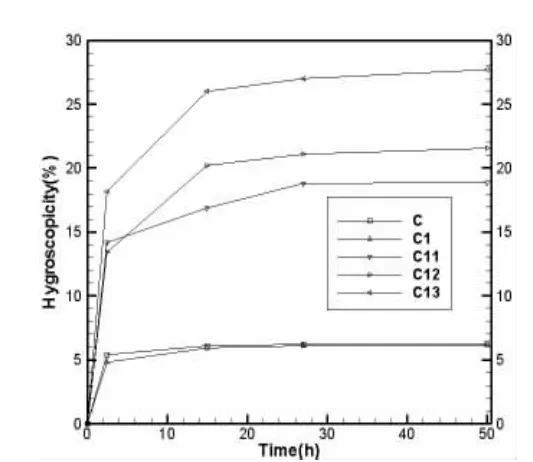
图6 样品 C、C1、C11、C12、C13 吸湿率

图7 样品 C、C1、C14、C15、C16、C17 吸湿率

图8 样品 B、B1、B14、B15、B16、B17 吸湿率

图9 样品 C01、C02、C03 及 C11、C12、C13 吸湿率

图10 样品 B04、B05、B06 及 B14、B15、B16 吸湿率
2.2.1 碱化处理对海泡石吸湿性能的影响
从图5可知,样品B1的吸湿率相对于样品B并没有太大的变化,从图6可知,样品C1的吸湿率相对于样品C并没有太大的变化,说明NaOH浸泡海泡石对其吸湿性能并没有太大的影响,对海泡石只起到去除杂质的作用。
2.2.2 酸化改性对海泡石吸湿性能的影响
从图5可知,样品B11、B12、B13的吸湿率相对于样品B1的吸湿率有明显提高;从图6可知,样品C11、C12、C13的吸湿率相对于样品C1的吸湿率也有明显提高。说明样品B1、C1经酸化改性后,吸湿率有明显的提高,并且样品吸湿率随着酸化改性硫酸浓度的升高(10%,15%,20%)而升高。从表2中可知,样品B13的吸湿率最高达到38.497%,是样品B1吸湿率(7.073%)的5.44倍,样品C13的吸湿率最高达到27.723%,是样品C1吸湿率(6.143%)的4.51倍。
从图9和表2中可知,吸湿50h后,酸化处理所得样品 C01、C02、C03的吸湿率是 21.890%、28.832%、43.288%,分别是样品 C(6.246%)吸湿率的 3.5、4.62、6.93倍,同样验证了样品的吸湿率随着酸化改性硫酸浓度的升高(10%,15%,20%)而升高。
2.2.3 氯化钙改性对海泡石吸湿性能的影响
从图7中可以看出,采用不同溶度相同量的CaCl2溶液对海泡石改性的方法能够提高海泡石的吸湿率,改性所得样品 C14、C15、C16、C17吸湿率随着 CaCl2溶液浓度的升高先升高后降低,但所得样品吸湿率都比改性前样品C1的吸湿率高。从表2可知,吸湿50h后,样品 C14、C15、C16、C17 的吸湿率分别为 7.752%、8.268%、14.4%、7.378%,分别是样品 C1吸湿率的1.26、1.35、2.34、1.2 倍,说明 CaCl2溶液浸泡海泡石,能够提高海泡石的吸湿率,CaCl2溶液浓度不同,对吸湿率的提高倍数不同,提高倍数随着CaCl2溶液浓度的升高,先升高后降低,当海泡石与无水氯化钙质量比为1:2时,CaCl2溶液改性海泡石的吸湿率达到最大的14.4%。
从图8中可以看出,采用相同溶度不同量的CaCl2溶液对海泡石改性的方法对其吸湿率有明显的提高,并且样品吸湿率随着 CaCl2质量份(1:0.5、1:1、1:2、1:4)的增加而升高;从表2可知,吸湿50h后,样品B14、B15、B16、B17 的吸湿率分别为 17.735%、20.253%、36.858%、66.215%,分别是样品 B1吸湿率的 2.51、2.86、5.21、9.36 倍。
对比图7和图8可知,采用相同溶度不同量的CaCl2溶液对海泡石改性的方法对提高海泡石的吸湿率更有利。
2.2.4 碱化处理对酸化改性海泡石吸湿性能的影响
从图9中可知,吸湿相同时间,样品C01、C02、C03的吸湿率分别高于碱化处理所得样品C11、C12、C13的吸湿率,样品C01、C02、C03的吸湿率分别为21.890%、28.832%、43.288%,而样品 C11、C12、C13 的吸湿率只有18.868%、21.562%、27.723%。可知,碱化处理后再进行酸化改性所得样品的吸湿率分别下降13.8%、25.2%、35.96%,说明碱化处理对酸化改性效果有阻碍作用,并且酸化浓度越高,阻碍作用越大。可能原因是:碱化处理后,样品中残留有NaOH,酸化改性时发生了中和反应,降低了酸化处理过程中酸的浓度,故酸化改性效果有所下降。
2.2.5 碱化处理对氯化钙改性海泡石吸湿性能的影响
从图10中可以看出,吸湿10h后,样品B14、B16的吸湿率高于样品B04、B06的吸湿率,而样品B15的吸湿率略低于样品B05的吸湿率;吸湿50h后,样品B04、B05、B06 的吸湿率分别为 13.819%、21.725%、27.919%,样品 B14、B15、B16吸湿率分别为 17.735%、20.253%、36.858%,碱化处理后再进行CaCl2改性所得样品吸湿率分别提高28.3%、-6.7%、32%。总体上来说,NaOH浸泡处理对CaCl2改性效果是有利的。
3 结论
1)产地不同,海泡石的比表面积存在差异,但比表面积相差不是很大。本文中,海泡石样品B的比表面积比样品C的比表面积大30%,但均低于100 m2/g。200目的海泡石粒度存在较大的变化范围,但海泡石表面都存在大量空隙,具有一定的吸湿能力。
2)未进行改性处理的海泡石吸湿率较低。吸湿50h后,样品B的吸湿率仅为6.847%,样品C的吸湿率仅为6.246%;
3)酸化改性可以大大提高海泡石的吸湿率,并且海泡石的吸湿率随着硫酸浓度的升高而升高。本文中,吸湿 50h后,样品 C01、C02、C03吸湿率为21.890%、28.832%、43.288%,吸湿率是样品C吸湿率的 3.5、4.62、6.93 倍;
4)相同溶度不同量的CaCl2溶液改性海泡石可以提高海泡石的吸湿率,吸湿率的提高幅度随着CaCl2的量的增多先升高后降低。不同溶度相同量的CaCl2溶液改性海泡石可以大大提高海泡石的吸湿率,故采用不同溶度相同量的CaCl2溶液改性海泡石的方案为最佳改性方案。
5)NaOH浸泡处理可去除海泡石中所含杂质,但对海泡石的吸湿性能没有太大影响;NaOH浸泡处理对酸化改性效果有阻碍作用,并且酸化浓度越高,阻碍作用越大。总体上,NaOH浸泡处理对CaCl2改性效果是有利的。
[1]American Society of Heating,Refrigerating and Air-Conditioning Engineers.ASHRAE Handbook-Fundamentals[M].Atlanta:AS-HRAE,1993
[2]侯国艳,冀志江.室内湿度对生活质量的影响[J].中国建材科技,2006,(3):74-76
[3]康玉梨.调湿涂料的研制与实验研究[D].北京:北京工业大学,2007
[4]Giora Rytwo,Dvora Tropp,Carina Serban.Adsorption of diquat,paraquat and methyl green on sepiolite:experimental results and model calculations[J].Appl Clay Sci,2002,20(6):273-282
[5]唐绍裘.海泡石的组成,结构,性能及其在陶瓷工业中的应用研究[J].硅酸盐通报,1989,8(4):77-86
