格列美脲改善胰岛素敏感性临床疗效研究
2012-09-06宋志成王东国吴群红
王 婧,孙 宏,宋志成,王东国,吴群红
糖尿病是由胰岛素相对或绝对缺乏引起的一种复杂的代谢性疾病,胰岛素皮下注射是治疗糖尿病的最有效手段之一。随着科学的发展,胰岛素治疗2型糖尿病有了很明显的进步,但胰岛素治疗中仍存在许多不良反应,尤其当使用剂量较大时,易出现低血糖反应、体质量增加、经济负担加重等问题;同时,外源性胰岛素注射仅是对内源性胰岛素不足的补充,但并不能模拟生理性胰岛素分泌,且存在胰岛素抵抗[1]。采用格列美脲联合胰岛素治疗方案,在有效降低血糖的同时,能减少胰岛素用量,对胰岛素有增敏作用,并能更好地模拟生理胰岛素分泌,改善胰岛素抵抗。本研究选取已采用胰岛素治疗的2型糖尿病患者为研究对象,在胰岛素应用剂量较大且血糖仍控制不佳的情况下,加用格列美脲,观察加用格列美脲治疗前后患者血糖水平、胰岛素用量、低血糖发生率等指标,评价格列美脲对胰岛素的增敏作用。
1 资料与方法
1.1 病例纳入标准 入选标准:2型糖尿病患者,符合1999年世界卫生组织 (WHO)糖尿病诊断标准;年龄≤75岁;性别、病程不限;已使用预混胰岛素 (或类似物),2次/d或3次/d皮下注射,剂量≥40 U/d;原有治疗方案已稳定≥1个月,血糖控制欠佳,空腹血糖 (FBG)≥8.0 mmol/L。排除标准:有严重心、肝、肺、肾等疾病者。
1.2 一般资料 选取2009年10月—2010年10月在大庆市第五医院门诊就诊及住院治疗的2型糖尿病患者56例,其中男30例,女26例;年龄38~66岁,平均 (50.2±4.1)岁;均符合上述病例纳入标准。按照随机对照的原则,将患者分为观察组 (30例)和对照组 (26例)。观察组中男17例,女13例;平均年龄 (41.7±6.1)岁;平均病程 (5.9±3.4)年。对照组中男12例,女14例;平均年龄 (43.2±5.8)岁;平均病程 (5.8±3.6)年。两组患者性别、年龄及病程间有均衡性。
1.3 方法 对照组在原胰岛素 (或胰岛素类似物)联合或不联合口服药的基础上增加胰岛素剂量,力争使FBG和餐后2 h血糖 (2 hPG)达标,但胰岛素剂量不宜超过60 U/次。观察8周,观察期间不增加其他降糖药。观察组患者在原胰岛素(或类似物)联合或不联合口服药的基础上加用格列美脲 (亚莫利,赛诺菲安万特公司生产,2 mg/片)治疗。观察组的治疗分两个阶段:第一阶段 (1~4周)为治疗方案调整期,原治疗方案不变,加用格列美脲起始剂量为1~2 mg/d,逐渐增加剂量,最大剂量可至6 mg/d。格列美脲服药时间不限,1次/d,特殊情况也可2次/d。直至FBG和2 hPG达标。血糖控制的目标:空腹、餐前、睡前血糖均控制在4.5~6.0 mmol/L,2 hPG控制在4.5~8.0 mmol/L。血糖达标后,格列美脲剂量不变,逐渐减少胰岛素剂量。第二阶段 (5~8周)为治疗方案维持期,维持原有治疗方案,若血糖≤5.3 mmol/L,应减少胰岛素剂量。
1.4 观察指标 比较两组患者治疗前后的体质指数 (BMI)、FBG、2 hPG、糖化血红蛋白 (HbA1c)、胰岛素用量及低血糖发生率。
1.5 统计学方法 采用SPSS 10.0软件进行统计学分析。计量资料以 (±s)表示,两组间均数比较采用t检验;计数资料采用χ2检验。检验水准α=0.05。
2 结果
2.1 治疗前后两组观察指标比较 治疗前,观察组患者的BMI、FBG、2 hPG、HbA1c、胰岛素用量与对照组比较,差异无统计学意义 (P>0.05);治疗8周后,两组患者 BMI、FBG、2 hPG、HbA1c、胰岛素用量及低血糖发生率与对照组比较,差异均有统计学意义 (P<0.05,见表1)。
2.2 低血糖发生率比较 观察组在第2周有1例 (3.3%)出现低血糖反应,症状较轻,在第4周后减少胰岛素用量后再无低血糖反应症状。对照组有6例 (23.1%)出现低血糖反应,即出现明显心悸、出汗、颤抖软弱无力等症状,最低血糖2.8 mmol/L。两组患者低血糖发生率比较,差异有统计学意义(χ2=2.265,P <0.05)。
表1 两组患者治疗前后观察指标比较 (±s)Table 1 Comparison of clinical data between two groups before and after the treatment
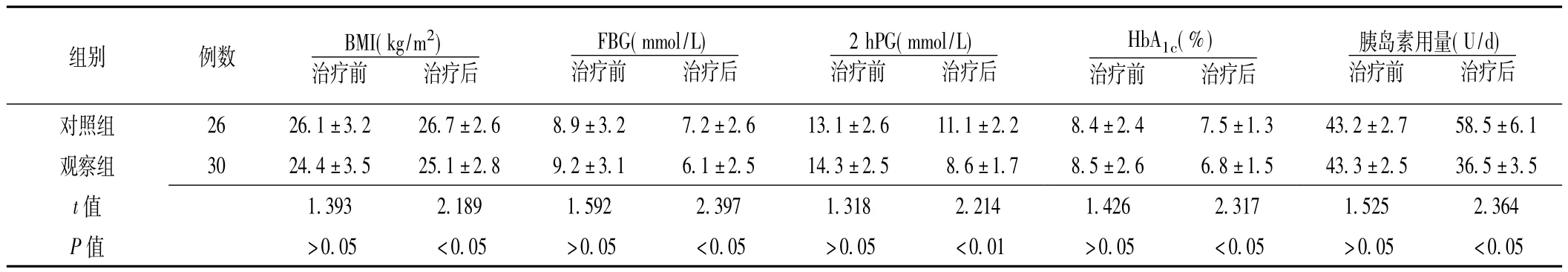
表1 两组患者治疗前后观察指标比较 (±s)Table 1 Comparison of clinical data between two groups before and after the treatment
注:BMI=体质指数,FBG=空腹血糖,2 hPG=餐后2 h血糖,HbA1c=糖化血红蛋白
组别 例数 BMI(kg/m2)治疗前治疗后对照组 26 26.1±3.2 26.7±2.6 8.9±3.2 7.2±2.6 13.1±2.治疗后FBG(mmol/L)治疗前 治疗后2 hPG(mmol/L)治疗前 治疗后HbA1c(%)治疗前 治疗后胰岛素用量(U/d)治疗前6 11.1±2.2 8.4±2.4 7.5±1.3 43.2±2.7 58.5±6.1观察组 30 24.4±3.5 25.1±2.8 9.2±3.1 6.1±2.5 14.3±2.5 8.6±1.7 8.5±2.6 6.8±1.5 43.3±2.5 36.5±3.5 t 值1.393 2.189 1.592 2.397 1.318 2.214 1.426 2.31 5 >0.05 <0.05 7 1.525 2.364 P值 >0.05 <0.05 >0.05 <0.05 >0.05 <0.01 >0.05 <0.0
3 讨论
良好的血糖控制对预防或减少糖尿病并发症具有重要意义,注射胰岛素是治疗2型糖尿病最有效的措施之一。以往治疗中认为口服药治疗血糖控制不佳时可加用胰岛素,但很少关注胰岛素剂量大、血糖控制仍不理想而加用双胍类或磺脲类促胰岛素分泌剂来使血糖下降,同时减少胰岛素用量这种治疗方式。近年来吴桢等[2]研究发现,胰岛素联合促泌剂治疗可使血糖更容易达标,更重要的是这种方案可以减少胰岛素用量,减轻胰岛素抵抗,对胰岛素分泌有增敏作用。
本研究结果表明,应用胰岛素治疗而血糖控制不理想的2型糖尿病患者加用格列美脲后BMI、FBG、2 hPG、HbA1c均显著低于对照组,且胰岛素用量低于对照组,对胰岛素有显著的增敏作用;且不增加低血糖的发生率,治疗过程安全。
格列美脲是被美国食品药品监督管理局 (FDA)批准的惟一可与胰岛素联用的磺脲类药物,具有生理性促进胰岛素分泌和减少胰岛素抵抗两大特点。与传统磺脲类药物作用于β细胞膜上的磺脲类受体140 KDa亚单位不同,格列美脲与65 kDa亚单位相结合。因与受体结合的部位不同,从而使格列美脲与受体结合及解离的速度较传统磺脲类药物更快,能更好地模拟生理性胰岛素的分泌[2]。格列美脲通过诱导葡萄糖转运蛋白4(GLUT4)去磷酸化,提高其在细胞膜上的表达,增加葡萄糖转运,增强外周肌肉、脂肪组织对葡萄糖的摄取,增加胰岛素敏感性,改善胰岛素抵抗。格列美脲与其他口服药相比,具有高效、作用时间长、用药量小、不良反应少的特点,适合糖尿病患者的长期治疗[3-4]。2008年,Defronzo教授在Banting奖获奖演说中指出,新诊断的2型糖尿病患者,其胰岛β细胞数量已下降了50%,并随着病程的进展,β细胞功能逐年衰退[5]。研究证实,早期使用胰岛素治疗不仅可以改善血糖控制,更重要的是可以保护β细胞功能。另外,高血糖代谢记忆效应的存在提示应尽早使血糖达标,早期强化胰岛素治疗可使患者持续获益[6]。体外研究证实,格列美脲可以使Zucker肥胖大鼠的脂肪细胞膜上的磷酸化GLUT4的数量减少,从而促进脂肪组织细胞对葡萄糖的摄取和利用;还可以通过磷脂酸肌醇3激酶途径,增加培养的人骨骼肌细胞胰岛素刺激的糖原合成作用[7-8]。Tsunekawa 等[9]采用高胰岛素正糖钳夹试验,观察格列美脲治疗12周后的老年2型糖尿病患者胰岛功能的变化,发现格列美脲可显著改善患者胰岛素抵抗指数,提高机体对葡萄糖的利用率。
综上所述,格列美脲与胰岛素联合应用可显著减少胰岛素用量,改善胰岛素抵抗,增加胰岛素敏感性。格列美脲为第三代磺脲类降糖药,刺激胰岛素分泌的作用较小,而胰外改善胰岛素抵抗的功能较强,可增加外周组织对胰岛素的敏感性,促进外周组织摄取和利用葡萄糖[10-11]。对于临床上胰岛素用量较大而降糖效果仍不理想的2型糖尿病患者,加用格列美脲或许是一个有效、安全的治疗方法。
1 McKeage K,Goa KL.Insulin glargine:a review of its therapeutic use as a long-acting agent for the management of the type 1 and 2 diabetes mellitus[J].Drugs,2001,61(11):1599-1624.
2 吴桢,周树娥.目前临床评价最优的磺脲类降糖药——格列美脲[J].实用糖尿病杂志,2008,4(6):54-55.
3 UK Prospective Diabetes Study(UKPDS)Group.Intensive blood glucose control with sulphonylureas or insulin compared with conventional treatment and risk of complication in patient with type 2 diabetes [J].Lancet,1999,354(9178):602.
4 颜云湘.第3代磺脲类降糖药——格列美脲 [J].中国临床药学杂志,2006,15(5):334-334.
5 Alvarsson M,Sundkvist G,Lager I,et al.Effects of insulin vs.glibenclamide in recently diagnosed patients with type 2 diabetes:a 4-year follow-up[J].Diabetes Obes Metab,2008,10(5):421-429.
6 Holman RR,Paul SK,Bethel MA,et al.10-year follow-up of intensive glucose control in type 2 diabetes[J].2008,359(15):1577-1589.
7 Müller G,Wied S.The sulfonylurea drug,glimepiride,stimulates glucose transport,glucose transporter translocation,and dephos- phorylation in insulin - resistant rat adipocytes in vitro[J].Diabetes,1993,42(12):1852-1867.
8 Haupt A,Kausch C,Dahl D,et al.Effect of glimepiride on insulinstimulated glycogen synthesis in cultured human skeletal muscle cells:a comparison to glibenclamide [J].Diabetes Care,2002,25(12):2129-2132.
9 Tsunekawa T,Hayashi T,Suzuki Y,et al.Plasma adiponectin plays an important role in improving insulin resistance with glimepiride in elderly type 2 diabetic subjects[J].Diabetes Care,2003,26(2):285-289.
10 张秋梅,于德民,李金金,等.加用格列美脲改善次大剂量胰岛素控制不佳的2型糖尿病胰岛素敏感性[J].中华内分泌代谢杂志,2010,26(12):1031-1034.
11 林蔚素,金尚福,曾斌华.格列美脲治疗2型糖尿病的疗效和安全性观察 [J].中国基层医药,2009,16(2):352.
