复方感冒灵片质量研究
2012-06-02高咏莉李国锋王淑红李军
高咏莉 李国锋 王淑红 李军
复方感冒灵片为复方制剂,主要由金银花、三叉苦等六味中药材和对乙酰氨基酚、咖啡因、马来酸氯苯那敏三种化学成分组成。现执行标准收载于《卫生部药品标准》中药成方制剂第十二册,含量测定项为滴定法测定对乙酰氨基酚含量。而处方中以马来酸氯苯那敏的含量最低,有效控制该成分的投料量及制剂工艺,以保证其含量的稳定性及均匀性是非常必要的。本文建立了马来酸氯苯那敏定量分析方法,并进行了含量均匀度检查,所采用的流动相有效改善了色谱峰的拖尾现象,从而保证了定量分析结果的准确性,具体过程如下。
1 仪器与试药
1.1仪器 XS205电子天平(Sartorius 0.01 mg);LC-20AD(岛津)高效液相色谱仪;SPD-M20A(岛津)二极管阵列检测器。
1.2药品与试剂 马来酸氯苯那敏对照品由中国药品生物制品检定所提供(批号100047-200606,纯度99.7%)。复方感冒灵片由3个生产厂家提供共8个批次样品。乙腈为色谱纯(Merck公司生产),其他试剂均为分析纯。
2 方法与结果
2.1对照品溶液的制备 精密称取马来酸氯苯那敏对照品适量,加甲醇制成每1 ml含马来酸氯苯那敏0.05 mg的溶液,摇匀,即得。
2.2供试品溶液的制备 取本品20片(包衣片除去包衣),精密称定,研细,精密称取适量(约相当于马来酸氯苯那敏1.34 mg),精密加入三氯甲烷25 ml,称定重量,超声处理30 min,放冷,再称定重量,用三氯甲烷补足减失的重量,摇匀,滤过,精密量取续滤液10 ml,回收溶剂至干,残渣加甲醇溶解并定容至10 ml量瓶中,摇匀,即得。
2.3色谱条件 色谱柱:Shiseido C18(5 μm,250 mm×4.6 mm);流动相:乙腈-磷酸盐缓冲液(取磷酸二氢铵11.5 g,加水适量使溶解,加磷酸1 ml,用水稀释至1000 ml)(25∶75);流速:1.0 ml/min;检测波长:262 nm;柱温:30℃。
2.4专属性实验 分别取对照品溶液、供试品溶液和阴性对照溶液各10 μl进样测定。结果表明:在此试验条件下,马来酸氯苯那敏的色谱峰分离良好,且阴性对照无干扰(见图2)。
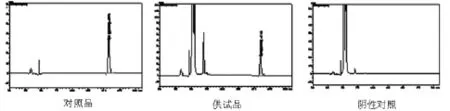
图1 HPLC色谱图
2.5方法学考察 ①线性关系的考察:精密称取马来酸氯苯那敏对照品适量,用甲醇配制成浓度分别为0.1、0.25、0.5、1.0、2.5 mol/ml的溶液。精密吸取上述对照品溶液各10 μl,注入液相色谱仪,以峰面积为纵坐标,浓度(μg)为横坐标进行线性回归,得回归方程Y=8.8883×10-7X-7.8906×10-4,r=0.9999,说明马来酸氯苯那敏在0.1003 ~2.595 μg内线性关系良好;②回收率:取同一批(厂家A,批号1002)已知含量的供试品(每片含马来酸氯苯那敏为标示量的94.3%)9份,分别精密加入马来酸氯苯那敏对照品,依法测定,计算回收率。结果平均回收率为102.7%,RSD=1.84%(见表1);③精密度:取同一批供试品6份,按样品测定项下方法测定,结果重复性良好,RSD=0.90%(n=6);④稳定性试验:取同一份供试品溶液,分别在 0、2、4、6、8、10、12 h 进样测定,记录峰面积积分值。结果RSD=0.56%,表明供试液在12 h内测定结果稳定。
2.6样品测定 取3个厂家、共8批样品,按照“2.3”项下供试品溶液制备方法试验,分别精密吸取供试品溶液各10μl,注入液相色谱仪,依法测定,结果见表2。
2.7含量均匀度检查 取含量测定结果合格的1个批次样品(厂家A,批号1002)进行均匀度检查。分别取本品10片,研细,照“2.2”及“2.3”项下的方法,依法测定,计算每片的含量。结果显示,马来酸氯苯那敏的含量均匀性存在一定的差异,含量范围为84.5% ~105.0%,A+1.80S=18.0。

表1 准确度试验结果表
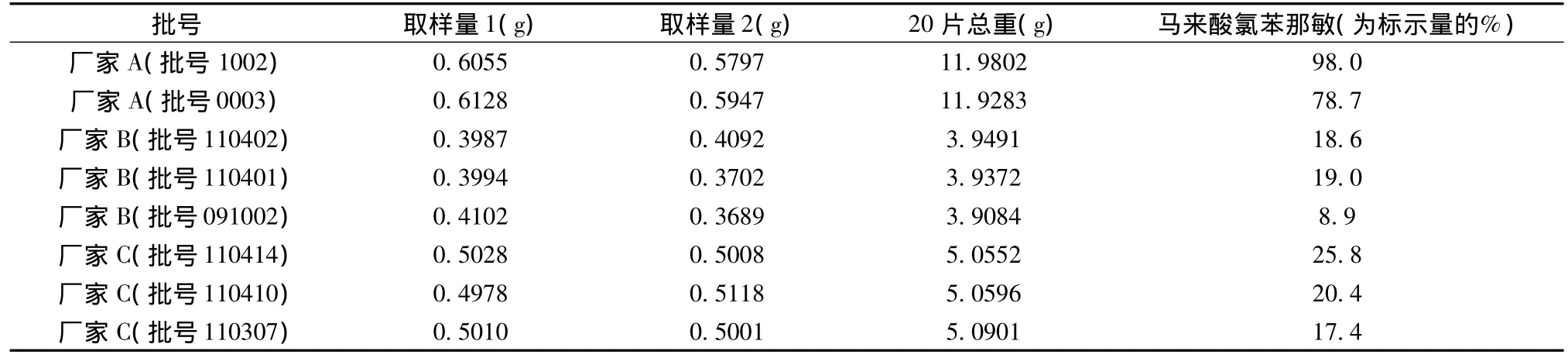
表2 样品含量测定结果表
3 讨论
3.1文献曾报道了几种流动相色谱条件:甲醇-庚烷磺酸钠醋酸混合液(600∶400)[2],甲醇-水-冰醋酸(20∶80∶2.5[3]),乙腈-1% 冰醋酸溶液(内含0.08% 的三乙胺)(50∶50)[4]。按照上述条件试验,马来酸氯苯那敏色谱峰均有较严重的拖尾现象,导致测定结果不稳定,无法准确定量。本试验采用乙腈-磷酸盐缓冲液为流动相,结果显示,色谱峰形较好,拖尾因子可以达到1.1,符合药典要求。
3.2含量测定结果显示,除厂家A的2批样品外,其余样品的含量均远远低于标示量;含量均匀度检查结果显示,制剂中马来酸氯苯那敏的均匀性存在一定的差异。目前全国约有70多个厂家生产该品种,本品又为复方制剂,有效控制处方中化学成分的投料量及制剂工艺,以保证其含量的稳定性及均匀性是非常必要的。因此,药品生产企业及监管部门应对该产品的质量研究与质量控制引起足够重视。
[1]刘乡乡,康志英,黄晓玲,等.复方感冒灵斤质量标准研究.中药材,2003,26(4):282-283.
[2]朱炳辉,陆惠文,梁艺英,等.重感片中安乃近及马来酸氯苯那敏的固相萃取高效液相色谱法测定.中成药,2001,23(4):246.
[3]吴静.高效液相色谱法测定维C银翘片中马来酸氯苯那敏的含量.现代中药研究与实践,2004,18(6):40.
[4]曹艳芳,黄夏敏,冯倩玲,等.对复方感冒灵胶囊中马来酸氯苯那敏的含量测定.今日药学,2009,19(3):19-22.
