六氮杂大环配合物[Cd2(C30H48N6O2)(H2O)2Cl2]·2CH3OH的合成及其晶体结构*
2011-11-24刘海燕乔秀丽孙红梅赵大伟
刘海燕, 乔秀丽, 孙红梅, 赵大伟
(绥化学院 化学与制药工程系,黑龙江 绥化 152061)
近年来,以氮原子替代冠醚体系中的氧原子的氮杂冠醚的合成、性质以及应用研究已经引起了人们的广泛兴趣[1,2]。这不仅由于氮原子的软碱性质,使其对过渡金属和重金属等离子显示出特异的络合作用,而且氮杂冠醚所具有的独特分子结构和配合性能,使其相应的金属-氮杂冠醚配合物可用来模拟生物体内生物蛋白酶的结构。通过研究这些配合物的结构和性质,对于深入了解金属活动中心的作用机制,认识金属蛋白和金属酶的生物功能,具有重要的意义[3]。尤其是多氮杂冠醚因含有多个氮原子,对过渡金属离子的络合尤为突出。随多氮杂冠醚化合物的空腔的扩大,可以形成双核络合及串联配合物。这些配合物在主客体化学、分子识别和信息传输中具有重要意义[4,5]。金属-氮杂冠醚类化合物的分子设计、合成以及性质研究已成为生物无机化学研究领域的热点之一[6,7]。
本文报道六氮杂大环化合物[3,7,11,19,23,27-六氮杂-33,34-二羟基-15,31-二甲基-三环-三十四烷-1(32),13,15,17(34),29(33),30-六烯(H2L)与CdCl2·2.5H2O在甲醇中反应,合成新型双核镉冠醚配合物[Cd2(L)(H2O)2Cl2]·2CH3OH(1)的方法。1的结构经IR,元素分析和X-射线单晶衍射分析表征。并研究了1在室温下的荧光性质。
1 实验部分
1.1 仪器与试剂
Magna 560 FT-IR型红外光谱仪(KBr压片);Carlo-Erba 1106型元素分析仪;Gemini R Ultra CCD型X-射线单晶衍射仪;FLSP 920艾丁博格荧光光谱仪。
H2L按文献[8]方法合成,其余所用试剂均为分析纯。
1.2 1的合成
在反应瓶中加入H2L 54 mg(0.1 mmol)和甲醇30 mL,搅拌使其溶解后加入CdCl2· 2.5H2O 46 mg(0.2 mmol),反应30 min(产生白色固体);滴加14%氨水(4 mL)直至固体完全溶解。过滤,滤液于室温放置4 d。过滤得无色块状单晶1,产率66%; IRν: 3 604, 3 410, 3 274, 3 242, 2 920, 2 851, 1 633, 1 607, 1 563, 1 467, 1 419, 1 297, 1 265, 1 167, 1 099, 1 045, 1 003, 971, 945, 915, 889, 865, 783, 693, 613, 565, 525, 473 cm-1; Anal.calcd for C32H60N6O6Cl2Cd2: C 41.75, H 6.57, N 9.13; found C 41.61, H 6.69, N 9.20。
1.3 晶体结构测定
选取1单晶(0.24 mm×0.20 mm×0.16 mm)置衍射仪上,于293 K用石墨单色化的MoKα射线(λ=0.710 73 Å)作衍射光源,收集衍射数据。晶体结构通过SHELXS-97[9,10]程序以直接法解出,并运用全矩阵最小二乘法进行精修。非氢原子用各向异性温度因子修正,除了亚氨基、水分子和羟基上的氢原子外,所有氢原子坐标由理论计算确定。
2 结果与讨论
2.1 晶体结构
1的分子结构见图1;主要键长和键角见表1,氢键键长和键角见表2。
结构解析表明,1属单斜晶系,P2(1)/n空间群,晶胞参数a=11.945 1(3) Å,b=7.418 5(2) Å,c=22.238 9(5) Å,β=99.830(2)°,V=1 941.76(8) Å3,Z=2,Dc=1.574 g·cm-3,μ=1.281 mm-1,F(000)=944,S=0.836,Rint=0.049 2,R1=0.036 9,wR2=0.072 2[I>2σ(I)], (Δρ)max/(Δρ)min=0.644/-0.359 e·Å3。
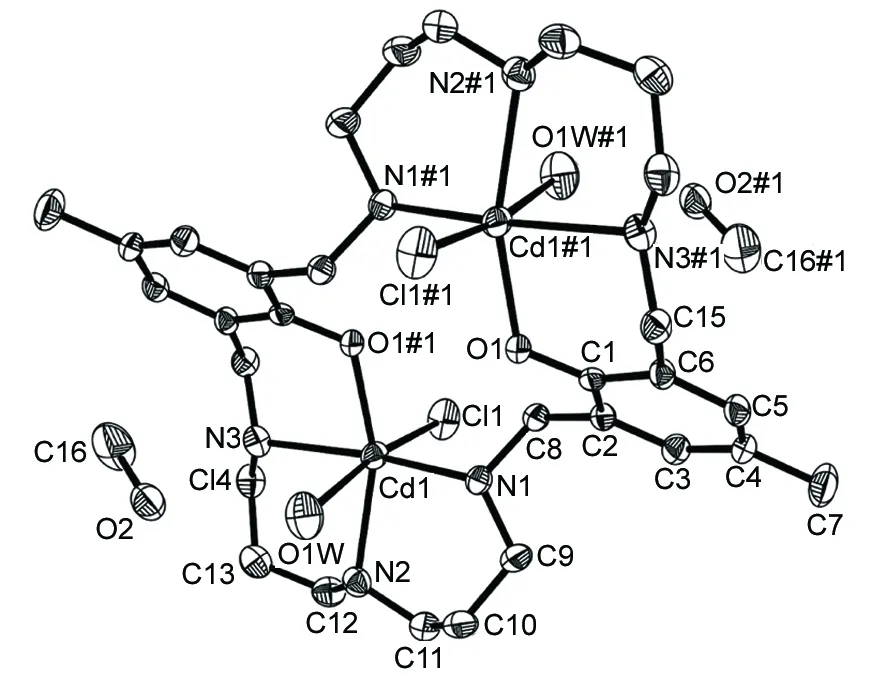
图 1 1的分子结构图
从图1可见,每个Cd(Ⅱ)采用的八面体配位方式,分别被处于赤道位的大环配体L2-上三个氮原子和一个酚羟基上的氧原子,以及处于轴向位置的一个氯离子和一个水分子配位。其中三个镉氮键的键长分别为2.326 0(2) Å[Cd(1)-N(1)], 2.335 0(3) Å[Cd(1)-N(2)]和2.359 0(3) Å[Cd(1)-N(3)];镉与酚羟基氧的键长为2.221 0(2) Å[Cd(1)-O(1)#1],与氯离子的键长{2.529 1(11)[Cd(1)-Cl(1)]}均属于正常的键长范围。然而与配位水分子的距离为2.696 0(2) Å,比正常的Cd-O的键略长,但也与有关报道的Cd-O键的距离相近[11]。晶体结构表明,大环配体以扭曲的构型与两个Cd(Ⅱ)配位,游离的溶剂甲醇分子位于大环的两侧。
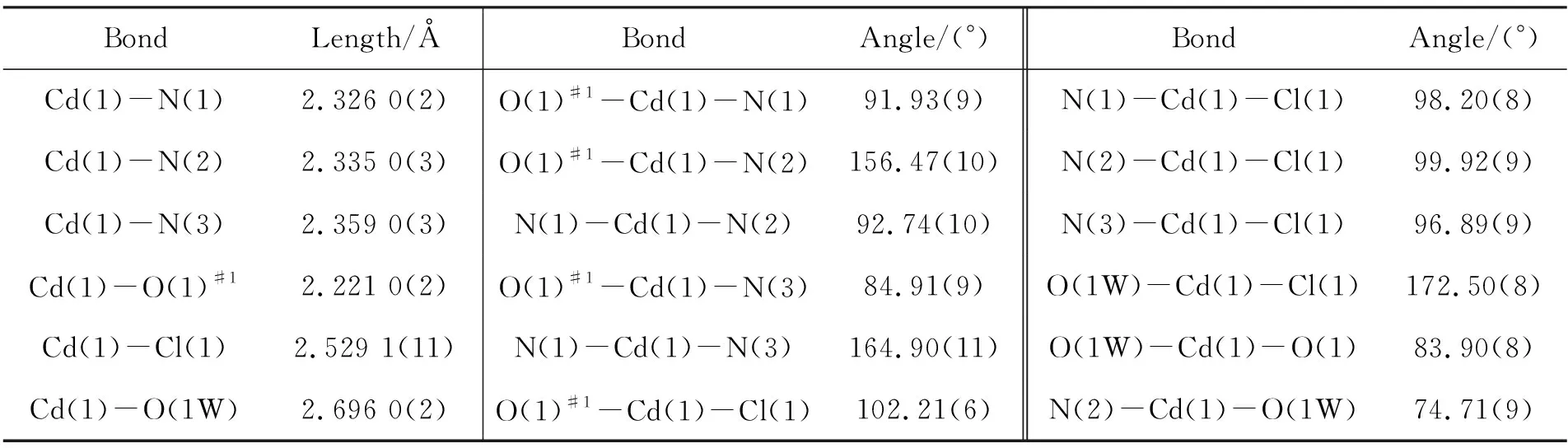
表 1 1的主要键长和键角
#1-x,-y,-z+1
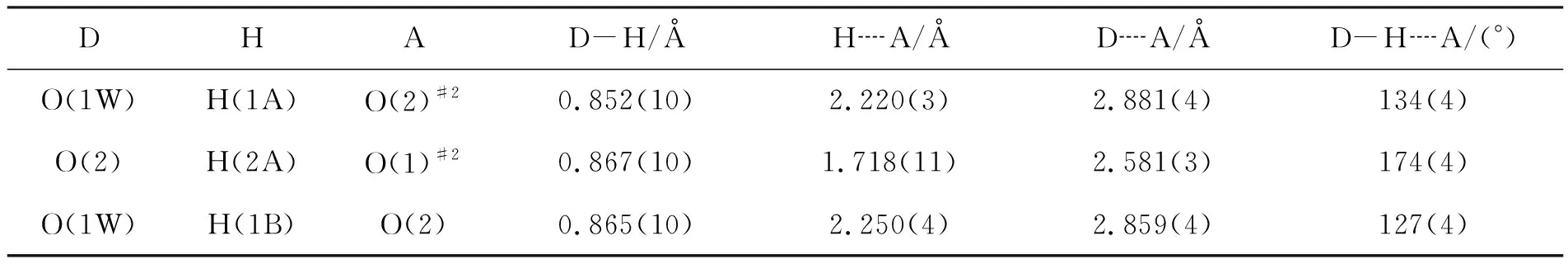
表 2 1的氢键键长和键角
#2-x,-y+1,-z+1
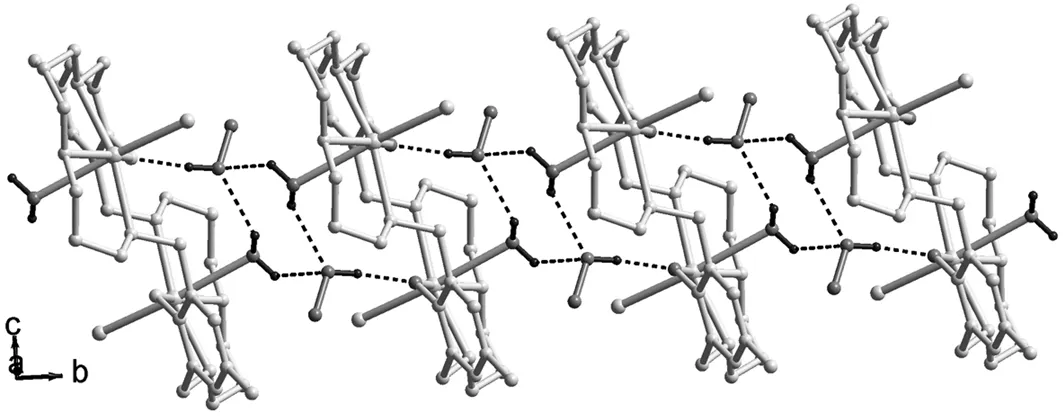
图 2 1的一维超分子链
λ/nm
在1的分子结构中存在着三种类型的分子间氢键作用(表2),通过这些配位的水分子、甲醇分子的羟基基团和大环配体上的酚羟基氧原子之间的氢键作用,将大环结构单元沿b轴方向连接成一维超分子链状结构(图2)。
2.2 1的荧光性质
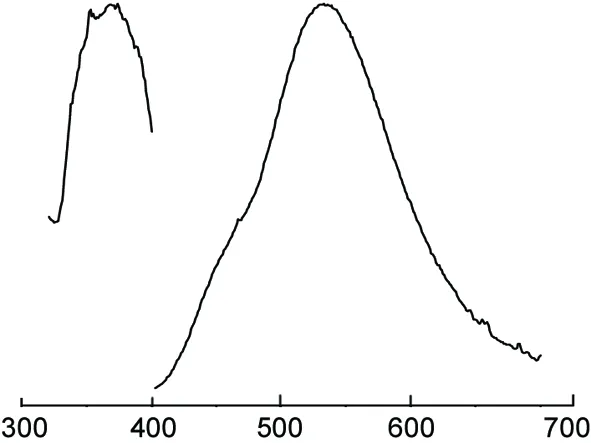
1的荧光激发和发射光谱见图3。由图3可见,1的激发带位于350 nm~375 nm,其最佳激发波长为360 nm,最大发射波长为530 nm,发射出绿光。这种发光方式既不是金属—配体电荷转移(MLCT),也不是配体—金属电荷转移(LMCT)[12],这种荧光是由于配体分子内部的n→π*或π→π*跃迁产生的,其特征是发射峰很宽。
[1] Krakowiak K E, Bradshaw J S, Zamecka-krakowiak D J. Synthesis of aza-crown ethers[J].Chem Rev,1989,89(4):929-972.
[2] Zhang X X, Buchwald S L. Efficient synthesis ofN-aryl-aza-crown ethers via palladium-catalyzed amination[J].J Org Chem,2000,65(23):8027-8031.
[3] Liobet A, Reibenspies J H, Martell A E. Oxydiacetic acid and copper(Ⅱ) complexes of a new hexaaza macrocyclic dinucleating ligand[J].Inorg Chem,1994,33(25):5946-5951.
[4] 刘育,张衡益. 冠醚的分子设计及其识别性质研究进展[J].有机化学,2002,22(2):91-100.
[5] 黄贵海,马淑兰,李新新,等. 三环氮杂取代冠醚配体及配合物的合成与表征[J].北京师范大学学报(自然科学版),2004,40(5):643-646.
[6] 陈实,鲁统部,冯小龙,等. 氮杂大环双核铜锌金属配合物的合成结构及溶液中配位稳定性研究[J].高等学校化学学报,2002,23(6):1004-1006.
[7] Costas M, Ribas X, Poater A,etal. Copper(Ⅱ) hexaaza macrocyclic binuclear complexes obtained from the reaction of their copper(Ⅰ) derivates and molecular dioxygen[J].Inorg Chem,2006,45:3569-3581.
[8] Wang J, Martell A E, Motikatis R J. The synthesis,crystal structure and complexation of a new octacoordinate hexaazamacrocyclic ligand[J].Inorg Chim Acta,2001,322:47-55.
[9] Sheldrick G M, SHELXS-97. Program for the Solution of Crystal Structures[K].University of Göttingen,Germany,1997.
[10] Sheldrick G M, SHELXL-97. Program for the Refinement of Crystal Structures[K].University of Göttingen,Germany,1997.
[11] Zang S Q, Su Y, Li Y Z,etal. Interweaving of triple-helical and extended metal-O-metal single-helical chains with the same helix axis in a 3D metal-organic framework[J].Inorg Chem,2006,45:3855-3857.
[12] Wen L L, Li Y Z,Lu Z D,etal. Syntheses and structures of four d10metal organic frameworks assembled with aromatic polycarboxylate and bix[bix=1,4-bis(imidazol-1-ylmethyl)benzene][J].Crystal Growth & Design,2006,6:530-537.
