Tb掺杂CeO2的制备及其光催化性能研究*
2024-01-25刘新棋凌丽婷王春英
高 艳,刘新棋,凌丽婷,李 民,王春英
(江西理工大学资源与环境工程学院,江西 赣州 341000)
近年来,随着环境现状无法满足人们对环境质量需求矛盾的增加,对污染环境的治理得到广泛的研究。其中,光催化法被公认为是对环境友好的污染物处理方法[1]。光催化法既可以降解无机污染物、还原重金属离子及降解剧毒污染物等,还能降解各类有机污染物,如苯酚[2]、双酚A[3]、苯[4]等,同时可用于消毒[5]和脱色处理[6]等。
在众多光催化剂中,由于具有特殊的电子和光学结构,优异的物理和化学性质,基于二氧化铈(CeO2)的光催化剂引起了研究者的重视[7]。CeO2除了可以做光催化材料,还可以作为抛光材料、太阳能电池材料、氧储存材料、紫外线遮光材料等[8]。因此,大量纳米CeO2的制备方法被报道,如溶胶-凝胶法[9]、电纺丝合成法[10]、化学沉淀法[11]、超声合成法[12]、喷雾反应法[13]、微乳法[14]等。本文以CeO2为研究对象,利用溶剂热合成法制备不同铽(Tb)掺杂量的CeO2纳米晶体,并用XRD、SEM、BET对焙烧得到的CeO2晶型、形貌和孔结构等进行比对考察,以揭示不同含量铽掺杂下对纳米CeO2的晶型、形貌和孔结构的影响问题;同时,以选矿药剂苯甲羟肟酸为目标污染物,考察合成材料对目标污染物的光催化降解特性。
1 实 验
1.1 试剂及仪器
试剂:六水合硝酸铽(Tb(NO3)3·6H2O),阿拉丁;六水合硝酸铈(CeN3O9·6H2O),阿拉丁;聚乙烯吡咯烷酮PVP((C6H9NO)n),麦克林;氢氧化钠(NaOH)、乙二醇(C2H6O2)、无水乙醇(CH3CH2OH)、磷酸(H3PO4),西陇科学股份有限公司;甲醇(CH3OH),国药集团化学试剂有限公司;苯甲羟肟酸(C7H7NO2),润友化学有限公司。除甲醇为色谱纯外,其他试剂均为分析纯。
仪器:XPA系列光化学反应仪,南京胥江机电厂;FO610C马弗炉,雅马拓科技贸易(上海)有限公司;TG16-WS台式高速离心机,湘仪离心机仪器有限公司;FL2200高效液相色谱仪,浙江福立分析仪器有限公司;ASAP 2460比表面积测定仪,麦克默瑞提克(上海)仪器有限公司;KQ-500DE超声清洗仪,昆山市超声仪器有限公司;ADP310C真空干燥箱,雅马拓科技贸易(上海)有限公司;Exceed-AD-08实验室用超纯水仪,成都康氏康宁科技发展有限公司。
1.2 Tb掺杂CeO2的制备
选择六水合硝酸铈作为前驱体,加入不同含量的六水合硝酸铽,再加入分散剂聚乙烯吡咯烷酮,搅拌均匀,与氢氧化钠溶液混合,提供强碱环境,分别加入30 mL乙醇和30 mL乙二醇,常温下搅拌2 h至完全均匀。将混合溶液转移至高温高压反应釜内衬中,密封,在160 ℃烘箱中放置24 h,取出冷却至室温,用去离子水及无水乙醇交叉洗涤3次,在80 ℃烘箱中真空干燥12 h。在马弗炉中500 ℃煅烧2 h,保持升温速率为10 ℃/min,冷却至室温后,用玛瑙研钵研磨待用。
1.3 光催化反应
先加入20 mg/L苯甲羟肟酸50 mL,并加入0.2 g/L的催化剂,进行避光搅拌60 min后,开启300 W的汞灯,进行催化降解反应。每隔30 min取样,经0.45 μm滤膜过滤后通过高效液相色谱测定苯甲羟肟酸浓度。
1.4 分析方法
实验使用FL2200型高效液相色谱分析仪测定反应溶液中的苯甲羟肟酸的浓度。仪器条件为:色谱柱型号为XB-C18(5 μm,4.6 mm×250 mm);检测波长为230 nm;流速为0.5 mL/min;进样体积为50 μL;流动相各成分体积比为甲醇∶水∶磷酸=65∶35∶4;柱温为25 ℃。
对光催化法降解污染物的实验效果可以通过苯甲羟肟酸的降解速率来反应。苯甲羟肟酸的降解速率可定义为:
降解率=1-C/C0×100%
式中:C和C0分别为苯甲羟肟酸的即时测试浓度和实验开始时的初始浓度。
2 结果与讨论
2.1 物相分析
图1为不同掺杂量Tb/CeO2的XRD图。由图1可以看出,实验所得不同掺杂量的CeO2复合材料的特征峰与标准卡片JCPDS NO.34-0394相匹配,其衍射峰对应的2θ角在28.6°、33.1°、47.5°、56.3°以及76.7°的位置均一一对应,说明成功制备了CeO2化合物。相对于未掺杂CeO2,Tb/CeO2的衍射峰强度增加,说明掺杂Tb的复合材料增强了其结晶度。
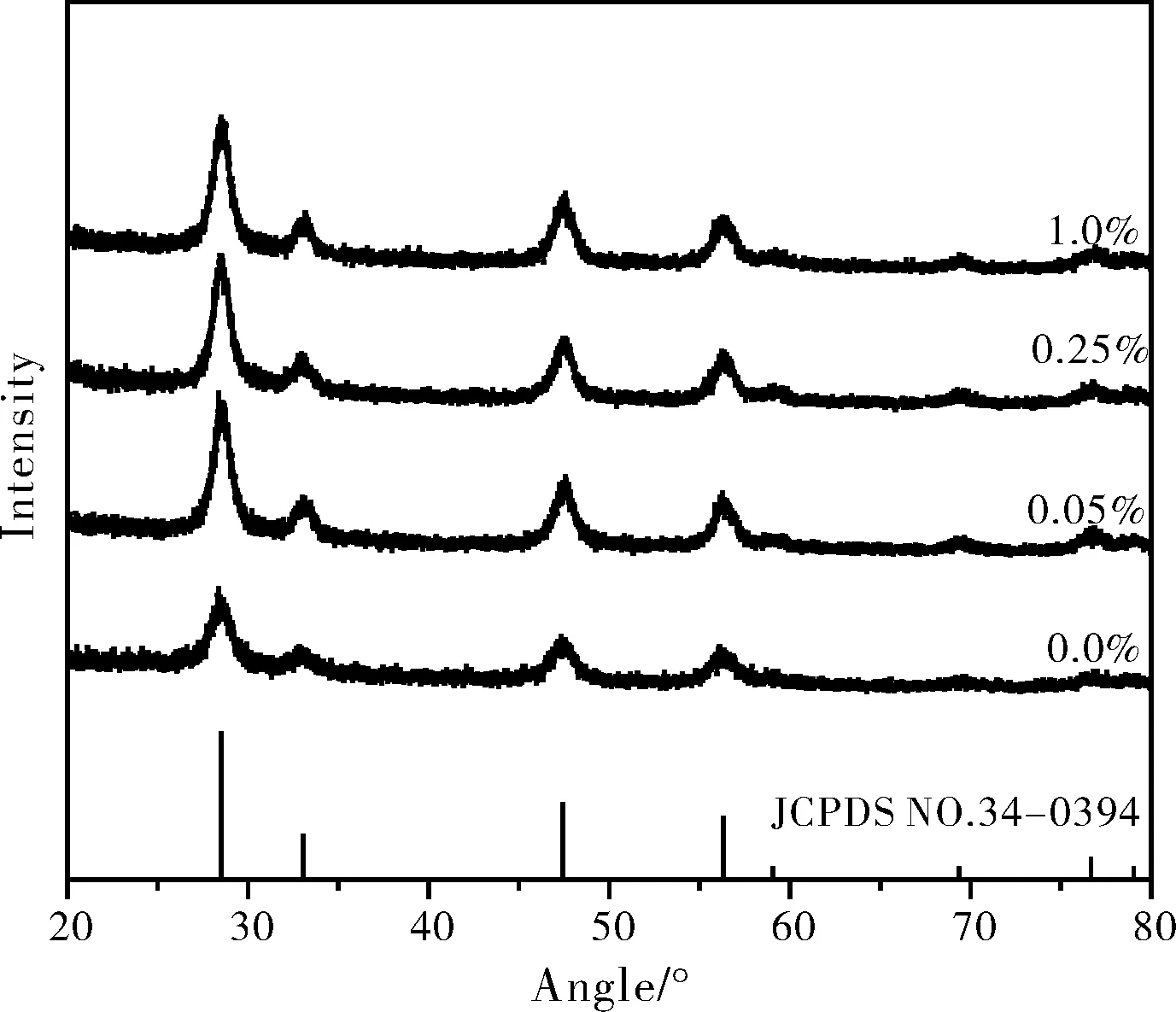
图1 不同掺杂量Tb/CeO2的XRD图
2.2 形貌分析
图2给出了不同掺杂量Tb/CeO2的形貌图。从图2中可以看出,制备所得的CeO2均为不规则立体形状,颗粒表面有着不均匀的凸起,且随着掺杂Tb含量的增大,CeO2颗粒逐渐团聚在一起,颗粒整体体积变大,与XRD结果一致。

图2 不同掺杂量Tb/CeO2形貌图
2.3 结构分析
图3、图4分别为掺杂不同含量Tb样品的N2吸附-脱附等温线及BJH孔径分布图。由图3可知,160 ℃掺杂不同摩尔百分比的Tb所制备样品的N2吸附-脱附等温线为IUPAC范畴中典型的Ⅳ型曲线,并且在高压区0.6~1.0 P/Po的压力范围内存在一个明显的H3滞后环[15],表明合成材料具有介孔结构。所得四种样品的比表面积分别为131.003 5 m2/g、119.586 5 m2/g、123.197 7 m2/g、119.388 7 m2/g,稀土Tb掺杂后,比表面积降低。从图4的孔径分布图中可以看出,孔径的大小主要集中在2~5 nm。
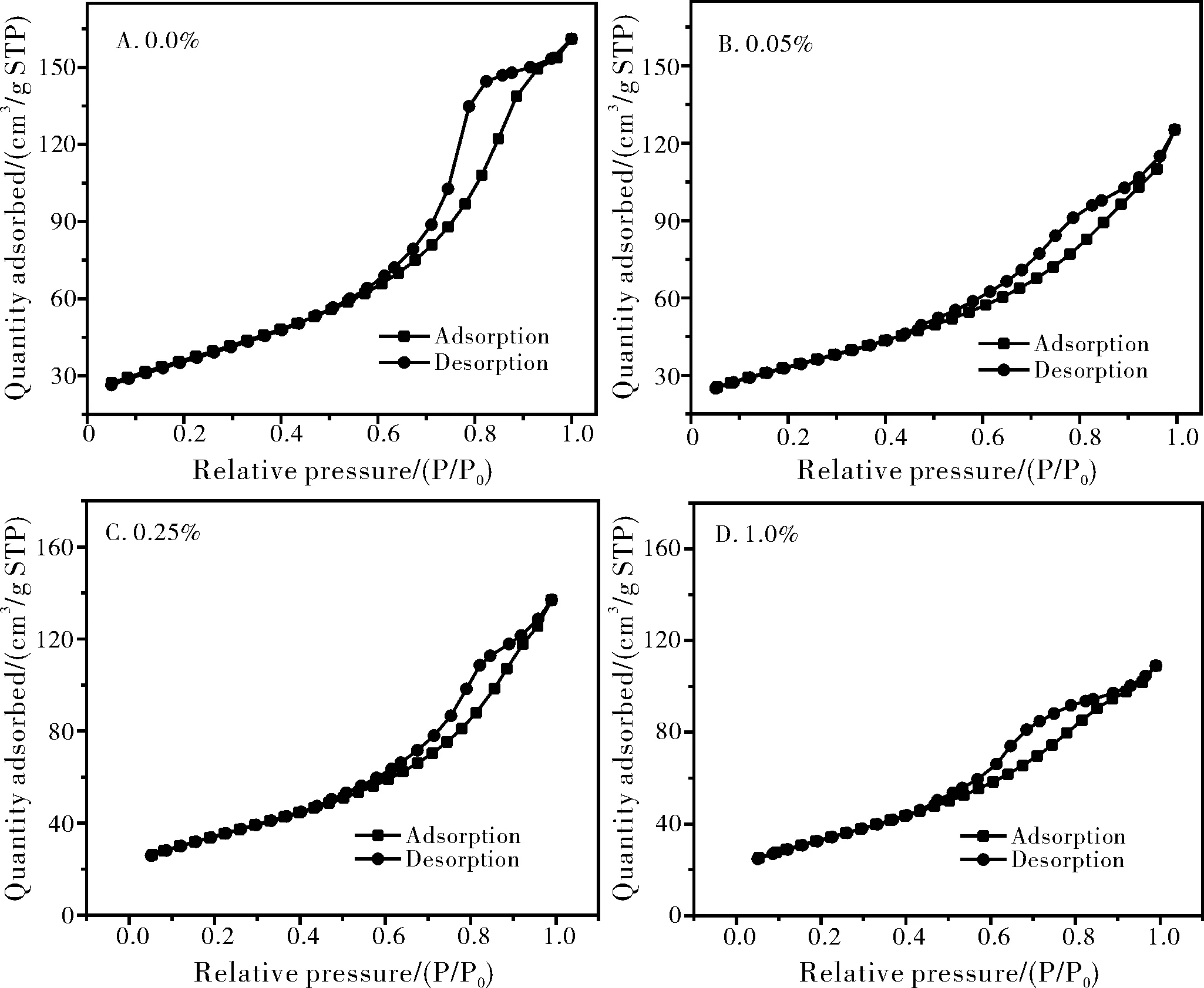
图3 不同掺杂量Tb/CeO2 氮气吸附-脱附等温曲线
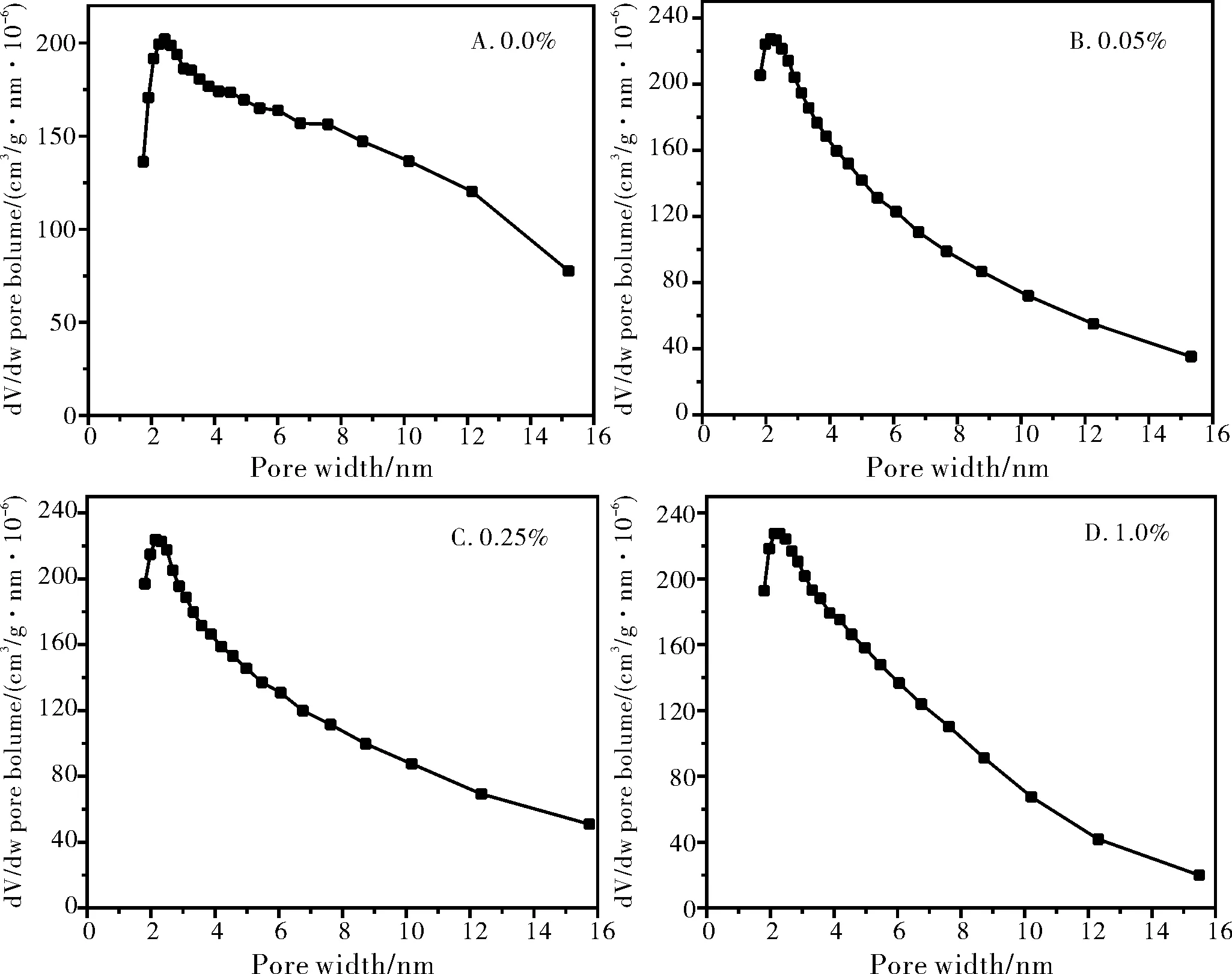
图4 不同掺杂量Tb/CeO2孔径分布图
2.4 苯甲羟肟酸降解效果
不同掺杂量Tb/CeO2光催化降解苯甲羟肟酸的实验结果如图5所示。从图5中可以看出,在避光吸附搅拌60 min过程中,未掺杂Tb的CeO2对苯甲羟肟酸的去除效果较好,吸附去除率高达71.5%,但在汞灯照射下的120 min内,光催化去除效率仅有11.0%;而掺杂0.05%、0.25%以及1.0%Tb的CeO2的吸附去除率虽然比较低,但在汞灯照射120 min内,其光催化去除效率分别高达58.0%、62.1 %、59.9%,约为未掺杂Tb的CeO2的光催化效率的5.3、5.7、5.5倍。证明实验所制的CeO2的光催化性能得到了较好的提升。对比其他掺杂量的CeO2,0.05% Tb/CeO2对苯甲羟肟酸的总体去除效果最佳,去除率为86.0%。
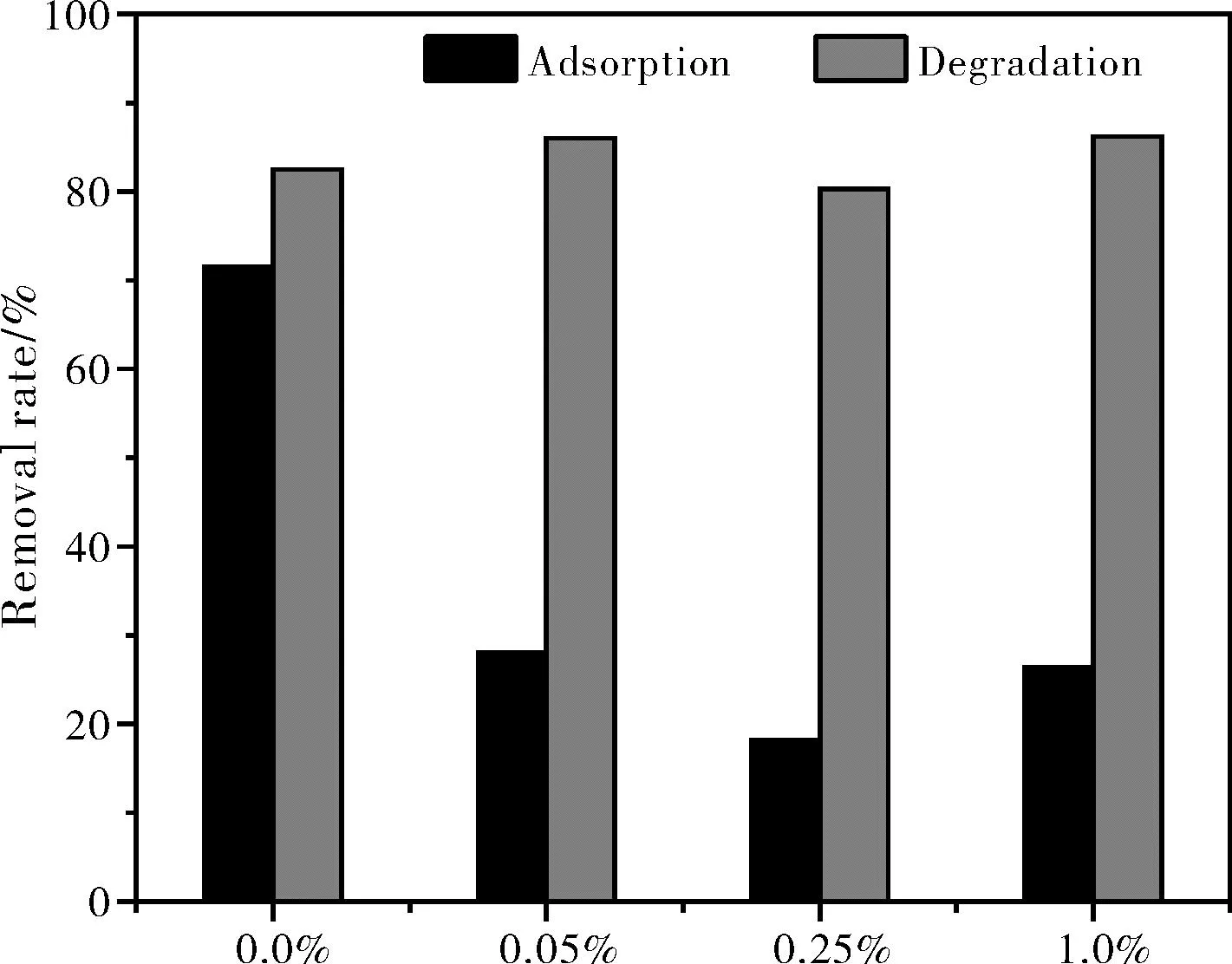
图5 不同Tb掺杂量制备的CeO2催化降解苯甲羟肟酸曲线
3 结 论
利用溶剂热合成法制备Tb/CeO2,利用XRD、SEM以及BET等方法对其进行表征,表征结果显示所制备的Tb/CeO2复合材料的纳米晶体颗粒随Tb掺杂量的增加逐渐团聚,并具有介孔结构,且材料的孔径多集中在2~5 nm;用所制备的Tb/CeO2对选矿药剂苯甲羟肟酸进行光催化降解实验,并用高效液相色谱法进行分析,结果表明,在300 W汞灯照射下,合成的Tb/CeO2对苯甲羟肟酸有明显的光催化降解效果,相对于纯CeO2,光照120 min后,0.25%Tb/CeO2对苯甲羟肟酸的光催化降解效果提升了4.7倍。
