新型生物材料用于年轻恒牙盖髓治疗的疗效观察
2024-01-13李爽英徐明卓
曹 娟,李爽英,徐明卓
年轻恒牙牙髓暴露基本上都是因为龋坏或医源性机械损伤所致,临床治疗的主要方法是直接盖髓术[1]。微创治疗口腔医学理念在近几年得到快速发展,这也极大地改变了儿童牙髓病的传统治疗理念,就是在治疗中尽量保存患儿牙髓活力[2]。良好的封闭性、抗菌性、生物相容性、操作性,同时能够促进组织愈合,是完美活髓保存材料的重要特性[3]。近年来,口腔医学迅速发展,多种盖髓材料应运而生,为牙髓暴露后的治疗提供了更多的选择,其中关注度最高的就是iRoot BP Plus[4],但其价格要高于多数盖髓材料,有待大量临床数据对其疗效进行验证。因此,本研究将iRoot BP Plus用于年轻恒牙直接盖髓术,并重点探究其临床疗效。
1 资料与方法
1.1 一般资料:选择2022年1月至8月到我院儿童口腔科门诊就诊的125例8~12岁年轻恒牙牙髓暴露患儿作为研究对象。按照操作所采用不同类型的盖髓材料,对患儿进行分组。iRoot组45例,其中男性22例,女性20例;三氧化矿物聚合物(MTA)组39例,其中男性20例,女性19例;氢氧化钙组44例,其中男性22例,女性22例。3组患儿一般资料比较,差异无统计学意义(P>0.05)。
1.1.1 纳入标准:①患牙经过去腐质后,肉眼可见露髓点,不过渗血情况并不严重者;②患者经检查无牙髓炎的情况;③临近牙周组织健康者;④在研究前就研究相关信息与患儿及家属进行沟通,其表示无异议,知情且同意,并签字。
1.1.2 标准排除:①热刺激患牙时反馈出现持续性疼痛症状者;②患牙根尖孔闭合者;③患有严重肝、心、肾等器官功能障碍等疾病者;④合并严重的牙周或牙龈疾病者;⑤治疗依存性差者[5]。
1.2 方法:全部入组患儿术前均需进行X线片检查,以此了解其牙齿龋坏深浅、牙周组织状况,同时了解牙根发育状况,患儿家长签署知情同意书。具体操作为实施局部浸润麻醉(碧兰麻),高速手机去除多数腐质,近髓处需要调整为低速球钻,将腐质彻底清理掉,进而让穿髓点完全暴露。①iRoot组处理为在露髓点放置iRoot BP Plus(使用加压器)垂直轻压,厚度1 mm;②MTA组处理为基于3∶1的比例混合MTA,让其充分混匀,在露髓点处以1 mm的厚度轻覆;③氢氧化钙组处理为制备糊剂,在露髓点处以1 mm的厚度轻覆。最后,严密充填所有患牙的冠部,放置Cavition暂封膏,光固化玻璃离子垫底,并以松风树脂充填密实。无菌操作是整个手术过程必须遵循的原则,术后1、3、6、12个月进行临床检查,并采用平行投照法拍摄患牙根尖片完成指标观察。以上操作及X线片检查分别由同一名医生完成。
1.3 观察指标:比较3组患儿直接盖髓后3、6、12个月牙齿完全牙本质桥形成时间、治疗效果、术后12个月发生根管钙化的情况。X线检查进行牙本质桥评估[6]标准为①形成部分牙本质桥,牙本质桥虽然封锁了露髓孔,但是仅封锁了局部,这在一定程度上减小了露髓孔;②形成完全牙本质桥,露髓孔彻底被牙本质桥封锁;③没有形成牙本质桥,治疗前、后露髓孔大小没发生变化。前两类都属于成功病例[1]。完全牙本质桥形成率表示在总体病例中,X线检查显示牙本质桥彻底封锁露髓孔病例的占比。
1.3.1 疗效评价标准:结果判定主要根据每次复查临床检查情况,同时考虑影像学检查所得结果。治疗成功标准[1]为术后未发生预后不良的问题,患儿未有疼痛,咀嚼未有异常,患儿顺利通过牙髓活力测试;叩诊后无不适,牙龈正常,牙齿牢固;通过X片检查排除了患牙病理性吸收,与此同时,检查并没有发现根尖低密度影,无异常根管钙化,而且可以观察到牙根继续发育[5]。治疗失败标准为只要出现了上述症状中的某一项,即表示失败。
1.3.2 分别于术后3、6、12个月复查,观察3组患牙髓腔发生钙化的情况:通过进行X线片检查,对比观察术前与术后12个月,患牙是否出现髓腔及根管变窄,轮廓不清晰的情况。

2 结果
2.1 3组患者年龄和性别构成比较:3组患者平均年龄分别为(10.1±1.2)、(9.7±1.5)和(10.3±0.8)岁,组间比较差异无统计学意义(F=2.705,P>0.05),性别构成组间对比,差异无统计学意义(P>0.05)。
2.2 3组术后疗效评价:术后3、6、12个月复诊,根据上面所提到的治疗成功标准来进行治疗效果情况的记录。治疗成功率比较,相比于氢氧化钙组,更高的2组为iRoot 组、MTA组(P<0.05);对比氢氧化钙组以外的2组,差异无统计学意义,见表1。

表1 3组患者术后近、远期疗效比较[n(%)]
2.3 完全牙本质桥形成时间比较:3组完全牙本质桥形成时间主要集中在行直接盖髓术后3个月。术后3个月内,在形成完全牙本质钙化桥方面,iRoot组、MTA组、氢氧化钙组的比例分别为95.2%、84.6%、54.5%。前2组对比差异无统计学意义(P>0.05)。前2组分别与氢氧化钙组对比,差异有统计学意义(P<0.05 ),见表2。

表2 术后完全牙本质桥形成率组间对比[n(%)]
2.4 术后12个月髓腔钙化发生率的比较:术后12个月患者接受复查,氢氧化钙组以外的2组经X线片检查排除了髓腔钙化,3例根管变窄、边界不清楚主要分布于氢氧化钙组。iRoot组对比氢氧化钙组,差异有统计学意义(χ2= 8.093,P<0.05),见表3。
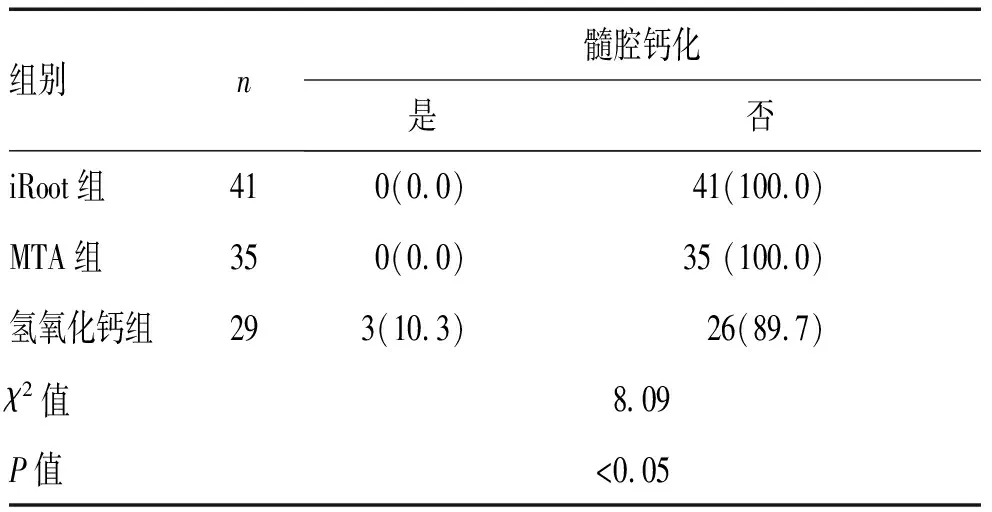
表3 术后12个月髓腔钙化形成率组间对比[n(%)]
3 讨论
年轻恒牙较容易发生龋坏,进而导致牙髓暴露,这与其较薄的牙釉质、较低的矿化度以及较高的溶解度有关,年轻恒牙牙髓含有较多的血管,具有较强的抗病能力、极强的修复功能。对于年轻恒牙深龋露髓患儿通常是以直接盖髓术为其进行治疗。这种技术是在暴露的牙髓创面上直接覆盖盖髓剂,其作用是恢复牙髓组织功能,而盖髓治疗成功的关键在于如何选择盖髓剂,临床最常用到的是MTA和氢氧化钙两类盖髓材料。不过氢氧化钙溶解的概率较高,易导致微渗漏、牙髓退行性变等情况,所以极大地限制了其应用效果[2]。1998年MTA正式被应用于牙髓治疗领域,由FDA审批通过,其在生物相容性、封闭性、抗菌性方面表现极为突出,且容易引导牙本质再生[7]。但也有文献提出,三氧化二铋存在于MTA中,这导致的问题是可引发细胞毒性,调拌后无法迅速硬固,并改变了牙齿的颜色[7],且让患者面临巨大的经济压力。近年来,一些新的生物活性材料应用于临床[8],iRoot BP Plus主要成分有氧化锆、硅酸三钙、磷酸钙和硅酸二钙等,其生物活性、生物相容性以及抗菌性都比较好[4]。
本研究主要目的是对iRoot BP Plus和MTA、氢氧化钙的应用效果进行对比。研究结果显示,iRoot BP Plus与MTA组相比,3、6、12个月治疗效果比较差异无统计学意义。这与iRoot BP Plus良好的抗菌性、生物相容性相关,而且其与牙体组织有黏结性,是非水溶性的,封闭性能良好。同时,与MTA相比,iRoot BP Plus为成品膏剂,不用调拌,操作简便,临床应用较方便。而氢氧化钙物理性能不稳定,发生微渗漏的概率大,因此治疗效果较差。
牙本质钙化桥形成于牙髓受刺激时,属于一种组织愈合现象,可实现对牙髓的保护[9],钙化桥的形成与盖髓剂的性能紧密相关,并对盖髓疗效有显著影响。本研究将iRoot BP Plus、MTA和氢氧化钙分别应用于年轻恒牙深龋露髓患牙,观察牙本质钙化桥形成情况。发现在诱导牙本质钙化桥形成方面,与氢氧化钙相比,iRoot BP Plus与MTA明显较快,多集中在术后3个月,其中,iRoot组有1例、MTA组有2例在术后3个月形成部分牙本质钙化桥,6个月以后形成完全牙本质钙化桥,明显优于氢氧化钙。
本研究结果显示,术后12个月,iRoot组与MTA组均没有出现髓腔钙化,而氢氧化钙组则出现了3例,这与之前将MTA应用于外伤后牙髓切断术的研究结果是一致的[5],也显示出iRoot BP Plus用于年轻恒牙直接盖髓术效果优于氢氧化钙。
本研究结果发现在年轻恒牙直接盖髓术中,与MTA相比,虽然1年内应用iRoot BP Plus的临床疗效、钙化桥形成时间、髓腔钙化发生率没有统计学差异,但MTA价格昂贵,使用需要将粉剂与蒸馏水混合调拌使用,而且临床观察会使牙齿变色,这与文献报道是一致的[10];与氢氧化钙比较,其操作更简便,盖髓后钙化桥形成时间短,且远期不容易发生髓腔钙化,故值得在临床中推广应用。
