HFPO-DA染毒对孕鼠甲状腺内分泌功能的影响
2023-12-14吕娣谭桂玲陈国威刘文东韩文超
吕娣,谭桂玲,陈国威,刘文东,韩文超
(1 青岛大学儿科学专业研究生,山东 青岛 266071; 2 青岛市市立医院; 3 大连医科大学研究生院)
全氟辛酸(PFOA)和全氟辛烷磺酸(PFOS)是最常见的两种全氟烷基化合物(PFASs)[1-2]。鉴于PFOA和PFOS对环境和人类具有不良影响,其生产和使用在全球范围内逐渐受到限制[3]。六氟环氧丙烷二聚体羧酸(HFPO-DA,商品名为GenX)作为PFOA的一种新型替代物而逐渐受到关注。自从2010年开始生产以来,HFPO-DA作为材料制造中新型的加工助剂在世界范围内逐渐被广泛使用。HFPO-DA已在全球范围内的多种物质如地表水、土壤、室内灰尘、农作物、果蔬及海洋动物等中被检测到[4-9],其在水中难以被有效清除且具有蓄积性,这对饮用水的安全是一个巨大的挑战[10]。目前,HFPO-DA已在人类和动物血清中被检测到[11-12]。毒理学研究显示,HFPO-DA可能具有与PFOA相似的毒性作用[13],对动物生长发育、代谢、肝脏以及心脏等具有毒性作用[14-18]。然而,HFPO-DA对甲状腺毒性的研究却鲜有报道。本研究以SD大鼠为受试对象,研究不同剂量HFPO-DA孕期染毒对SD大鼠甲状腺组织形态、分泌功能以及子代生长发育的影响,为探讨HFPO-DA是否为内分泌干扰物提供基础资料,为评估其对人体健康的风险提供理论支持。
1 资料与方法
1.1 试剂和仪器
主要试剂:HFPO-DA(纯度≥97%,上海麦克林生化科技有限公司); 40 g/L多聚甲醛溶液(Sigma-Aldrich,USA);促甲状腺激素(TSH)、总四碘甲状腺原氨酸(TT4)、总三碘甲状腺原氨酸(TT3) 酶联免疫吸附试剂盒(江苏晶美生物有限公司);内标贮备液(Sigma-Aldrich,USA);内标13C4-PFOA (Sigma-Aldrich,USA);甲醇、乙腈(Merck Drugs &Biotechnology,Germany)。 主要仪器:低温冷冻离心机(Thermo Scientific);-80 ℃超低温冰箱(Thermo Scientific);超声仪(KQ3200DE,昆山超声仪器有限公司); 高效液相色谱-串联质谱仪(Agilent Technologies Inc,USA);SQP 电子分析天平(Sartorius, Germany);数码照相机(Cannon,EOS R6)。
1.2 实验动物
选择10周龄雄性和雌性SPF级别SD大鼠各32只,体质量250~270 g,由济南朋悦实验动物繁育有限公司提供。SD大鼠饲养在带有灭菌垫料的聚丙烯笼中,室内温度为(23±1)°C,光照明暗周期为12 h-12 h。本文实验获得青岛市市立医院伦理委员会的批准。
1.3 实验方法
1.3.1实验动物分组及处理 10周龄SD大鼠适应性饲养1周后,将雄雌大鼠按照1∶1合笼交配,次日清晨6:00检查雌鼠阴道,有阴栓者或阴道涂片显微镜下可观察到精子者定义为妊娠0.5 d(GD0.5)。将GD 0.5孕鼠随机均分为对照组(去离子水)和HFPO-DA低剂量组(1 mg/kg)、中剂量组(10 mg/kg)、高剂量组(100 mg/kg),每组8只。用去离子水和HFPO-DA配制HFPO-DA溶液,在孕鼠妊娠0.5~19.5 d期间每日固定时间段(8:00-10:00)称体质量,然后通过经口灌胃的方式给予孕鼠HFPO-DA水溶液进行染毒。实验期间,大鼠自由摄食、饮水。
1.3.2标本的采集与处理 孕鼠妊娠19.5 d灌胃2 h后,给予100 g/L的水合氯醛麻醉,心脏采血后断头处死孕鼠,4 ℃下以2 500 r/min离心15 min,取上清液,-80 ℃储存,用于HFPO-DA血清浓度分析;取孕鼠甲状腺称质量,40 g/L多聚甲醛溶液固定,用于甲状腺组织的形态学观察;剖腹取胎鼠称体质量,数码相机拍照,使用Image J软件测量胎鼠身长和尾长。
1.3.3孕鼠血清HFPO-DA浓度检测 使用高效液相色谱-串联质谱法检测孕鼠血清中HFPO-DA的浓度。按照参考文献方法[19]进行操作。
1.3.4孕鼠血清TSH、TT3、TT4的浓度测定 将-80 ℃冷冻的血清样品解冻,应用酶联免疫吸附试剂盒测定血清中TSH、TT4、TT3浓度,按试剂盒说明书方法进行操作。
1.3.5孕鼠甲状腺组织形态学观察 取40 g/L多聚甲醛固定的甲状腺组织,乙醇脱水后,石蜡包埋,5 μm厚切片,苏木精-伊红(HE)染色,光学显微镜下观察甲状腺组织的形态学变化。
1.4 统计学处理

2 结 果
2.1 各组胎鼠生长发育情况比较
各组胎鼠出生时均存活且无发育畸形。与对照组比较,HFPO-DA中剂量和高剂量组胎鼠的出生体质量、身长降低(F=8.26、38.64,P<0.05),高剂量组尾长降低(F=8.61,P<0.05)。孕鼠产胎鼠量各组差异无统计学意义(P>0.05)。见表1。

表1 各组胎鼠生长发育比较
2.2 各组孕鼠血清HFPO-DA浓度比较
经过孕期19.5 d的染毒,孕鼠血清中HFPO-DA的浓度与染毒剂量呈正相关关系。孕鼠血清中HFPO-DA的浓度为非正态分布,低、中和高剂量组中HFPO-DA的中位浓度(M)分别为0.15、0.57和3.92 mg/L,下四分位数(P25)浓度分别为0.14、0.53和3.74 mg/L,上四分位数(P75)浓度分别为0.18、0.59和4.12 mg/L。见图1。

图1 各组孕鼠血清中HFPO-DA浓度
2.3 各组孕鼠血清TSH、TT3、TT4水平和TT3/TT4比值比较
经孕期19.5 d的染毒后,与对照组比较,中剂量和高剂量组TSH浓度均显著升高,差异有统计学意义(t=11.17、12.17,P<0.05),高剂量组血清TT3浓度和TT3/TT4比值显著升高(t=5.07、8.65,P<0.05);各组孕鼠血清TT4浓度差异无显著性(P>0.05)。见图2。
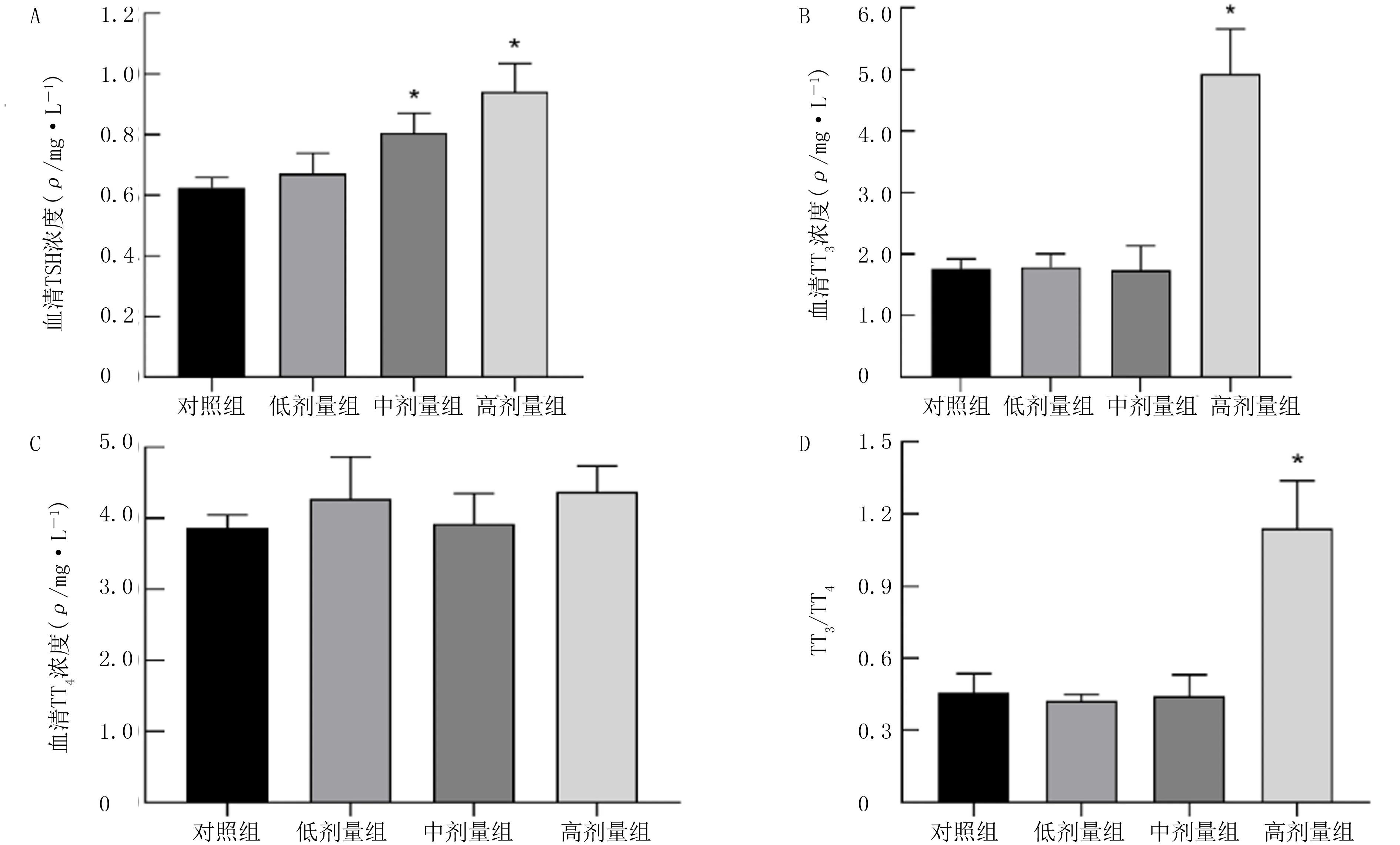
A:各组TSH水平比较;B:各组TT3水平比较;C:各组TT4水平比较;D:各组TT3/TT4比值比较。与对照组比较,*P<0.05。
2.4 各组孕鼠甲状腺组织形态比较
HE染色观察显示,对照组孕鼠甲状腺滤泡大小较为均一,滤泡腔内胶质充盈、均匀(图3A);低剂量组和中剂量组孕鼠甲状腺组织未发生明显的形态学改变,呈现大致正常的甲状腺结构(图3B和3C);高剂量组孕鼠甲状腺滤泡出现形态学变化,部分滤泡增生活跃,滤泡腔变小,胶质减少(图3D)。
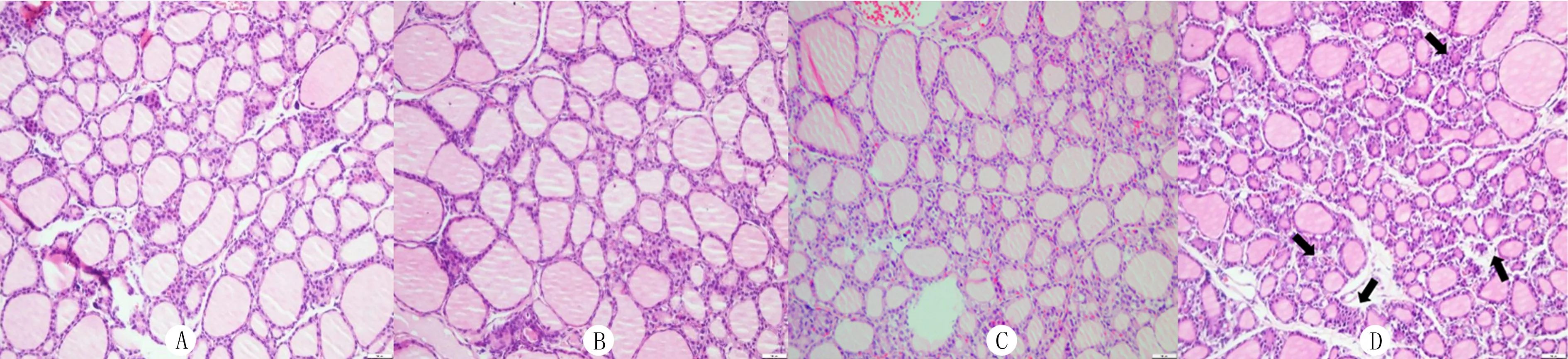
A:对照组;B:低剂量组;C:中剂量组;D:高剂量组,孕鼠部分甲状腺滤泡腔变小,胶质减少(黑色箭头所示)。HE染色,200倍。
3 讨 论
HFPO-DA作为PFOA的替代物已在全世界范围内被广泛应用,但是其环境持久性和生物蓄积性以及生态毒性应引起重视。目前,HFPO-DA已在人类和动物血清中被检测到,孕妇及胎儿作为易感人群,HFPO-DA对其毒性作用受到了高度关注。本研究结果显示,孕期中剂量和高剂量HFPO-DA染毒可使胎鼠出生体质量和出生身长显著下降,而高剂量染毒可导致胎鼠尾长缩短。BLAKE等[14]研究显示,CD-1小鼠整个孕期(0.5~17.5 d)暴露于10 mg/kg的HFPO-DA,可导致胎儿出生体质量下降。CONLEY等[18]关于SD大鼠孕期(14~18 d)HFPO-DA染毒研究显示,暴露剂量≥30 mg/kg时胎鼠出生体质量下降,孕鼠血清中HFPO-DA的浓度≥10 mg/L胎鼠出生时的死亡率会增加。本研究结果与其一致。本研究结果显示,高剂量组孕鼠血清中HFPO-DA浓度中位数仅为3.92 mg/L,同时也未发现胎鼠死亡率的增加。既往有研究结果显示,宫内暴露PFASs不仅严重影响新生胎鼠的存活率,而且会导致存活幼鼠生长发育迟缓并伴有高甲状腺素血症[20]。
甲状腺素(THs)对生长发育、生殖繁育及能量代谢等生理过程具有重要的调节与控制作用。甲状腺受下丘脑-垂体-甲状腺轴的调节,通过下丘脑合成促甲状腺激素释放激素,刺激垂体产生TSH,从而促进甲状腺合成T4和T3。动物研究表明,PFOA染毒导致血清T3和(或)T4降低[21],并且T4降低的程度更加明显[22]。挪威的两项人群研究结果显示,血清中PFOS每增加1 ng,孕妇TSH水平将增加0.8%[23-24]。有两项研究探讨了HFPO-DA染毒对THs水平的影响,其结论完全相反。其中CONLEY等[18]研究显示,大鼠孕期HFPO-DA染毒剂量≥30 mg/kg,会显著降低其血清中TT3的水平;而染毒剂量≥125 mg/kg时,TT4水平降低。然而,BLAKE等[14]对CD-1小鼠研究却发现,孕期小鼠HFPO-DA染毒增加了胎盘中TT4水平。本研究结果表明,高剂量组孕鼠血清TT3和TSH水平均显著增加,血清TT3、TT4和TSH之间未发现负反馈调节。导致不同研究结果不同的原因尚不清楚。既往关于PFASs甲状腺毒性的机制研究也尚未得出一致的结论,认为PFASs通过以下机制发挥作用:①与TSH受体直接相互作用,对TSH依赖的信号通路产生不同的影响[25];②影响T4从肝脏摄取和排出的关键肝脏转运蛋白的活性[26];③影响甲状腺中将T4转化为T3的碘甲腺原氨酸脱碘酶Ⅰ的浓度[27]等途径导致T3、T4、TSH的调节紊乱。
甲状腺组织的基本结构和功能单元是甲状腺滤泡,滤泡的结构改变可作为甲状腺功能的指标。本文研究结果显示,高剂量组孕鼠的甲状腺组织结构发生明显的变化,其部分滤泡腔变小,腔内胶质减少,这说明甲状腺功能相对活跃,与TT3水平增加相吻合。提示HFPO-DA对甲状腺组织产生了损伤作用。目前有两项细胞水平研究认为,HFPO-DA能够导致甲状腺细胞活性和增殖能力的降低,但其机制不一致。COPERCHINI等[28]研究结果显示,HFPO-DA能够促进甲状腺细胞DNA损伤,并影响甲状腺转录因子基因的表达;而另有研究则认为HFPO-DA作用主要是导致THs合成相关的基因异常表达。目前尚无体内研究探讨HFPO-DA的甲状腺毒性作用的可能机制。
综上,高剂量(100 mg/kg)HFPO-DA染毒可以损伤孕鼠甲状腺组织及影响机体内甲状腺激素的水平,进而导致子代胎鼠宫内生长发育落后。有关HFPO-DA对甲状腺内分泌功能干扰效应的机制还需进一步深入研究。
