核壳结构ZnS纳米颗粒协同碳毡提升锌离子电池的能量密度
2023-11-03刘国珏赖中元李小成
刘国珏,刘 涛,赖中元,李小成
(1.江西理工大学材料冶金化学学部,江西赣州 341000;2.江西理工大学江西省动力电池及材料重点实验室,江西赣州 341000)
由于水系电池固有的安全性以及金属锌价格低和较高的理论容量等优点,以金属锌为负极的水系锌离子二次电池在大规模储能领域吸引了众多学者的研究兴趣。目前为止,有多种金属锌电池已经成功商业化,如Zn-MnO2干电池[1]、Zn-Ag2O2电池、锌空气电池[2]等。然而,上述电池受到相对较低的理论容量或较高的价格的限制,不足以满足人们日益增长的需求,探索一种新型阴极材料显得尤为重要。
硫元素是天然气、石油和其他矿物生产提纯过程中产生的副产物之一,但目前对于这些副产物的应用并不足以消耗所有硫元素,价格仅为MnO2的十分之一。硫拥有极高的理论比容量(1 675 mAh/g)以及独特的双电子转移反应,这些特点使硫成为水系锌离子电池应用中极具吸引力的正极材料之一。
目前已经有多人研究基于硫正极的二次电池,如碱性Al-S 电池[3]、Mg-S 电池[4]和水系电解质的Na-S 电池[5],证明了硫正极在二次电池中拥有巨大的潜力。本文使用ZnS 作为正极材料,金属锌作为负极,构建具有高能量密度的Zn-S 电池体系,并使用碳毡[6]延缓正极材料的溶解。
1 实验
1.1 材料制备
ZnS 的制备:首先将0.5 g 壳聚糖溶解在40 mL 冰醋酸水溶液[0.6%(质量分数)]中并搅拌30 min,随后将30 mmol 的Zn(NO3)2和45 mmol 硫代乙酰胺(TAA)溶于20 mL 去离子水中。将完全溶解的Zn(NO3)2与TAA 溶液缓慢倒入壳聚糖溶液中,并保持搅拌30 min。将获得的透明溶液转移到100 mL聚四氟乙烯内衬不锈钢高压釜中,加热至160 ℃并保温12 h,冷却至室温后,用真空抽滤泵抽滤并用去离子水和无水乙醇洗涤三次,并在60 ℃真空干燥箱中干燥12 h,在500 ℃下用管式气氛炉在氩气气氛中保温2 h,升温速率为3 ℃/min,最终得到纳米ZnS 正极材料。
核壳结构ZnS@C 的制备:将获得的ZnS 纳米材料在氩气和乙炔(体积比1∶3)混合气体中退火。化学气相沉积(CVD)过程中的总气体流量恒定保持在24 mL/min。在500 ℃下加热10 min,在此期间乙炔(C2H2)气体作为碳源,以包覆ZnS 纳米颗粒。在纯氩气(Ar)气氛中加热至600 ℃并保温2 h,除去材料中的结晶水,获得核壳结构的ZnS@C。
碳毡(CF)的制备:将普通的商业宣纸用于碳化处理,在Ar 气氛中加热至900 ℃保温3 h 后,得到产物CF,制备的CF的面密度约为1.03 mg/cm2。
1.2 材料结构与形貌表征
采用德国Bruker D8 Advance 型转靶衍射仪进行X 射线衍射(XRD)分析。采用德国蔡司ZEISS EVO/MA10 型扫描电镜(SEM)及牛津能谱仪(EDS)对材料进行表面形貌观察和元素分布分析;采用美国Thermo escalab 250xi 型X 射线光电子能谱仪(XPS)进行XPS 元素分析。
1.3 电化学性能测试
实验通过纽扣电池(CR2032 型)来评估制备正极材料的电化学性能。以9∶1 的质量比将活性物质和聚偏二氟乙烯(PVDF)混合并分散在N-甲基吡咯烷酮(NMP)中,随后涂覆到直径为12 mm 的碳纸上并在60 ℃的真空烘箱中干燥12 h 来制备正极极片。0.05 mm 厚的锌箔作负极,玻璃纤维作隔膜,1 mol/L Zn(CH3COO)2水溶液作电解质,自然环境下组装锌离子电池。在新威电池测试柜上测试其电化学性能,测试条件为:25 ℃,恒流充放电测试,电压范围为0.25~1.6 V。使用电化学工作站(CHI 660E)测试电池的电化学阻抗谱(EIS)。
2 结果与讨论
2.1 材料结构与形貌分析
采用溶剂热法制备得到ZnS 纳米颗粒并对其使用CVD进行碳包覆后得到样品ZnS@C,对样品ZnS 进行X 射线衍射检测,结果如图1 所示,样品ZnS 纳米颗粒在28.5°、47.4°、56.3°存在衍射峰,这些峰在角度与峰强度上都能够与ZnS(PDF#77-2100)的(111)、(220)、(311)晶面匹配且其中无杂峰出现,表示成功制备出结晶性较高的纯相ZnS 纳米颗粒。
ZnS 纳米颗粒材料表面形貌如图2 所示,图2(a)为采用溶剂热法合成的ZnS 纳米颗粒,多数呈现为较不规则的颗粒状,粒径约为50~100 nm,少量ZnS 纳米颗粒粒径1~5 μm 且呈现团聚状态,其中多数为不规则形状团聚,少量为规则球状团聚。ZnS 纳米颗粒进行CVD 包覆碳层后形貌如图2(b)所示,ZnS@C 颗粒尺寸较为均匀,粒径无明显的增加(图2(b)中小图为团聚后的ZnS@C 纳米颗粒)。图2(c)为ZnS@C 纳米颗粒进行团聚后的形貌,选取规则球状团聚部分进行EDS 能谱元素分析,通过测量CVD 前后材料的质量变化,计算出所得ZnS@C 纳米复合材料中的碳含量约为15%(质量分数),结合EDS 能谱测试结果,表明Zn、S、C 三种元素在样品里分布均匀,已经对ZnS 纳米颗粒成功进行碳包覆,获得产物ZnS@C。
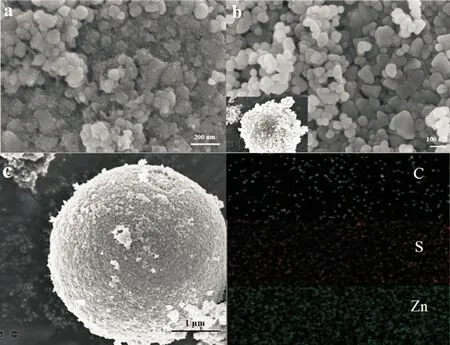
图2 ZnS 纳米颗粒(a)、ZnS@C纳米颗粒的SEM图像(b)以及放大后的ZnS@C纳米颗粒的SEM图像与EDS能谱元素分析图(c)
由于ZnS 在电化学反应过程中存在活性物质溶解、电导率较差等问题,所以引入碳毡以期改善ZnS 的电化学性能。碳毡的表面形貌如图3 所示,碳纤维导电网络上分布着氧化物颗粒,结合EDS 能谱测试结果可知,CF 中存在大量Si、O、Ca 等元素并且均匀地分布在CF 表面。进行元素分析后,这些元素约占CF 的10%(质量分数)。所有这些金属[7]或非金属氧化物[8]是通过宣纸特殊制造工艺遗留的,可作为硫化物吸附剂[7,9]引入正极材料或者改性隔膜。CF 对电池体系的提升优化作用在电化学性能分析中验证。本文采用制备ZnS@C复合材料并协同碳毡为抑制正极材料溶解的优化手段,以期得到优良电化学性能的锌离子电池。
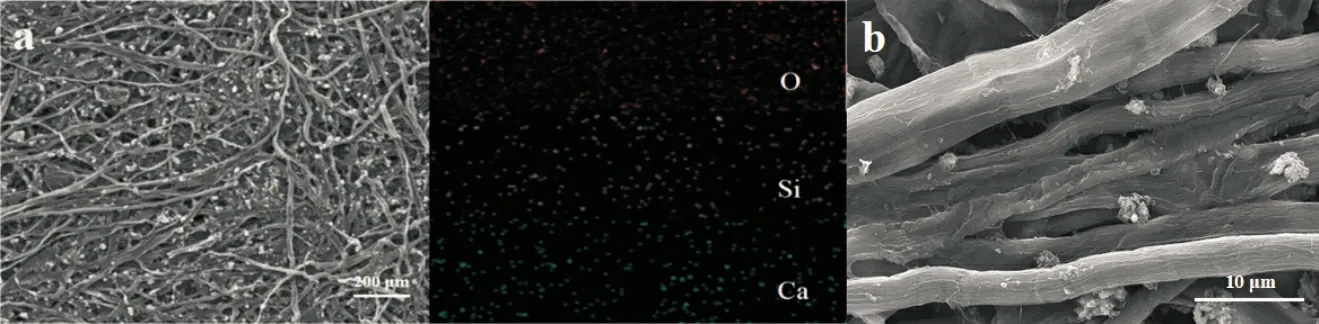
图3 CF的SEM与EDS图像(a)以及高倍数下CF的SEM图像(b)
2.2 电化学性能分析
尽管Zn-S 电池体系能够提供较高且可逆的容量,虽然简单的硫碳复合材料的导电性有所提升,但存在较强的电压滞后效应。图4(a)是添加CF 的ZnS@C 纳米材料、S@科琴黑(KB)硫碳复合材料、采用Li 等[10]报道的S@CNTs 复合方法所制备的材料作为正极材料,组装成电池后的首次充放电曲线对比图。S@KB 复合材料的电压滞后大于1 V,S@CNTs 复合材料经过改性后存在0.584 V 的电压滞后,ZnS@C 复合材料在加入碳毡后电压滞后仅为0.437 V,在不引入I2的情况下降低了电压滞后效应,提升了放电电压平台。这归因于纳米颗粒包覆了碳膜,形成了优良的导电网络,不仅优化了正极材料电导率,还缓解了ZnS 导电效率低所导致的离子传输效率低,有效地优化了电压滞后效应。ZnS@C 加入碳毡后放电平台为0.75 V,首次放电比容量为1 357 mAh/g。除去图4(d)中所知的CF 提供比容量后,首次放电比容量为1 307 mAh/g,比能量为976.5 Wh/kg,远高于锌离子电池正极材料MnO2(~370 Wh/kg)[11]与锂离子电池正极材料NCM811(~485 Wh/kg)[12]。
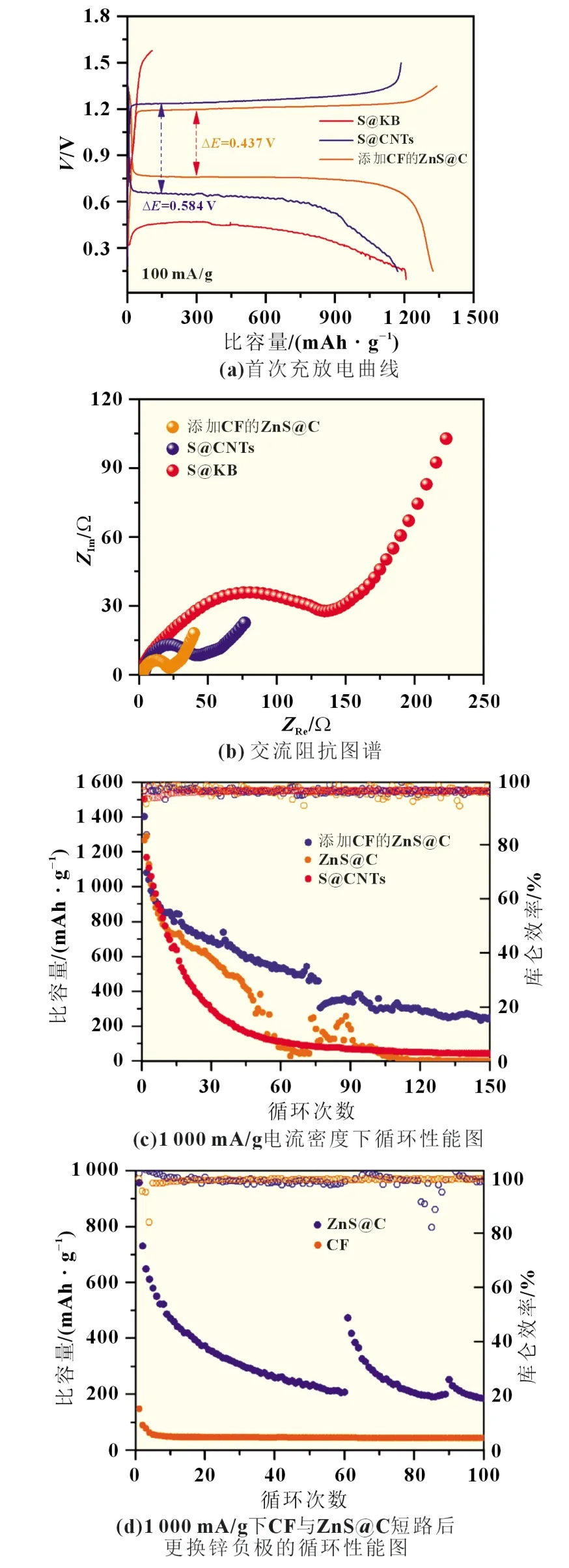
图4 S@KB、S@CNTs、添加CF的ZnS@C 首次充放电曲线、交流阻抗谱图与1 000 mA/g电流密度下循环性能图以及CF与ZnS@C短路后更换锌负极的循环性能图
复合材料的不同电压可归因于复合材料的不同界面电荷转移电阻(Rct),其中ZnS@C 的Rct最低,如图4(b)所示,因为低Rct有利于电池反应动力学[13]。如图4(c)所示,未进行改性的硫基正极材料循环稳定性有待提高。如图5(b)所示,电池体系中只有正极极片在含有硫元素的前提下,通过EDS 能谱测试得知负极区域存在硫元素,佐证了ZnS 会在电化学反应中溶解。因此,硫基水系电池在循环中会造成容量损失,CF中含有的金属及非金属氧化物可以起到锚定硫化物中S2-的作用[14],降低ZnS 与水的反应速率,延缓正极材料的不可逆损失。如图4(c)所示,添加CF 夹层的ZnS@C 正极材料组成的电池首次放电比容量为1 403.13 mAh/g,循环至第75 次放电比容量为459.75 mAh/g,在第76 次循环时发生了短路,更换隔膜与CF 后损失了部分被锚定在CF 上的ZnS,所以电池比容量下降(第76 次循环放电比容量为306.89 mAh/g),同时,硫正极在中性电解质中拥有更高的稳定性和更低的电压滞后效应,因为硫化物在酸性环境中容易发生歧化反应[10],会造成容量的损失。而ZnS 与水反应生成的SO42-会增加电解液的氢离子浓度。图4(c)中添加CF 夹层的ZnS@C 与图4(d)中未添加CF 的ZnS@C 都更换了锌箔和电解液,前者同时更换了CF,因为CF 表面锚定有ZnS 活性物质,所以前者的容量降低;后者仅更换电解液,改善了因ZnS 溶解造成的电解质酸化,容量有所回升(第60 次循环放电比容量为201.44 mAh/g)。正极材料的溶解会导致活性物质质量减少,重组后的电池在第61 次放电比容量为476.73 mAh/g。
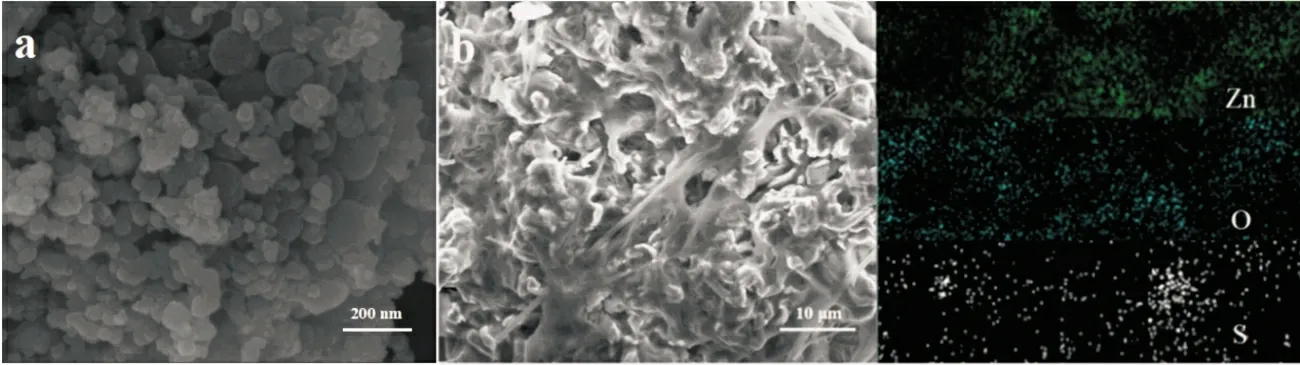
图5 循环后ZnS@C 的SEM图(a)与循环后锌负极的SEM与EDS图像(b)
图5(a)为ZnS@C 循环60 次后的极片形貌,图中有较多规则球形与小粒径颗粒,表明ZnS 与水发生反应后溶解,使ZnS的形貌发生改变,称量得知极片质量减少15.4%;再次组成电池进行测试,其比容量保持率为首次的42.5%,如图4(d)所示。图5(b)为对循环后的Zn 负极极片进行EDS 能谱元素分析结果,电池体系中只有ZnS 正极材料拥有硫元素的前提下,EDS 能谱元素分析检测出Zn 负极极片含有大量S 元素,证明ZnS 正极材料会在电化学反应中溶解至电解液中且迁移至负极区域。
2.3 电化学机理分析
制备ZnS@C 正极极片,将极片样品用于组装纽扣电池并充电至1.6 V,对ZnS@C 正极极片进行X 射线衍射检测,测试结果如图6(a)所示,ZnS 的特征峰消失,同时在26.6°出现集流体碳纸C(PDF#26-1076)特征峰,表明反应生成的S 为非晶态。将样品放电至0.5 V 时,在28.5°、47.4°、56.3°重新出现ZnS 的衍射峰;样品放电至0.25 V 时,ZnS 的衍射峰峰强度增强,C的衍射峰强度不变。上述测试结果说明ZnS 在充电过程中会逐渐转化为非晶态的S 单质,放电过程中S 单质逐渐还原为ZnS,由此可证明Zn-S 电池体系中的电化学反应可双向进行。

图6 ZnS@C样品以及充放电后极片的XRD 图谱、ZnS@C极片充电后的X 射线光电子能谱图与ZnS@C样品、充放电后极片、循环后电解液的X射线光电子能谱图
对样品ZnS@C 的S 2p 和Zn 2p 轨道进行XPS 能谱分析,观察样品以及电解液进行充电后的变化。如图6(b)所示,ZnS@C 样品在结合能为1 022.4 和1 046.1 eV 处可以观测到Zn2+的两个强峰,充电至1.6 V 后,峰强度减弱,表明Zn2+的脱出过程。
如图6(c)所示,对ZnS@C 样品的XPS 检测中,结合能为161.9 和163.1 eV 处出现明显的S2-峰值[15],材料充电至1.6 V时,S2-的峰强度减弱。放电至0.25 V 时,S2-峰强度增强,说明S2-在充放电过程中为可逆反应;电解液样品的检测中,在168.9 eV 处出现了S6+的特征峰[16],表明材料中S 元素可被氧化为SO42-。没有其他价态的S 能证明在电化学反应中不存在ZnSx。上述XPS 测试结果揭示了ZnS@C 的容量衰减机制:形成SO42-的反应一旦完成,其中的S 元素不再参与后续电化学反应,降低了电极反应的可逆性;副反应中,水也会参与电化学反应,反应过程如下:
放电过程:
充电过程:
副反应所产生的SO42-在形成后会溶解在水性电解质中,进一步导致电池容量下降。因此,通过优化合成策略以减少复合材料暴露在电解液中的几率、减缓ZnS 与水的反应速率、降低电解液中溶解的O2浓度都有利于提高锌硫电池循环性能。
3 结论
通过溶剂热法制备了ZnS 纳米颗粒,随后在Ar-C2H2气氛中对其进行核壳结构的碳包覆,制备出了ZnS@C 纳米材料。ZnS@C 纳米颗粒在还原成S 后依旧为纳米级,较小的粒径能避免大颗粒中心无法参与反应造成的容量损失,并且在碳层的保护下ZnS 减少了与水的接触,使容量衰减得以延缓。碳层还能为纳米级的S 之间增加导电网络,从而节省了导电剂的添加,进一步降低了成本,最终制备得到高比能量(976.5 Wh/kg)、低成本的水系锌离子电池。
用简单方式制备碳毡,并通过CF 夹层的加入进一步延缓了ZnS 与水进行反应,并且能够提升锌硫电池中的反应动力,显著降低电压的滞后效应,在100 mA/g 的电流密度下从未改性的大于1 V 降低至0.437 V,使锌硫电池体系的能量密度提高60%以上。研究表明,核壳结构ZnS@C 在碳毡的协同作用下延缓ZnS 与水反应的方法为锌离子硫基电池正极材料的改性提供了一种新的思路。
