不同TNM分期老年直肠癌术后患者血清黏蛋白-1、胸苷激酶1水平变化及临床意义
2023-10-19燕启田
燕启田
(商丘市第四人民医院检验科,河南 商丘 476000)
直肠癌是临床常见恶性肿瘤,好发于40岁以上中老年人,尤其是老年群体身体机能逐渐退化,更易患病,其在消化道恶性肿瘤发病率、死亡率中高居第2位,严重威胁人类健康[1]。随着腹腔镜结直肠癌根治术不断进步与完善,已能较好清除病灶,但直肠癌仍然是全球60~79岁患者癌症相关死亡的第二大原因,也是80岁及以上患者死亡的第三大原因[7]。因此,积极探究如何准确评估直肠癌术后预后情况意义重大。
腹腔镜结直肠癌根治术是临床针对直肠癌的常用治疗方式,具有创伤小、康复快、并发症少等优势,但由于直肠血供丰富且直肠癌细胞易转移等特点,术后仍有较高复发转移风险[2]。因此,探究直肠癌术后预测复发转移的生物标志物,对早期准确评估预后以及时进行干预治疗具有重要意义。
黏蛋白-1(MUC-1)是一种大分子糖蛋白,可参与细胞黏附及迁移过程[3]。胸苷激酶1(TK1)可介导实体肿瘤细胞增殖分化[4]。由此,推测上述指标可能有助于评估老年直肠癌术后预后情况。因此,本研究拟比较不同TNM分期老年直肠癌术后患者血清MUC-1、TK1水平变化,并探究其临床意义。
1 资料与方法
1.1 一般资料
经我院伦理委员会审批通过,选取2018年3月至2021年12月期间于我院行腹腔镜结直肠癌根治术治疗且均完成随访的78例老年直肠癌患者作为研究对象。纳入标准:①符合直肠癌相关诊断标准[5];②年龄≥60岁;③均行腹腔镜结直肠癌根治术;④患者及家属了解本研究内容(已签署同意书)。排除标准:①其他恶性肿瘤;②心、肝等功能障碍;③精神疾病;④中途退出者;⑤凝血功能障碍;⑥临床资料不完整。
根据入院时TNM分期的不同将患者分为I~Ⅱ期组(32例)和Ⅲ~Ⅳ期组(46例)。其中I~Ⅱ期组男21例,女11例;年龄60~83岁,平均(66.37±3.18)岁。Ⅲ~Ⅳ期男29例,女17例;年龄61~84岁,平均(67.04±3.01)岁。两组间性别、年龄均衡可比。
1.2 方法
1.2.1 血清黏蛋白-1、胸苷激酶1水平检测方法
分别于术前、术后1 d、术后3 m、6 m采集患者外周肘静脉血(空腹)5 mL,采用TD5A自动脱盖离心机(厂家:长沙英泰)离心(半径10 cm,转速3000 r·min-1,时间10 min)处理,采集血清,以酶联免疫吸附法(试剂盒厂家:武汉莱瑞特)检测血清MUC-1水平,采用酶免疫点印迹化学发光法(试剂盒厂家:上海康朗生物)检测血清TK1水平。检测操作均严格按照相关试剂盒说明书进行。
1.2.2 复发情况
术后随访1年,根据术后1年复发转移情况,将患者分为复发转移患者和未复发转移患者。
1.3 观察指标
(1)分析比较不同分期患者的临床资料;(2)分析比较复发转移和未复发转移患者的血清MUC-1、TK1水平;(3)分析术前血清MUC-1、TK1水平与TNM分期之间相关性;(4)分析血清MUC-1、TK1水平联合预测术后复发转移的价值。
1.4 统计学方法
以SPSS22.0对结果进行分析。计量资料以平均数±标准差(±SD)表示、行t检验。相关性采用Spearman或Pearson分析。受试者工作特征(ROC)曲线及曲线下面积(AUC)评价预测价值。P<0.05表示差异有统计学意义。
2 结果
2.1 两组血清MUC-1、TK1水平比较
2组术前血清MUC-1、TK1水平比较,Ⅲ~Ⅳ期组血清MUC-1、TK1水平高于Ⅰ~Ⅱ期组,差异有统计学意义(P<0.05)。见表1。
表1 2组血清MUC-1、TK1水平比较(±SD)

表1 2组血清MUC-1、TK1水平比较(±SD)
组别 n MUC-1(U·mL-1) TK1(pmol·L-1)Ⅰ~Ⅱ期组 32 21.68±4.19 3.25±0.74Ⅲ~Ⅳ期组 46 37.91±5.03 8.64±1.17 t 14.984 23.028 P <0.001 <0.001
2.2 复发转移和未复发转移患者血清MUC-1、TK1水平比较
术前、术后1 d 2组血清MUC-1、TK1水平比较,差异无统计学意义(P>0.05);与未复发转移患者相比,术后3 m、6 m复发转移患者血清MUC-1、TK1水平较高(P<0.05)。见表2。
表2 复发转移和未复发转移患者血清MUC-1、TK1水平比较(±SD)
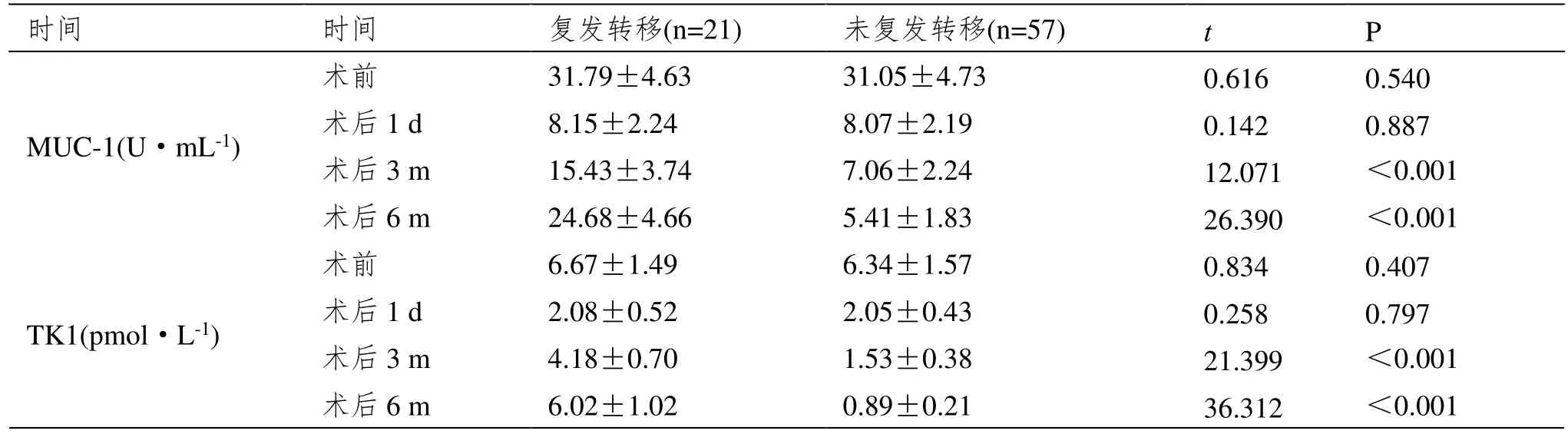
表2 复发转移和未复发转移患者血清MUC-1、TK1水平比较(±SD)
时间 时间 复发转移(n=21) 未复发转移(n=57) t P MUC-1(U·mL-1)术前 31.79±4.63 31.05±4.73 0.616 0.540术后1 d 8.15±2.24 8.07±2.19 0.142 0.887术后3 m 15.43±3.74 7.06±2.24 12.071 <0.001术后6 m 24.68±4.66 5.41±1.83 26.390 <0.001 TK1(pmol·L-1)术前 6.67±1.49 6.34±1.57 0.834 0.407术后1 d 2.08±0.52 2.05±0.43 0.258 0.797术后3 m 4.18±0.70 1.53±0.38 21.399 <0.001术后6 m 6.02±1.02 0.89±0.21 36.312 <0.001
2.3 血清MUC-1、TK1水平与TNM分期的相关性分析
相关性分析结果显示,术前血清MUC-1、TK1水平与TNM分期呈正相关(TNM分期赋值:I期=1,Ⅱ期=2,Ⅲ期=3,Ⅳ期=4;r1=0.687,P1<0.05;r2=0.624,P2<0.05)。
2.4 血清MUC-1、TK1水平联合预测术后复发转移的价值分析
以术后复发转移患者为阳性标本,以术后未复发转移为阴性样本,绘制ROC曲线。结果显示,术后3 m血清MUC-1、TK1水平联合预测术后复发转移的AUC为0.731,最佳敏感度、特异度分别为80.95%、64.91%;术后6 m血清MUC-1、TK1水平联合预测术后复发转移的AUC为0.829,最佳敏感度、特异度分别为95.24%、70.18%。见表3。

表3 ROC分析
3 讨论
随着腹腔镜结直肠癌根治术不断进步与完善,已能较好清除病灶,但直肠癌仍然是全球60~79岁患者癌症相关死亡的第二大原因,也是80岁及以上患者死亡的第三大原因[6]。因此,积极探究如何准确评估直肠癌术后预后情况意义重大。
MUC-1由黏膜上皮分泌,多分布于呼吸道、胃肠道等组织上皮中,可保护、润滑黏膜。但当机体发生炎症及癌变时,可呈现异常高表达状态[7]。研究发现,卵巢癌与卵巢良性肿瘤患者病灶组织中MUC-1阳性表达率差异显著,且与肿瘤恶性程度呈正相关[8]。研究表明,MUC-1可通过调控上皮间质转化、肿瘤细胞增殖等过程,促使肿瘤免疫逃逸,诱导癌细胞转移[9]。
本研究结果显示,术前Ⅲ~Ⅳ期组血清MUC-1水平高于I~Ⅱ期组,且其表达水平与TNM分期呈正相关(P<0.05)。由此可见,MUC-1可直接影响直肠癌患者肿瘤侵袭浸润过程,提高肿瘤恶性程度。且经相关性分析发现,其表达水平与TNM分期呈正相关。分析其原因在于,TK1可诱导胸苷嘧啶核苷酸向单磷酸胸腺嘧啶转化,随细胞增殖其表达水平逐渐上升,促使肿瘤细胞增殖分化,增加肿瘤转移及浸润程度[10]。
本研究还发现,术后3 m、6 m复发转移患者血清MUC-1、TK1水平高于未复发转移患者。提示血清MUC-1、TK1水平可能与直肠癌患者术后复发转移关系密切。其原因在于,血清MUC-1、TK1水平异常高表达可诱导肿瘤细胞增殖分化,促使肿瘤细胞侵袭浸润,进而增加直肠癌患者术后复发转移风险。进一步通过ROC分析发现,术后3 m、6 m血清TK1水平单独预测直肠癌术后复发转移的AUC分别为0.628、0.692,预测效能较差。但袁颖等[11]研究显示,血清TK1水平单独预测老年直肠癌患者化疗后预后情况的AUC为0.801,具有较高预测效能。与本研究结果存在一定差异。这可能与直肠癌患者采用治疗方式不同有关。此外,本研究经ROC分析发现,术后3 m、6 m血清MUC-1、TK1水平联合预测术后复发转移的AUC分别为0.731、0.829,具有较高预测效能,且显著高于各指标单一预测,提示血清MUC-1、TK1水平联合预测直肠癌术后复发转移具有可行性。
综上所述,血清MUC-1、TK1水平与直肠癌恶性程度呈正相关,联合检测可有效辅助临床评估直肠癌患者行腹腔镜结直肠癌根治术后复发转移风险,具有较高预测效能。
