国产与原研利奈唑胺对革兰阳性菌体外PK/PD比较研究
2023-05-30杨凯张舜天黄晨王雪婷嵇金如沈萍肖永红
杨凯 张舜天 黄晨 王雪婷 嵇金如 沈萍 肖永红
摘要:目的 通过体外药动学(PK)/药效学(PD)研究,比较国产利奈唑胺(恒捷)及原研利奈唑胺(斯沃)对革兰阳性菌的抗菌效果。方法 利用体外PK自动模拟系统PASS400持续24 h模拟国产及原研利奈唑胺(600mg iv. q12 h, 静滴0.5 h)对金黄色葡萄球菌ATCC25923,耐甲氧西林金黄色葡萄球菌52118、耐甲氧西林表皮葡萄球菌54994、耐万古霉素屎肠球菌52820临床分离株的时间杀菌曲线及体外PD参数,使用GraphPad Prism 8.0分析数据。结果 研究菌株对国产与原研利奈唑胺均敏感,最低抑菌浓度0.25~1 μg/mL。在预设给药方式下,两种利奈唑胺对测定细菌均具有良好杀菌效应,且二者杀菌效果一致,24 h内二者时间杀菌曲线几乎重叠。PD参数中,两种利奈唑胺对4株细菌最大杀菌量(MKD)及24 h杀菌量(ΔlgN24)均接近2 lgCFU/mL,殺菌曲线下面积在23~33 lgCFU/(mL·h)之间,再生至初始菌量时间均大于24 h,54994菌株组杀菌曲线与空白对照对照曲线面积差接近13 lgCFU/(mL·h),其余各组IE(药物杀菌曲线与细菌生长空白对照曲线面积差)均在29~35 lgCFU/(mL·h)之间,两种药物对4株细菌杀菌速率浮动于约0.1~0.7 lgCFU/(mL·h)之间。国产与原研利奈唑胺各组间PD参数均无差异。结论 国产利奈唑胺(恒捷)与原研利奈唑胺(斯沃)对常见革兰阳性菌具有相似的体外PK/PD特征及杀菌效应。
关键词:利奈唑胺;药动学/药效学;国产药;原研药;体外
中图分类号:R978.1 文献标志码:A
Comparison of antibacterial efficacy of generic and branded linezolid against Gram-positive bacteria with in vitro pharmacokinetics/ pharmacodynamics model
Yang Kai1, Zhang Shun-tian1, Huang Chen2, Wang Xue-ting1, Ji Jin-ru1, Shen Ping1, and Xiao Yong-hong1
(1 State Key Laboratory for Diagnosis and Treatment of Infectious Disease, the First Affiliated Hospital, Zhejiang University School of Medicine, Hangzhou 310003; 2 Department of Respiratory and Critical Care Medicine, Ningbo Medical Center Li Huili Hospital, Ningbo 315040)
Abstract Objective To compare the antibacterial efficacy of generic and branded linezolid against Gram-positive bacteria with in vitro pharmacokinetics (PK)/pharmacodynamics (PD) model. Methods The in vitro PK simulation system PASS400 was used to simulate the concentration-time curve after intravenous administration of linezolid at 600 mg q12 h for 24 hours (infusion time of 0.5 h). The bactericidal curves and PK/PD parameters of generic and branded linezolid against the reference strain of Staphylococcus aureus (ATCC25923), clinical strains of methicillin-resistant Staphylococcus aureus 52,118, methicillin-resistant coagulase-negative Staphylococcus epidermidis 54994 and vancomycin-resistant Enterococcus faecium 52,820 were compared. The GraphPad Prism 8.0 software was used for data analysis. Results All the four selected strains were susceptible to both generic and branded linezolid, and the minimum inhibitory concentrations were 0.25~1 μg/mL. Both agents demonstrated outstanding and similar bactericidal effects, and their bacterial sterilization curves were almost unanimous. For the two agents, the maximum kill down was close to 2 lgCFU/mL, the area under kill curves was between 23~33 lgCFU/(mL·h), and the bacterial re-growth time was longer than 24 hours. The area difference between the control growth and bacterial killing curves against 54994 was around 13 lgCFU/(mL·h), and all against the others were 29~35 lgCFU/(mL·h), killing rate of the two agents against the four strains fluctuated between about 0.1~0.7 lgCFU/(mL·h). All PD parameters showed no difference between the generic and branded linezolid. Conclusion The generic and branded linezolid showed similar in vitro bactericidal ability and in vitro PK/PD effects against Gram positive bacteria.
Key words Linezolid; Pharmacokinetics/Pharmacodynamics; Generic; Branded; In vitro
利奈唑胺是第一个应用于临床的恶唑烷酮类抗生素,对主要革兰阳性菌,包括耐甲氧西林葡萄球菌、耐万古霉素肠球菌等都具有强大的抗菌活性[1-2],全国血流感染细菌耐药检测联盟(BRICS)2018—2019年全国血流感染细菌耐药监测报告中,利奈唑胺对各类敏感及耐药葡萄球、肠球菌、链球菌敏感率均维持在88.2%~100%[3]。目前该药主要用于敏感菌所致的医院或社区获得性皮肤软组织及肺部感染等。原研利奈唑胺(商品名:斯沃)由美国辉瑞(Pfizer)公司开发,2000年美国上市,并于2007年引入我國[4]。
目前全球范围内有多家公司对利奈唑胺进行仿制并上市[5],我国仿制利奈唑胺注射液由江苏豪森公司开发(商品名:恒捷)。于淑颖等[6]及安友仲等[7]对国产与原研利奈唑胺进行了体外抗菌活性比较,结果显示二者对常见革兰阳性球菌最低抑菌浓度无差异[6]。然而,在药物一致性评价中,除常规的体外抗菌活性及药物质量等评估外,更应重视药动学/药效学(pharmacokinetics/pharmacodynamics,PK/PD)特点,通过PK/PD研究比较药物杀菌活性及杀菌特征,可以更全面地对原研药与仿制药的一致性进行分析,并指导临床药物选择。
相较人体研究而言,体外PK/PD模型不仅性价比更高,且无伦理方面限制,可以更自由且不受限制地对多种给药方式、剂量、间隔乃至适应症等进行模拟,相较普通体外杀菌实验拥有更接近真实人体内环境,结果可信度更高的优势。因此本研究利用体外PK/PD模拟系统,模拟利奈唑胺人体PK参数下,比较国产与原研利奈唑胺的体外抗菌活性,以期对二者一致性进行评估,为临床用药提供参考。
1 材料与方法
1.1 材料
1.1.1 药品与培养基
原研利奈唑胺(斯沃,Fresenius Kabi Norge AS,Norway,批号19K04U02,有效期至2021年10月);国产利奈唑胺(恒捷,江苏豪森药业集团生产,批号700109837,有效期至2021年7月)均为市场销售产品,剂型均为注射剂。阳离子调节Mueller Hinton肉汤(MHB)购于英国Oxoid公司;Tryptose Soya琼脂(TSA)购于英国Oxoid公司。
1.1.2 实验菌株
金黄色葡萄球菌标准株ATCC25923;临床分离耐甲氧西林金黄色葡萄球菌52118(S. aureus 52118)、耐甲氧西林表皮葡萄球菌54994(S. epidermidis 54994),耐万古霉素屎肠球菌52820(E. faecium 52820)均为临床菌株,分离后于本实验室内保存。
1.2 方法
1.2.1 最低抑菌浓度(minimum inhibitory concentration, MIC)测定
测定方法参照美国临床和实验室标准研究所(CLSI)推荐标准流程[8],两种利奈唑胺对4株细菌的MIC值选用微量肉汤稀释法进行测定。
1.2.2 体外血药浓度模拟PK/PD实验
利用体外PK自动模拟系统PASS400(Dainippon Seiki,日本)对人体内利奈唑胺(600 mg iv. q12 h)药动学过程进行体外模拟。将原装药液加入无菌蒸馏水中稀释,将药液浓度配置为50 μg/mL(浓度通过PASS400系统模拟得出),以在 0.5 h内将配置药液以等速泵入中央室,每12 h泵药1次,之后将培养基泵出中央室,根据系统模拟所得不同消除速度自动调整泵出速度,再以相同速度将新鲜的基质通过注射泵泵入中央室,保证模拟过程中中央室内液体体积稳定,模拟出不同给药方案下的药物浓度时间曲线。细菌接种到中央室(初始浓度在105~6 CFU/mL)后连续孵育24 h,在预定时间点(0、2、4、6、8、10、14、18和24 h)收集1 mL样品,在接种前用0.9%生理盐水稀释后利用螺旋涂布仪(Interscience公司,法国)接种至TSA平板,计数在恒温37℃下继续孵育20 h后进行。国产与原研2种利奈唑胺分别与上述4株细菌在体系内共同孵育,每株细菌重复模拟3次,各时间点细菌计数计平均值。
1.2.3 利奈唑胺PK参数
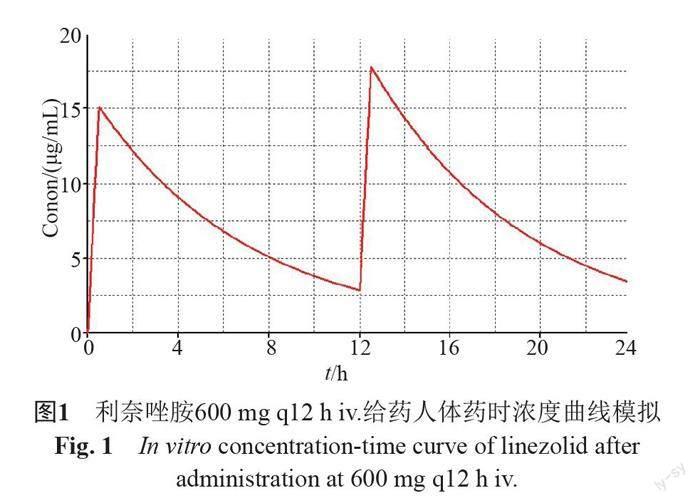
根据药品说明书设定给药方案为600 mg iv. q12 h,每次静滴0.5 h,共24 h。目前国产与原研利奈唑胺说明书中所提供PK参数完全相同,故对两种药物统一取健康成年人给药后的PK参数进行模拟[1],具体为:峰浓度(Cmax) 15.1 μg/mL,半衰期(T1/2 )4.8 h,清除率(CL)123 mL/min,分布容积(V)45 L,给药后12 h药时曲线下面积(AUC0-12)89.7 μg·h/mL,并根据一房室模型绘制药时浓度曲线(图1)。
1.2.4 PD参数测定
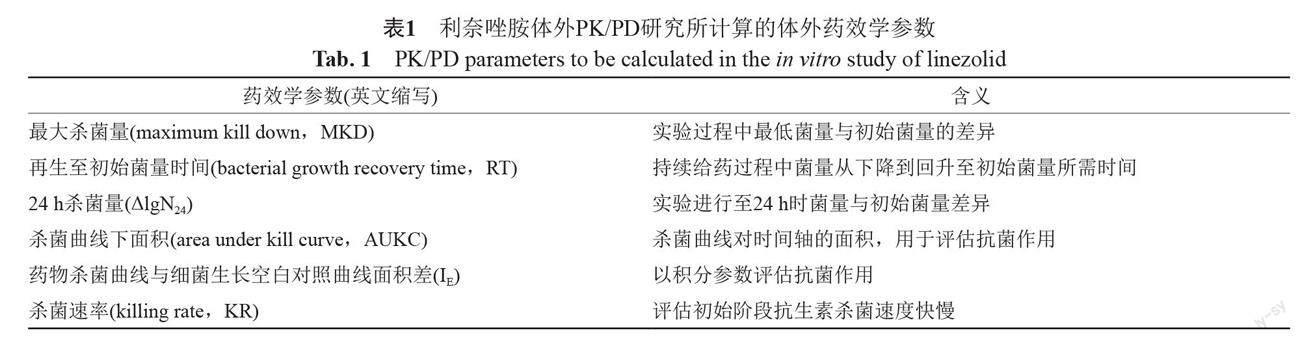
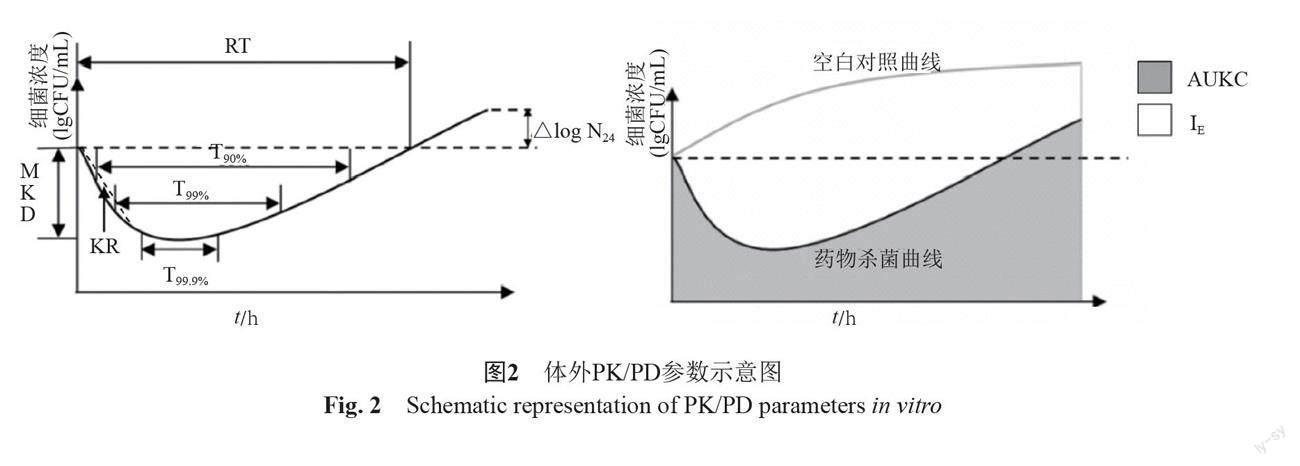
杀菌效果曲线依据不同时间点的菌落计数绘制,以此计算PK/PD参数,本研究涉及的PK/PD参数包括:最大杀菌量(MKD)、再生至初始菌量时间(RT)、24 h杀菌量(ΔlgN24)、杀菌曲线下面积(AUKC)、药物杀菌曲线与细菌生长空白对照曲线面积差(IE)、杀菌速率(KR),详见表1及图2。MKD、RT、AUKC、ΔlgN24使用PASS-400系统分析得出,IE使用GraphPad Prism 8.0软件(GraphPad Software,美国)通过梯形法积分计算,杀菌速率计算:各时间点给药组减去对照组菌落计数,然后0与2 h菌落计数差值相减再除以时间差。RT和IE是目前公认的反应抗菌药物PK/PD的主要指标,尤其是IE,能更全面、无偏倚地评估各个抗菌药物不同给药方案下的治疗效果[9](图2)。
1.2.5 统计分析
使用GraphPad Prism 8.0软件对数据进行统计分析,计量资料以(x±s)表示,采用独立样本t检验,P<0.05为差异具有统计学意义。
2 结果
2.1 药敏实验
4株细菌对国产及原研利奈唑胺均敏感,其MIC值基本一致,均在0.25~1 μg/mL之间(表2)。
2.2 体外PK/PD结果
2.2.1 国产与原研利奈唑胺时间杀菌曲线比较(图3)
重复3次实验后绘制各组杀菌曲线,国产与原研利奈唑胺对4株细菌的时间杀菌曲线无明显差异。肠球菌空白对照在24 h培养后细菌浓度增加至11 lgCFU/mL左右,其余3株细菌浓度增加至约8 lgCFU/mL。国产及原研利奈唑胺均表现出良好的杀菌效果,以600m q12 h iv.给药24 h后,各组细菌浓度均由6 lgCFU/mL下降至4 lgCFU/mL左右,两组间杀菌效果一致。
2.2.2 国产与原研利奈唑胺PD参数比较
两种药物对4株细菌的MKD在1.5~2.2 lgCFU/mL之间,ΔlgN24在1.4~2.0 lgCFU/mL之间;两种药物的杀菌曲线下面积(AUKC)23~33 lgCFU/(mL·h);24 h内各菌株均未发现再生现象,故再生至初始菌量时间(RT)均记为大于24 h;表皮葡萄球菌54994组杀菌曲线与空白对照曲线面积差(IE)偏小,约13 lgCFU/(mL·h),其余各组IE处于29~35 lgCFU/(mL·h)之间。上述参数国产与原研利奈唑胺无统计学差异。杀菌速率上两种药物对4株细菌杀菌速率在0.1~0.7 lgCFU/(mL·h)之间波动,不同组内两种药物杀菌速率均无统计学差异(表3)。
3 讨论
与原研药相比,仿制药通常有研发成本及市场价格较为低廉的优势,一项对9000余名患者使用多种原研与仿制抗生素治疗尿路感染的疗效与费用对比研究,发现2500名仿制药使用患者预后与原研药一致,且花费更少[10]。我国作为一个人口基数庞大的发展中国家,研发仿制药物对于改善药品供应压力,缓解药物所致社会经济负担而言意义重大。但如何保证仿制药的质量、安全性、疗效等与原研药等同,是临床一直关注的问题[11]。对于口服制剂,一般采用一致性评价的方法确定两者的等效[12],对注射制剂并没要求开展人体和临床研究,特别对抗菌药物而言,其直接作用对象为细菌,因此进行药物一致性评价时直接对比仿制药与原研药抗菌效果差异可以更为直接可靠地评判两者异同。单纯的体外抗菌活性(如MIC)测定与真实人体内环境差异过大,所得结论与临床差别较大。PK/PD是药物评估的重要内容和方法,本研究所使用的体外PK/PD模拟方法可以通过模拟抗菌药物在人体代谢条件下的血药浓度动态变化,使药物及细菌在接近真实人体药物代谢过程的条件下相互作用,且不受实验动物限制,相较体外MIC测定结果更为真实可靠,同时操作较为简便,可重复性强,极其适用于药物一致性评价[13]。
本研究中选用4株对利奈唑胺敏感细菌进行研究,结果国产与原研利奈唑胺对4株细菌体外敏感性一致,24 h杀菌曲线基本重合,相关PD参数也无差异,可以认为利奈唑胺杀菌效果可靠,且国产与原研利奈唑胺具有相同的杀菌效果。在24 h内,国产与进口利奈唑胺均对所选细菌均表现出良好杀菌作用,杀菌率达99%作用,RT均大于24 h。Cha等[14]持续48 h的体外PK/PD研究中,利奈唑胺以600 mg q12 h iv.给药时对多株敏感菌杀菌率在24 h达到接近99%,在24~48 h时内部分菌株对部分菌株杀菌率可升至99.9%,其杀菌效果与本研究中原研及国产药均相似。本研究中表皮葡萄球菌组两种药物IE均为12 lgCFU/(mL·h)左右,较其他菌株组偏低,但该组其余PD指标均与各组一致,考虑主要由该组空白对照组初始细菌接种量较低导致,曲线下面积偏小所致,可能存在一定实验误差。本文中未将T90%、T99%和T99.9%纳入分析,这是由于在24 h的实验过程中,所有组菌量均持续减少未达恢复期,使用PASS400系统估算上述参数数值均为大于24 h,无法对比分析,考虑后续研究可通过增加体外模拟时长的方式使得对T90%、T99%和T99.9%评估可行。
需要注意的是,虽然体外PK/PD研究较传统体外敏感性测定结果更能反映药物的杀菌效果,且有研究表明体外模型与动物模型结果差异不显著[15],但仍无法完全还原细菌与人体内环境的相互作用,如免疫、生理环境等差异,体外PK/PD研究的结论可以作为重要参考,弥补临床研究的不足。国产利奈唑胺相关临床研究稀缺,目前仅见贾民勇等[16]的单中心研究中,其结论42名接受国产利奈唑胺治疗的重症革兰阳性菌肺炎患者有效率高于38名原研利奈唑胺治疗患者,但该研究设计并非双盲实验,结果需要进一步验证。本研究也有以下不足:由于缺乏国产利奈唑胺的PK参数,国产与进口利奈唑胺使用了相同参数设置的药时曲线,研究也仅模拟1种给药方式;同时,PASS-400系统根据预设药时曲线参数及初始药液浓度计算后自动模拟给药,此过程中无法验证混合体系内药液浓度是否符合预期并干预;在实验过程中,表皮葡萄球菌空白组初始浓度偏低,可能存在一定误差。
Treyaprasert等[17]曾建立了抗生素体外PK/PD参数分析模型,具体公式见下,该模型以非参数拟合方式比较不同药物在模型参数方面(Kg, Nm, Kmax, γ)的差异:其中,N和t分别为菌落计数对数和时间。Kg表示细菌生长速率,Nm表示菌落计数对数的最大值。Kmax为最大杀菌速率,KC50表示达到50% Kmax所需的药物浓度。γ表示杀菌速率曲线随利奈唑胺藥物浓度(C)的变化梯度。该模型可更深入细致地评估原研药与仿制药的一致性,但本研究过程中未进行药物浓度测定,故未使用该模型进行评估,在后续研究中有待完善。
本研究表明,国产仿制利奈唑胺(恒捷)与进口原研利奈唑胺(斯沃)对常见耐药阳性球菌均有良好的体外杀菌效果,且二者PD特性一致,可以推测二者有相似的临床疗效,临床药物选择可以参考,但仍需高质量临床研究进一步确认。
致谢:本研究受肖永红教授课题组内张舜天等对替加环素等其他抗生素体外PK/PD研究启发,实验及论文写作过程中受到了肖永红教授及师兄张舜天悉心指导,本文中图2中左侧示意图据其论文《体外PK/PD对国产与原研替加环素抗菌效果比较》中相关示意图基础上修改绘制[18],并已征得作者同意。在此表示诚挚谢意!
参 考 文 献
Food and Drug Administration. Label of Linezolid [DB/OL]. [2021-7-20].https://www.accessdata.fda.gov/drugsatfda_docs/label/2018/021130s037,021131s030,021132s035lbl.pdf.
Moellering R. Linezolid: The first oxazolidinone antimicrobial [J]. Ann Inter Med, 2003, 138(2): 135-142.
陈云波, 嵇金如, 应超群, 等. 2018—2019年度全国血流感染细菌耐药监测报告[J]. 中华临床感染病杂志, 2021, 14(1): 32-45.
杨倩, 何瑜, 尤启冬, 等. 利奈唑胺的国内知识产权现状及建议[J]. 中国新药杂志, 2014, 23(21): 2475-2480.
张辉, 马秋娟, 邓声菊. 利奈唑胺首仿策略演绎分析[J]. 中国新药杂志, 2016, 25(23): 2653-2658.
于淑颖, 肖盟, 杨文航, 等. 评估国产利奈唑胺对葡萄球菌和肠球菌体外抗菌活性[J]. 中国感染与化疗杂志, 2019, 19(4): 400-404.
安友仲. 国产利奈唑胺(恒捷)与进口利奈唑胺体外药敏活性比对研究结果[C]. 2017年北京药学年会论文集, 2017: 291-292.
Clinical And Laboratory Standards Institute. Performance Standards for Antimicrobial Susceptibility Testing[S]. 2017: M100-S23.
Firsov A, Vostrov S, Shevchenko A, et al. Parameters of bacterial killing and regrowth kinetics and antimicrobial effect examined in terms of area under the concentration-time curve relationships: Action of ciprofloxacin against Escherichia coli in an in vitro dynamic model[J]. Antimicrob Agents Chemother, 1997, 41(6): 1281-1287.
Lin Y S, Jan I S, Cheng S H. Comparative analysis of the cost and effectiveness of generic and brand-name antibiotics: The case of uncomplicated urinary tract infection[J]. Pharmacoepidemio Drug Saf, 2017, 26(3): 301-309.
鲍坤希, 何晓静, 菅凌燕. 国外医生和药师及患者对仿制药临床应用的认知现状[J]. 医药导报, 2019, 38(12): 1681-1685.
国家药品监督管理局.关于仿制药质量和疗效一致性评价有关事项的公告[EB/OL] [2021-7-20]. https://www.nmpa.gov.cn/directory/web/nmpa/xxgk/zhcjd/tjzhc/ 20190109170001421.html.
王林, 刘伟, 李昕, 等. 体外PK/PD模型在优化抗菌药物给药方案中的应用[J]. 中国感染控制杂志, 2014, 13(1): 58-61.
Cha R, Akins R L, Rybak M J. Linezolid, levofloxacin, and vancomycin against vancomycin-tolerant and fluoroquinolone-resistant Streptococcus pneumoniae in an in vitro pharmacodynamic model[J]. Pharmacotherapy, 2003, 23(12): 1531-1537.
Bonapace C R, Friedrich L V, Bosso J A, et al. Determination of antibiotic effect in an in vitro pharmacodynamic model: Comparison with an established animal model of infection[J]. Antimicrob Agents Chemother, 2002, 46(11): 3574-3579.
贾民勇, 牛建伟, 王少芳, 等. 国产利奈唑胺治疗革兰氏阳性球菌感染重症肺炎患者疗效评价及其影响因素分析 [J]. 中国现代应用药学, 2019, 36(3): 343-348.
Treyaprasert W, Schmidt S, Rand K H, et al. Pharmacokinetic/pharmacodynamic modeling of in vitro activity of azithromycin against four different bacterial strains [J]. Int J Antimicrob Agents, 2007, 29(3): 263-270.
张舜天, 黄晨, 嵇金如, 等. 体外PK/PD对国产与原研替加环素抗菌效果比较[J]. 中华临床感染病杂志, 2020, 13(4): 264-269.
收稿日期:2022-01-26
作者简介:杨凯,男,生于1994年,在讀硕士研究生,主要研究方向为抗生素与细菌耐药,E-mail: yk94007@163.com
通讯作者,E-mail: xiao-yonghong@163.com
