3 种三唑类药物血药浓度测定方法的建立*
2023-05-26林志燕黄晓会
林志燕,黄晓会
(上海交通大学医学院附属新华医院,上海 200092)
近年来,真菌感染尤其是深部真菌感染严重威胁患者的健康,抗真菌药物以三唑类在临床应用广泛且疗效较好,代表药物有氟康唑、伏立康唑、伊曲康唑、泊沙康唑等。但因其在吸收、分布、代谢、排泄等药物代谢动力学(简称药动学)方面的差异和药物相互作用的影响,导致不同患者血药浓度的个体差异较大。如肾功能不全或中枢神经系统真菌感染患者体内氟康唑的血药浓度会显著升高[1]。伏立康唑具有非线性药动学特征,其量效关系难测[2]。泊沙康唑为第2 代三唑类抗真菌药,具有抗菌谱广、抗菌活性强、安全性高等特点,但其药动学的个体差异明显[3-4]。临床实践表明,抗真菌药物的血药浓度和药物的临床疗效及药品不良反应相关,其治疗药物监测(TDM)结果可为临床给药方案的制订提供指导[5]。本研究中建立了同时测定氟康唑、伏立康唑和泊沙康唑血药浓度的超高效液相色谱串联质谱(UPLC-MS/MS)法,以为临床抗真菌药物的合理使用提供参考。现报道如下。
1 仪器与试药
1.1 仪器
Agilent 1290 型超高效液相色谱仪,Agilent 6460 型三重四极杆质谱仪,配有电喷雾离子源(ESI)、B05.00 Masshunter色谱工作站(美国Agilent公司)。
1.2 试药
氟康唑对照品(批号为100314 - 201906,含量99.8%),伊曲康唑对照品(批号为100631-201402,含量99.2%),均购自中国食品药品检定研究院;伏立康唑对照品(European Pharmacopoeia Reference Standard,批号Y0001395,含量99.9%);泊沙康唑对照品(Panphy Chemicals Corporation 公司,批号171228 - 49 - 2,含量100%);乙腈、甲醇、甲酸为质谱纯,水为超纯水。
2 方法与结果
2.1 试验条件
色谱条件:色谱柱为Agilent SB - C18柱(50 mm ×2.1 mm,1.8 μm);流动相为含0.1%甲酸的乙腈(A)-水(B),梯度洗脱(0~2 min 时5%A→80%A,2~4 min时80%A→95%A,4~5 min时95%A);流速为0.3 mL/min;柱温为40 ℃;进样量为2 μL。
质谱条件:ESI,正离子多反应监测(MRM)模式。干燥气和雾化气均为氮气,干燥气温度320 ℃,干燥气流量7 L/ min,雾化器压力45 psi,鞘气温度350 ℃,鞘气流量12 L/ min,毛细管电压4 000 V,喷嘴电压0 V。氟康唑、伏立康唑、泊沙康唑和伊曲康唑的MRM 参数见表1,二级全扫描质谱图见图1。

图1 二级质谱图A.Fluconazole B.Voriconazole C.Posaconazole D.ItraconazoleFig.1 Secondary mass spectrum

表1 4种三唑类化合物的MRM参数Tab.1 MRM parameters of four triazole compounds
2.2 溶液制备与血清样品预处理
混合对照品溶液:分别称取氟康唑、伏立康唑、泊沙康唑对照品各适量,精密称定,用甲醇溶解并稀释成质量浓度分别为1 000,200,200 μg/mL 的混合对照品溶液。-20 ℃避光保存(下同)。
标准曲线工作液:取混合对照品溶液适量,加甲醇倍比稀释,制成氟康唑质量浓度为7.812 5,15.625,31.25,62.5,125,250,500,1 000 μg/ mL,伏立康唑为1.562 5,3.125,6.25,12.5,25,50,100,200 μg/mL,泊沙康唑为1.562 5,3.125,6.25,12.5,25,50,100,200 μg/mL的标准曲线工作液。
质控工作液:同标准曲线工作液制备方法制备,氟康唑、伏立康唑、泊沙康唑质量浓度分别为25,150,750 μg/mL,5,30,150 μg/mL,5,30,150 μg/mL。
内标溶液:称取伊曲康唑对照品适量,精密称定,用甲醇溶解并制成质量浓度为65 μg/mL的溶液。
血清样品预处理:取血清样品180 μL,置1.5 mL离心管中,加入内标溶液20 μL、甲醇400 μL,涡旋1 min,15 000 r/ min 离心10 min,取上清液,经0.22 μm 微孔滤膜滤过,取续滤液,即得。
2.3 方法学考察
专属性考察:精密吸取人空白血清样品,以等体积甲醇替代内标溶液;取人空白血清样品适量,加入混合对照品溶液;取给药后人血清样品,加入内标溶液,以上溶液均按2.2 项下血清样品预处理方法处理。取上述溶液及混合对照品溶液各适量,按2.1 项下试验条件进样测定,记录色谱图。结果空白血清在对应色谱峰保留时间内均无干扰峰,氟康唑、伏立康唑、泊沙康唑和伊曲康唑的保留时间分别为1.578,2.198,2.485,2.887 min,方法专属性良好。详见图2。

图2 总离子流图1.Fluconazole 2.Voriconazole 3.Posaconazole 4.ItraconazoleA.Blank serum B.Blank serum+mixed reference solution+internal standard solution C.Mixed reference solution+internal standard solution D.Test serum containing fluconazole+internal standard solution E.Test serum containing voriconazole+internal standard solution F.Test serum containing posaconazole+internal standard solutionFig.2 Total ion chromatograms
线性关系考察:精密吸取标准曲线工作液20 μL,加入内标溶液20 μL、人空白血浆160 μL ,涡旋混匀,再加甲醇400 μL,制成氟康唑质量浓度为0.781 25 ,1.562 5,3.125,6.25,12.5,25,50,1 00 μg/mL,伏立康唑为0.156 25,0.312 5,0.625,1.25,2.5,5,10,20 μg/mL,泊沙康唑为0.156 25,0.312 5,0.625,1.25,2.5,5,10,20 μg/mL 的标准曲线血清工作液。按2.2 项下血清样品预处理方法处理,在按2.1 项下试验条件进样测定,记录峰面积。以待测成分质量浓度(X,μg/mL)为横坐标、待测成分与内标峰面积比值(Y)为纵坐标进行线性回归,得回归方程。详见表2。

表2 线性关系考察结果(n=8)Tab.2 Results of the linear relation test(n=8)
定量限考察:分别精密量取2.2 项下3 种对照品溶液适量,倍比稀释,并按2.1项下试验条件进样测定,以信噪比(S/N)为10∶1 时的待测成分质量浓度为定量限,结果氟康唑、伏立康唑和泊沙康唑分别为0.084,0.007,0.016 μg/mL。
准确度与精密度试验:取2.2项下低、中、高质量浓度的混合质控工作液进样分析,每个质量浓度平行制备5 份,进行标准曲线分析,将待测成分峰面积/ 内标峰面积的结果代入标准曲线,计算待测成分的质量浓度,以待测成分实测浓度/理论加入浓度的结果计算方法准确度。以同一日内测得的6次待测成分浓度计算日内精密度;连续测定3 d,计算日间精密度。结果各待测物的准确度最低为91.36%,最高为113.92%(n= 3),日内和日间精密度的RSD均小于10%,表明该方法准确度较高,精密度较好。详见表3。
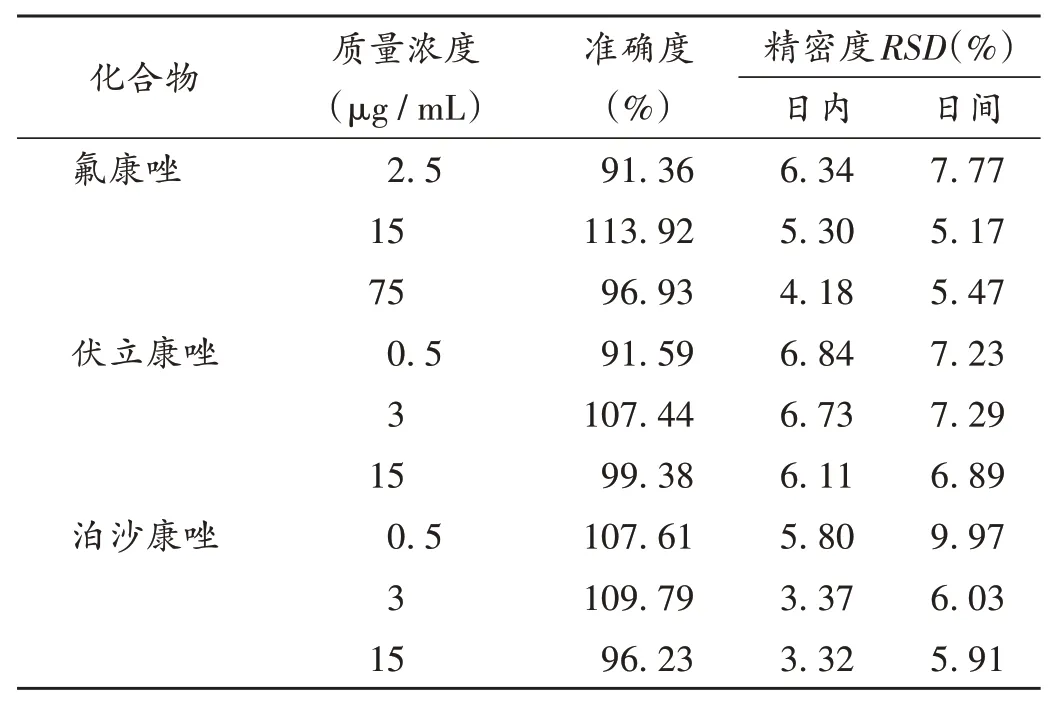
表3 3种化合物的准确度和精密度Tab.3 Accuracy and precision of three compounds
提取回收率与基质效应考察:取不同来源的空白血清,按2.2项下方法制备低、中、高质量浓度的混合质控样品,前处理后按2.1 项下色谱条件进样测定,将对照品与内标峰面积的比值记为A;用甲醇替代空白血清,加入内标溶液,将混合对照品稀释为与A 中质量浓度相同的样品,按2.1 项下试验条件进样分析,对照品与内标峰面积的比值记为B;空白血清预处理后加入混合对照品溶液制备得到与A中质量浓度相同的样品,对照品和内标峰面积比值记为C。以A/C×100%计算各化合物的提取回收率,以C/B× 100%计算基质效应。结果显示,氟康唑的提取回收率为81.99%~96.97%,RSD<14.25%,基质效应为90.80%~119.94%,RSD<14.06%;伏立康唑的提取回收率为85.19%~97.83%,RSD<14.82%,基质效应为94.38%~117.81%,RSD<13.89%;泊沙康唑的提取回收率为81.00%~93.76%,RSD<14.21%,基质效应为95.65%~109.08%,RSD<13.47%。
稳定性考察:考察血清样品在- 80 ℃与室温间反复冻融3 次的稳定性,血浆样品在-80 ℃下放置30 d的稳定性,给药后血清样品在4 ℃进样器中放置0,12,24,48 h 的稳定性,给药后血清样品在室温放置0,6,12 h 的稳定性。结果的RSD均<10%,表明血清样品在上述条件下基本稳定。
2.4 血药浓度测定
收集我院2020 年7 月至2022 年9 月因治疗需要接受氟康唑(38例)、伏立康唑(48例)、泊沙康唑(14例)治疗的患者。治疗7 d 后,当日用药前30 min 抽取患者静脉血2 mL,按本研究中所建立的方法当日测定血清药物浓度。结果见表4至表6。

表4 氟康唑血药浓度测定结果(n=38)Tab.4 Results of blood - concentration determination of fluconazole(n=38)

表5 伏立康唑血药浓度测定结果(n=48)Tab.5 Results of blood-concentration determination of voriconazole(n=48)

表6 泊沙康唑血药浓度测定结果(n=14)Tab.6 Results of blood-concentration determination of posaconazole(n=14)
3 讨论
目前报道的三唑类抗真菌药物测定方法有微生物法和高效液相色谱法,微生物法准确度相对较低,高效液相色谱法分析周期较长。本研究中建立了同时测定人血清中3种三唑类抗真菌药物(氟康唑、伏立康唑、泊沙康唑)的UPLC-MS/MS 法,考虑到同位素内标价格昂贵,成本较高,故选择伊曲康唑为内标,其色谱保留行为和质谱条件与待测物较接近,且信号稳定性好。采用甲醇沉淀蛋白的前处理方法,简单快捷,且每个样品分析时间仅需5 min,满足临床检测高通量要求。临床服用以上3 种药物的患者均可采用本方法进行血药浓度监测,无需切换试验方法。方法学验证结果显示,该方法专属性强、灵敏度高、准确稳定,适用于临床血药浓度的监测。
本研究中血药浓度测定结果显示,氟康唑和泊沙康唑检测浓度均在所设线性范围内,伏立康唑有2 例低于定量限。表明氟康唑、伏立康唑和泊沙康唑个体药动学差异较大。
目前报道的各药物的有效浓度范围,氟康唑参考有效浓度范围应超过20 μg/mL[6],伏立康唑在各国指南中推荐的谷浓度下限范围为0.5~2.0 μg/mL,上限范围为4~6 μg/mL,目标范围为1.0~5.5 μg/mL[7-11],临床研究和指南推荐,泊沙康唑用于预防侵袭性真菌感染时,稳态谷浓度应大于0.7 μg/mL,治疗浓度应大于1.25 μg/ mL[12-16]。但以上血药浓度参考范围针对成人设置,关于儿童血药浓度推荐范围的相关研究较少。本研究结果显示,38例患者中有21例氟康唑血药浓度大于20 μg/mL,48例患者中有37例伏立康唑血药浓度在0.5~6.0 μg/mL,14 例患者中有9 例泊沙康唑血药浓度大于0.7 μg/mL,其中有5例大于1.25 μg/mL。
根据血药浓度监测结果进行剂量调整是TDM 的重要内容,此外,在调整给药剂量、发生药品不良反应或疗效欠佳、加用或停用可能发生相互作用的药物时,还需再次进行TDM。对于临床患者,维持有效的血药浓度范围能获得较好的疗效,并降低药品不良反应发生率。因此有必要对使用氟康唑、伏立康唑和泊沙康唑治疗的患者实施血药浓度监测,以提高临床疗效,确保用药安全。本研究不足之处在于临床样本较少,后续将进一步扩大样本量,为临床制订个体化给药方案提供参考。
