沉默CSE1L对急性髓系白血病细胞阿糖胞苷敏感性的影响及作用机制研究*
2023-03-10刘小玉李旭东关坤萍
刘小玉, 李旭东, 关坤萍
沉默对急性髓系白血病细胞阿糖胞苷敏感性的影响及作用机制研究*
刘小玉1, 李旭东2, 关坤萍3△
(1山西医科大学基础医学院生物化学与分子生物学教研室,山西 太原 030001;2山西医科大学第二临床医学院,山西 太原 030001;3山西医科大学第二医院检验科,山西 太原 030001)
探讨敲减染色体分离1样蛋白()对急性髓系白血病细胞株THP-1细胞生物学行为及阿糖胞苷(Ara-C)敏感性的影响,并分析相关作用机制。采用RT-qPCR法检测CSE1L的 mRNA表达水平,流式细胞术检测细胞周期及凋亡水平,LinkedOmics及DAVID数据库进行基因本体论(gene ontology,GO)功能注释和京都基因与基因组百科全书(Kyoto Encyclopedia of Genes and Genomes,KEGG)通路富集分析, Western blot法检测细胞周期素D1(cyclin D1)、原癌基因-、促凋亡蛋白Bax和抗凋亡蛋白Bcl-2的相对表达水平。与对照组相比,空载(sh-NC)组及敲减(sh-CSE1L)组标记绿色荧光蛋白(GFP)的THP-1细胞占比均>90%。与空载组相比,敲减组CSE1L的mRNA相对表达量降低至40%,凋亡率显著升高0.01。敲减组比空载组G0/G1期细胞占比升高(0.05),S期细胞占比降低(<0.05),而G2/M期无明显差异。在1 μmol/L阿糖胞苷处理24 h后,敲减组细胞活力最低(<0.05),凋亡率最高(0.01)。此外,敲减可下调Bcl-2、cyclin D1和c-Myc蛋白表达水平,上调Bax蛋白表达水平(<0.05)。生物信息学分析显示CSE1L主要参与细胞周期等通路。敲减可阻滞THP-1细胞周期,诱导细胞凋亡,提高细胞对阿糖胞苷的敏感性,其可能通过调控细胞周期相关分子发挥作用。
阿糖胞苷;急性髓系白血病;染色体分离1样蛋白;细胞周期;细胞凋亡
急性髓系白血病(acute myeloid leukemia, AML)是一种骨髓髓系细胞分化受阻,正常血细胞生成受抑制而引发的严重血液学疾病[1]。以阿糖胞苷(cytarabine, Ara-C)为代表的化疗药物是一种抑制DNA复制的嘧啶类似物,是治疗AML的主要药物[2-3]。常规剂量的阿糖胞苷可使AML缓解率超过70%,然而超过60%的AML患者复发[4-5]。高剂量阿糖胞苷强化治疗可提高AML患者的总体生存率、降低复发率,但增加了药物的副作用[6]。染色体分离1样蛋白(chromosome segregation 1-like, CSE1L),又称为细胞凋亡易感基因(cellular apoptosis susceptible, CAS),位于人染色体20q13,分子量为110 kD[7]。CSE1L作为一种核转运因子,参与多种细胞功能,包括细胞增殖、细胞周期、细胞凋亡、微囊形成及肿瘤转移等[8-10]。据报道,CSE1L在多种实体瘤中高表达,包括肺癌、乳腺癌和胃癌等[11-14]。本课题组前期研究证实CSE1L在AML患者骨髓组织中高表达,且与患者的不良预后相关[15],但其与阿糖胞苷化疗敏感性的关系及作用机制尚不明确。本研究以急性髓系白血病THP-1细胞为模型,进一步探讨CSE1L对THP-1细胞周期和凋亡的影响,及其与阿糖胞苷敏感性的关系,为提高阿糖胞苷敏感性提供理论依据。
材料和方法
1 实验材料和试剂
细胞周期及凋亡试剂盒购自北京索莱宝生物科技有限公司;阿糖胞苷购自阿拉丁生物公司;抗c-Myc、细胞周期素D1(cyclin D1)、Bcl-2及Bax抗体购自万类生物科技有限公司;抗β-actin抗体购自北京中杉金桥生物技术有限公司;抗CSE1L抗体购自Abcam;RPMI-1640购自Gibco;特级胎牛血清(fetal bovine serum, FBS)购自武汉普诺赛生命科技有限公司;携带HBLV-h-CSE1L shRNA1-ZsGreen-Puro的sh-CSE1L慢病毒和携带HBLV-ZsGreen-Puro的无义表达sh-NC慢病毒由上海汉恒生物科技有限公司设计并合成。
2 实验方法
2.1数据来源及生物信息学分析基于LinkedOmics(http://www.linkedomics.org/)数据库在线分析CSE1L正相关的基因,并通过DAVID(https://david.ncifcrf.gov/home.jsp)在线网站进行相关基因分析,以<0.05、Statistic>0为阈值筛选,进行基因本体论(gene ontology, GO)功能注释和京都基因与基因组百科全书(Kyoto Encyclopedia of Genes and Genomes, KEGG)通路富集分析。
2.2细胞培养及分组THP-1细胞株由山西医科大学第二医院血液中心实验室赠送。THP-1细胞使用RPMI-1640培养基(含10% FBS及1%青霉素和链霉素),在37 ℃、5% CO2的培养箱中培养。细胞分为5组:(1)对照(control)组:未经任何处理的THP-1细胞;(2)空载(sh-NC)组:携带空载体的慢病毒感染THP-1细胞;(3)敲减(sh-CSE1L)组:携带CSE1L干扰基因的慢病毒感染THP-1细胞;(4)sh-NC+Ara-C组:经1 μmol/L阿糖胞苷[16]处理24 h的sh-NC组THP-1 细胞;(5)sh-CSE1L+Ara-C组:经1 μmol/L阿糖胞苷处理24 h的sh-CSE1L组THP-1 细胞。
2.3CCK-8法检测细胞活力分别接种8 000个THP-1细胞到96孔细胞培养板,并将处理组加入1 μmol/L阿糖胞苷。24 h后,向每孔中加入10 μL CCK-8试剂。在孵箱孵育2 h后,用酶标仪在450 nm处测定各孔吸光度()值。计算细胞活力,细胞活力(%)=(加药组-空白组)/(对照组-空白组)×100%。
2.4Western blot检测蛋白表达水平收集一定数量THP-1细胞,使用RIPA强裂解液裂解细胞。30 min后,在4 ℃、12 000 r/min条件下离心15 min。收集上清液,使用BCA法测蛋白浓度,随后100 ℃变性蛋白5 min。取30 μg总蛋白经电泳分离后转移到0.45 μm的PVDF膜上。使用5%脱脂奶粉溶液封闭1 h后,加入Ⅰ抗4 ℃孵育过夜。Ⅱ抗孵育1 h后,ECL曝光检测相应蛋白的表达信号。用ImageJ软件进行蛋白条带灰度值分析。
2.5RT-qPCR检测mRNA表达水平收集一定数量THP-1细胞,用Trizol试剂提取各组细胞总RNA。测定总RNA浓度后,利用反转录试剂盒将RNA反转录为cDNA。以此cDNA为模板,设定RT-qPCR程序: 95 ℃ 30 s; 95 ℃ 5 s, 60 ℃ 34 s,40个循环; 95 ℃ 15 s, 60 ℃ 1 min, 95 ℃ 15 s。CSE1L的上游引物序列为5'-ATTAAGCTTGTTCTGGATGCCTTTG-3',下游引物序列为5'-GAGGCATTTGCATGGGTA-3';内参照β-actin的上游引物序列为5'-TGGCACCCAGCACAATGAA-3',下游引物序列为5'-CTAAGTCATAGTCCGCCTAGAAGCA-3'。采用2-ΔΔCt法进行数据分析。
2.6DNA含量法检测细胞周期收集一定数量的THP-1细胞,预冷PBS洗涤2次后,加入70%预冷乙醇4 ℃固定过夜。预冷PBS洗去固定液,然后加入100 μL RNaseA溶液在37 ℃水浴,30 min后,加入400 μL PI溶液,4 ℃避光孵育30 min。最后在波长488 nm处上机检测。
2.7Annexin V-PE/7-AAD双染法检测细胞凋亡收集一定数量的THP-1细胞,预冷PBS洗涤2次后,用去离子水按1∶3稀释结合缓冲液重悬细胞。加入5 µL Annexin V/PE溶液,混匀后在室温避光孵育5 min。然后加入10 µL 7-AAD溶液,并加400 µL PBS,立刻进行流式检测。
3 统计学处理
用SPSS 26.0和GraphPad Prism 8进行统计分析及作图。两基因的相关性使用Pearson相关分析。计量资料以均数±标准差(mean±SD)表示。组间比较采用检验或检验。以0.05为差异有统计学意义。
结果
1 用慢病毒载体携带shRNA-CSE1L构建急性髓系白血病细胞模型的效果
前期,同课题组成员已通过免疫组化实验证实CSE1L在急性髓系白血病中高表达[15]。本研究以急性髓系白血病THP-1细胞为模型进一步探讨敲减对THP-1细胞周期、凋亡的影响及其与阿糖胞苷敏感性的关系。经嘌呤霉素筛选的空载组及敲减组THP-1细胞绿色荧光蛋白(green fluorescent protein, GFP)表达水平均大于90%(图1A),提示慢病毒感染效果较好。RT-qPCR结果显示,与空载组相比,敲减组细胞CSE1L的mRNA水平降低到40%(图1B),提示敲减效果较好。
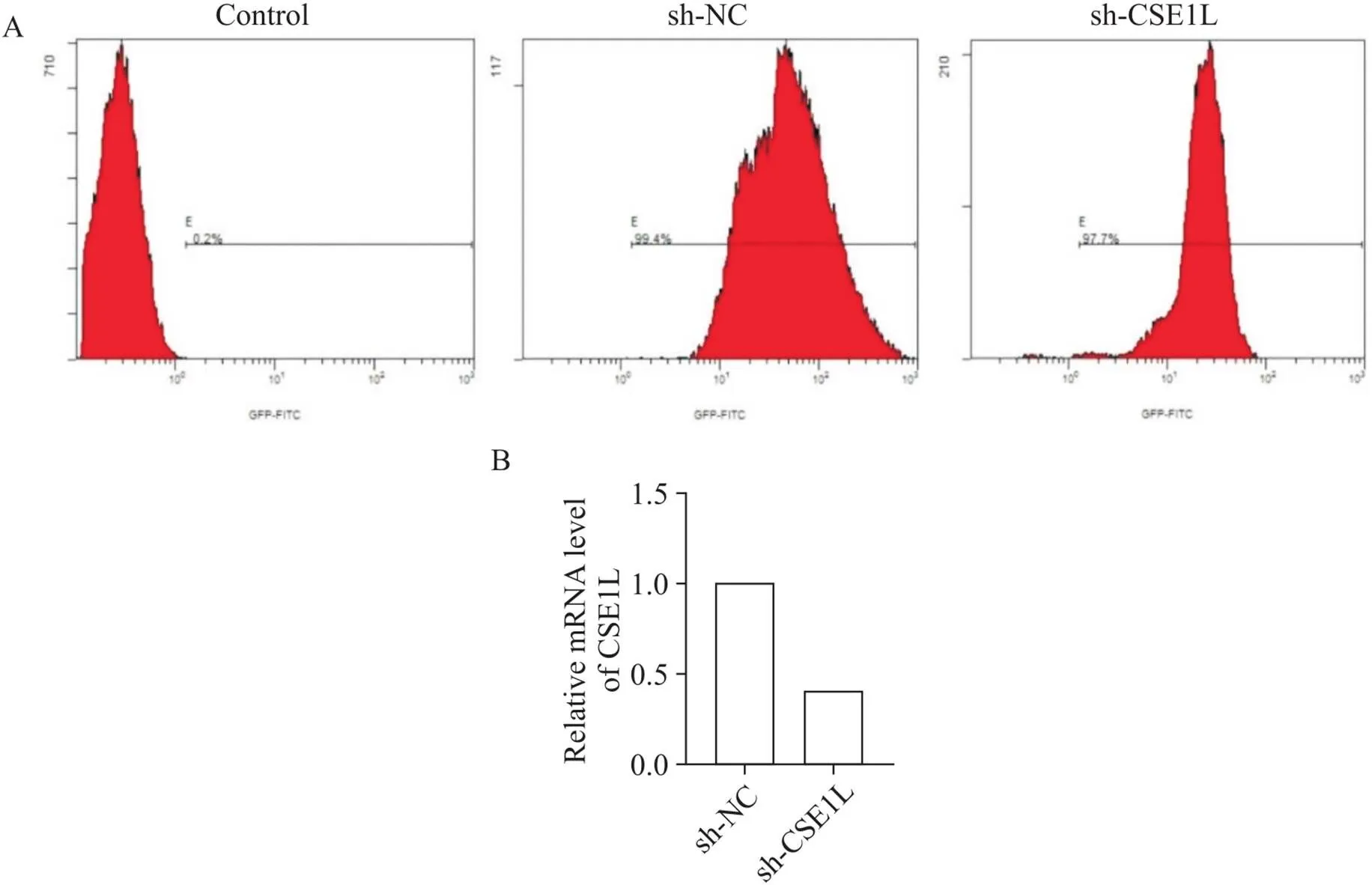
Figure 1. Establishment of a stably transfected cell line of CSE1L knockdown THP-1 cells. A: flow cytometry was used to detect the expression of GFP; B: the knockdown efficiency of sh-CSE1L was verified by RT-qPCR.
2 敲减CSE1L对THP-1细胞周期的影响
流式细胞术结果显示,与空载组相比,敲减组G0/G1期细胞占比升高(0.05),S期细胞占比降低(0.05),G2/M期无显著差异(图2A)。Western blot结果显示,与空载组相比,敲减组cyclin D1和c-Myc蛋白表达水平均显著降低(0.05或0.01),见图2B。
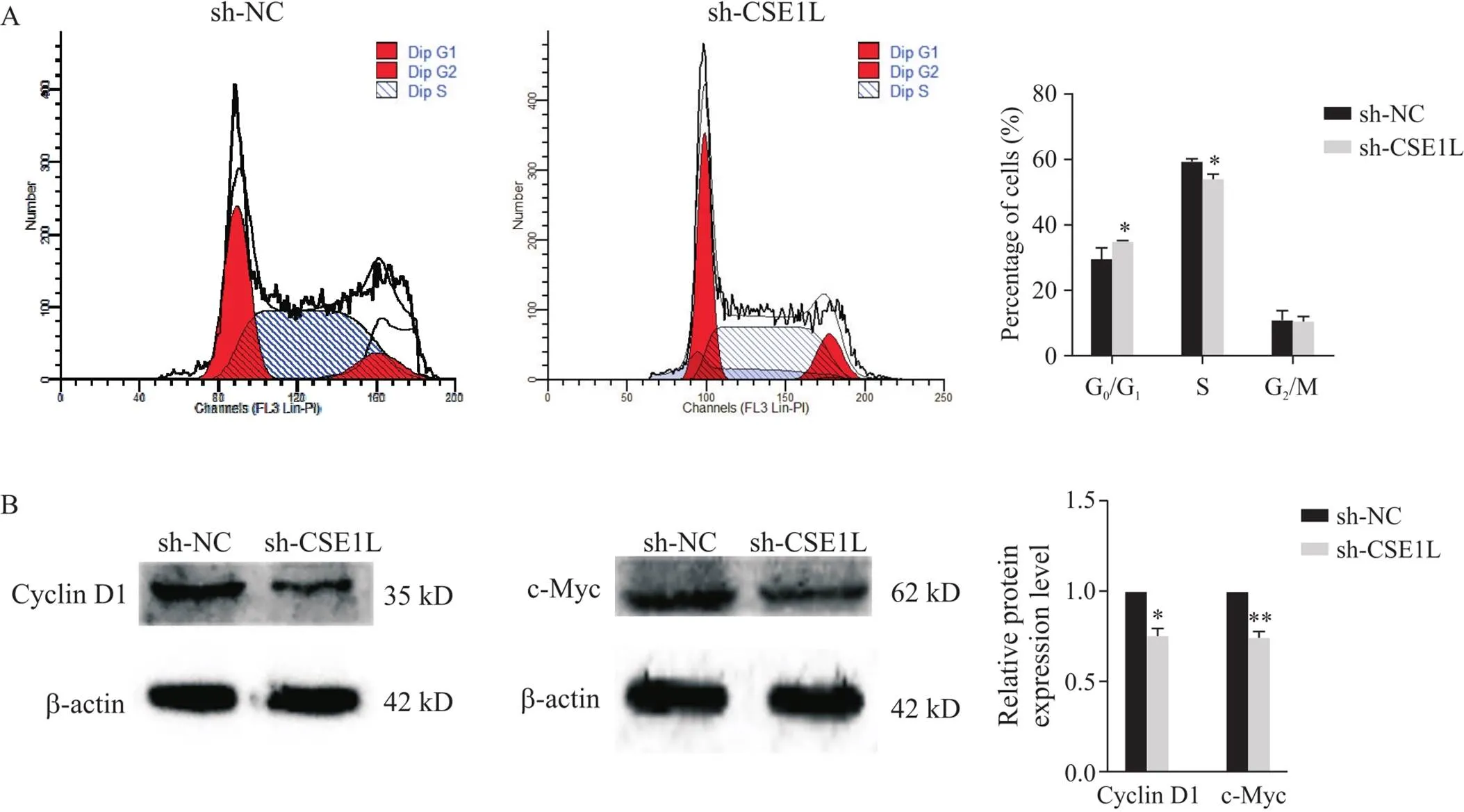
Figure 2. Effect of CSE1L knockdown on THP-1 cell cycle. A: knockdown of CSE1L blocked the THP-1 cell cycle; B: effect of CSE1L knockdown on the protein expression levels of cyclin D1 and c-Myc in THP-1 cells. Mean±SD. n=3. *P<0.05, **P<0.01 vs sh-NC group.
3 敲减CSE1L对THP-1细胞凋亡的影响
流式细胞凋亡检测结果显示,与空载组相比,敲减组凋亡率显著高于空载组(<0.01),见图3A。Western blot结果显示,与空载组相比,敲减组Bax蛋白相对表达水平显著升高(<0.05),而Bcl-2蛋白显著降低(<0.05),见图3B。
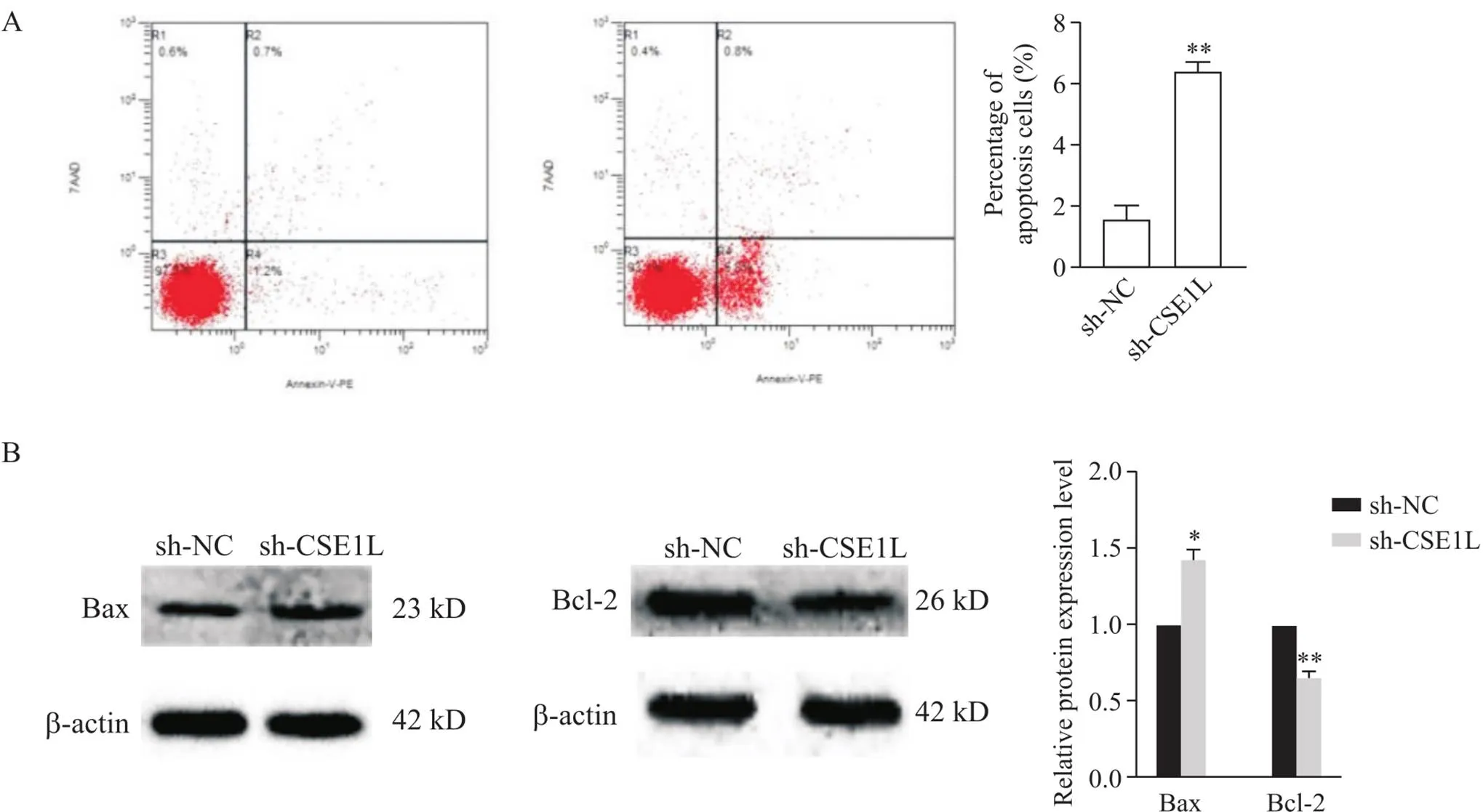
Figure 3. Effect of CSE1L knockdown on apoptosis of THP-1 cells. A: knockdown of CSE1L induced apoptosis of THP-1 cells; B: effect of CSE1L knockdown on the expression levels of apoptosis-related proteins in THP-1 cells. Mean±SD. n=3. *P<0.05,**P<0.01 vs sh-NC group.
4 各组细胞经阿糖胞苷处理后细胞活力及凋亡率的比较
细胞活力结果显示,经阿糖胞苷处理的敲减组细胞活力最低(<0.05),见图4A。流式细胞凋亡实验结果显示,经阿糖胞苷处理的敲减组细胞,凋亡率显著高于其他组(<0.01),见图4B。
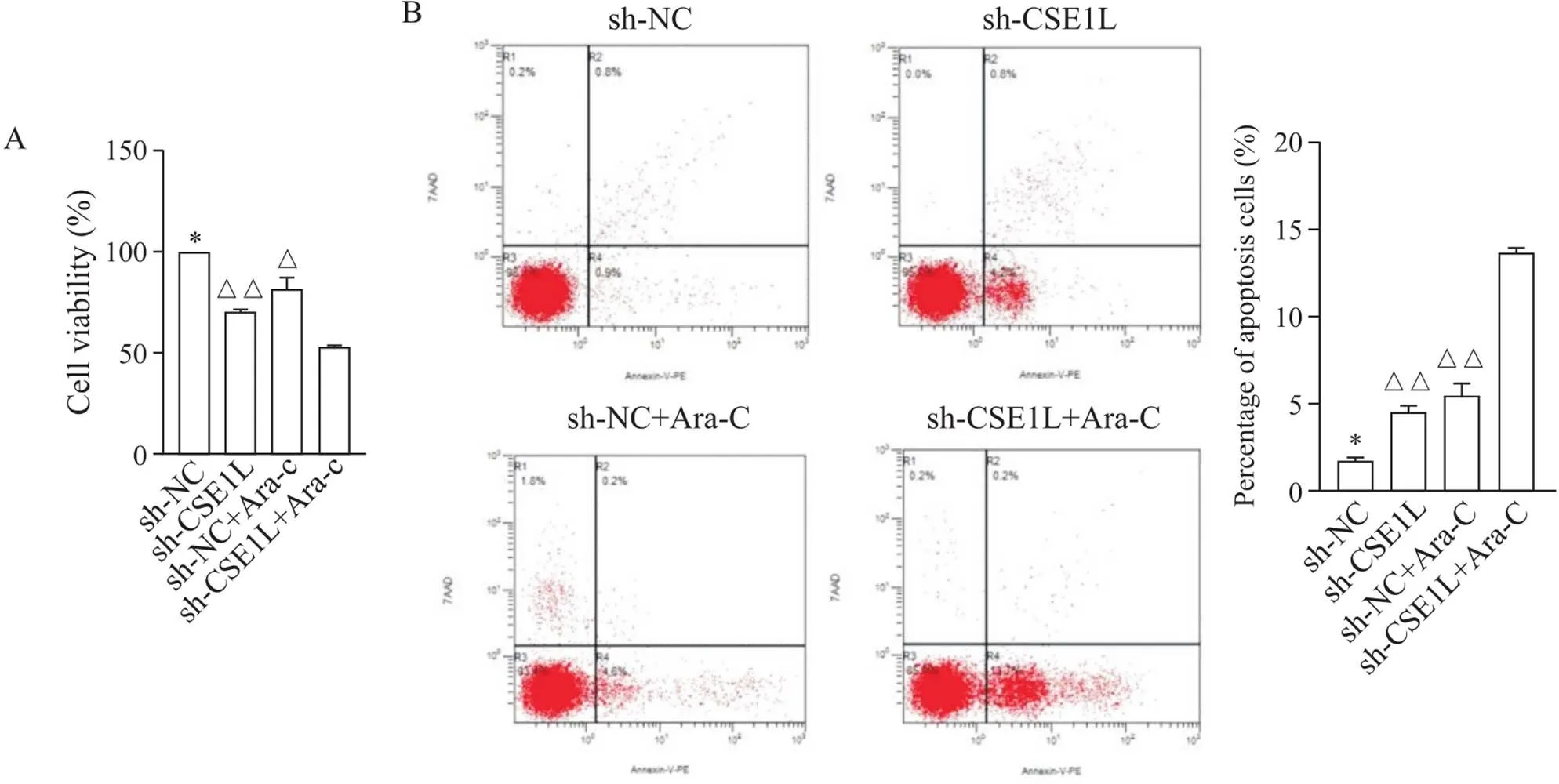
Figure 4. Changes in THP-1 cell viability (A) and apoptosis (B) in different Ara-C treatment groups. Mean±SD. n=3. *P<0.05 vs sh-CSE1L group; △P<0.05, △△P<0.01 vs sh-CSE1L+Ara-C group.
5 GO功能注释和KEGG通路富集分析
基于LinkedOmics数据库,筛选出与CSE1L正相关的基因5 044个,选择前50个作图(图5A)。基于DAVID数据库,将CSE1L相关性最靠前的1 000个正相关基因做通路富集分析,以0.05,FDR<0.05为阈值筛选,选择count值靠前的10个通路作图(图5B)。GO功能注释结果显示,这些正相关基因主要富集在细胞质,其次是细胞核;参与的生物过程主要是DNA修复,其次是细胞周期;发挥的生物学功能主要是蛋白质结合,其次是RNA结合。KEGG通路富集结果显示,CSE1L及其相关基因主要参与细胞周期、核质运输和FNA复制等信号通路。为进一步探究CSE1L正相关基因在细胞周期中的位置及作用,我们将细胞周期通路中的相关基因带入KEGG网站,生成相应的路线图(图5C),并将相关基因用红色标志。可以看出,大部分正相关基因与细胞周期的S、G2/M期相关。
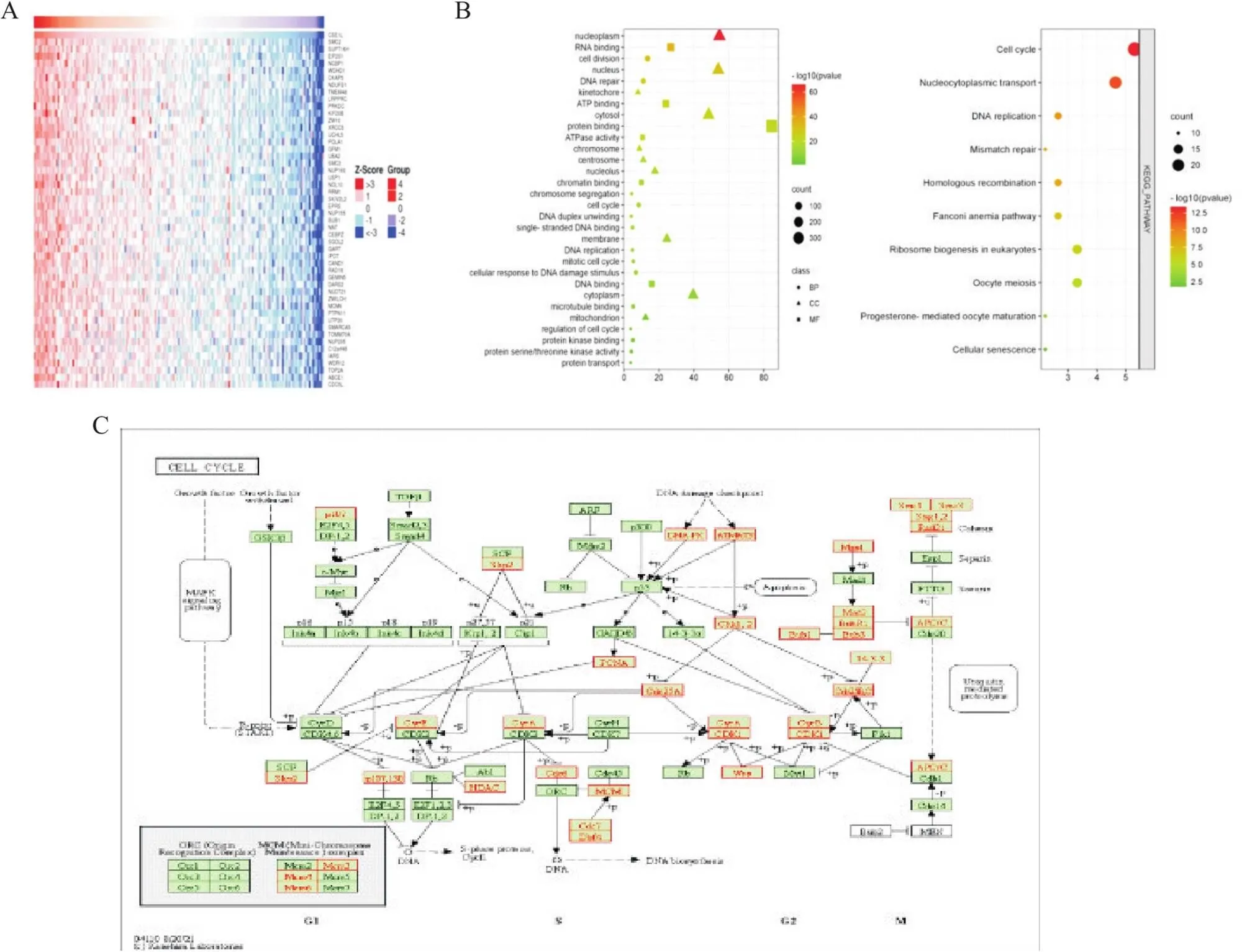
Figure 5. Positive correlation gene analysis for CSE1L. A: top 50 positive genes associated with CSE1L; B: enrichment analysis of GO and KEGG pathways; C: position relationship of CSE1L positive related genes during the cell cycle.
讨论
AML因其预后差、生存率低和容易复发等特点,严重威胁患者的健康[17]。阿糖胞苷通过抑制细胞DNA的合成干扰细胞增殖,是目前临床上用于治疗多种类型白血病的常用药[18-19]。尽管阿糖胞苷等多种基因毒性药物具有强杀伤力,但肿瘤细胞往往通过其固有的DNA修复能力来减轻药物引起的DNA损伤,从而产生毒副作用,导致肿瘤患者的5年生存率不足30%[20-21]。近年来,已有研究者注意到将特异性小分子抑制剂与AML标准化疗药物联合使用可能是一种理想的治疗选择[16]。因此,寻找新的特异性小分子抑制剂作用靶点以实现联合治疗迫在眉睫。
CSE1L最早发现于乳腺癌,其在维持细胞增殖与凋亡的平衡中扮演重要角色[22]。CSE1L已被发现在多种实体瘤中高表达。Luo等[23]研究表明,敲减可降低鼻咽癌细胞的增殖,增加肿瘤细胞的凋亡。Liu等[24]研究结果显示,敲减可影响肺癌细胞增殖,诱导细胞凋亡。本课题组前期已证实CSE1L在AML骨髓组织中表达水平高[15],但CSE1L在AML细胞中的作用尚无相关研究。为了研究CSE1L在AML细胞中作用的具体机制,我们以急性髓系白血病THP-1细胞为例,构建靶向敲减慢病毒,并感染THP-1细胞形成稳定敲减的细胞株。细胞周期检查点的破坏已被证实是肿瘤的一个标志[25]。本研究结果显示,敲减可阻滞THP-1细胞周期由G0/G1期向S期转变。此外,敲减引起周期相关蛋白cyclin D1和c-Myc表达水平降低。细胞凋亡是一种程序性细胞死亡,是参与肿瘤细胞死亡的代表性机制[26]。本研究结果显示,敲减可诱导THP-1细胞凋亡。同时凋亡相关蛋白Bcl-2表达水平降低,Bax蛋白表达水平升高。在阿糖胞苷处理条件下,敲减的细胞活力降低,凋亡率增加,表明抑制CSE1L可改善THP-1细胞对阿糖胞苷的敏感性。
迄今为止,CSE1L在AML中的分子作用机制尚不明确。因此,我们基于LinkedOmics数据库分析CSE1L在AML中正相关的基因。结果显示CSE1L正相关基因、和等均参与了AML的发生发展。Thol等[27]研究表明,基因突变与AML的不良预后高度相关。Fobare等[28]研究证实,基因突变与AML患者较高的早期死亡率相关。Zikmund等[29]研究显示,抑制可抑制AML细胞周期的进展,阻止细胞增殖。结果提示CSE1L在AML的发生发展中存在复杂的分子交互关系。基于DAVID数据库对CSE1L及其正相关前1 000个基因进行GO功能注释及KEGG通路富集分析,显示这些基因主要富集在细胞周期、DNA修复和蛋白质结合等过程。可视化参与细胞周期调控的相关基因,大部分与细胞周期的S和G2/M期相关。本研究提示CSE1L在AML中可能通过调控相关分子,影响生物合成,改变细胞周期等通路,进而调控AML的发生发展。
综上所述,敲减可诱导THP-1细胞凋亡,降低细胞活力,阻滞细胞周期,提高该细胞对阿糖胞苷的敏感性。我们建议对CSE1L进行抑制,并与标准化疗药物阿糖胞苷联合治疗,可以作为一种治疗CSE1L高表达的AML病例的新治疗策略。在未来的研究中,我们将从体内和体外继续研究敲减CSE1L对AML多种化疗药物敏感性的影响及更详细的分子机制。
[1] Löwenberg B, Rowe JM. Introduction to the review series on advances in acute myeloid leukemia (AML)[J]. Blood, 2016, 127(1):1.
[2] Watts JM, Bradley T. The Hi's and Lo's of cytarabine in acute myeloid leukemia[J]. Clin Cancer Res, 2020, 26(13):3073-3076.
[3] Momparler RL. Optimization of cytarabine (ARA-C) therapy for acute myeloid leukemia[J]. Exp Hematol Oncol, 2013, 2:20.
[4] Malani D, Murumägi A, Yadav B, et al. Enhanced sensitivity to glucocorticoids in cytarabine-resistant AML[J]. Leukemia, 2017, 31(5):1187-1195.
[5] Negoro E, Yamauchi T, Urasaki Y, et al. Characterization of cytarabine-resistant leukemic cell lines established from five different blood cell lineages using gene expression and proteomic analyses[J]. Int J Oncol, 2011, 38(4):911-919.
[6] Li Z, Guo JR, Chen QQ, et al. Exploring the antitumor mechanism of high-dose cytarabine through the metabolic perturbations of ribonucleotide and deoxyribonucleotide in human promyelocytic leukemia HL-60 cells[J]. Molecules, 2017, 22(3):499.
[7] Alnabulsi A, Agouni A, Mitra S, et al. Cellular apoptosis susceptibility (chromosome segregation 1-like,) gene is a key regulator of apoptosis, migration and invasion in colorectal cancer[J]. J Pathol, 2012, 228(4):471-481.
[8] Liu C, Wei J, Xu K, et al. CSE1L participates in regulating cell mitosis in human seminoma[J]. Cell Prolif, 2019, 52(2):e12549.
[9] Nagashima S, Maruyama J, Honda K, et al. CSE1L promotes nuclear accumulation of transcriptional coactivator TAZ and enhances invasiveness of human cancer cells[J]. J Biol Chem, 2021, 297(1):100803.
[10] Lin HC, Li J, Cheng DD, et al. Nuclear export protein CSE1L interacts with P65 and promotes NSCLC growth via NF-κB/MAPK pathway[J]. Mol Ther Oncolytics, 2021, 21:23-36.
[11] Li Y, Yuan S, Liu J, et al. CSE1L silence inhibits the growth and metastasis in gastric cancer by repressing GPNMB via positively regulating transcription factor MITF[J]. J Cell Physiol, 2020, 235(3):2071-2079.
[12] Wang YS, Peng C, Guo Y, et al. CSE1L promotes proliferation and migration in oral cancer through positively regulating MITF[J]. Eur Rev Med Pharmacol Sci, 2020, 24(10):5429-5435.
[13] Pimiento JM, Neill KG, Henderson-Jackson E, et al. Knockdown ofgene in colorectal cancer reduces tumorigenesis[J]. Am J Pathol, 2016, 186(10):2761-2768.
[14] Lorenzato A, Biolatti M, Delogu G, et al. AKT activation drives the nuclear localization of CSE1L and a pro-oncogenic transcriptional activation in ovarian cancer cells[J]. Exp Cell Res, 2013, 319(17):2627-2636.
[15] 郭浩然. CAS在急性白血病中的表达及临床相关性研究[D]. 太原: 山西医科大学, 2021.
Guo HR. Expression and clinical correlation study of CAS in acute leukemia[D]. Taiyuan: Shanxi Medical University, 2021.
[16] Menendez-Gonzalez JB, Sinnadurai S, Gibbs A, et al. Inhibition of GATA2 restrains cell proliferation and enhances apoptosis and chemotherapy mediated apoptosis in human GATA2 overexpressing AML cells[J]. Sci Rep, 2019, 9(1):12212.
[17] 张海鹏, 陈景, 陈秀云, 等. 和厚朴酚增强NK-92细胞对KG-1a细胞的杀伤作用及机制研究[J]. 中国病理生理杂志, 2021, 37(3):475-480.
Zhang HP, Chen J, Chen XY, et al. Honokiol enhances killing effect of NK-92 cells on KG-1a cells[J]. Chin J Pathophysiol, 2021, 37(3):475-480.
[18] Krauss AC, Gao X, Li L, et al. FDA approval summary: (daunorubicin and cytarabine) liposome for injection for the treatment of adults with high-risk acute myeloid leukemia[J]. Clin Cancer Res, 2019, 25(9):2685-2690.
[19] Murphy T, Yee KWL. Cytarabine and daunorubicin for the treatment of acute myeloid leukemia[J]. Expert Opin Pharmacother, 2017, 18(16):1765-1780.
[20] Song Y, Park SY, Wu Z, et al. Hybrid inhibitors of DNA and HDACs remarkably enhance cytotoxicity in leukaemia cells[J]. J Enzyme Inhib Med Chem, 2020, 35(1):1069-1079.
[21] Heuser M, Ofran Y, Boissel N, et al. Acute myeloid leukaemia in adult patients: ESMO clinical practice guidelines for diagnosis, treatment and follow-up[J]. Ann Oncol, 2020, 31(6):697-712.
[22] Behrens P, Brinkmann U, Wellmann A. CSE1L/CAS: its role in proliferation and apoptosis[J]. Apoptosis (London), 2003, 8(1):39-44.
[23] Luo Y, Qu X, Kan D, et al. The microRNA-451a/chromosome segregation 1-like axis suppresses cell proliferation, migration, and invasion and induces apoptosis in nasopharyngeal carcinoma[J]. Bioengineered, 2021, 12(1):6967-6980.
[24] Liu W, Zhou Z, Li Y, et al. CSE1L silencing impairs tumor progression via MET/STAT3/PD-L1 signaling in lung cancer[J]. Am J Cancer Res, 2021, 11(9):4380-4393.
[25] Barnaba N, LaRocque JR. Targeting cell cycle regulation via the G2-M checkpoint for synthetic lethality in melanoma[J]. Cell Cycle, 2021, 20(11):1041-1051.
[26] Pistritto G, Trisciuoglio D, Ceci C, et al. Apoptosis as anticancer mechanism: function and dysfunction of its modulators and targeted therapeutic strategies[J]. Aging (Albany NY), 2016, 8(4):603-619.
[27] Thol F, Bollin R, Gehlhaar M, et al. Mutations in the cohesin complex in acute myeloid leukemia: clinical and prognostic implications[J]. Blood, 2014, 123(6):914-920.
[28] Fobare S, Kohlschmidt J, Ozer HG, et al. Molecular, clinical, and prognostic implications of PTPN11 mutations in acute myeloid leukemia[J]. Blood Adv, 2022, 6(5):1371-1380.
[29] Zikmund T, Paszekova H, Kokavec J, et al. Loss of ISWI ATPase SMARCA5 (SNF2H) in acute myeloid leukemia cells inhibits proliferation and chromatid cohesion[J]. Int J Mol Sci, 2020, 21(6):2073.
Effect ofsilencing on cytarabine sensitivity of acute myeloid leukemia cells
LIU Xiaoyu1, LI Xudong2, GUAN Kunping3△
(1,,,030001,;2,030001,;3,,030001,)
To investigate the effect of chromosome segregation 1-like (CSE1L) on biological behavior and cytarabine (Ara-C) sensitivity of acute myeloid leukemia THP-1 cells, and to analyze its mechanism.The THP-1 cells were divided into control group, negavtive control (sh-NC) group, sh-CSE1L group, sh-NC+Ara-C group, and sh-CSE1L+Ara-C group. The mRNA expression of CSE1L was detected by RT-qPCR. Cell cycle and apoptosis were detected by flow cytometry. Gene ontology (GO) functional annotation and KEGG pathway enrichment analysis were performed by LinkedOmics and DAVID databases. The protein levels of cyclin D1, c-Myc, Bax and Bcl-2 were detected by Western blot.The expression of green fluorescent protein (GFP) was more than 90% in both the sh-NC and sh-CSE1L groups when compared with control group. Compared with sh-NC group, the mRNA expression level of CSE1L was reduced to 40% in sh-CSE1L group, and the apoptosis rate was significantly higher (<0.01). The cell cycle G0/G1phase was significantly higher (<0.05), and the S phase was significantly lower (<0.05) in sh-CSE1L group than in sh-NC group, while there was no significant difference in G2/M phase. Cell viability was the lowest (<0.05) and apoptosis was the highest (<0.01) in sh-CSE1L group after treated with Ara-C. In addition, silencing ofdown-regulated Bcl-2, cyclin D1 and c-Myc protein levels (<0.05), but up-regulated Bax protein level (<0.05). Bioinformatic analysis concluded that CSE1L is mainly involved in the cell cycle and other pathways.Knockdown ofblocks THP-1 cell cycle, induces apoptosis, and improves the sensitivity to Ara-C, which may act by regulating cell cycle-related molecules.
cytarabine; acute myeloid leukemia; chromosome segregation 1-like; cell cycle; apoptosis
R733.71; R363.2
A
10.3969/j.issn.1000-4718.2023.02.009
1000-4718(2023)02-0269-07
2022-09-06
2022-11-30
[基金项目]山西省重点研发计划项目(No. 201903D321093)
Tel: 13700514558; E-mail: guankunping5135@126.com
(责任编辑:宋延君,李淑媛)
