胱天蛋白酶11介导的Hippo信号通路在脑缺血再灌注小鼠血脑屏障破坏中的作用和机制*
2023-03-10张创余孝君唐波江威谢君
张创, 余孝君, 唐波, 江威, 谢君
胱天蛋白酶11介导的Hippo信号通路在脑缺血再灌注小鼠血脑屏障破坏中的作用和机制*
张创, 余孝君△, 唐波, 江威, 谢君
(长沙市第一医院神经内科,湖南 长沙 410000)
探讨胱天蛋白酶11(caspase-11)在脑缺血再灌注小鼠血脑屏障(blood-brain barrier, BBB)破坏中的作用和机制。将72只小鼠[包括36只(编码caspase-11的基因)敲减(knockdown, KD)小鼠和36只野生型(wild-type, WT)小鼠]分为4组(每组18只):WT组、KD组、大脑中动脉闭塞/再灌注损伤(middle cerebral artery occlusion/reperfusion injury, MCAO/R)组和KD+MCAO/R组。其中,MCAO/R组和KD+MCAO/R组分别采用WT小鼠和KD小鼠建立MCAO/R模型,其他组在不干扰动脉的情况下进行了相同的外科手术。此外,将脑微血管内皮细胞系bEnd.3分为4组:正常对照(normal control, NC)组、KD组、氧糖剥夺/再灌注损伤(oxygen-glucose deprivation/reperfusion injury, OGD/R)组和KD+OGD/R组。其中,KD组和KD+OGD/R组bEnd.3细胞进行敲减转染,OGD/R组和KD+OGD/R组细胞建立OGD/R模型。通过TTC、HE和尼氏染色分析脑损伤的程度。通过伊文思蓝染料渗漏、紧密连接(tight junction, TJ)蛋白的表达和经内皮电阻(transendothelial electrical resistance, TEER)的测量来研究BBB的破坏情况。MCAO/R后,caspase-11在小鼠脑内皮细胞中表达上调(<0.05)。KD+MCAO/R组小鼠较MCAO/R组脑梗死体积减少,内皮屏障通透性降低,TJ蛋白ZO-1和occludin表达增加(<0.05)。在体外,OGD/R显著增加了bEnd.3细胞caspase-11的蛋白水平(<0.05),并降低了TJ蛋白ZO-1和occludin的蛋白水平(<0.05)。敲减通过促进TJ蛋白表达和增加TEER来保护BBB完整性。敲减逆转了MCAO/R和OGD/R诱导的脑内皮细胞中Hippo信号通路哺乳动物不育系20样激酶1(mammalian sterile 20-like kinase 1, MST1)磷酸化水平的升高(<0.05)。此外,用p-MST1抑制剂XMU-MP-1治疗可减轻caspase-11对BBB分解的影响(<0.05)。抑制caspase-11至少部分通过调节Hippo信号通路来保持脑缺血再灌注小鼠BBB的完整性。
胱天蛋白酶11;缺血性卒中;血脑屏障;Hippo信号通路;哺乳动物不育系20样激酶1
缺血性卒中是一种危及生命的疾病,具有高死亡率、高残疾率和高复发率。卒中急性期的能量和氧气损失会导致神经元凋亡、炎症、活性氧积累、兴奋性毒性和血脑屏障(blood-brain barrier, BBB)损伤,从而进一步加剧神经功能缺损[1-2]。由于卒中治疗窗口期很窄,大量患者错过了最佳治疗期。因此,寻找新的靶点和方法来治疗卒中,特别是在急性期,是必要和关键的。胱天蛋白酶11(caspase-11)作为一种非经典炎症小体,最初在肿瘤相关研究中被发现,据报道可促进多种类型的肿瘤进展[3-4]。caspase-11可招募凋亡斑点样蛋白和caspase-1,形成多蛋白复合物,以支持白细胞介素(interleukin, IL)-1β和IL-18的成熟和分泌,从而诱导炎症细胞中的炎症反应[5]。最近的一项研究表明,caspase-11主要定位于脑卒中后认知障碍小鼠的内皮细胞[6]。此外,先前研究表明,caspase-11的选择性抑制剂wedelolactone通过抑制星形胶质细胞中caspase-11的激活,防止甲基苯丙胺诱导的神经炎症发生[7]。尽管如此,caspase-11在缺血性卒中损伤中的作用,尤其是在BBB破坏中的作用尚不清楚。在本研究中,我们通过建立大脑中动脉闭塞/再灌注(middle cerebral artery occlusion/reperfusion, MCAO/R)小鼠模型来研究caspase-11在急性期缺血性卒中中的作用。同时我们在脑微血管内皮细胞系bEnd.3中使用了氧糖剥夺/再灌注损伤(oxygen-glucose deprivation/reperfusion injury, OGD/R)模型以进一步验证caspase-11的潜在机制。
材料和方法
1 实验动物和分组
使用CRISPR/Cas9技术制作的(编码caspase-11的基因)敲减(knockdown, KD)小鼠36只,54只年龄匹配的C57BL/6J同窝小鼠用作野生型(wild-type, WT)对照,以上小鼠均为SPF级,购自南京大学模式动物研究所[生产许可证号:SCXK(苏)2018-0008]。在平均体重为22~25 g的8周龄雄性小鼠上进行实验。小鼠在12 h明暗循环中每笼饲养6只,并在适当的温度(22±2) ℃和湿度55%±5%条件下获得充足的食物和水供应。为了确定caspase-11在MCAO/R损伤后大脑中的表达情况,将18只WT小鼠分为6组,每组3只:假手术(sham)组、MACO 0.5 h组、MACO 1 h组、MCAO 1 h/R 1 h组、MCAO 1 h/R 6 h组和MCAO 1 h/R 24 h组。将72只小鼠(包括36只KD小鼠和36只WT小鼠)分为4组,每组18只:WT组、KD组、MCAO/R组和KD+MCAO/R组,其中MCAO/R组和KD+MCAO/R组分别采用WT小鼠和KD小鼠建立MCAO/R模型,其他组在不干扰动脉的情况下进行相同的外科手术。
2 主要方法
2.1MCAO/R模型的建立参照文献方法[8],使用基于腔内细丝的方法诱导MCAO/R。在构建模型之前用1.5%异氟醚麻醉小鼠。为了阻断小鼠大脑同侧半球的血液供应,通过将4-0尼龙单丝缝合线插入右侧颈内动脉来阻断右侧大脑中动脉。动物接受MCAO相应时间,然后通过小心撤出细丝进行再灌注。假手术组小鼠,在不干扰动脉的情况下进行相同的外科手术。在整个过程中,小鼠放置在加热毯上维持体温。
2.22,3,5-三苯基氯化四唑(2,3,5-triphenyl tetrazolium chloride, TTC)染色再灌注后24 h迅速取出大脑,进行TTC染色以评估组织活力并测量梗死面积。在ImageJ软件中测量梗死面积。梗死面积=对侧正常脑组织半球面积-患侧正常脑组织面积。梗死体积=每个切片上的梗死面积×切片厚度。梗死体积表示为每个同侧半球梗死的百分比。
2.3神经功能缺损评估参照文献方法[9],采用Longa测试对实验动物的神经功能缺损按18分制进行分级。在再灌注后24 h对小鼠进行测试。Longa测试的指标包括:自发活动,运动对称性,前肢对称性,攀爬,对触摸的反应,以及对触须触摸的反应。所有6项单项测试均以3、2、1或0分的四分制评分。通过将每个单项测试记录的分数相加获得最终分数,在健康动物中观察到的最高分数为18。
2.4组织病理学评估MCAO/R后处死小鼠,用生理盐水从心脏灌注至体循环,直至肝脏呈白色,再灌注4 ℃的4%多聚甲醛溶液。将大脑取出,在4 ℃的4%甲醛溶液中浸泡过夜。之后,大脑通过分级乙醇和二甲苯进行处理。通过使用脑基质,前脑被冠状切开成两个等距的切片,并在分离后脑后嵌入石蜡块中。将位于冠状平面中前囟后面1.5 mm的脑切片用vibratome (Leica)切成5 µm切片并置于载玻片上。切片在二甲苯中脱蜡并在100%至70%梯度乙醇中再水化。最后进行苏木精-伊红染色(HE染色),切片用双蒸水洗涤,乙醇脱水,二甲苯清洗,使用BX-51光学显微镜(Olympus)检查。对于尼氏染色,将切除的脑组织用4%甲醛固定,切成薄片并用甲苯啶蓝染色,光学显微镜用于图像捕获,神经元中圆形和轻微染色的细胞核被称为存活细胞。
2.5伊文思蓝(Evans blue, EB)分析通过尾静脉注射EB染色剂渗漏到大脑中来评估BBB渗透性。在对动物实施安乐死前2 h,将含2% EB(Sigma Aldrich)的生理盐水以剂量为0.01 mL/ g体重注射到每只动物中。再灌注后24 h处死小鼠,快速取出大脑。然后将小鼠用生理盐水灌注。对于EB泄漏进行定量测量,取出同侧半球并在1 mL三氯乙酸中均质化,然后以12 000×离心20 min。通过用分光光度计测量上清液在620 nm处的吸光度()来定量测定EB浓度。使用标准曲线将EB含量量化为每克组织的微克EB。
2.6免疫荧光染色在再灌注后24 h用PBS和4%多聚甲醛灌注3 min后,取出脑组织并置于4 ℃的4%多聚甲醛中。1 d后,脑组织用40%蔗糖脱水5 d,包埋在OTC中,-70 ℃冷冻。使用冷冻切片机(Leica)将脑组织切成10 µm厚的切片,然后放置在粘附显微镜载玻片上。将脑切片或培养细胞固定在4%多聚甲醛中,用0.3% Triton X-100渗透,5%正常驴血清封闭,并在4 ℃下用特异性Ⅰ抗(caspase-11,1∶200, Abcam;p-MST1,1∶200, CST;CD31、GFAP、Iba1和NeuN,1∶200, Santa Cruz)孵育过夜。然后,将切片与相应的Ⅱ抗在室温下孵育。DAPI 用于染色细胞核。对于免疫染色分析,使用FV1000共聚焦显微镜(Olympus)或IX73荧光显微镜(Olympus)拍摄图像以检查染色的脑切片。
2.7细胞培养脑微血管内皮细胞系bEnd.3购自中国科学院上海细胞生物学研究所,接种在含有10%胎牛血清、1×105U/L青霉素和100 mg/L链霉素的DMEM培养基中37 ℃培养。培养环境为5% CO2和95%空气。将细胞分为4组:正常对照(normal control,NC)组、KD组、OGD/R组和KD+OGD/R组。其中,KD组和KD+OGD/R组bEnd.3细胞进行敲减(shCASP11转染24 h)。然后,OGD/R组和KD+OGD/R组细胞建立OGD/R模型。
2.8OGD/R模型建立参照文献方法[8],在体外复制OGD/R。为了在体外通过OGD/R产生I/R样条件,将bEnd.3细胞置于37 ℃厌氧室(0.2% O2、5% CO2、95% N2)中并在无葡萄糖培养液中培养6 h。在氧-葡萄糖剥夺后,将细胞置于含有10%胎牛血清和葡萄糖的DMEM中,然后在常氧条件下孵育24 h以模拟再灌注。对照组取自在正常条件下培养的细胞。根据先前的报道[10],选择性哺乳动物不育系20样激酶1(mammalian sterile 20-like kinase 1, MST1)抑制剂XMU-MP-1(上海蓝木化工有限公司)的有效剂量为50 nmol/L,用于受损的内皮细胞。
2.9Western blot再灌注后24 h处死小鼠,快速取出大脑。在OGD/R后迅速收集细胞。将细胞或组织置于玻璃匀浆器中在1∶107 (/)冰冷的蛋白质提取缓冲液中匀浆。收集可溶性蛋白,4 ℃、12 000×离心10 min,取上清液检测caspase-11、MST1、p-MST1、ZO-1、occludin和总蛋白质。采用BCA蛋白检测试剂盒测定蛋白质浓度。每组等量的蛋白裂解物(50 μg)用8%和12% SDS-PAGE分离。随后将凝胶上的蛋白质转移到硝酸纤维素膜上(260 mA,2 h)。将膜用含5%脱脂牛奶的PBST室温封闭2 h,然后分别与兔Ⅰ抗(caspase-11,1∶800, Abcam;MST1和p-MST1,1∶500, CST;ZO-1和occludin,1∶500,Abcam)4 ℃孵育过夜。然后洗涤膜并与Ⅱ抗(抗兔IgG,1∶3 000,Proteintech)室温下孵育1.5 h。抗GAPDH抗体(1∶1 000,Proteintech)作为对照。用增强的化学发光试剂观察蛋白质条带,并使用蛋白质印迹检测系统(Bio-Rad)量化信号密度。
2.10经内皮电阻(transendothelial electrical resistance, TEER)的测量使用上皮伏欧计(EVOM, World Precision Instruments)测量培养的单层bEnd.3细胞的TEER。实验进行3次,记录平均值。
3 统计学处理
所有计量数据均使用SPSS 18.0软件进行分析,并表示为平均值±标准误(mean±SEM)。通过Shapiro-Wilk 检验分析数据分布的正态性。为了比较两组之间的差异,正态分布的连续变量通过Student's检验进行比较,而非正态分布的变量通过Mann-Whitney检验进行比较。对于3组或多组之间的多重比较,使用单因素方差分析,如果数据呈正态分布,则使用Bonferroni事后检验;如果数据非正态分布,则使用Kruskal-Wallis检验。以<0.05为差异有统计学意义。
结果
1 caspase-11在体内和体外遭受MCAO/R或OGD/R的脑微血管内皮细胞中高表达
为了确定caspase-11在缺血性卒中的具体作用,我们首先使用Western blot和免疫荧光分析测量了MCAO/R损伤后大脑中caspase-11的表达。结果显示,与假手术组相比,MCAO 1 h/R 1 h组caspase-11表达显著增加(<0.05),并且高表达一直保持到再灌注后24 h(图1A)。细胞分布研究表明,caspase-11在MCAO 1 h/R 1 h后主要分布在脑微血管内皮细胞(brain microvascular endothelium cells, BMECs)中,在小胶质细胞、星形胶质细胞和神经元中分布较少(图1B)。为了证实caspase-11在脑MCAO/R损伤早期主要在BMECs中表达,我们在体外OGD/R模型中评估了caspase-11在脑源性内皮细胞系bEnd.3细胞中的表达。在OGD 6 h/R 1 h后caspase-11表达逐渐增加(<0.05),见图1C。免疫荧光分析显示caspase-11的高表达发生在OGD 6 h/R 1 h (图1D),这与体内研究的结果一致。
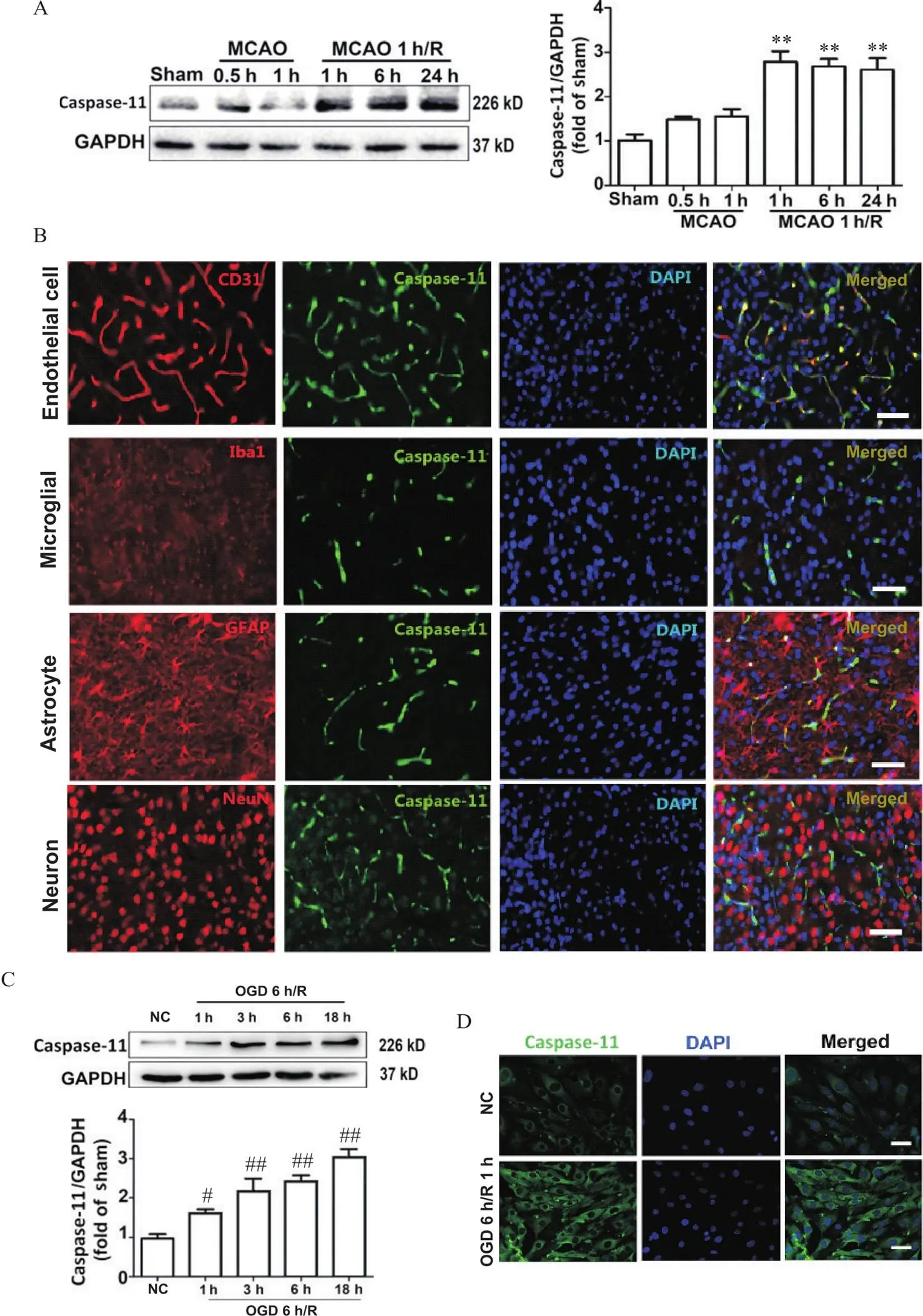
Figure 1. Expression of caspase-11 in cerebral microvascular endothelial cells with ischemia/reperfusion injury. A: time course of brain MCAO/R-induced total protein expression of caspase-11 in mice detected by Western blot; B: anti-caspase-11 (green), anti-CD31 (red, to label endothelial cells), anti-GFAP (red, to label astrocytes), anti-Iba1 (red, to label microglia), anti-NeuN (red, to label neurons) antibodies, and DAPI (blue) were combined to detect MCAO/R-induced total caspase-11 protein expression; C: bEnd.3 cells were exposed to 6 h of OGD, and 1 h, 3 h, 6 h and 18 h of reoxygenation, and time course of OGD/R-induced caspase-11 total protein expression in bEnd.3 cells was detected by Western blot; D: bEnd.3 cells underwent 6 h of OGD and 1 h of reoxygenation, and OGD/R-induced total protein expression of caspase-11 was detected (scale bar=20 μm). Mean±SEM. n=3. **P<0.01 vs sham group; #P<0.05, ##P<0.01 vs NC group.
2 CASP11敲减可减轻MCAO/R诱导的神经损伤
根据Western blot结果,caspase-11在KD小鼠中的敲减效率约为50%~60%(图2A)。在KD小鼠中构建MACO/R模型后,我们检测了梗死体积。与WT组相比,MACO/R组小鼠脑梗死体积显著增加(<0.05),KD+MACO/R组小鼠脑梗死体积显著降低(<0.05),见图2B。HE染色和和尼氏染色显示,KD+MACO/R组小鼠脑组织中的空泡形成、死亡神经元数量较MACO/R组小鼠减少,神经功能缺损评分显著增加(<0.05),见图2C~E。
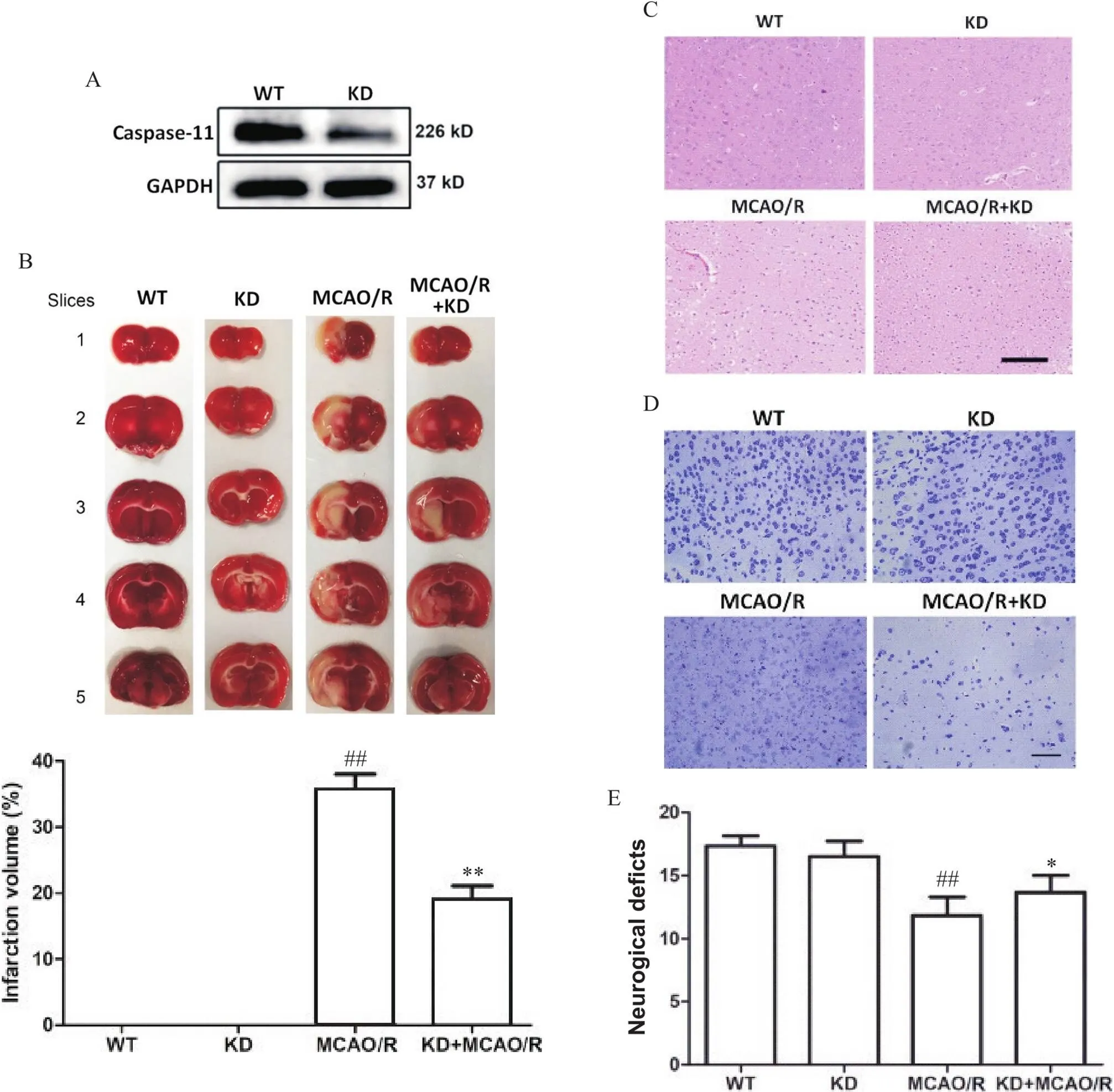
Figure 2. Effect of CASP11 knockdown on brain injury induced by MCAO/R in mouse brain. A: Western blot verification of CASP11 knockdown efficiency in KD group; B: representative photos of mouse brains stained with TTC [the tissue was stained red to indicate no infarction, and unstained (white) to indicate the infarct area], and quantitative analysis of infarct volume in different groups; C: morphological changes of MCAO/R mouse brains under light microscope (HE staining, scale bar=50 µm; normal tissue was purple-red, with round and full nuclei and dense texture; the damaged tissue was whitish, pyknosis, numerous holes, and signs of hemorrhage); D: Nissl staining showing neuronal death in the MCAO/R mouse brain (scale bar=50 µm); E: neurological deficit scores in different groups (the lower the score, the more serious the damage). Mean±SEM. n=5. ##P<0.01 vs WT group; *P<0.05, **P<0.01 vs MCAO/R group.
3 CASP11敲减减轻脑MCAO/R损伤引起的BBB破坏
与MCAO/R组相比,KD+MACO/R组小鼠EB渗漏显著减少(<0.05),脑组织中ZO-1和occludin表达显著升高(<0.05),见图3。
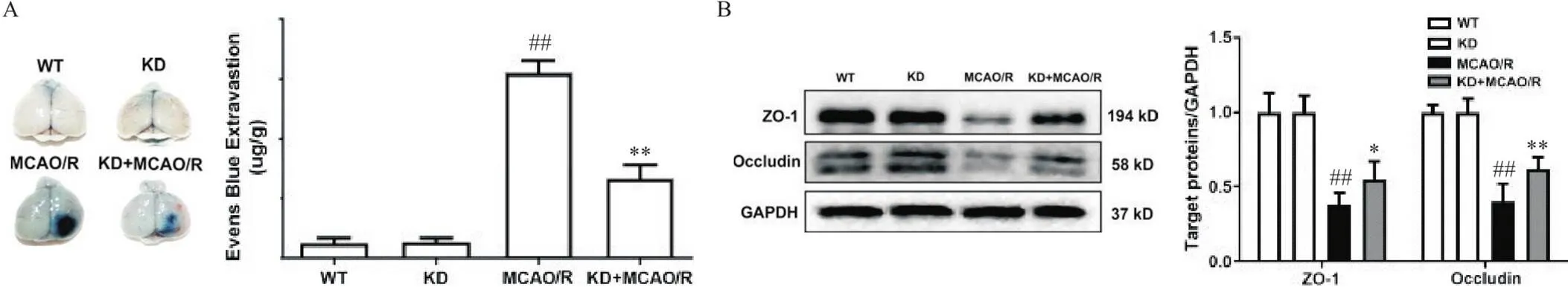
Figure 3. Effects of CASP11 knockdown on blood-brain barrier disruption induced by MCAO/R in mouse brain. A: representative gross appearance of Evans blue-stained brains in mice of different groups; B: representative Western blot pictures of ZO-1 and occludin expression in mouse brain tissues of different groups. Mean±SEM. n=5. ##P<0.01 vs WT group; *P<0.05, **P<0.01 vs MCAO/R group.
4 CASP11敲减减轻了体外OGD/R引起的BBB相关损伤
在体外用慢病毒在内皮细胞中沉默CASP11表达。通过Western blot评估shCASP11的转染效率,显示被成功敲减(图4A)。TEER测定用于评估体外BBB完整性,如图4B所示,与NC组相比,OGD/R组TEER显著降低(<0.05),但OGD/R+KD组TEER显著高于OGD/R组(<0.05)。此外,OGD/R组ZO-1和occludin表达较NC组显著降低(<0.05),而OGD/R+KD组OGD/R组ZO-1和occludin表达显著升高(<0.05),见图4C。
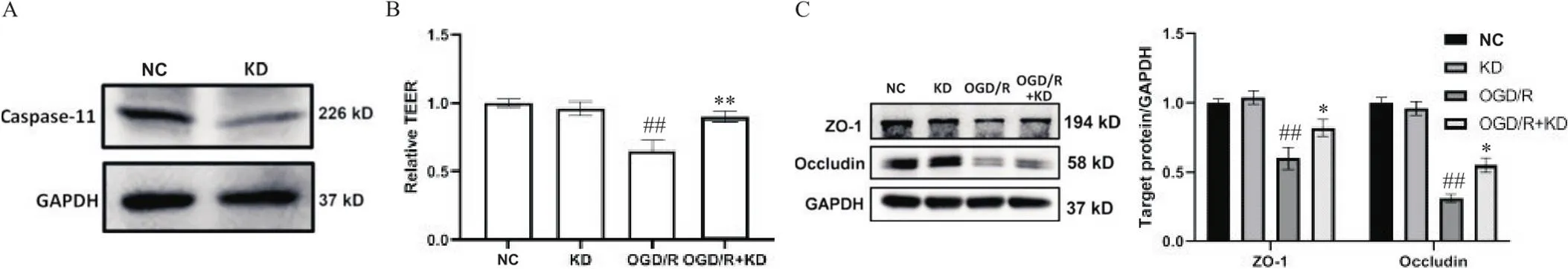
Figure 4. The effect of CASP11 knockdown on OGD/R-induced blood-brain barrier decomposition. A: Western blot was used to verify the efficiency of CASP11 knockdown in endothelial cells of KD group; B: quantification of transendothelial permeability by TEER assay; C: Western blot analysis of ZO-1, occludin and GAPDH after OGD/R. Mean±SEM. n=3. ##P<0.01 vs NC group; *P<0.05, **P<0.01 vs OGD/R group.
5 CASP11敲减在体内和体外均参与调节Hippo信号通路
与WT组相比,MCAO/R组脑组织中p-MST1水平显著提高(<0.05),但MCAO/R+KD组p-MST1水平显著低于MCAO/R组(<0.05),见图5A。为了进一步研究内皮细胞中p-MST1的水平是否发生变化,我们在MCAO/R后小鼠大脑的完整和同侧半影区进行了p-MST1和CD31双重染色来标记。与WT组相比,MCAO/R组的p-MST1和CD31的共定位数量显著增加(<0.05),但MCAO/R+KD组p-MST1和CD31的共定位数量显著低于MCAO/R组(<0.05),见图5B。此外,与体内观察到的模式相似,OGD/R组p-MST1表达显著提高(<0.05),而OGD/R+KD组则显著降低(<0.05),见图5C。与NC组相比,OGD/R组p-MST1和caspase-11水平显著增加(<0.05)。然而,XMU-MP-1预处理逆转了OGD/R后p-MST1表达的增加(<0.05),而不影响caspase-11的水平(图5D)。此外,OGD/R+XMU-MP-1组的TEER显著高于OGD/R组(<0.05),见图5E。
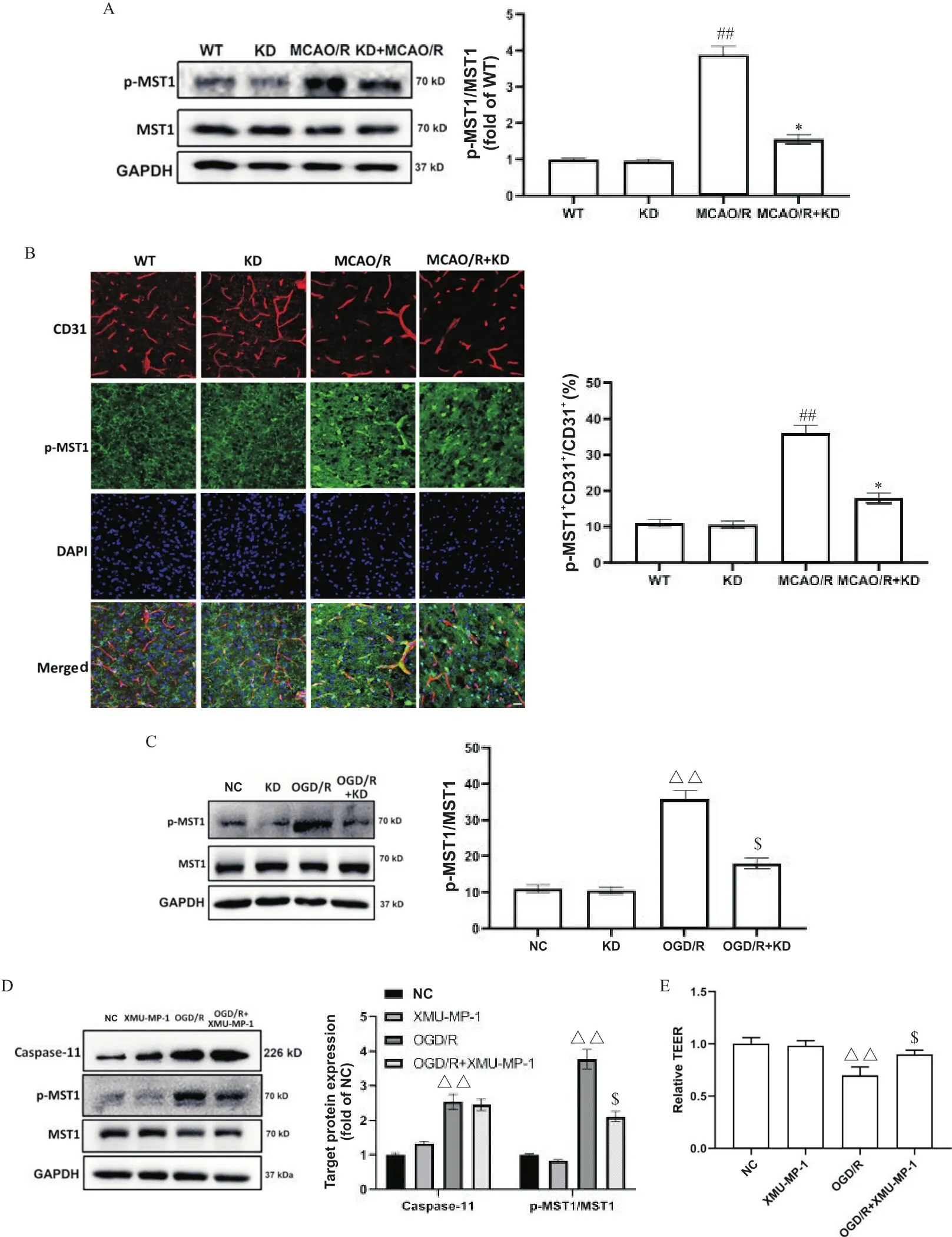
Figure 5. The effect of CASP11 knockdown on Hippo signaling pathway in vivo and in vitro. A: representative Western blot pictures of MST1 and p-MST1 expression in mouse brain tissues of different groups (n=5); B: MCAO/R induced CD31+ p-MST1+ vessel length versus total CD31+ vessel length detected by immunofluorescence in mice using a combination of anti-p-MST1 (green), CD31 (red) and DAPI (blue) (n=5); C: Western blot analysis of MST1, p-MST1 and GAPDH after OGD/R (n=3); D: Western blot analysis of the effect of XMU-MP-1 on the expression of caspase-11, MST1, p-MST1 and GAPDH after OGD/R (n=3); E:the effect of XMU-MP-1 (p-MST1 inhibitor) on transendothelial permeability after OGD/R was determined by TEER analysis (n=3). Mean±SEM. ##P<0.01 vs WT group; *P<0.05 vs MCAO/R group; △△P<0.01 vs NC group; $P<0.05 vs OGD/R.
讨论
本研究旨在探讨caspase-11对缺血性卒中后BBB完整性的影响,并在小鼠脑缺血再灌注损伤后观察到caspase-11在脑微血管中的表达增加。的敲减改善了小鼠脑缺血再灌注损伤诱导的BBB功能障碍。研究证实,caspase-11参与调节脑缺血再灌注损伤中Hippo信号传导,并通过促进紧密连接(tight junction, TJ)蛋白降解来破坏脑BBB完整性。因此,在小鼠脑缺血再灌注期间抑制caspase-11表达是促进缺血性卒中恢复的新策略。
BBB是一个复杂的多维网状屏障,可阻止有害物质进入中枢神经系统,脑缺血可破坏其结构和功能[11-12]。最近,越来越多的证据表明,炎症小体参与许多疾病中的BBB损伤。caspase-11被证明是革兰氏阴性细菌脂多糖(lipopolysaccharide, LPS)的直接传感器,其通过和LPS的脂质A部分之间的相互作用形成LPS-caspase-11复合物,进而导致caspase-11非正常炎症体的激活和随后诱导的炎症反应[13]。研究显示,caspase-11非经典炎性体诱导的K+流出是NLRP3炎性体通过细胞膜损伤和细菌成孔毒素以及膜孔激活的必要步骤[14]。此外,caspase-11非经典炎症小体的激活还诱导下游效应分子caspase-1的蛋白水解活化,导致caspase-1介导的蛋白水解成熟和促炎细胞因子IL-1β和IL-18通过膜孔[15]。然而到目前为止,缺血性卒中条件下caspase-11表达变化的时间过程、具体作用以及维持BBB完整性的调节机制仍不清楚。本研究显示,在脑缺血再灌注损伤时,BMECs中caspase-11的表达变化最早,并在再灌注期间达到最高水平。此外,caspase-11在小胶质细胞、星形胶质细胞和神经元中分布较少,因此我们假设BMECs是caspase-11在缺血性卒中BBB损伤中的主要靶细胞。为了进一步探索caspase-11在脑缺血再灌注损伤诱导的BMECs中的功能,我们构建了敲减小鼠。在约50%至60%的敲减效率下,敲减减少了脑梗死体积和死亡神经元数量,改善了神经功能缺损。我们的结果表明敲减改善了MCAO/R诱导的小鼠脑损伤。
BBB内皮细胞通过TJ蛋白连接,在MCAO/R后TJ相关蛋白的mRNA和蛋白水平显著降低[16]。许多增加TJ蛋白表达的药物已被证明可以减少卒中后BBB渗漏[1-2]。相反,TJ的分解和重新分布导致BBB高渗透性,并诱导液体和小分子从血液外渗到中枢神经系统,进一步破坏BBB并允许大分子最终渗漏[17]。本研究中,敲减可以降低伊文思蓝渗漏,并增加TJ蛋白(ZO-1和occludin)的表达。此外,体外实验也得到类似的结果,表明敲减可以通过促进TJ保存来维持内皮屏障的完整性。因此,caspase-11可能是维持MCAO/R小鼠BBB完整性的重要靶分子。
最近的研究证明,Hippo信号通路参与了脑缺血再灌注损伤诱导的BBB的破坏[11]。MST1是Hippo信号通路中的主要成员,其通过和Sav1激酶形成复合物,抑制了Hippo通路中的主要下游效应子YAP/TAZ[18]。许多研究表明,MST1参与炎症、应激反应和细胞凋亡的进展[19]。在神经疾病方面,基因敲除通过调节抑郁样小鼠的神经活动来防止工作记忆受损[20]。此外,MST1抑制通过逆转相关的有丝分裂吞噬作用减轻非酒精性脂肪肝损伤[21]。研究显示,MST1与脑缺血引起的神经炎症有关,并且的基因敲减可减少神经元死亡并改善创伤性脑损伤的神经损伤[22]。基于这些观察,我们假设CASP11缺失通过影响MST1激活促进了BBB完整性,并通过体内、体外实验证实了的敲减通过调节Hippo/MST1信号通路减轻MCAO/R、OGD/R诱导的BBB通透性增加。这些观察丰富了我们对TJ信号传导调控机制的认识,并为TJ在病理过程中的潜在作用提供了证据。然而,caspase-11影响MST1磷酸化的具体机制需要进一步研究。
综上所述,抑制caspase-11表达在一定程度上有利于拮抗MCAO/R小鼠脑损伤诱导的内皮高通透性。作为一种非经典炎症小体,敲减通过调节Hippo信号通路的启动并维持MCAO/R小鼠脑内皮屏障的完整性。此外,我们的研究结果扩展了目前对TJ调控机制的理解,并为开发有效的预防和治疗药物提供了潜在的新靶点。
[1] Zhao B, Zhu J, Fei Y, et al. JLX001 attenuates blood-brain barrier dysfunction in MCAO/R rats via activating the Wnt/β-catenin signaling pathway[J]. Life Sci, 2020, 260:118221.
[2] Nakagawa S, Aruga J. Sphingosine 1-phosphate signaling is involved in impaired blood-brain barrier function in ischemia-reperfusion injury[J]. Mol Neurobiol, 2020, 57(3):1594-1606.
[3] Wu M, Shi J, He S, et al. cGAS promotes sepsis in radiotherapy of cancer by up-regulating caspase-11 signaling[J]. Biochem Biophys Res Commun, 2021, 551:86-92.
[4] Flood B, Manils J, Nulty C, et al. caspase-11 regulates the tumour suppressor function of STAT1 in a murine model of colitis-associated carcinogenesis[J]. Oncogene, 2019, 38(14):2658-2674.
[5] Wang J, Sahoo M, Lantier L, et al. Caspase-11-dependent pyroptosis of lung epithelial cells protects from melioidosis while caspase-1 mediates macrophage pyroptosis and production of IL-18[J]. PLoS Pathog, 2018, 14(5):e1007105.
[6] Liu C, Fu Q, Mu R, et al. Dexmedetomidine alleviates cerebral ischemia-reperfusion injury by inhibiting endoplasmic reticulum stress dependent apoptosis through the PERK-CHOP-caspase-11 pathway[J]. Brain Res, 2018, 1701:246-254.
[7] Du SH, Qiao DF, Chen CX, et al. Toll-like receptor 4 mediates methamphetamine-induced neuroinflammation through caspase-11 signaling pathway in astrocytes[J]. Front Mol Neurosc, 2017, 10:409.
[8] Qu XY, Zhang YM, Tao LN, et al. XingNaoJing injections protect against cerebral ischemia/reperfusion injury and alleviate blood-brain barrier disruption in rats, through an underlying mechanism of NLRP3 inflammasomes suppression[J]. Chin J Nat Med, 2019, 17(7):498-505.
[9] Wu KW, Lv LL, Lei Y, et al. Endothelial cells promote excitatory synaptogenesis and improve ischemia-induced motor deficits in neonatal mice[J]. Neurobiol Dis, 2019, 121:230-239.
[10] Zhang P, Wang T, Zhang D, et al. Exploration of MST1-mediated secondary brain injury induced by intracerebral hemorrhage in rats via hippo signaling pathway[J]. Transl Stroke Res, 2019, 10(6):729-743.
[11] Gong P, Zou Y, Zhang W, et al. The neuroprotective effects of insulin-like growth factor 1 via the Hippo/YAP signaling pathway are mediated by the PI3K/AKT cascade following cerebral ischemia/reperfusion injury[J]. Brain Res Bull, 2021, 177:373-387.
[12] 袁俊亮, 李卓然, 胡文立. 应加强生物学标志物在脑小血管病发病机制中的研究[J]. 中华医学杂志, 2020, 100(43):3381-3384.
Yuan JL, Li ZR, Hu WL. Research on biological markers in the pathogenesis of cerebral small vessel disease should be strengthened [J]. Chin J Med Sci, 2020, 100(43):3381-3384.
[13] Finethy R, Dockterman J, Kutsch M, et al. Dynamin-related Irgm proteins modulate LPS-induced caspase-11 activation and septic shock[J]. EMBO Rep, 2020, 21(11):e50830.
[14] Yi YS. Caspase-11 non-canonical inflammasome: emerging activator and regulator of infection-mediated inflammatory responses[J]. Int J Mol Sci, 2020, 21(8):2736.
[15] Deng M, Tang Y, Li W, et al. The endotoxin delivery protein HMGB1 mediates caspase-11-dependent lethality in sepsis[J]. Immunity, 2018, 49(4):740-753.e7.
[16] Zhao Y, Ma X, Zhou Y, et al. DDAH-1, via regulation of ADMA levels, protects against ischemia-induced blood-brain barrier leakage[J]. Lab Invest, 2021, 101(7):808-823.
[17] Yong YX, Yang H, Lian J, et al. Up-regulated microRNA-199b-3p represses the apoptosis of cerebral microvascular endothelial cells in ischemic stroke through down-regulation of MAPK/ERK/EGR1 axis[J]. Cell cycle, 2019, 18(16):1868-1881.
[18] Moya IM, Halder G. Hippo-YAP/TAZ signalling in organ regeneration and regenerative medicine[J]. Nat Rev Mol Cell Biol, 2019, 20(4):211-226.
[19] Tian Y, Song H, Jin D, et al. MST1-Hippo pathway regulates inflammation response following myocardial infarction through inhibiting HO-1 signaling pathway[J]. J Recept Signal Transduct Res, 2020, 40(3):231-236.
[20] Chen B, Zhang Q, Yan Y, et al. MST1-knockdown protects against impairment of working memory via regulating neural activity in depression-like mice[J]. Genes Brain Behav, 2022, 21(2):e12782.
[21] Zhou T, Chang L, Luo Y, et al. MST1 inhibition attenuates non-alcoholic fatty liver disease via reversing Parkin-related mitophagy[J]. Redox Biol, 2019, 21:101120.
[22] Li D, Ni H, Rui Q, et al. Deletion of MST1 attenuates neuronal loss and improves neurological impairment in a rat model of traumatic brain injury[J]. Brain Res, 2018, 1688:15-21.
Role and mechanism of caspase-11-mediated Hippo signaling pathway in disruption of blood-brain barrier in mice with cerebral ischemia-reperfusion
ZHANG Chuang, YU Xiaojun△, TANG Bo, JIANG Wei, XIE Jun
(,,410000,)
To explore the role and mechanism of caspase-11 in the disruption of blood-brain barrier (BBB) in mice with cerebral ischemia-reperfusion.Seventy-two mice, including 36(caspase-11-encoding gene) knockdown (KD) mice and 36 wild-type (WT) mice, were divided into 4 groups: WT group, KD group, middle cerebral artery occlusion/reperfusion injury (MCAO/R) group and KD+MCAO/R group,with 18 mice in each group. The MCAO/R model was established in MCAO/R group and KD+MCAO/R group using WT mice and KD mice, respectively, while the mice in the other groups underwent the same surgical operation without disturbing the arteries. Brain microvascular endothelial cell line bEnd.3 was divided into 4 groups: normal control (NC) group, KD group, oxygen glucose deprivation/reperfusion injury (OGD/R) group and KD+OGD/R group. Thein bEnd.3 cells was knocked down in KD group and KD+OGD/R group, and the OGD/R model of the cells was established in OGD/R group and KD+OGD/R group. The degree of brain injury was analyzed using 2,3,5-triphenyltetrazolium chloride staining, hematoxylin-eosin staining and Nissl staining. The BBB breakdown was investigated with leakage of Evans blue dye, expression of tight junction (TJ) proteins, and measurement of transendothelial electrical resistance (TEER).Caspase-11 expression was up-regulated in endothelial cells after MCAO/R (<0.05). Reduced infarct volume and endothelial barrier permeability, and increased expression levels of TJ proteins ZO-1 and occludin after MCAO/R were observed in KD mice (<0.05)., OGD/R significantly increased the protein level of caspase-11 and decreased the protein levels of TJ proteins ZO-1 and occludin in bEnd.3 cells (<0.05).knockdown protected BBB integrity by promoting TJ protein expression and increasing TEER (<0.05).knockdown reversed MCAO/R and OGD/R-induced increases in mammalian sterile 20-like kinase 1 (MST1) phosphorylation of the Hippo signaling pathway in brain endothelial cells (<0.05). Furthermore, treatment with p-MST1 inhibitor XMU-MP-1 attenuated the effect of caspase-11 on BBB breakdown (<0.05).Inhibition of caspase-11 preserves the integrity of the BBB in cerebral ischemia-reperfusion mice at least in part by modulating the Hippo signaling pathway.
caspase-11; ischemic stroke; blood-brain barrier; Hippo signaling pathway; mammalian sterile line 20-like kinase 1
R743.31; R363.2
A
10.3969/j.issn.1000-4718.2023.02.007
1000-4718(2023)02-0250-09
2022-04-18
2022-09-27
[基金项目]湖南省创新型省份建设专项资助项目(No. S2021JJKWLH0160)
Tel: 15700761995; E-mail: sgyhy987@163.com
(责任编辑:李淑媛,余小慧)
