冻融循环次数对超声改性玉米淀粉凝胶特性和结构的影响
2023-02-07许秀颖侯景瑶齐佳伟吴天昊许志凌云吴玉柱刘景圣
韩 蕊,许秀颖,侯景瑶,齐佳伟,吴天昊,许志凌云,吴玉柱,刘景圣
(吉林农业大学食品科学与工程学院,小麦和玉米深加工国家工程研究中心,吉林 长春 130118)
速冻谷物制品因其烹饪方便受到消费者的青睐。淀粉是谷物制品的重要组分,直接决定其品质的优劣。玉米淀粉作为世界第一大粮食作物——玉米的重要组分,因存在加工性能差、贮藏时易发生老化等现象,使其制品失水变硬、弹性降低,严重影响产品性能和质量[1]。在冷冻-解冻的过程中,天然淀粉凝胶内部形成冰晶,受到物理压力,发生相分离,使水分溢出。冻融稳定性是表征速冻制品物理变化的重要指标,而评估冻融稳定性的指标为析水率[2]。为降低冻融循环对产品的伤害,可通过添加外源物质提高冻融稳定性。Zhang Yifu等[3]的研究发现以天然大米淀粉作对照,加入了大米蛋白的大米淀粉凝胶中水流动性显著减弱,横向弛豫时间(T2)明显减少,持水力提高。Chen Long等[4]通过研究普鲁兰多糖的加入,使大米淀粉凝胶的硬度降低,T2值减小,限制了水的流动,改善了淀粉凝胶结构。此外,还可通过对淀粉进行改性,提高其冻融稳定性。张颖[5]在不同压力下,对白果淀粉进行超高压处理,发现压力为200 MPa时淀粉凝胶不易失水,冻融稳定性最好。周伟[6]研究了微波辅助制备羟丙基玉米淀粉,发现随着取代度的增加,凝胶保水能力增强,冻融稳定性提高。
超声处理作为绿色、高效的物理方法,被广泛应用于淀粉、蛋白质等食品重要组分改性研究中。超声波产生的空化效应使淀粉颗粒在介质中受到气泡的作用,分子降解形成自由基[7];其产生的机械效应使淀粉分子受到剪切、分散等作用力,导致淀粉分子共价键的断裂[8]。Chan等[9]研究发现,超声处理马铃薯淀粉、玉米淀粉、绿豆淀粉及西米淀粉,会使淀粉链发生断裂,直链淀粉含量升高。Okonkwo等[10]研究发现,超声处理大米淀粉冻融循环后,随着超声处理次数增加,析水率逐渐降低。而对超声改性玉米淀粉冻融循环过程中其凝胶特性和结构变化的研究却鲜见报道。
本研究采用流变仪、物性分析仪、低场强核磁共振仪、傅里叶变换红外光谱仪及X射线衍射仪等技术,以天然玉米淀粉作对照,研究冻融循环1~5 次超声改性玉米淀粉凝胶特性和结构的变化,这可为速冻谷物食品加工和食用品质提升提供一定理论参考。
1 材料与方法
1.1 材料与试剂
玉米淀粉(分析纯,≥98%) 上海瑞永生物科技有限公司;溴化钾、二甲基亚砜(dimethyl sulfoxide,DMSO)、碘、碘化钾 国药集团化学试剂有限公司;直支链淀粉试剂盒(K-TSTA) 爱尔兰Megazyme公司;化学试剂均为国产分析纯。
1.2 仪器与设备
JY92-2D超声波细胞粉碎机 宁波新芝生物科技股份有限公司;MesoMR23-040V-I低场强核磁共振仪上海纽迈电子科技有限公司;LAMBDA 850紫外分光光度计 珀金埃尔默仪器(上海)有限公司;MCR-302流变仪 奥地利Anton Paar公司;TA-XT Plus物性测定仪英国Stable Micro Systems公司;VERTEX 70傅里叶变换红外光谱仪 德国Bruker公司;D/MAX2500 X射线衍射仪 日本理学株式会社;Alpha1-4 LD plus真空冷冻干燥机 德国Christ有限公司。
1.3 方法
1.3.1 超声改性玉米淀粉的制备
在前期预实验的基础上,选择用去离子水配制质量分数为6%的玉米淀粉乳,将淀粉乳通过磁力搅拌充分混合均匀,在超声功率120 W、超声时间20 min(探针作用4 s,间歇1 s)条件下,获得超声改性玉米淀粉,将超声改性玉米淀粉(记为UCS)和普通玉米淀粉(记为CS)作为冻融循环样品的对照。
1.3.2 不同冻融循环次数玉米淀粉凝胶的制备
按照Ye Jiangping等[11]的方法并稍作修改。将普通玉米淀粉和超声改性玉米淀粉放入95 ℃恒温水浴锅中,糊化25 min,冷却至室温。将约20 mL淀粉糊转移至50 mL圆柱形离心管中,置于-20 ℃冰箱中冷冻22 h,取出后放入30 ℃恒温水浴锅中解冻2 h,为一个冻融循环过程(记为FT)。同样条件下,冻融循环5 次。冻融循环1~5 次的超声改性玉米淀粉凝胶分别记为FT1-UCS、FT2-UCS、FT3-UCS、FT4-UCS及FT5-UCS。冻融循环1~5 次的普通玉米淀粉凝胶分别记为FT1-CS、FT2-CS、FT3-CS、FT4-CS及FT5-CS。
1.3.3 析水率的测定
根据宁吉英等[12]的方法并稍作修改。将1.3.2节的不同冻融循环次数玉米淀粉凝胶分别装入带有滤纸和孔洞的20 mL注射器中,再放置于50 mL离心管中,4000 r/min离心20 min,取出带有凝胶的注射器,称量水和离心管的质量。实验重复3 次,按照下式计算析水率:式中:m1为注射器质量;m2为离心管质量;m3为注射器和离心管的总质量;m4为离心管和水的质量。
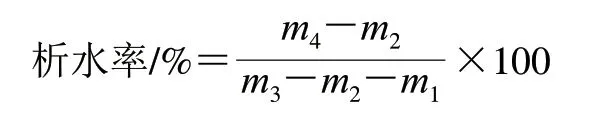
1.3.4 动态流变学的测定
根据Yamazaki等[13]的方法进行修改,使用流变仪测定凝胶的流变学性质。将1.3.2节的不同冻融循环次数玉米淀粉凝胶分别直接放到流变仪实验操作台上。使用直径为25 mm的平板流变仪,设置平板间的间隙1 mm,测量温度25 ℃,扫描应变1%,角频率范围为0.1~100 rad/s,探究样品的储能模量(G’)、损耗模量(G”)及损耗角正切值(tanδ)随角频率的变化。
1.3.5 质构特性的测定
根据Zhang Chen等[14]的方法并稍作修改,使用物性测定仪测定凝胶的质构特性。按1.3.1节和1.3.2节方法将糊化后的淀粉糊混合均匀后倒入铝盒,室温冷却。采用TPA模式,参数设置为:使用P/0.5探头,测试速率5 mm/s,下压10 mm,停留时间2 s,触发力5 g。
1.3.6 直链淀粉含量的测定
利用直/支链淀粉试剂盒,按照说明书测定不同冻融循环次数玉米淀粉凝胶的直链淀粉含量。
1.3.7 碘结合力的测定
根据Miao Ming等[15]的方法并稍作修改,使用紫外分光光度计测定淀粉凝胶与碘结合能力。将不同冻融循环次数凝胶进行真空冷冻干燥,得到冻干样品。准确称量100 mg冻干样品溶于10 mL的体积分数90% DMSO溶液中,然后用去离子水稀释至50 mL。取5 mL样品,加入用0.2% I2和2% KI溶液配制成的碘溶液1 mL,定容至50 mL,涡旋充分混匀,室温静置15 min。在450~800 nm波长范围内进行全波段扫描,在635 nm波长处测定样品的吸光度(A635nm),记为碘蓝值,在520 nm波长处测定其吸光度(A520nm),计算A635nm/A520nm值,记为碘结合力值。
1.3.8 水分分布的测定
根据Yu Wenjie等[16]的方法并稍作修改,使用低场强核磁共振仪测定凝胶的水分分布。用移液枪将糊化淀粉糊注入核磁管中,放入-20 ℃冰箱冷冻22 h,30 ℃恒温水浴2 h。将不同冻融循环次数的样品利用多脉冲回波序列测量样品的T2。设置参数:采样点数为1000054,重复扫描4 次,回波数为10000,回波时间为0.5 ms,弛豫衰减时间为7500 ms。
1.3.9 短程有序结构的测定
根据Ye Jiangping等[17]的方法并稍作修改,使用傅里叶变换红外光谱仪测定凝胶的短程有序结构。将不同冻融循环处理后的玉米淀粉凝胶样品冻干粉碎,称量2 mg样品,与0.2 g溴化钾充分研磨压片,溴化钾薄片为对照,扫描范围为4000~500 cm-1,分辨率为4 cm-1,扫描次数为64 次。采用OMNIC 8.0软件对1200~800 cm-1谱图进行反卷积处理。
1.3.10 结晶结构的测定
根据Zhang Chen等[18]的方法并稍作修改,使用X射线衍射仪测定凝胶的结晶结构。将不同冻融循环次数冷冻干燥后的样品,在40 kV和40 mA条件下,利用CuKα射线进行扫描,范围为5°~40°,扫描速率为2°/min,扫描步幅为0.02°。
1.4 数据处理
每个实验重复3 次。使用Origin 2018软件绘图。使用SPSS 25软件进行方差分析和差异显著性分析,P<0.05,差异显著。
2 结果与分析
2.1 不同冻融循环次数玉米淀粉凝胶的析水率分析
如图1所示,未冻融时,UCS的析水率比CS显著提高了5.17%(P<0.05),原因在于超声处理使玉米淀粉分子受到机械断键作用,分子聚合度降低,提高了直链淀粉含量,造成析水率升高,与Okonkwo等[10]的研究结果一致。同一冻融循环次数下,超声改性玉米淀粉凝胶的析水率均低于天然淀粉凝胶,而且FT4-UCS的析水率比FT4-CS显著降低了5.19%(P<0.05),差异最显著。原因可能是在冷冻过程中形成冰晶,对凝胶结构产生物理破坏,羟基被暴露出来。而超声的空穴效应使淀粉分子链变短,产生自由基,氢键减少,淀粉分子间相互作用力减弱,直链淀粉间距离增大,并且反复冻融形成的海绵状结构也可以吸收更多的水,使留在凝胶内部的水分增多,造成析水率降低。这与吴立夏等[19]和王冠青[20]的研究结果一致。因此,超声可以改善玉米淀粉凝胶的冻融稳定性,并在冻融循环第4次时效果最显著。

图1 冻融循环过程中超声改性玉米淀粉凝胶的析水率变化Fig.1 Changes in water separation of ultrasonically modified corn starch gels during freeze-thaw cycles
2.2 不同冻融循环次数玉米淀粉凝胶的动态流变学分析
由图2可知,超声改性玉米淀粉凝胶和天然玉米淀粉凝胶的G’值均高于G”值,凝胶网络结构稳定,tanδ均小于1,表现为淀粉凝胶是典型的弱凝胶,类似固体的特征。CS的G’值大于UCS的G’值,表明其流变学行为更弱,与梁云浩等[21]研究结果一致。由于超声的空化作用使淀粉结构松散,有序性降低,降低凝胶的黏弹性,与Kaur等[22]的解释一致。随着冻融次数的增加,玉米淀粉凝胶的G’值和G”值整体呈逐渐增加趋势,tanδ呈现相反趋势。同一冻融循环次数下,超声改性玉米淀粉凝胶的G’值和G”值低于天然玉米淀粉凝胶。由图2C可知,FT4-UCS和FT5-UCS的tanδ值高于FT4-CS和FT5-CS的tanδ值,表明反复冻融处理使水与淀粉分子相互作用,冷冻-解冻过程中抑制直链淀粉和水分的渗出,使凝胶留住更多的水分,并且能保持稳定的流变学行为,这与宁吉英等[12]和董贝贝[23]的研究结果一致,也与本实验析水率结果一致。

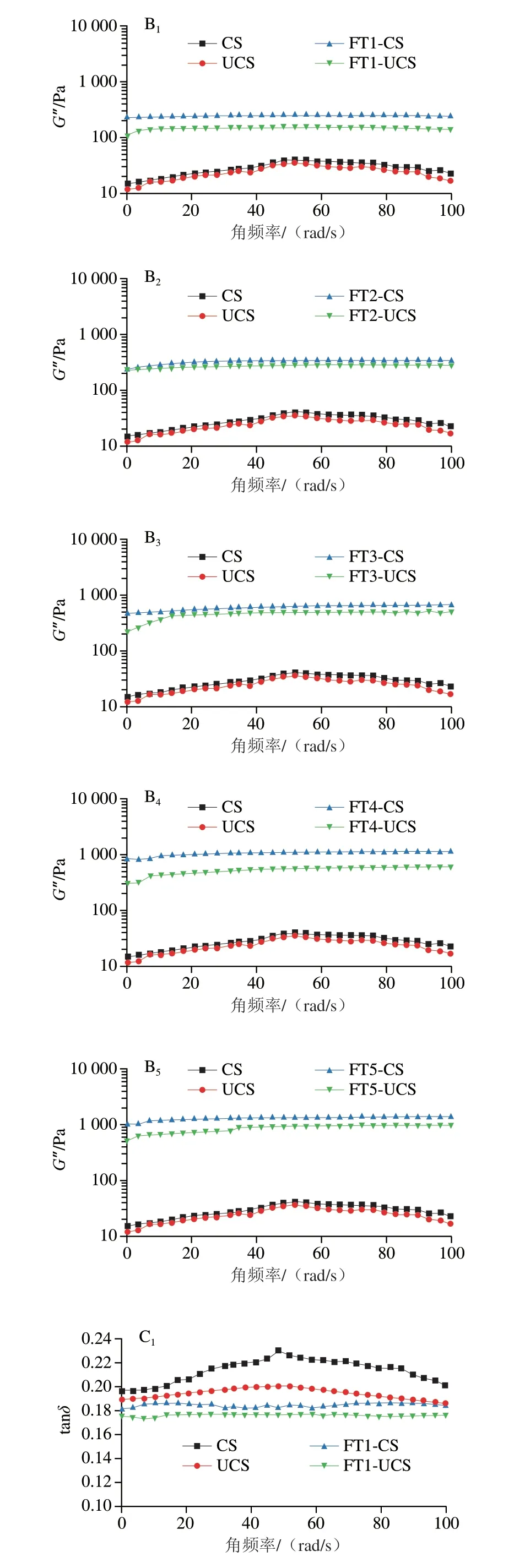
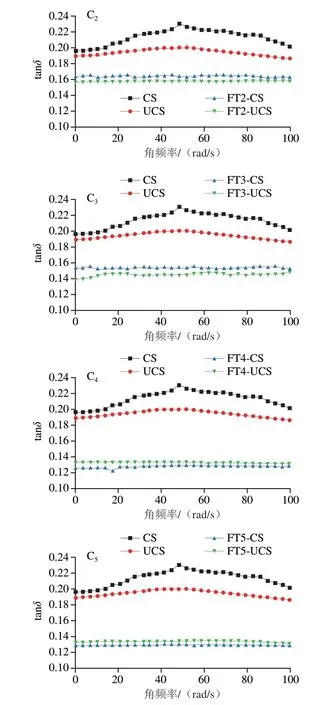
图2 冻融循环过程中超声改性玉米淀粉凝胶流变学变化Fig.2 Rheological changes in ultrasonically modified corn starch gels during freeze-thaw cycles
2.3 不同冻融循环次数玉米淀粉凝胶的质构特性分析
由表1可知,未冻融时,UCS的硬度、弹性和胶黏性均低于CS,原因可能是超声的机械作用使相互缠绕的淀粉链结构打开,降解分子链,双螺旋结构形成被抑制,导致凝胶强度降低,与Mojarrad等[24]的解释一致。冻融后淀粉凝胶的硬度、弹性及胶黏性均大于未冻融,原因可能是冻融使凝胶结构更稳定,呈现“类固体”,与汪兰等[25]的研究结果一致。同一冻融循环次数下,超声改性玉米淀粉凝胶的硬度、弹性、内聚性及胶黏性均低于天然玉米淀粉凝胶,而FT4-UCS的硬度值比FT4-CS显著降低了10.83%(P<0.05),变化最显著。原因可能是冷冻-解冻过程中,淀粉链之间或淀粉与水分子之间通过氢键相互结合[14,26],直链淀粉含量与硬度密切相关,造成超声改性玉米淀粉凝胶的硬度值低于天然玉米淀粉凝胶,与本研究流变学结果一致。

表1 冻融循环过程中超声改性玉米淀粉凝胶质构参数Table 1 Textural parameters of ultrasonically modified corn starch gels during freeze-thaw cycles
2.4 不同冻融循环次数玉米淀粉凝胶的碘结合力分析
碘蓝值是一种表征淀粉与碘结合能力强弱的重要指标,反映了直链淀粉的相对浓度水平[20]。由表2可知,未冻融时,UCS中的碘蓝值、碘结合力和直链淀粉含量都高于CS,其原因主要为超声破坏了淀粉的结构,引起淀粉的快速降解,直链淀粉含量升高,提升了淀粉分子与碘结合能力,与Chen Bingyan等[27]的研究结果一致。同一冻融循环次数下,淀粉凝胶的碘蓝值、碘结合力值及直链淀粉含量均不低于未冻融,原因可能是玉米淀粉在糊化过程中双螺旋结构被打开,冻融处理导致直链淀粉分子溢出,发生了定向迁移并重新排列。冷冻-解冻的过程中,FT3-UCS和FT4-UCS的直链淀粉含量均比FT3-CS和FT4-CS降低了0.15%,原因可能是凝胶水分析出,短直链淀粉分子重新结合形成了双螺旋结构,使游离的淀粉分子减少与碘离子结合,造成了超声改性玉米淀粉凝胶的碘蓝值和直链淀粉含量低于天然玉米淀粉凝胶,并且碘结合能力也下降。
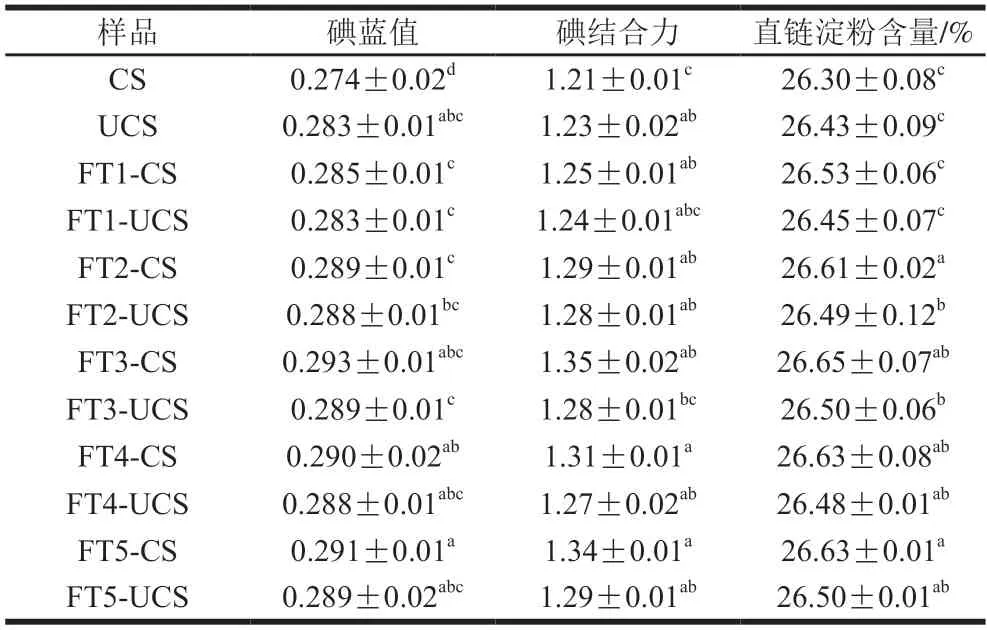
表2 冻融循环过程中超声改性玉米淀粉凝胶碘蓝值、碘结合力及直链淀粉含量参数Table 2 Iodine blue value,iodine binding capacity and amylose content of ultrasonically modified corn starch gels during freeze-thaw cycles
2.5 不同冻融循环次数玉米淀粉凝胶的水分分布分析
T2的特征峰代表不同的水分子,其峰面积代表水分子含量。强结合水的T2范围为0.1~10 ms,弱结合水的T2范围为10~100 ms,自由水的T2大于100 ms[3]。由图3A可知,相比于天然玉米淀粉凝胶,超声改性玉米淀粉凝胶的T2曲线整体左移,自由水含量下降。原因可能是强结合水和弱结合水的流动性降低,冻融使分子间交联结合紧密,水分迁移被抑制,与高焌茹[28]的解释一致。由图3B可知,冻融循环过程中,淀粉凝胶的结合水比例呈整体降低趋势,自由水比例呈整体升高趋势,表明冻融处理使淀粉分子排列成有序结构,减少结合水位点,与Gong Yvyuan等[29]的解释一致。同一冻融循环次数下,超声改性玉米淀粉凝胶的自由水比例低于天然玉米淀粉凝胶,且FT4-UCS的自由水比例比FT4-CS显著降低了2.57%(P<0.05)。原因可能是超声产生的短直链淀粉更易重排,与水分子结合后,降低水分子的流动性,造成析水率降低,这与梁云浩等[21]的解释一致。
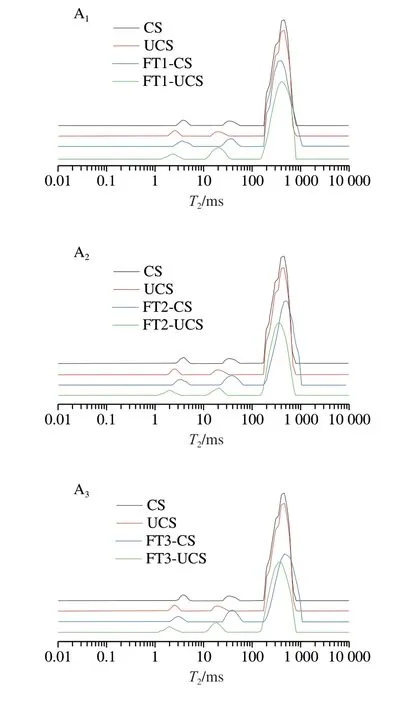
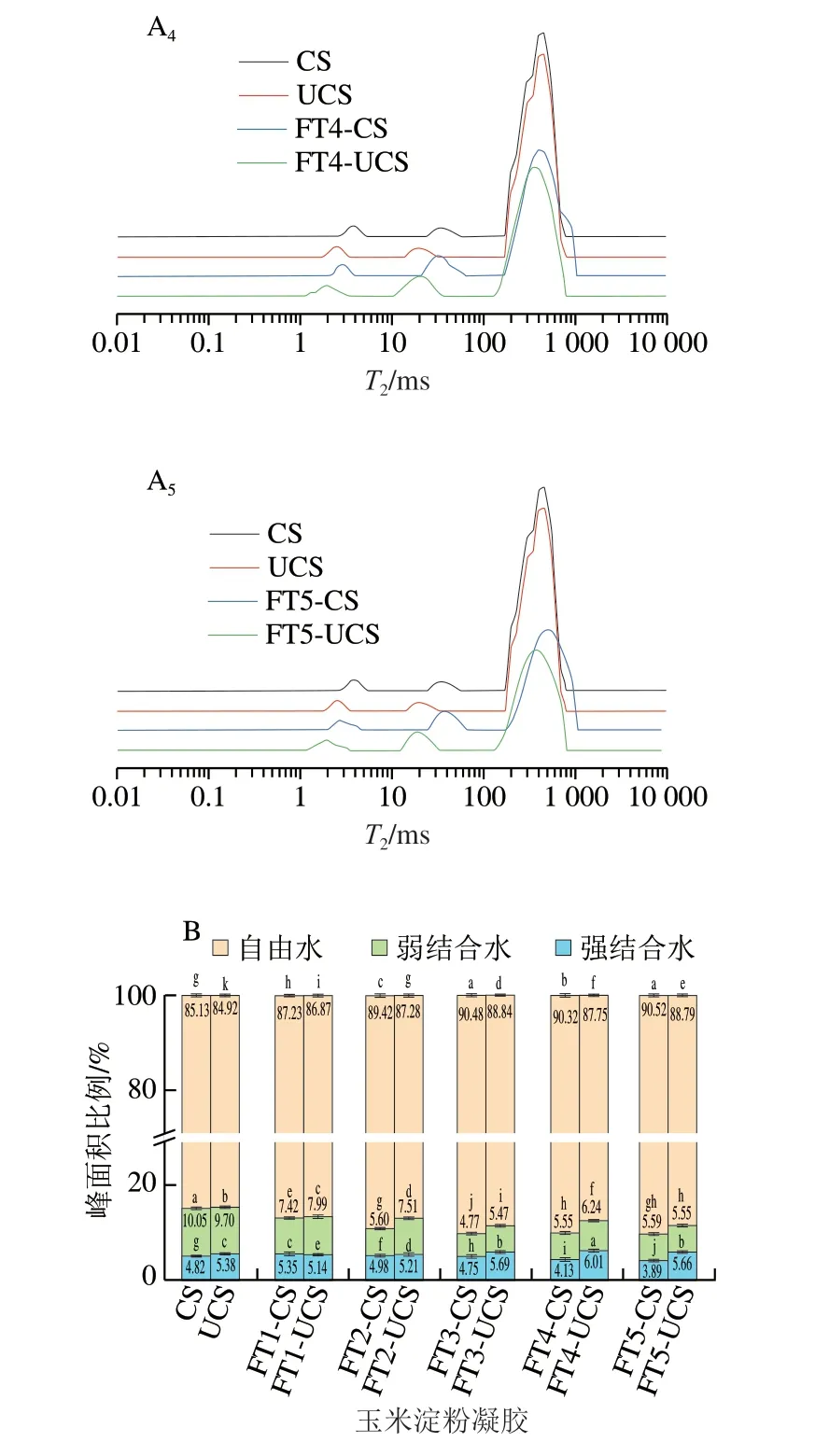
图3 冻融循环过程中超声改性玉米淀粉凝胶水分分布变化Fig.3 Changes in moisture distribution of ultrasonically modified corn starch gels during freeze-thaw cycles
2.6 不同冻融循环次数玉米淀粉凝胶的短程有序结构分析
由图4A可知,在4000~500 cm-1范围内,所有样品的红外图谱吸收峰位置及形状大致相同,无新的吸收峰出现或特征峰消失,没有产生新的基团。在3500~3200 cm-1范围内观察到一个宽的—OH伸缩振动吸收峰,可与氢键相连[20]。由图4B可知,在1200~800 cm-1范围内,1054 cm-1和1022 cm-1处反卷积比值(R1054/1022)代表短程有序性,而1022 cm-1和991 cm-1处反卷积比值(R1022/991)代表双螺旋结构组织状态[30]。由表3可知,UCS的R1054/1022和R1022/991低于CS,表明超声处理使淀粉结晶区的有序性降低,双螺旋结构变弱。冻融循环后淀粉凝胶的R1054/1022高于CS和UCS,R1022/991低于CS和UCS,说明冻融使淀粉的短程结构有序性增强。同一冻融循环次数下,超声改性玉米淀粉凝胶的R1054/1022低于天然玉米淀粉凝胶,原因可能是超声处理使淀粉分子之间的交联程度降低,抑制有序结构的形成;超声改性玉米淀粉凝胶的R1022/991高于天然玉米淀粉凝胶(除FT3-UCS外),表明淀粉分子之间或者淀粉分子与水分子之间形成的氢键减少,冻融促使淀粉链重新排列,双螺旋结构的形成被抑制[31]。此外,FT4-UCS的R1054/1022比FT4-CS显著减小0.056(P<0.05),FT4-UCS的R1022/991比FT4-CS显著增大0.191(P<0.05);相比于其他冻融次数,第4次冻融时数值变化最显著。

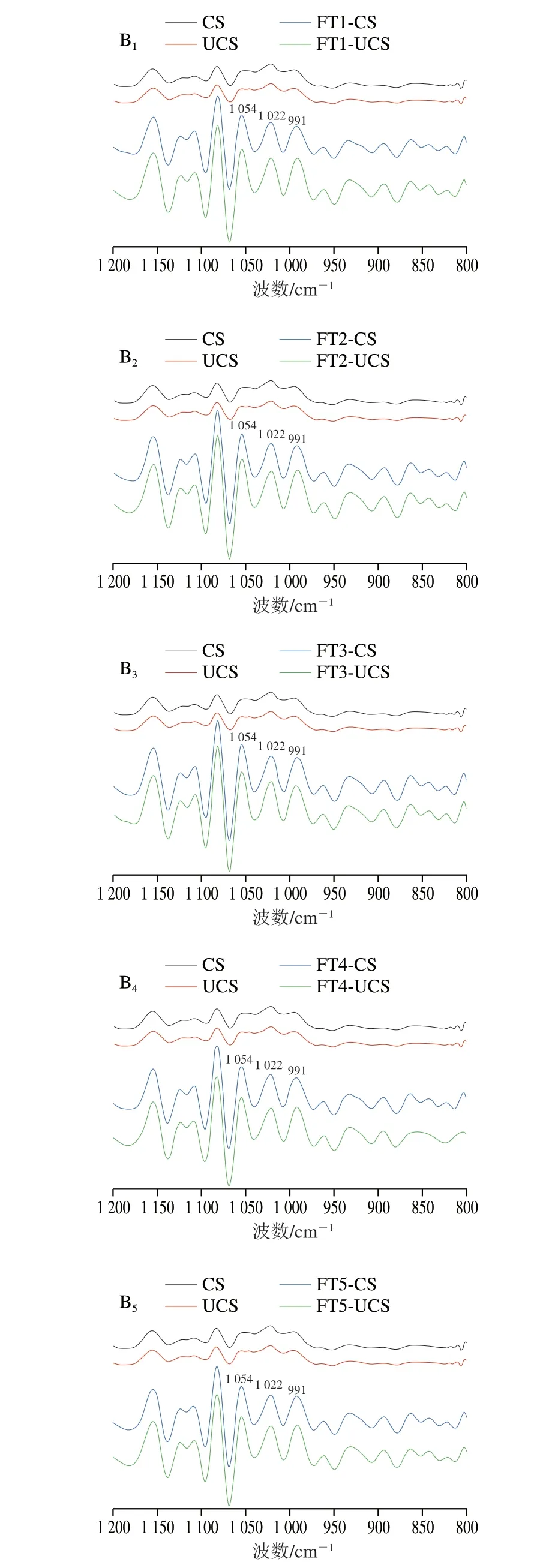
图4 冻融循环过程中超声改性玉米淀粉凝胶短程有序结构变化Fig.4 Short-range ordered structure changes of ultrasonic modified corn starch gel during freeze-thaw cycles

表3 冻融循环过程中超声改性玉米淀粉凝胶短程有序结构参数Table 3 Short-range ordered structural parameters of ultrasonically modified corn starch gels during freeze-thaw cycles
2.7 不同冻融循环次数玉米淀粉凝胶的结晶结构分析
如图5所示,出现衍射峰的位置大致相同,超声和冻融循环处理没有改变玉米淀粉的晶型。未冻融时,CS和UCS的相对结晶度分别为10.33%和10.21%,原因可能为超声的机械和空化作用造成其结晶区结构被破坏,晶体间距发生变化,导致相对结晶度改变[8]。冻融循环后超声改性玉米淀粉凝胶的相对结晶度均高于未冻融,原因可能是冷冻过程中,凝胶内部淀粉形成富集区,双螺旋结构更加紧密,造成相对结晶度增加。同一冻融循环次数下,超声改性玉米淀粉凝胶的相对结晶度均低于天然玉米淀粉凝胶。第4次冻融时,FT4-UCS的相对结晶度为15.38%,超声处理后的玉米淀粉凝胶中相对结晶度最大,与本研究红外光谱的结果一致。原因可能是超声使淀粉无定形区结构增加,抑制了超声改性淀粉凝胶在反复冷冻-解冻过程中的水分析出,增大了水与淀粉之间的结合,降低了水分的迁移,阻碍了淀粉分子间交联,抑制其重结晶,这与周大年[32]的研究结果一致。
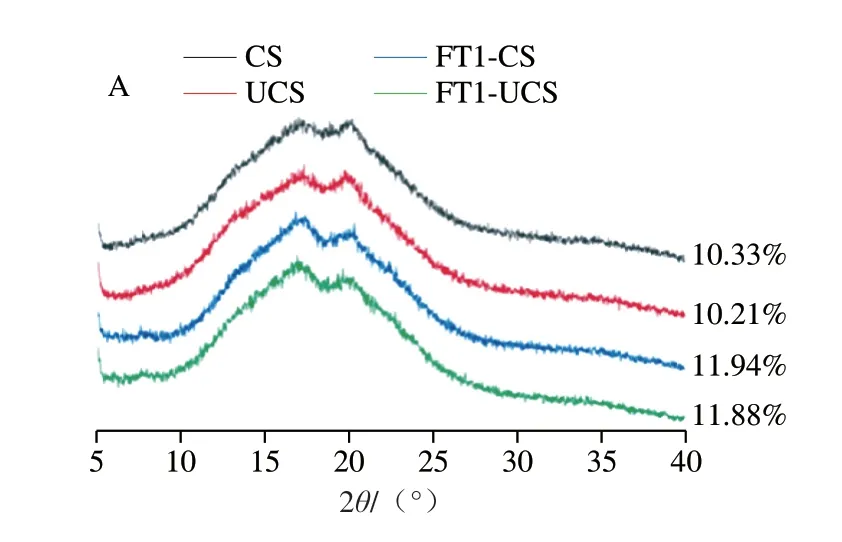
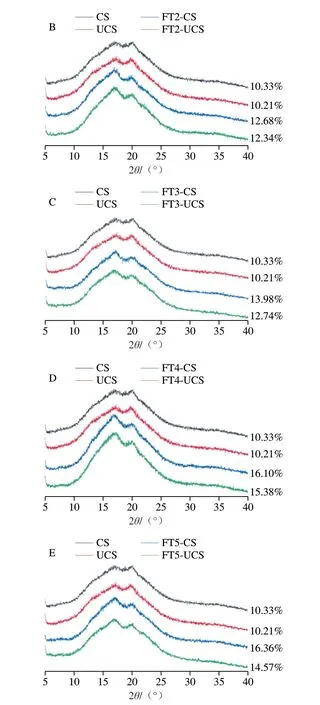
图5 冻融循环过程中超声改性玉米淀粉凝胶结晶结构变化Fig.5 Changes in the crystalline structure of ultrasonically modified corn starch gels during freeze-thaw cycles
3 结论
探讨了冻融循环次数对超声改性玉米淀粉凝胶特性和结构的影响。结果表明,不同冻融循环次数下,以天然玉米淀粉凝胶作对照,超声改性玉米淀粉凝胶的析水率下降,G’和G”降低,凝胶强度变弱,硬度降低;且FT4-UCS的析水率比FT4-CS析水率显著降低了5.19%(P<0.05),硬度显著降低了10.83%(P<0.05)。此外,与天然玉米淀粉凝胶相比,冻融循环后超声改性玉米淀粉凝胶中直链淀粉含量下降,淀粉与碘结合能力减弱,T2曲线整体左移,且反卷积红外光谱中R1054/1022降低,R1022/991升高(除FT3-UCS外),短程有序结构减弱,相对结晶度下降。表明超声改性降低了淀粉分子间的交联,抑制了水分迁移。综上,超声处理通过改变玉米淀粉凝胶的分子结构,明显改善其冻融稳定性,为速冻谷物食品的实际生产提供了可靠的基础数据和理论参考。
