循环盐雾环境中电镀锌和锌铝涂覆涂层的腐蚀行为
2022-12-19陈亚军孙利成王汉森
陈亚军,孙利成,王汉森
(1.中国民航大学中欧航空工程师学院,天津300300;2.中国民航大学航空工程学院,天津300300)
飞机腐蚀给社会带来了巨大的经济损失和资源浪费。当飞机长期服役于腐蚀性盐雾大气环境中时,结构表面会形成一层微液膜[1],使不同紧固件连接结构之间形成电导通,从而引发电偶腐蚀,造成安全隐患[1-2]。飞机中紧固件的使用数量高达几十万件,其重要性不言而喻[3],航空紧固件的耐蚀性直接影响着飞机结构的安全性水平[4]。镀锌涂层作为航空紧固件表面的一种常用防护涂层,可在腐蚀环境中对飞机紧固件起到阳极保护作用[5],大幅延长零件的使用寿命。锌铝涂层是一种将超细锌鳞片和铝鳞片叠合包裹在特殊黏结剂中的无机涂层[6],其中的铝可快速形成一层Al2O3保护膜,显著提高涂层的耐蚀性。
盐雾试验是目前国内外检验涂镀层耐蚀性的重要手段之一[7],具有试验周期短、可操作性强和过程稳定等特点[8],可以在室内条件下快速评价飞机结构用材的耐蚀性。盐雾试验一般分为4大类:中性盐雾试验(NSS)、醋酸盐雾试验(ASS)、铜加速醋酸盐雾试验(CASS)和循环盐雾试验(CCT)[7]。
刘凯等[9]研究了镀锌板与常见冷轧板(SPCC)在中性盐雾试验与循环腐蚀试验中的腐蚀差异,发现中性盐雾下两种材料的腐蚀速率更大,镀锌板耐防腐蚀性能优于SPCC,但是没有进行腐蚀机理和电化学行为分析。冯利军等[10]对比研究了镀锌板在中性盐雾环境、中性盐雾加周浸环境和中性盐雾加湿热环境中的腐蚀行为,结果表明镀锌板在中性盐雾环境中的腐蚀最为严重,在中性盐雾加湿热环境中的腐蚀情况最轻微。HU等[11]分别用辊涂和喷淋两种工艺加工热浸镀锌板,通过中性盐雾试验比较了他们的耐蚀性,发现辊涂工艺的防腐蚀效果优于喷淋工艺。
锌铝涂层由于同时具有锌的电化学保护作用和铝的耐蚀性,在耐蚀性方面的研究也最为集中、成果较为突出[12-14]。侯蓉等[15]通过中性盐雾试验,研究了锌铝镀层热轧板的耐蚀性,发现镀锌铝工艺可以显著提高热轧板的耐蚀性,并且在JMA方程的基础上建立了镀锌铝热轧板腐蚀动力学模型。苏枫[16]研究了Zn-15Al和Zn-50Al合金涂层在中性盐雾中的耐蚀性,发现Zn-15Al的耐蚀机制主要是锌的腐蚀产物自封闭,而Zn-50Al的耐蚀机制主要是铝氧化物的屏蔽。张永法[17]将自制纯Zn、纯Al以及3种不同铝含量的Zn-Al涂层进行中性盐雾试验和浸泡试验,通过对比分析5种涂层的腐蚀形貌、腐蚀产物及腐蚀电化学行为随腐蚀时间的变化规律,研究了其腐蚀行为。LI等[18]研究了铝含量对热浸镀锌铝合金涂层耐蚀性的影响,结果表明随着涂层中铝含量的增加,涂层耐蚀性增强。
综上所述,目前关于镀锌涂层和锌铝涂层研究的不足之处包括:温湿度交替腐蚀环境因素作用下的涂层失效行为深入分析,腐蚀电流和腐蚀电位等电化学参数评价腐蚀过程的可靠性及相关腐蚀机理的研究。与中性盐雾腐蚀相比,循环盐雾腐蚀更加接近真实的大气腐蚀环境。本工作以电镀锌涂层(加工工艺为电镀锌工艺)和锌铝涂覆涂层(加工工艺为涂覆工艺)为研究对象,通过电化学测试、微观形貌观察和腐蚀产物分析等考察了他们在循环盐雾试验环境中的腐蚀行为。
1 试验
1.1 试验材料
基体材料选用常见的冷轧板(SPCC),化学成分如表1所示。

表1 SPCC冷轧板的化学成分
将SPCC冷轧板加工成150 mm×70 mm×1 mm的试样,并将2种涂层分别制备在SPCC冷轧板上,工艺参数如表2所示。按照ISO 17872—2007《色漆和清漆在腐蚀测试用金属板涂层上划线标记的入门指南》在试样表面划刻“X”字划痕,以观察各腐蚀阶段的腐蚀宽度变化情况。

表2 电镀锌涂层和锌铝涂覆涂层的工艺参数
1.2 试验方法
循环盐雾腐蚀试验参照GMW 14872—2013《Cyclic Corrosion Laboratory Test》标准进行,分别配制0.9%(质量分数,下同)NaCl溶液、0.1% CaCl2溶液和0.075% NaHCO3复合盐溶液。使用CCX 2000型高级循环腐蚀测试箱,盐雾试验以每24 h为一个循环,一共进行42个循环。
采用美国阿特克公司生产的PARSTAT2273电化学工作站对经过不同时间盐雾腐蚀的涂层试样进行电化学测试。测试过程中,首先进行开路电位测试直至开路电位稳定;随后进行电化学阻抗谱测试,施加20 mV正弦波信号,频率为0.01 Hz~100 kHz;最后进行极化曲线测试,扫描速率0.5 mV/s,扫描范围为开路电位±0.5 V。
将腐蚀后的试样切割成15 mm×15 mm块状,进行微观形貌观察。采用Hitachi S-3400N型扫描电子显微镜(SEM)进行微观形貌观测,并用其配备的能谱仪(EDS)分析腐蚀产物的元素组成。采用SmartLab型X射线衍射仪(XRD)进行物相分析,选用Cu靶作为靶材,扫描速率为4°/min,2θ扫描区间为10°至90°。
2 结果与讨论
2.1 腐蚀形貌
2.1.1 宏观形貌
由图1可见:锌铝涂覆涂层试样的腐蚀程度明显低于电镀锌涂层试样。经过7 d循环盐雾腐蚀后,电镀锌涂层试样表面沿着划痕方向开始出现白锈,在非划痕区域也出现了分布不均匀的白锈;腐蚀14 d时,白锈面积明显增多,并在试样边缘出现了红锈;腐蚀21 d时红锈面积明显增大,并且集中在没有划痕的部位;腐蚀28 d后,试样的绝大部分区域被红锈覆盖;腐蚀42 d后,电镀锌涂层完全失效,红锈覆盖整个试样表面。而锌铝涂覆涂层经过循环盐雾腐蚀后,其腐蚀产物集中出现在划痕区域,非划痕区域腐蚀程度较低。随着腐蚀时间的延长,腐蚀产物沿着划痕缓慢向外不断扩展。

(a) 电镀锌涂层
2.1.2 微观形貌
由图2可见:腐蚀7 d后,电镀锌试样表面呈现树枝状结晶的形貌,也出现了少量黑斑;腐蚀14 d后,晶粒棱角模糊,晶界变宽,树枝状结晶变密集;腐蚀21 d时,针状物明显变多,并有颗粒状物存在;腐蚀28 d后,试样表面出现了大量颗粒物,直径约2 μm;腐蚀35 d后,颗粒物明显增大,并且颗粒越来越大,腐蚀42 d后,腐蚀产物呈现球状,球径约20 μm。结合宏观形貌,此阶段的试样表面被红锈覆盖,电镀锌涂层完全失效,疏松多孔的大颗粒更容易让腐蚀介质进入。

(a) 7 d
由图3可见:锌铝涂覆涂层试样经过7 d腐蚀后,表面腐蚀产物为致密细小的针状结构,可以起到延缓腐蚀的作用;腐蚀14 d后,表面出现了大量枝状结构;延长腐蚀时间至24~42 d,枝状腐蚀产物逐渐伸长,成为连续均匀的细长枝状结构。

(a) 7 d
2.2 腐蚀产物成分
2.2.1 能谱分析结果
由图4可见:电镀锌涂层腐蚀14 d后,腐蚀产物中的主要元素为Zn、O、Cl,还有少量Fe,此时的腐蚀产物主要为锌的氧化物和氯化物,腐蚀反应主要在涂层上进行;随着腐蚀时间从28 d延长到42 d,锈层中的Zn含量降低至0.70%,Fe含量增加到61.22%。断定此时锌镀层破损,基体暴露,产生了基体元素的腐蚀产物,根据锈层颜色判断,此时锈层的腐蚀产物主要为铁的氧化物。
由图4还可见:锌铝涂覆涂层腐蚀14 d和28 d后,腐蚀产物中含有Zn、O、Cl等,此外还有少量的Al和Fe等,此阶段的腐蚀产物为锌的氧化物和氯化物等,腐蚀反应主要在涂层上进行,只有少量的Al参与反应;腐蚀42 d后,锈层中的Fe含量明显增加,Zn、C含量减少,说明此时部分基体元素参与反应,铁的氧化物逐渐增多。
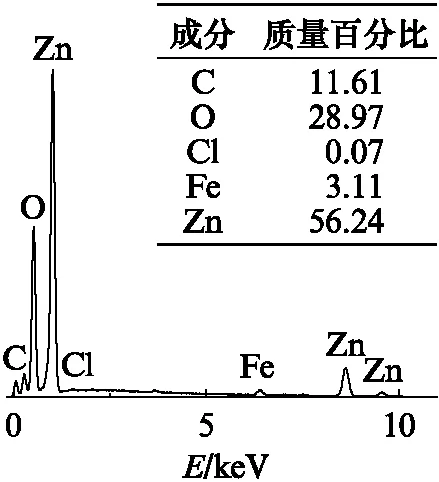
(a) 电镀锌涂层腐蚀14 d
2.2.2 X衍射光谱
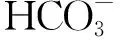

Zn5(CO3)2(OH)6+4H2O
(1)
(2)
5ZnO+2CO2+3H2O=Zn5(CO3)2(OH)6
(3)
5ZnO+2Cl-+6H2O=
Zn5(OH)8C12·H2O+2OH-
(4)
腐蚀28~42 d后,腐蚀产物主要为Fe3O4和FeOOH。说明此时电镀锌涂层已经完全失去了保护作用,腐蚀介质与基体直接反应,表面被Fe3O4和FeOOH覆盖。
由图5还可见:锌铝涂覆涂层试样腐蚀14 d后,表面腐蚀产物主要由ZnO、Zn5(CO3)2(OH)6以及Zn5(OH)8Cl2·H2O及Al2O3组成。呈现最强峰的是涂层中没有被腐蚀的Zn涂层。Al很快形成了Al2O3薄膜,主要是涂层中的Zn参与了反应,生成了ZnO、Zn5(CO3)2(OH)6和Zn5(OH)8Cl2·H2O,分别见式(1)、(3)和(4)。腐蚀28 d后,Al2O3薄膜被局部破坏,锌铝涂层表面的A13+和H2O反应形成氢氧化铝,均匀附着在涂层表面,随着时间的延长,逐渐形成一层锌铝化合物层[19-20]。如果环境中的碱度太高,Zn5(OH)8C12·H2O就会分解,导致式(4)所示反应逆向进行,Cl-会被释放,离子越多,导电性就会越强,促使了新腐蚀的进行[21]。因而产物中的Zn5(OH)8Cl2·H2O减少。腐蚀42 d后,部分腐蚀介质与基体钢发生了反应,Fe3O4逐渐增多。

(a) 电镀锌涂层
2.3 电化学行为
2.3.1 极化曲线
通过极化曲线分析可以获得镀层在腐蚀液中的腐蚀动力学信息[22]。一般而言,涂层的腐蚀电位(Ecorr)越高,腐蚀电流密度(Jcorr)越小,涂层的腐蚀速率越小,该涂层的耐蚀性越好[23-24]。
由图6和表3可见:电镀锌涂层试样的腐蚀电位随着腐蚀时间的延长先下降后上升。腐蚀前21 d,试样的腐蚀电位很低,这是因为锌作为活泼金属,本身的电位很低。在湿热循环交替的环境中,腐蚀介质与镀锌涂层发生强烈的电化学反应,耐蚀性减弱,因此试样的腐蚀电位负移,在此期间腐蚀电流密度有所增加。结合宏观形貌可见,此阶段腐蚀面积快速增加,故此阶段为快速腐蚀阶段。腐蚀至28 d,试样的腐蚀电位大幅正移至-0.64 V,延长腐蚀时间至35 d后,腐蚀电位基本稳定,而腐蚀电流密度明显增大。结合此前的分析结果,腐蚀21 d后的电化学反应主要是在腐蚀介质和钢基体之间进行的,电镀锌涂层完全失效。
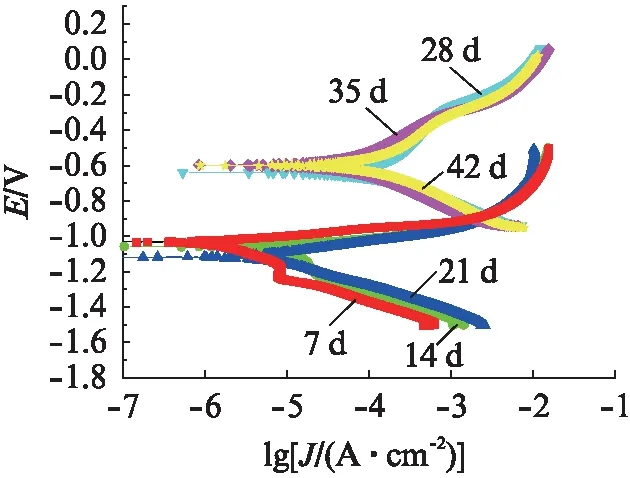
图6 电镀锌涂层试样经过不同时间盐雾腐蚀后的极化曲线

表3 电镀锌涂层试样的极化曲线拟合结果
由图7和表4可见:随着腐蚀时间的延长,锌铝涂覆涂层试样的腐蚀电位增加,腐蚀电流密度则先减小后增大再减小;腐蚀7~14 d,腐蚀电位由-0.95 V增加到-0.85 V,同时电流密度减小,腐蚀反应速度减缓,这可能是铝形成的氧化铝物薄膜,和其他腐蚀产物共同阻挡了进一步腐蚀,耐蚀性增强;腐蚀14~28 d,腐蚀电位变化不大,但是腐蚀电流密度由5.52×10-9A·cm-2增加到5.19×10-7A·cm-2,腐蚀速率明显提高,这可能是氧化铝物薄膜被局部破坏;腐蚀28~42 d,孔隙内的腐蚀产物越来越多,逐渐堆积在孔隙内表面,腐蚀产物屏蔽作用减缓了腐蚀进程,使得试样的腐蚀电位正移,同时此阶段腐蚀电流密度不断减小,腐蚀速率减慢。结合宏观形貌,此阶段锌铝涂层并没有完全失效。对比电镀锌涂层在循环盐雾试验中的表现,发现锌铝涂覆涂层在相同腐蚀时间段的腐蚀电流密度更小,最大腐蚀电流密度为5.19×10-7A·cm-2,远小于电镀锌涂层的最大腐蚀电流密度,腐蚀更慢。
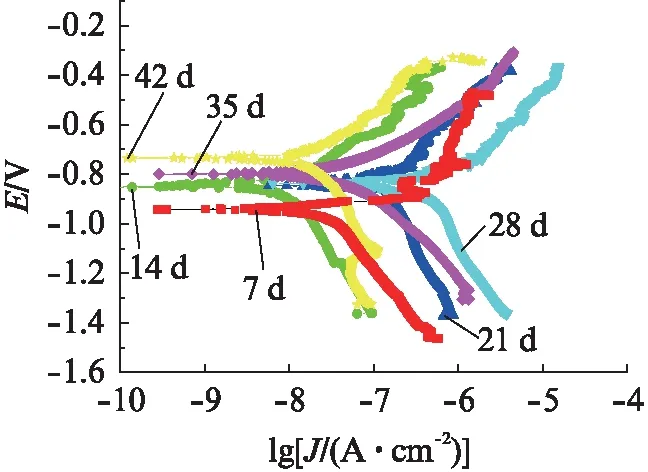
图7 锌铝涂覆涂层试样经过不同时间盐雾腐蚀后的极化曲线

表4 锌铝涂覆涂层试样的极化曲线拟合结果
2.3.2 电化学阻抗谱
电化学抗谱可以详细反映涂层的溶液/涂层界面和涂层/金属基体界面的腐蚀情况,是评价涂层耐蚀性能和研究涂层/基体体系的腐蚀行为最有效的方法之一[25]。由图8可见:容抗弧半径随着腐蚀时间的延长而减小,且低频区阻抗模值也随着腐蚀时间的延长而减小,这表明其耐蚀性随着腐蚀时间的延长而减弱。
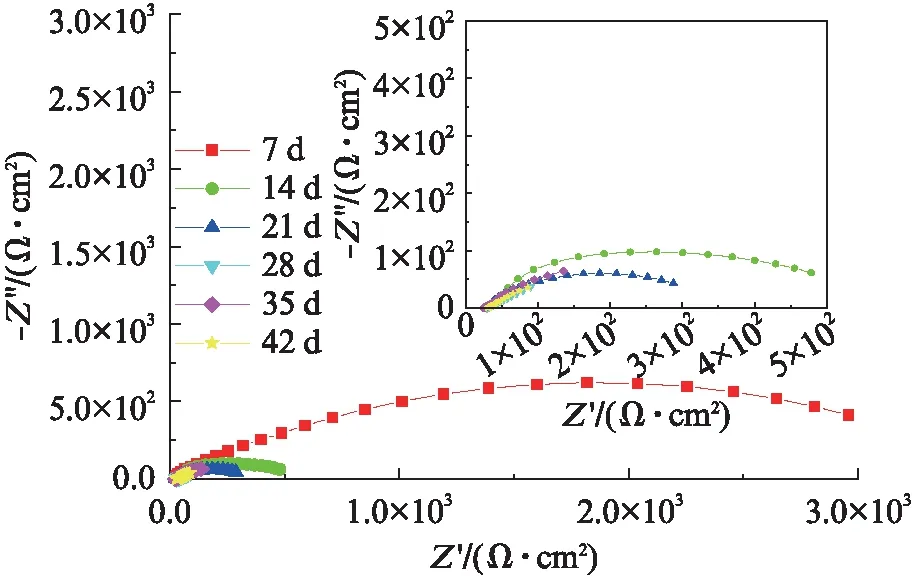
(a) Nyquist图
采用如图9所示的R(Q(R(QR)))电路对电镀锌涂层EIS数据进行拟合,拟合误差(Error)都在10%以内,拟合电路选择合适,拟合得到5个参数。其中,Rs为电解质溶液电阻,Cdl为低频对应的时间常数来自于双层界面电容。Rct为双层界面电荷转移电阻,可以衡量材料与溶液界面发生电化学反应时电荷转移的难度,一般电荷转移电阻越大,电化学反应受到的的阻碍作用越大[26]。Rc为涂层电阻,对于一个涂层体系来说,涂层电阻反映涂层阻挡电解质溶液穿透涂层的能力,是评价涂层耐蚀性能的重要参数[27]。一般来说,涂层电阻Rc越大,其抗渗透性能越好,即防护性能越好[28]。实际腐蚀过程中,由于镀锌钢表面弥散效应的存在,可用常相位角元件Q来表示电极表面的非理想电容[29]。Q通常由参数Y0和n表示,Y0代表CPE的导纳,n代表CPE的弥散指数,n取值为0~1,越接近1说明材料表面光洁度越好,CPE越接近于一个理想电容。电镀锌涂层阻抗谱等效电路拟合参数如表5所示。

图9 电镀锌涂层试样的电化学阻抗谱等效电路
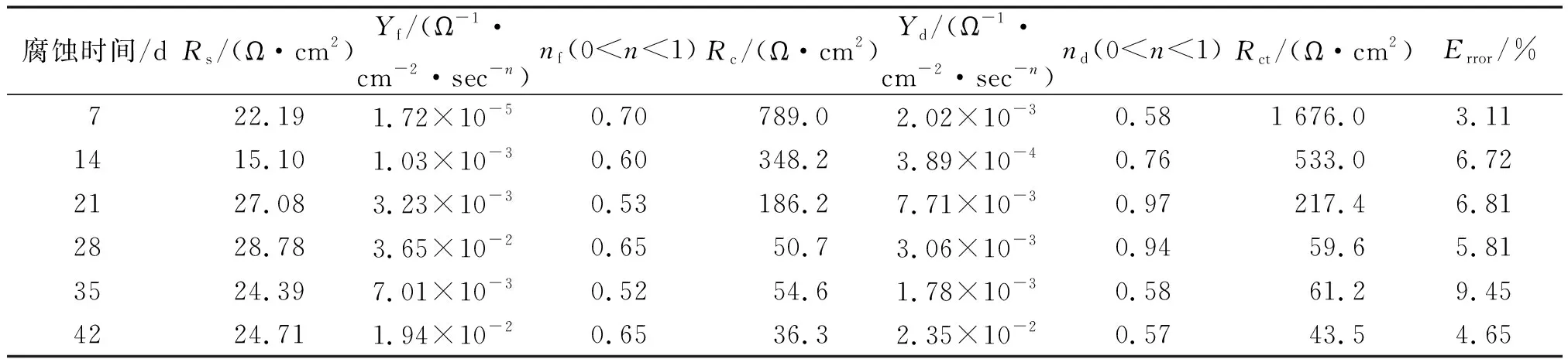
表5 电镀锌涂层试样的电化学阻抗谱拟合结果
由表5可见,电镀锌涂层试样的电荷转移电阻和涂层电阻都是随着腐蚀时间的延长先减小后小幅度波动。随着腐蚀时间从7 d延长到21 d,电镀锌涂层的电荷转移电阻由1 676.0 Ω·cm2大幅度减小到217.4 Ω·cm2,涂层电阻也由789.0 Ω·cm2减小到186.2 Ω·cm2,耐蚀性减弱,结合前述分析,处于快速腐蚀阶段。腐蚀28 d,电荷转移电阻和涂层电阻分别降低到59.6 Ω·cm2和50.7 Ω·cm2后,波动幅度较小,腐蚀42 d,电荷转移电阻和涂层电阻分别为43.5 Ω·cm2和36.3 Ω·cm2。结合之前的微观形貌观察结果,随着基体腐蚀产物不断增多,腐蚀产物结构趋于疏松,腐蚀介质更容易进入,耐蚀性减弱,此阶段镀锌涂层完全失效。
由图10可见:锌铝涂覆涂层试样的Nyquist曲线显示两个容抗弧,且随着腐蚀时间的延长,低频区的阻抗模值先增大后减小,然后继续增大,表明其耐蚀性先增大后减小然后再增大。

(a) Nyquist图
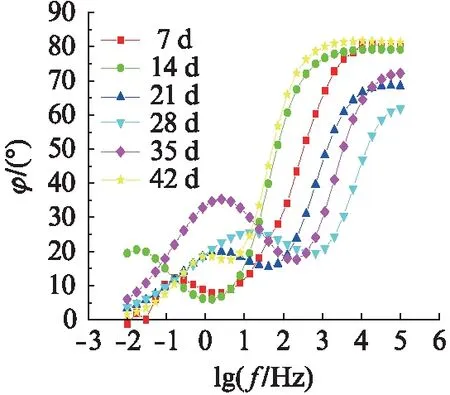
(c) 相位角曲线
采用如图11所示的R(QR)(QR)电路对锌铝涂覆涂层试样的EIS数据进行拟合,拟合误差也都在10%以内,拟合得到5个参数。其中,Rs为溶液电阻,Rc为涂层电阻,Rct为电荷转移电阻,Qf和Qd都是非理想电容。锌铝涂覆涂层阻抗谱等效电路拟合参数如表6所示。
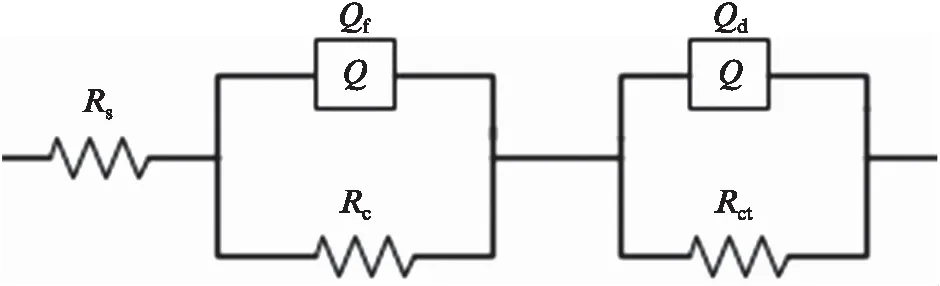
图11 锌铝涂覆涂层试样的电化学阻抗谱等效电路
由表6可见:锌铝涂覆涂层试样的电荷转移电阻和涂层电阻随着腐蚀时间的延长先增大后减小再增大。随着腐蚀时间从7 d延长至14 d,其电荷转移电阻由4.55×105Ω·cm2增加到2.23×106Ω·cm2,涂层电阻也由4.53×105Ω·cm2增加到2.54×106Ω·cm2,这说明在腐蚀初期,试样表面形成了具有保护作用的Al2O3薄膜,具有较强的耐蚀性。继续延长腐蚀时间至28 d,电荷转移电阻减小到1.19×105Ω·cm2,涂层电阻也减小到9.00×103Ω·cm2,结合之前的物相分析结果,Zn5(OH)8C12·H2O分解,释放出Cl-,提高了体系的电导率,从而增大电化学腐蚀的速率[30]。继续延长腐蚀时间,电荷转移电阻和涂层电阻不断增加,腐蚀42 d后的电荷转移电阻和涂层电阻分别为3.92×106Ω·cm2和2.65×106Ω·cm2。
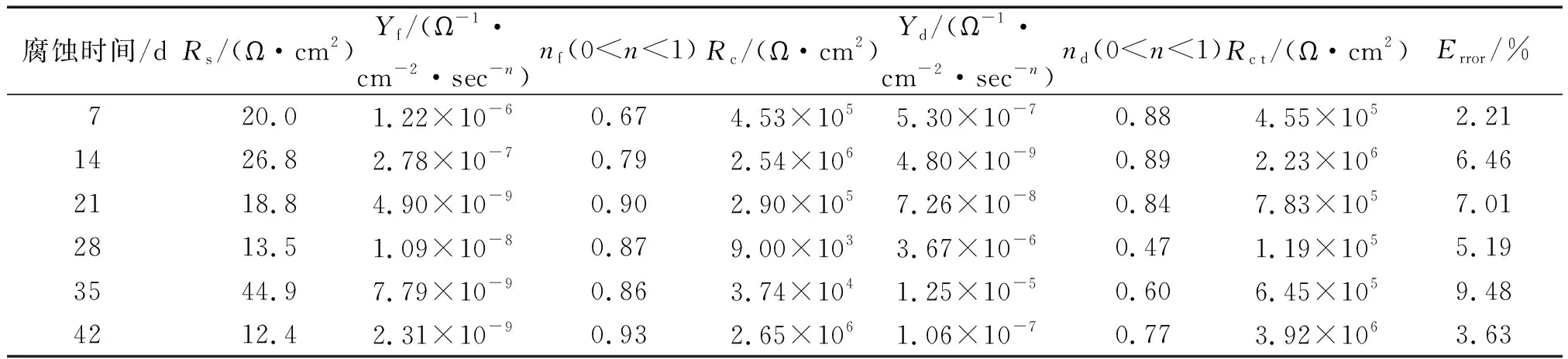
表6 锌铝涂覆涂层试样的电化学阻抗谱拟合结果
对比电镀锌涂层试样的循环盐雾腐蚀试验结果,锌铝涂覆涂层试样经过相同腐蚀时间后的电荷转移电阻和涂层电阻也都更大,腐蚀42 d后,电镀锌涂层的电荷转移电阻只有43.5 Ω·cm2,而锌铝涂覆涂层的电荷转移电阻达到了3.92×106Ω·cm2。这也证明锌铝涂覆涂层比电镀锌涂层更耐腐蚀。这是由于锌铝涂覆涂层中的铝能迅速形成致密的Al2O3薄膜,延缓了腐蚀。
3 结论
(1)锌铝涂覆涂层的耐腐蚀性强于电镀锌涂层。电镀锌涂层经过28 d循环盐雾腐蚀就完全失效,而锌铝涂覆涂层经过42 d循环盐雾腐蚀后还未完全失效。
(2)电镀锌涂层的腐蚀产物主要为ZnO、Zn5(CO3)2(OH)6、Zn4CO3(OH)6、Zn5(OH)8Cl2·H2O、Fe3O4和FeOOH。而锌铝涂覆涂层的腐蚀产物主要为ZnO、Zn5(CO3)2(OH)6、Zn5(OH)8Cl2·H2O、Fe3O4和Al2O3。
