CoNi双金属改性石墨相氮化碳的制备及光催化性能的研究
2022-12-14孙有为马会霞苑兴洲胡绍争
孙有为 ,王 曦 ,周 峰 ,马会霞 ,苑兴洲 ,胡绍争,* ,张 健,*
(1. 辽宁石油化工大学, 辽宁 抚顺113001;2. 中国石油化工股份有限公司大连石油化工研究院, 辽宁 大连 116000)
可持续能源的开发是目前最有前景且能有效解决化石燃料储备和环境污染问题的方法,太阳能具有取之不尽、用之不竭和可再生等优点,近年来,利用太阳能的光催化技术被认为是一种简单、有效且廉价的环境治理手段,特别是在对水中有机污染物降解的方面[1]。当半导体受到合适的光照时,电子会由价带跃迁到导带形成光生电子与空穴,电子会与氧气反应生成超氧自由基,空穴可以直接与污染物进行反应也可以与水发生反应生成羟基自由基,进而进行降解污染物的反应。
近年来,石墨氮化碳(g-C3N4)由于其具有良好的化学稳定性、合适的带隙宽度(≈2.7 eV)以及独特的电子结构等优点在光催化领域引起了广泛的关注[2]。但是在光催化过程中,光生电子和空穴聚集在g-C3N4表面,这不仅增加了电子-空穴复合的概率,而且影响了材料的长期稳定性[3]。为了减少电子-空穴的复合,通常采用金属,特别是贵金属如铂、金、银,作为助催化剂负载在半导体表面[4-6]。助催化剂不仅有效地减少电子与空穴复合的概率,同时也能为反应提供更多的活性位点。但由于贵金属成本较高,会影响工业化的应用。因此,开发高效、低成本的非贵金属助催化剂来进一步提升光催化性能的研究是有价值的。同时与单金属相比,双金属助催化剂能更有效地提升光催化反应的效率,一方面是因为半导体中的光生电子更容易迁移到双金属合金中[7];另一方面,双金属可以通过调控其自身组成来影响反应物以及反应中间体进而改变反应的途径以及产物[8]。因此,双金属助催化剂能够在优化电荷迁移路径的同时,增加反应的活性位点并增进反应物与催化剂之间的相互作用,更好地提升光催化反应的活性。Lin等[9]将CuNi合金负载在TiO2纳米棒(NRs)上。与Cu/TiO2NRs、Ni/TiO2NRs和Pt/TiO2NRs相比,CuNi/TiO2NRs表现出更高的催化活性。通过第一性原理计算出CuNi合金不仅能够增加氢原子的吸附能和功函数,而且减少了H2分子吸附能,有利于H2的生成。Wei等[10]将CoNi合金改性后的RGO用于太阳能电池(DSSCs)对电极,与RGO对电极相比,CoNi-RGO对电极能增加太阳能电池的能量转换效率。Yang等[11]报道了一种性能良好的双功能电催化剂,利用CoNi合金来改性氮掺杂的多孔碳(CoNi/NG),由于CoNi合金的协同作用以及丰富的活性位点,以CoNi/NG为氧电极的锌空气电池表现出良好的充放电性能、较高的最大功率密度和良好的循环稳定性。郑小刚等[12]制备了双金属位的Ag-Ni/g-C3N4光催化剂,利用银的表面等离子体谐振效应与镍的共格界面效应增强了催化剂对可见光的吸收,增强了对亚甲基蓝的降解效果。
在本研究中,通过简单的化学还原反应将CoNi双金属纳米合金负载在g-C3N4纳米片上,为了节约金属材料,将金属负载量固定为催化剂总质量的0.5 %。详细考察了CoNi/ g-C3N4复合催化剂的形貌、理化性能,并对不同CoNi物质的量比下的催化剂进行了降解RhB的实验以考察双金属间的协同作用。结果表明,与g-C3N4、Co/g-C3N4、Ni/g-C3N4相比,CoNi/g-C3N4复合材料表现出了更为优异而稳定的光催化性能。
1 实验部分
1.1 试剂与仪器
试剂: 尿素(CN2H4O)、六水合硝酸镍(Ni(NO3)2·6H2O)、六水合硝酸钴(Co(NO3)2·6H2O)、硼氢化钠(NaBH4)、异丙醇(IPA)、对苯醌(BQ)和碘化钾(KI)。所有化学试剂均为分析级,无需进一步纯化即可直接使用。
仪器: 磁力搅拌器(DF-101S,巩义市予华仪器有限公司);循环水式真空泵(SHZ-D,巩义市予华仪器有限公司);超声波清洗器(KQ220B,昆山市超声仪器有限公司);分析天平(M214Ai,伯拉莫贝林(上海)精密仪器有限公司);离心机(HDL-4,金坛市鸿科仪器厂);真空干燥箱(DZ-2BCIV,天津市泰斯特仪器有限公司);马弗炉(YFX7/12Q-GC,上海意丰电炉有限公司);可见分光光度计(721,上海佑克仪器有限公司)。
1.2 材料的制备方法
1.2.1 g-C3N4纳米片的制备方法
首先将尿素放于坩埚中,盖上盖子,在550 ℃下,焙烧2 h,升温速率为5 ℃/min。所得产物冷却至室温后再在敞口的坩埚中以5 ℃/min升温至500 ℃,煅烧2 h,冷却至室温后研磨得到g-C3N4纳米片。
1.2.2 CoNi/g-C3N4的制备方法
取一定量的g-C3N4纳米片并分散在去离子水中,超声处理30 min; 再向其中分别加入5 mmol/L所需比例的Ni(NO3)2·6H2O和Co(NO3)2·6H2O溶液,搅拌30 min,然后加入新配置的NaBH4溶液(NaBH4与CoNi物质的量比为10∶1),室温下持续搅拌2 h。将产物离心,用去离子水和乙醇洗涤后,在真空干燥箱中于60 ℃干燥过夜,得到CoNi/g-C3N4催化剂。采用相同的方法,分别在只添加Ni(NO3)2·6H2O或Co(NO3)2·6H2O溶液的条件下制得Ni/g-C3N4以及Co/g-C3N4催化剂。
1.3 材料的表征
X射线衍射(XRD)分析采用日本岛津公司的XRD-7000型X射线衍射仪,CuKα辐射源,5°-80°扫描;紫外可见漫反射光谱(UV-vis DRS)由日本JASCA公司的UV-550型紫外-可见光谱仪测试。透射电子显微镜(TEM)使用JEOL JEM2010型仪器对催化剂进行测试;X射线光电子能谱(XPS)采用赛默飞世尔科技有限公司Thermo ESCALAB 250型光电子能谱仪对催化剂进行测试; 光致发光(PL)使用日本HORIBA公司的FluoroMax-4光致发光光谱仪,激发波长为360 nm;使用CHI 660E电化学工作站测试催化剂的电化学阻抗。
1.4 光催化性能评价
1.4.1 光降解RhB实验过程
在30 ℃,80 mL/min的氧气加入量下,使用250 W钠灯为模拟光源(80 lm/W),将100 mL RhB溶液(10 mg/L)置于具有冷凝回流的反应器中,并向其中加入20 mg制备好的催化剂,反应过程持续搅拌,先进行30 min暗反应,之后进行3 h光反应,每30 min取5 mL样品,进行吸光度测试。
1.4.2 RhB标准曲线
在552 nm波长处测试不同浓度的RhB溶液的吸光度,并绘制出标准曲线(图1):y= 0.20142x+0.01468,R2= 0.99933。
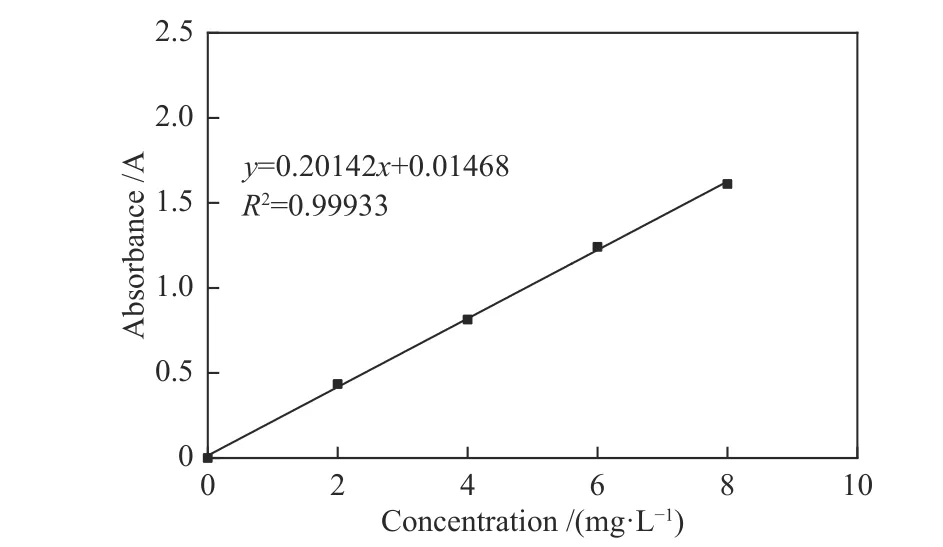
图 1 RhB标准曲线Figure 1 Standard curve of RhB
RhB降解率公式:
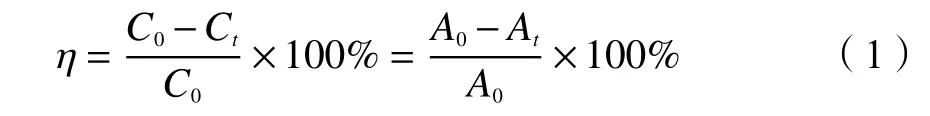
式中,η:RhB的降解率,C0:反应前RhB的质量浓度A0:反应前RhB的吸光度,Ct:反应t时RhB的质量浓度,At:反应t时RhB的吸光度。
2 结果与讨论
2.1 材料的表征
2.1.1 X射线衍射分析
通过XRD研究了g-C3N4、Co/g-C3N4、Ni/g-C3N4以及CoNi/g-C3N4的晶体结构与组成,具体见图2。
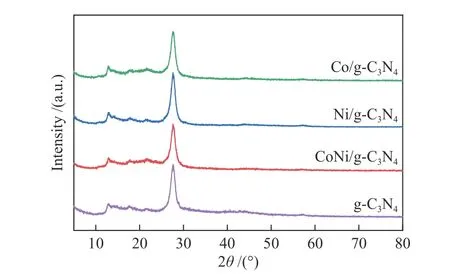
图 2 不同催化剂的XRD谱图Figure 2 XRD patterns of different catalysts
在图2中g-C3N4出现两个不同强度的衍射峰,其中,在27.5°处出现一个强峰,是由于共轭芳族体系的特征性层间堆积的(002)晶面引起的;同时,在12.9°处的弱峰是由3-s-三嗪单元的层间结构堆积的(100)晶面引起的[13]。同样在Ni/g-C3N4、Co/g-C3N4以及CoNi/g-C3N4样品的XRD谱图中也观察到两个峰的存在,表明CoNi合金的负载并没有引起g-C3N4晶体结构的变化。但由于金属助催化剂的负载量较低且较为分散,因此,并没有显示出其他物质的特征峰。
2.1.2 透射电镜分析
图3(a)-(d)分别是普通g-C3N4、g-C3N4纳米片和CoNi/g-C3N4的透射电子显微镜TEM照片。从图3(a)可以看出,普通g-C3N4具有较厚的二维层状结构,且表面非常光滑。而g-C3N4纳米片(图3(b))则表现出较薄的二维片层,并且可以观察到表面存在着许多孔状结构,这是由于g-C3N4二次煅烧所造成的,较薄的二维纳米片能够通过减少电荷扩散距离来促进电荷分离[14]。多孔的g-C3N4能够增强对光的吸收,并能促进光生电子和空穴转移到催化剂的表面,形成更多的活性位点[15],这是提高光催化性能的有效方法之一。图3(c)-(d)为CoNi/g-C3N4催化剂的透射电镜照片,CoNi/g-C3N4催化剂呈现出典型的二维层状结构,说明CoNi合金的负载并没有改变g-C3N4的结构特征。对图3(c)指定区域放大,经过HRTEM的进一步分析,可以清楚地看到有序的晶格条纹(图3(d)),晶格间距为0.21 nm,对应着CoNi合金的(111)晶面[16],这证明了CoNi合金已经成功负载在g-C3N4上,两种材料之间紧密的界面接触也为光生载流子提供了最佳的迁移路径。同时,合成的CoNi合金也表现出较小的颗粒尺寸,这种小尺寸的双金属合金拥有更多的低配位表面原子,能够增强催化剂与反应物之间的相互作用[8],进一步提升光催化性能。

图 3 (a)普通g-C3N4,(b)二次煅烧后的g-C3N4, ((c), (d))CoNi/g-C3N4的TEM照片Figure 3 TEM images of (a) Plain g-C3N4, (b) g-C3N4 after secondary calcination, ((c), (d)) TEM images of CoNi/g-C3N4
2.1.3 X射线能谱分析
采用XPS表征来进一步确定了催化剂的化学组成,如图4所示。在C 1s谱图中(图4(a))可以拟合出两个特征峰,其中,在284.6 eV左右为石墨碳(C-C)的特征峰,以及在288.0 eV左右为s-三嗪环中的sp2键碳(N-C=N)[17]。图4(b)为催化剂的N 1s谱图,分别在398.5、399.6和400.7 eV处拟合出三个峰,可以归因于sp2杂化的氮(C-N=C)、sp3杂化的N-(C)3键和氨基功能N-H基团[18,19]。图4(c)-(d)分别为Co 2p和Ni 2p的XPS谱图,其中,位于780.8和796.3 eV的两个强峰分别对应Co02p3/2和Co02p1/2,证明了金属Co的存在[20],而在785.4和802.4 eV处出现的两个弱峰,可能是由于在保存或测试时部分金属发生表面氧化而形成了一些Co的氧化物,类似的现象也在其他的文献中出现[21,22]。同样金属Ni也出现了相似的情况,其中,位于855.1 eV的峰对应着Ni02p3/2,Ni02p1/2则出现在872.7 eV处,而位于860.9和878.6 eV的峰则是表面氧化所造成的[23]。
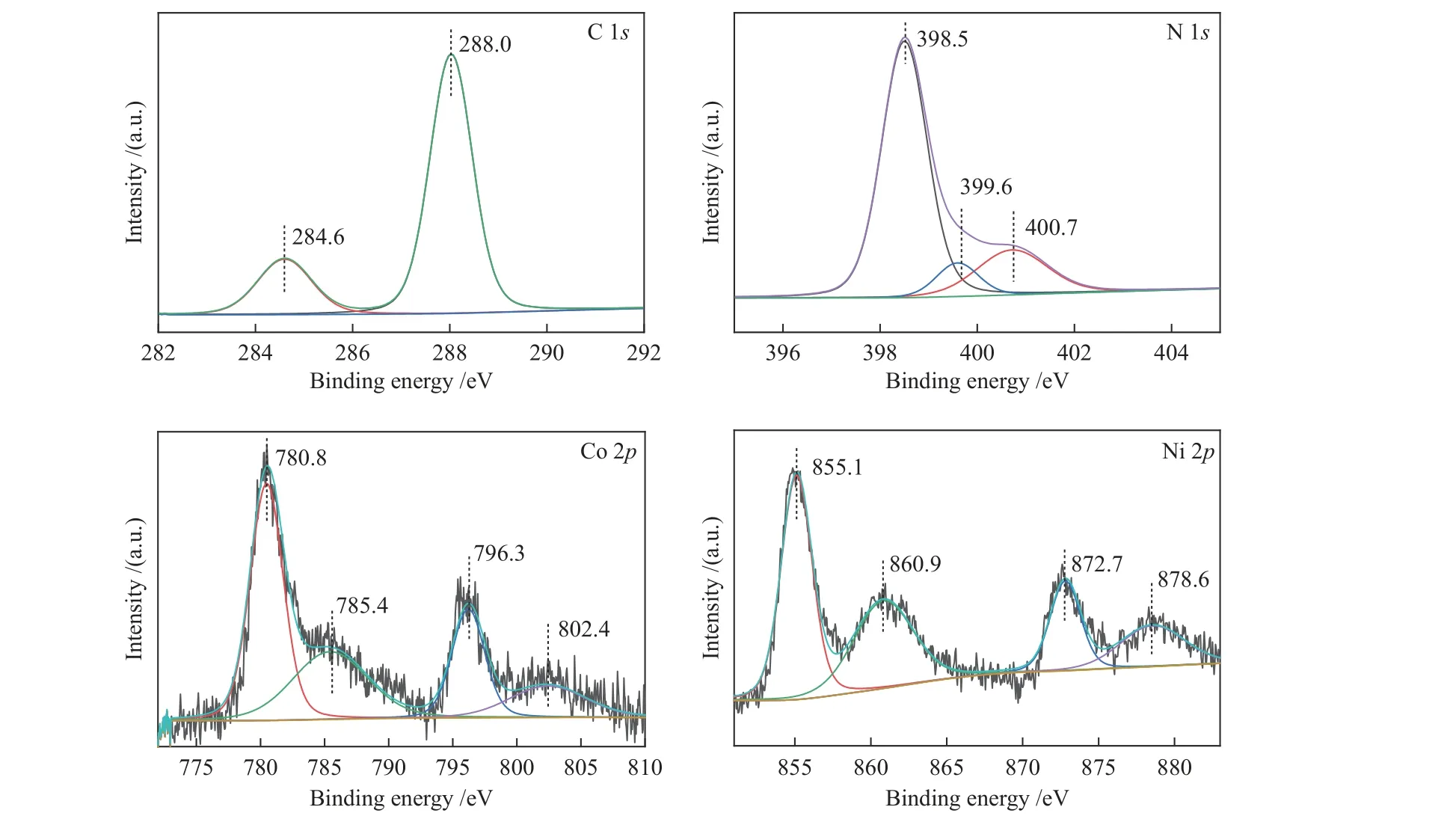
图 4 CoNi/g-C3N4的XPS谱图Figure 4 XPS spectra of CoNi/g-C3N4
2.1.4 紫外可见光漫反射分析
如图5所示,CoNi/g-C3N4的吸光曲线与普通g-C3N4相似,都能够在紫外和可见光下对光有较强的吸收。普通g-C3N4的吸收边在460 nm左右,负载CoNi合金之后,其吸收边的位置没有出现明显的偏移,说明CoNi合金是负载在g-C3N4表面,而并非掺杂进g-C3N4的内部结构[24]。同时,当波长> 460 nm,由于金属与g-C3N4之间的相互作用,催化剂的吸光度得到了进一步的提升,这说明金属助催化剂可以帮助g-C3N4捕获更多的光子,有效地提升对可见光的利用率。CoNi/g-C3N4表现出最强的吸光能力,证明与单金属助催化剂相比,双金属能进一步提升催化剂对光的吸收。此外,Ni/g-C3N4催化剂在600 nm左右出现了一个较弱吸光区域,这与Chen等[25]和Zhu等[26]所报道的一致,可能是由于金属镍纳米颗粒的d-d电子跃迁所造成的。最后利用公式Eg= 1240/λ计算g-C3N4的禁带宽度[27],发现其禁带宽度约为2.70 eV。
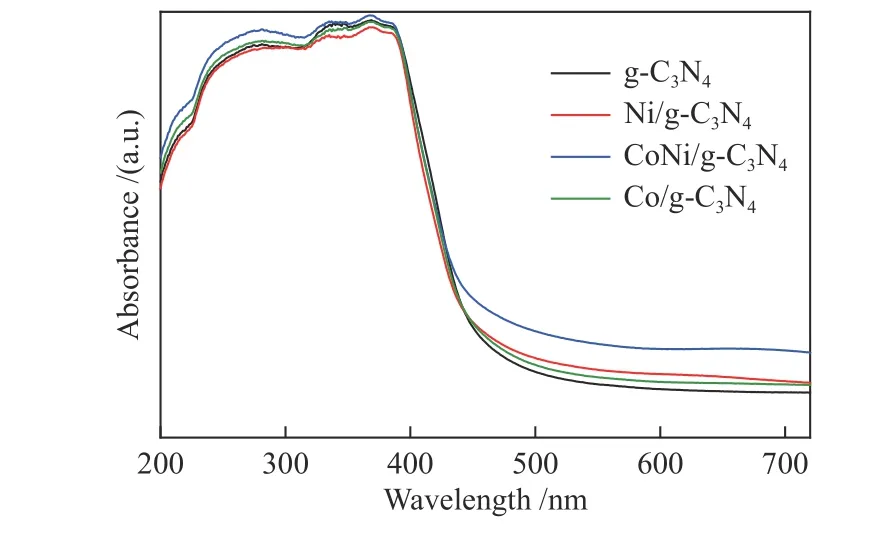
图 5 不同催化剂的UV-vis DRS谱图Figure 5 UV-vis DRS spectra of different catalysts
2.1.5 光致发光分析
通过在室温下进行光致发光分析(PL)测试了催化剂的光生电荷载流子的复合率[28],以探究合金在复合材料中对电子-空穴分离的作用。在光照条件下,电子-空穴的复合会产生荧光,进而出现发射峰。如图6(a)所示,普通g-C3N4由于其光生电子-空穴对的快速复合,在460 nm处表现出最强的光致发光。与普通g-C3N4相比,金属助催化剂的负载降低了发射峰的强度 (g-C3N4> Co/g-C3N4> Ni/g-C3N4> CoNi/g-C3N4)。这表明,金属助催化剂能有效地抑制光生电子-空穴对在界面上的复合,同时,CoNi合金表现出最低的发射峰强度。说明与单金属相比,双金属合金能通过电子的二次迁移来进一步优化电子迁移路径,进而更有效地帮助g-C3N4提升载流子的分离效率。

图 6 不同催化剂的PL与EIS谱图Figure 6 PL and EIS spectra of different catalysts
2.1.6 电化学阻抗分析
通过电化学阻抗(EIS)对界面电荷迁移能力进行了分析。一般情况下,圆弧半径越小,电荷在界面中迁移的阻抗越小[29]。从图6(b)中可以看出,CoNi/g-C3N4的圆弧半径最减小,表明在g-C3N4表面负载CoNi合金可以更有效地改善界面上的电子转移和分离。因此,与单金属相比,从半导体中激发的电子更容易迁移到双金属合金中。
2.2 光催化性能测试
为了考察CoNi/g-C3N4催化剂的实际性能,以罗丹明B (RhB)染料为污染物,研究了CoNi/g-C3N4在可见光照射下的光催化活性,并根据一级反应动力学方程计算出反应的动力学常数。图7(a)显示了所有样品对RhB的光催化降解效率,可以发现由于g-C3N4的表面结构较为光滑,对可见光的利用率较低以及载流子复合程度较高等不足,其光催化性能最弱,仅能降解48.9%的RhB。相同条件下,改性后的催化剂30 min暗吸附值约为13.5%,而普通g-C3N4的这一数值仅为8.4%,这是因为经过二次煅烧后的g-C3N4形成了许多孔状结构,正是因为这些孔状结构的存在增强了催化剂对底物的吸附。并且单金属Co与单金属Ni负载后催化剂的光催化性能也有所提升,分别可以降解77.5%和82.4%的RhB,而负载CoNi合金后,这一数值可以提升到95.4%。这是因为CoNi合金不仅能提升催化剂对可见光的利用,同时通过双金属间的协同作用,更有效地促进电子-空穴的分离,进而提升催化剂的光催化能力。
随后,分别考察了不同CoNi物质的量比 (1∶3、1∶2、1∶1、2∶1、3∶1) 对RhB降解性能的影响(图7(b)),以确定不同的CoNi物质的量比对光催化反应的影响。可以发现,CoNi物质的量比为1∶1时,降解速率最高。当CoNi物质的量比分别为1∶3、1∶2、1∶1、2∶1、3∶1时,在相同条件下对RhB的降解率为88.2%、92.5%、89.1%以及86.6%的RhB,也优于单金属改性的催化剂以及纯g-C3N4。这可能是由于Ni的电子功函数(Φ≈ 5.35 eV)略高于Co的电子功函数(Φ≈ 5.00 eV)[30]。Xiao等[31]的研究表明,当两种功函数不同的金属接触时,电子会在两种金属间发生二次的迁移直至达到平衡,进而形成了化学势相等的合金。同时较大的电子迁移数能促进光催化反应的进行。因此,当CoNi合金中两种金属物质的量比约为1∶1时降解效果最佳,可能是因为该物质的量比下Co、Ni双金属之间迁移的电子数最大。这些性质增强了反应物与催化剂之间的相互作用,有利于光催化反应的进行。根据一级动力学方程绘制出-ln(C/C0)与时间t线性相关的直线(图7(c)),由直线斜率得出速率常数k值,拟合的k值如表1所示,其中,CoNi/g-C3N4的速率常数最高,是g-C3N4的3.9倍。图7(d)所示为甲基蓝(MB)在g-C3N4和CoNi/g-C3N4催化剂作用下的降解率。图中显示出与降解RhB相同的降解趋势,助催化剂负载后甲基蓝的降解率显著提高,说明此方法改性催化剂适用于降解多种有机污染物。将合成的CoNi/g-C3N4与其他已发表的结果进行光催化降解效率比较,结果见表2。通过对比,本研究获得的CoNi/g-C3N4光催化性能具有一定的竞争优势。

表 1 不同催化剂对RhB降解拟合曲线的k值Table 1 k value of fitting curve of RhB degradation by different catalysts
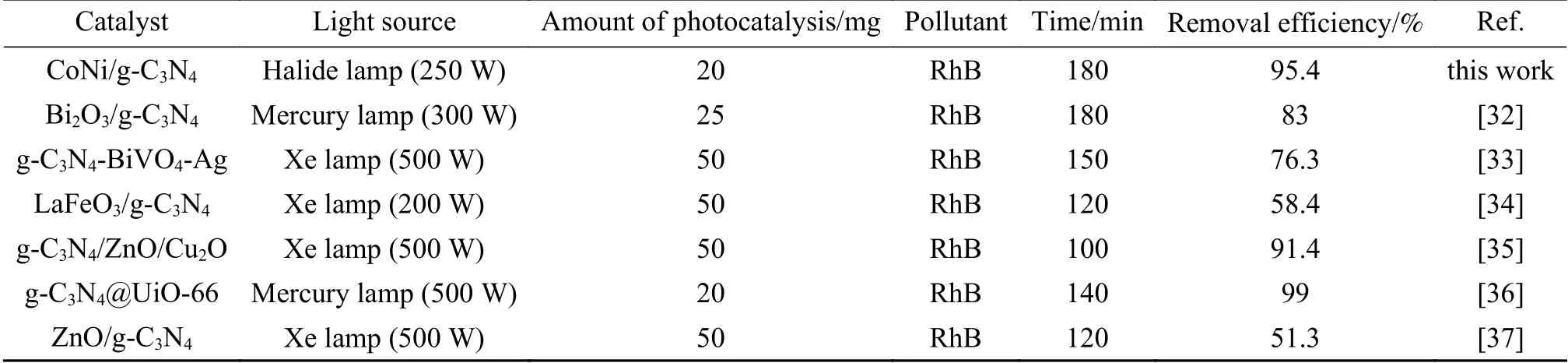
表 2 不同复合材料在可见光照射下光催化降解RhB的性能比较Table 2 Comparison of photocatalytic removal of RhB under visible light irradiation using different composite materials

图 7 ((a)、(b)) 不同催化剂对RhB的降解活性,(c) 降解动力学拟合,(d) 不同催化剂对MB的降解活性Figure 7 ((a), (b)) Degradation activity of different catalysts for RhB, (c) Degradation kinetic fit,(d) Degradation activity of different catalysts for MB
随后对CoNi/g-C3N4进行了催化稳定性测试,结果如图8所示。将实验后的试剂进行离心分离得到催化剂并用去离子水和乙醇洗涤三次后干燥,经过五次循环实验,观察到催化剂对RhB的降解性能略有降低,这可能是由于在洗涤和离心过程中催化剂的少量损失造成的,也可能是因为少量的RhB残留在催化剂表面,占据了部分活性位点。但是这仍能证明CoNi/g-C3N4可作为一种具有良好循环稳定性能的光催化剂。
为了探究反应机理和主要的反应物,用异丙醇(IPA)、对苯醌(BQ)和碘化钾(KI)分别作为羟基自由基(·OH)、超氧自由基()和空穴(h+)的捕获剂[38]。如图9所示,当反应溶液中加入BQ时,催化剂的降解效率明显下降,反应180 min后的降解率仅有39.1%,这说明是光降解RhB反应中的主要活性组分。KI的加入也减弱了催化剂降解能力,180 min后的降解率为58.3%。而当IPA加入到反应溶液中时,发现其对RhB的降解影响较弱,这意味着·OH不是反应的主要活性物质。
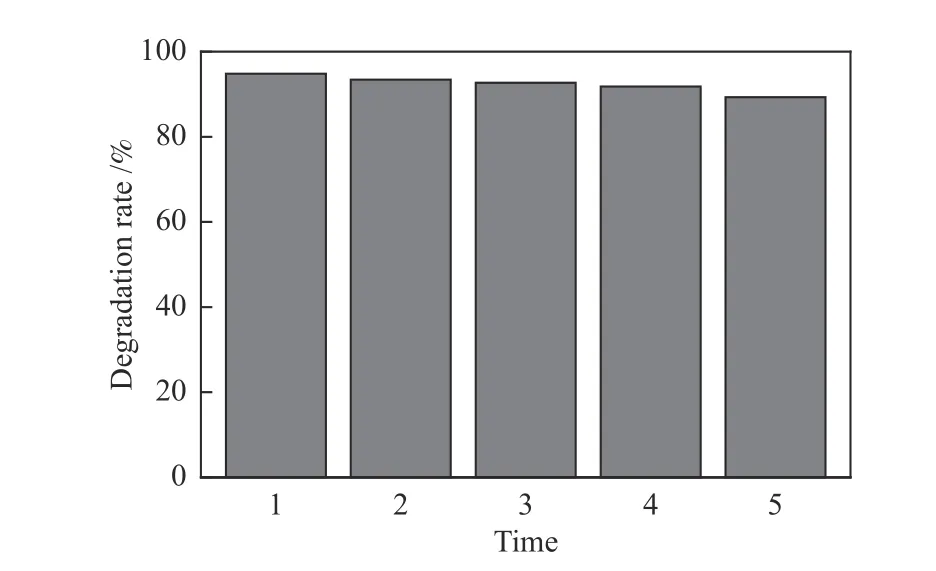
图 8 CoNi/g-C3N4稳定性实验Figure 8 Catalytic stability of CoNi/g-C3N4

图 9 各种捕获剂对 RhB 降解率的影响Figure 9 Effects of various scavenger agents on RhB degradation rate
根据以上实验结果,提出了CoNi/g-C3N4材料光催化降解RhB可能的机理(图10)。当CoNi双金属负载在g-C3N4后,能增强催化剂对可见光的吸收以及电子-空穴的分离效率。在可见光照射下,g-C3N4可以被激发,使得价带(VB)上的电子(e-)能够跃迁到导带(CB)上,同时在VB上形成空穴(h+)。然而,光生e-和h+在没有助催化剂的情况下易于发生复合。通过在g-C3N4上负载CoNi双金属助催化剂形成肖特基结。一方面增强了催化剂对光的利用率;另一方面e-转移到CoNi合金上,形成了e-和h+在空间上的分离,阻碍了电子-空穴的复合。对于CoNi/g-C3N4性能优于Co/g-C3N4和Ni/g-C3N4,可能是因为Ni的功函数为5.35 eV对应Evacuum(0.85 eV vs NHE),Co的功函数为5.00 eV对应Evacuum(0.50 eV vs NHE),比g-C3N4的导带(CB)更正。因此,e-会从g-C3N4转移到金属上。而金属的功函数小,电子迁移驱动力弱[30],金属功函数高则会在两种材料之间形成较高的肖特基势垒,抑制e-从g-C3N4向金属转移。因此,当形成CoNi合金后,功函数会处于两者之间[39],更有利于e-从g-C3N4向CoNi合金转移,更好地实现电子-空穴在空间上的分离。
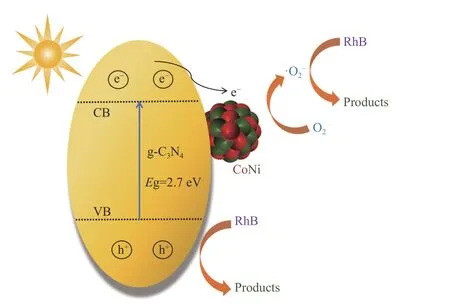
图 10 光催化降解RhB的机理Figure 10 Photocatalytic degradation mechanism of RhB
3 结 论
通过化学还原法在g-C3N4纳米片上原位形成了小尺寸的CoNi合金。CoNi合金一方面能增强g-C3N4对可见光的利用;另一方面通过双金属间的协同作用,使得光生电子-空穴对更有效的分离。经过二次煅烧制备的g-C3N4纳米片不仅能减少电荷扩散距离,形成更多的活性点。还可以增加催化剂对底物的吸收。
与g-C3N4相比,引入CoNi双金属助催化剂表现出显著提升的光催化性能,3 h内对RhB光催化降解率约为95.4%,降解效率是g-C3N4的3.9倍。
经过五次光催化循环实验后,CoNi/g-C3N4依然保持良好的稳定性和光催化活性,具有良好的应用前景。
