生物基两性离子型表面活性剂在不同驱油体系中的乳化稳定动力学
2022-11-16于洪洋李翠勤
黄 金, 于洪洋, 李 锋, 张 宇, 张 坤, 王 俊, 李翠勤
(1.东北石油大学 化学化工学院 石油与天然气化工省重点实验室,黑龙江 大庆 163318;2.大庆师范学院 油田应用化学与技术省重点实验室,黑龙江 大庆 163712)
随着对能源需求的不断增加以及常规油气资源开发难度的日益增大,致密油藏和页岩油藏等非常规油气资源受到广泛关注[1]。然而,这些非常规油藏油层物性差、渗透率低、纵向分布零散、非均质严重、黏土含量高,表面活性剂吸附损耗严重[2]。传统驱油用的烷基苯磺酸盐和石油磺酸盐阴离子型表面活性剂由于具有耐盐耐温性差、吸附损耗大等缺点[3],难以满足非常规油气资源的开采。
两性离子型表面活性剂随所在体系酸碱性的变化呈现不同的离子特性,不易受无机电解质的影响,不易形成疏水表面,相较于传统表面活性剂具有更好的耐高温和耐盐性能,作为一种驱油助剂广泛应用于高温高盐油藏地区[4]。目前国内对甜菜碱型两性表面活性剂的研究十分踊跃,但由于壬基酚甜菜碱两性表面活性剂和辛基酚甜菜碱型两性表面活性剂等石油基甜菜碱型表面活性剂的原料对环境污染较大,生物基表面活性剂成为该领域研究的热点之一[5-7]。Moslemizadeh等[8]以桑树叶为原料合成了一种新型生物基表面活性剂,该表面活性剂作为驱油剂可提高原油采收率达16.4%。Bian等[9]以可再生油酸为基本原料制备了一种新型含有支链烷基团的生物基苯磺酸盐表面活性剂,该表面活性剂具有较好的界面活性,可将水的表面张力降低至32.54 mN/m,将油/水界面张力降低至10-2mN/m。生物基表面活性剂因其可再生性、低毒性、易生物降解性及较高的乳化性能和界面活性受到广泛关注,成为未来表面活性剂的主要发展方向之一[10]。
以笔者所在课题组合成的一类生物基两性离子型表面活性剂(结构如图1所示)为研究对象,通过实验和分子模拟研究了该生物基两性离子型表面活性剂的界面特性,分析其结构对油/水界面特性的影响以及对不同体系的适应性。重点采用分水体积法研究了该类生物基两性离子型表面活性剂的乳化稳定性动力学,考察了乳化条件和体系组成对模拟乳状液稳定性动力学的影响,确定了该生物基两性离子型表面活性剂形成稳定乳状液的最佳体系和组成。

图1 生物基两性离子型表面活性剂的结构Fig.1 Chemical structure of bio-based zwitterionic surfactant
1 实验部分
1.1 原料和试剂
氯化镁、氯化钙、氯化钠和氢氧化钠,均为分析纯,科密欧化学试剂有限公司产品;部分水解聚丙烯酰胺(HPAM,黏均相对分子质量为2.5×107),中国石油大庆炼化公司提供;生物基两性离子型表面活性剂(CNBS),实验室自制[11];脱水原油,大庆油田有限责任公司第四采油厂提供,20 ℃标准密度为0.8557 g/cm3,45 ℃运动黏度为20.208 mm2/s,凝点为22.75 ℃。
1.2 界面张力的测定
将氯化钠、氯化镁和氯化钙按照质量比60∶3∶4配制一定矿化度的模拟注入水,然后采用模拟注入水配制不同浓度的系列生物基两性离子型表面活性剂水溶液,采用TX-500型全自动界面张力仪测定系列生物基两性离子型表面活性剂水溶液的界面张力,测试条件:温度为45 ℃,转速为5000 r/min。
1.3 乳化稳定动力学参数的测定
按照表1的实验方案配制含生物基两性离子型表面活性剂的水溶液,将溶液与脱水原油置于45 ℃的恒温水浴中预热30 min;采用FA25型高速剪切分散乳化机以10000 r/min对含生物基两性离子型表面活性剂溶液剪切1 min,然后与预热后的脱水原油按一定比例混合,在45 ℃下以10000 r/min剪切乳化5 min,获得模拟乳状液。将模拟乳状液置于100 mL具塞量筒中,45 ℃恒温静止并每隔5 min记录析出水体积,连续记录至90 min。设定φA为t时刻油相含水率(体积分数,下同),根据乳状液破坏过程(液滴絮凝,聚结,油、水分离) 及乳状液破乳的一级速率方程(式(1))[12],通过积分得到积分速率方程(式(2)),将乳状液破乳一半(1/2φA0)的时间定义为半衰期T1/2(式(3))。根据实验测得不同时间下乳状液析出水的体积,结合式(2)和式(3),得到不同体系和不同条件下形成乳状液的乳化稳定动力学参数:破乳速率常数hc、半衰期T1/2、90 min时油相的含水率φA90。
v=dφA/dt=hcφA
(1)
(2)
T1/2=ln2/hc
(3)
式中:v为乳状液的破乳速率,%/min;φA为不同时间下油相的含水率(体积分数),%;φA0为乳状液中初始含水率(体积分数),%;φA90为90 min时油相的含水率(体积分数),%;hc为破乳速率常数,min-1;t为静沉时间,min;T1/2为半衰期,min。

表1 乳化稳定动力学研究的实验方案Table 1 Experimental scheme for the research of emulsion-stabilizing kinetics
1.4 界面微观特性分子模拟方法
生物基两性离子型表面活性剂在油/水界面的微观特性模拟采用全原子分子动力学模拟技术,全部模拟计算使用Gromacs2020程序[13]完成,力场选择Gromos54a7力场,以十一烷代表油[14]。生物基表面活性剂分子使用Automated topology builder version 3.0进行结构优化并获得分子模拟用文件[15]。使用Gromacs命令构建5 nm×5 nm×9 nm的盒子(见图2),沿y轴划分为2 nm(油)+5 nm(水)+2 nm(油)共3个区域;油区域填充入十一烷,水区域填充水获得油+水体系(如图2(a)所示);水区域填充水和生物基两性离子型表面活性剂获得油+水+CNBS体系(如图2(b)所示)。对油/水、油/水/CNBS、油/水/CNBS/NaCl和油/水/CNBS/NaCl/NaOH等4个体系进行模拟,各体系中十一烷分子数量为127个,除油/水体系外其他体系中CNBS分子数量为4个,油/水/CNBS/NaCl体系和油/水/CNBS/NaCl/NaOH体系中按照质量浓度32 g/L加入NaCl(根据界面活性实验结果),油/水/CNBS/NaCl/NaOH体系按照质量分数1.00%加入NaOH(根据界面活性实验结果)。分子模拟全过程温度为45 ℃,先进行能量最小化优化,然后进行压力为0.1 MPa的等温等压(NPT)系综模拟,模拟总时长为300 ps,时间步长为2 fs。根据模拟后体系获得的密度曲线,计算油/水界面厚度、总能量Etotal、油相能量Eoil和水相能量Ewater,根据式(4)计算油/水界面能Einterface,能量单位均为kJ/mol。
Einterface=Etotal-Eoil-Ewater
(4)
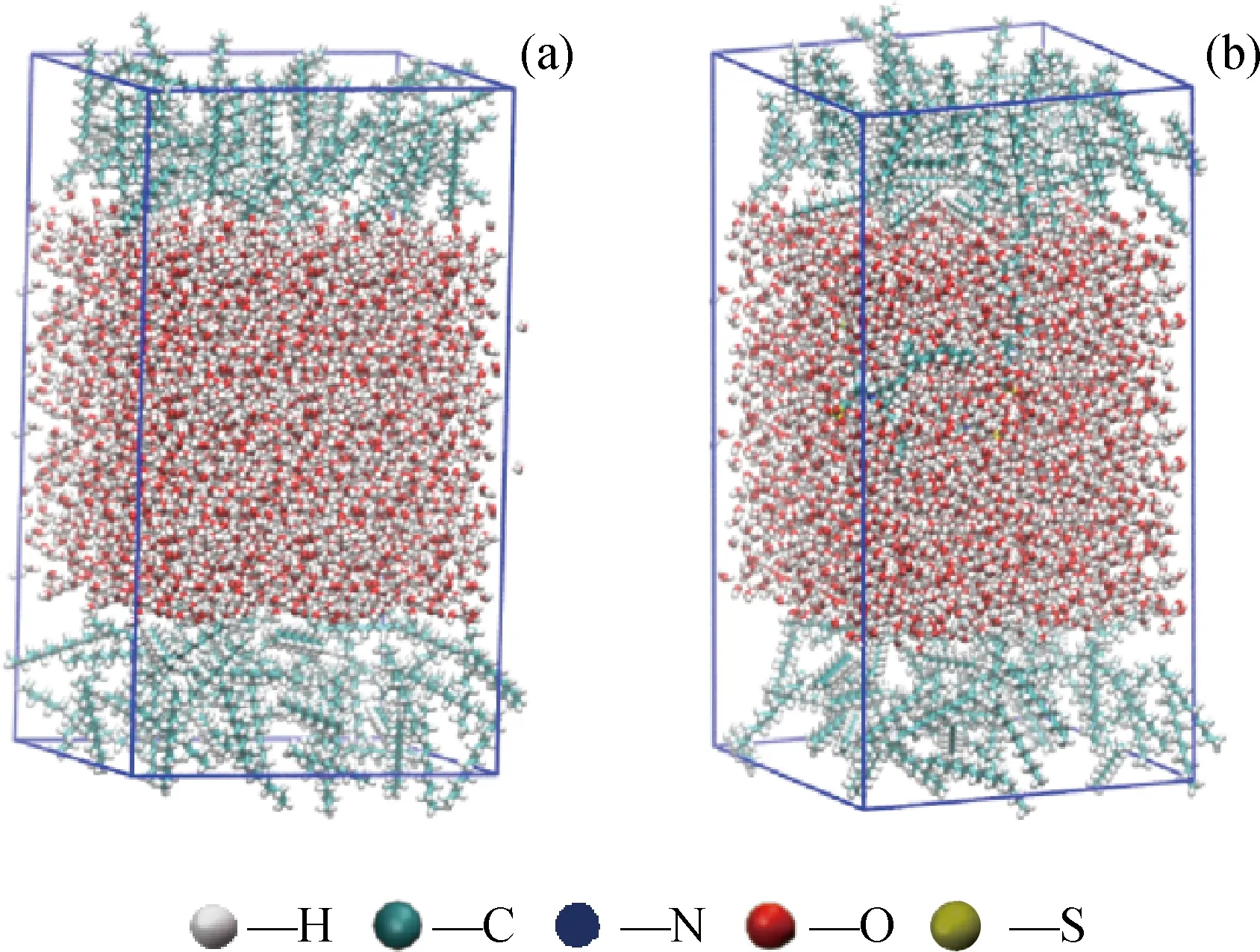
图2 分子模拟体系盒子Fig.2 Box of molecular simulation system(a) Oil+Water system; (b) Oil+Water+CNBS system
2 结果与讨论
2.1 乳化体系组成对生物基两性离子型表面活性剂界面活性的影响
固定总矿化度为5 g/L,配制不同生物基两性离子型表面活性剂浓度的溶液,按照1.2节中方法检测界面张力并绘制曲线,见图3(a)中曲线(1)。由图3(a)中曲线(1)可知,单一的生物基两性离子型表面活性剂体系,油/水界面张力未达到超低界面张力(1×10-3mN/m)。当体系中生物基两性离子型表面活性剂质量浓度低于1.5 g/L时,随其质量浓度增大,油/水界面张力下降;当表面活性剂质量浓度达到1.5 g/L时,继续增大表面活性剂浓度,界面张力变化很小。这主要是因为,较低浓度的两亲性表面活性剂分子在油/水界面上排布比较疏松;随着浓度增大,吸附在油/水界面的表面活性剂分子排布比较紧密;当表面活性剂质量浓度接近1.5 g/L时,表面活性剂在油/水界面达到饱和吸附。且通过图3(a)中曲线(1)得到该生物基两性离子型表面活性剂在该体系中的临界胶束质量浓度为1.29 g/L,此浓度下的油/水界面张力为3.28×10-2mN/m。与课题组合成的单一阴离子型生物基表面活性剂(3.68 g/L)[16]相比,由于该生物基两性离子型表面活性剂双亲水基电荷的中和作用,使其在较低的质量浓度下(1.29 g/L)就能在油/水界面达到饱和吸附。
固定生物基两性离子型表面活性剂的质量浓度为1.29 g/L,配制不同矿化度的生物基两性离子型表面活性剂溶液,按照1.2节中测定界面张力并绘制曲线,见图3(a)中曲线(2)。由图3(a)中曲线(2)可知:随着体系矿化度增大,生物基两性离子型表面活性剂的界面活性增加;但当体系矿化度达到32 g/L时,继续增大体系的矿化度,界面张力变化较小。这主要是由于该生物基表面活性剂为两性离子型表面活性剂,分子中含有阳离子亲水基团和阴离子亲水基团;随着体系矿化度的增大,体系中无机盐在水中电离的阳离子和阴离子浓度增大,这些离子与表面活性剂分子中的离子相互作用,使得表面活性剂分子中亲水基团之间的电荷斥力作用减弱,表面活性剂分子在油/水界面排列紧密,界面张力降低,界面活性增大;但当体系中的矿化度增大到一定值时,表面活性剂亲水基团附近与其所带电荷相反的无机离子浓度增大到一定值时,电荷之间的作用达到平衡,继续增大体系矿化度对表面活性剂分子在油/水界面上的吸附性能影响较小,界面张力几乎不变化[17]。因此,针对该类生物基两性离子型表面活性剂所形成的油/水乳状液体系,较适宜的矿化度为32 g/L。
固定生物基两性离子型表面活性剂质量浓度为1.29 g/L、矿化度为32 g/L,NaOH质量分数对含有生物基两性离子型表面活性剂溶液的油/水界面张力的影响见图3(b)中曲线(1)。由图3(b)中曲线(1)可知,随着体系中NaOH质量分数增大,界面张力逐渐降低。当NaOH质量分数增加至1.0%时,界面张力为9.96×10-3mN/m,达到了超低界面张力(10-3mN/m);继续增大NaOH质量分数,界面张力继续降低,在NaOH质量分数增大到2.5%时,界面张力降为9.60×10-4mN/m。这表明碱的加入有利于降低生物基两性离子型表面活性剂体系的油/水界面张力,这是由于一方面碱与油相中的脂肪酸反应形成表面活性物质,与表面活性剂分子在油/水界面形成混合界面膜[18];另一方面碱电离出的离子与生物基两性离子型表面活性剂的亲水基反应,降低表面活性剂分子间的斥力,使得表面活性剂分子在油/水界面排列更加紧密,从而降低界面张力。但当碱的用量过大时,会对地层造成伤害。因此,针对该类生物基两性离子型表面活性剂所形成的油/水乳状液体系,较适宜的NaOH质量分数为1.0%。
固定表面活性剂质量浓度为1.29 g/L、矿化度为32 g/L、NaOH质量分数为1.0%,HPAM质量浓度对含有生物基两性离子型表面活性剂溶液的油/水界面张力的影响见图3(b)中曲线(2)。由图3(b)中曲线(2)可知:生物基两性离子型表面活性剂溶液中引入HPAM,油/水界面张力变化较小;当HPAM质量浓度小于500 mg/L时,随着HPAM浓度的增大,界面张力变化较小;当HPAM质量浓度达到500 mg/L时,继续增大HPAM浓度,界面张力增加幅度较大。这是由于加入体系中的HPAM,会与表面活性剂在油/水界面上发生竞争吸附,导致油/水界面上吸附的有效表面活性剂分子浓度降低,界面张力增大[19]。
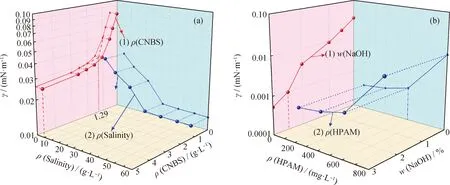
图3 乳化体系组成对生物基两性离子型表面活性剂界面活性的影响Fig.3 Effect of the composition of emulsion system on interfacial activity of bio-based zwitterionic surfactant(a)—(1) Effect of CNBS mass concentration on interfacial tension (γ), condition: ρ(Salinity)=5 g/L;(a)—(2) Effect of salinity on interfacial tension (γ), condition: ρ(CNBS)=1.29 g/L;(b)—(1) Effect of NaOH mass fraction on interfacial tension (γ), conditions: ρ(Salinity)=32 g/L;ρ(CNBS)=1.29 g/L;(b)—(2) Effect of HPAM mass concentration on interfacial tension (γ), conditions: ρ(Salinity)=32 g/L;ρ(CNBS)=1.29 g/L; w(NaOH)=1.0%
2.2 体系总含水量对生物基两性离子型表面活性剂乳化稳定动力学的影响
根据2.1节中界面张力的研究结果,当生物基两性离子型表面活性剂质量浓度为1.29 g/L、NaOH质量分数为2.5%、HPAM质量浓度为500 mg/L、矿化度为32 g/L时界面张力最低,以此条件配制溶液,以不同总含水量进行油/水混合,按照1.3节中方法研究体系总含水体积分数对生物基两性离子型表面活性剂乳化稳定动力学性能的影响,结果见图4和表2所示。

φA—The water volume fraction in the oil phase图4 体系总含水体积分数对模拟乳状液乳化稳定性的影响Fig.4 Effect of the bulk volume fraction of water contenton stability of the simulated emulsionConditions: ρ(Salinity)=32 g/L; ρ(CNBS)=1.29 g/L;w(NaOH)=2.5%; ρ(HPAM)=0.5 g/L
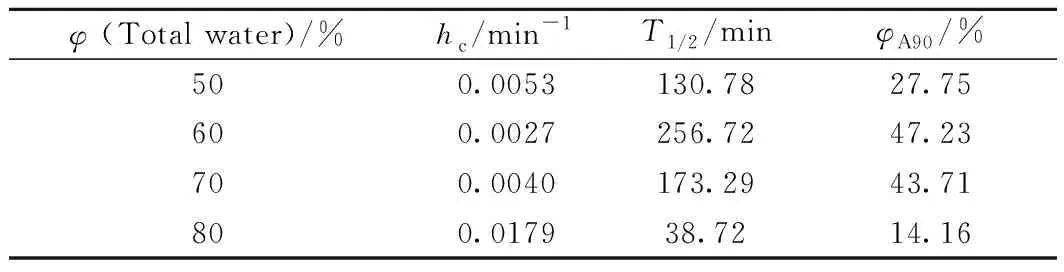
表2 体系总含水体积分数对模拟乳状液乳化稳定动力学参数的影响Table 2 Effect of the bulk volume fraction ofwater content on parameters regarding theemulsion-stabilizing kinetics of the simulated emulsion
由图4可知,随着静沉时间延长,不同含水量的乳状液体系中油相含水率φA均降低,乳状液最终因不稳定而破乳。这是由于乳状液是热力学不稳定体系,随着静沉时间的延长,乳状液中的微油滴(微水滴)发生运动碰撞,界面膜破裂,油滴(水滴)聚并,导致乳状液稳定性下降。总含水体积分数为60%的乳状液油相含水率下降幅度较小,表明当体系总含水率为60%时,该生物基两性离子型表面活性剂的油/水界面膜较稳定。由表2可知,随着总含水量增大,破乳速率常数hc先增大后减小,半衰期T1/2和90 min时油相含水率φA90先升高后降低。破乳速率常数hc越小、半衰期T1/2和90 min时油相含水率φA90越大,对应的乳状液越稳定。当乳化体系总含水率为60%时,破乳速率常数hc最小,半衰期T1/2和90 min时油相含水率φA90达到最高值,分别为256.72 min和47.23%。这进一步表明,当总含水率等于60%时,形成的乳化体系稳定性较高,且乳状液以W/O型为主。另外,随着体系总含水率的增大,半衰期T1/2降低,体系稳定性下降,但90 min时油相含水率φA90大于0,这表明该生物基两性离子型表面活性剂由于其原料饱和腰果酚分子中长链亲油烷基以及在反应过程中表面活性剂分子中引入的2个丁烷基团增加了该表面活性剂的亲油性,体系中该表面活性剂的添加易于形成W/O型乳状液。体系总含水率影响结果初步证实该生物基两性离子型表面活性剂在总含水体积分数为60%时具有良好的乳化稳定性。
2.3 生物基两性离子型表面活性剂浓度对其乳化稳定动力学的影响
固定总矿化度为32 g/L和体系总含水体积分数为60%时,分析该生物基两性离子型表面活性剂质量浓度对模拟乳状液稳定动力学的影响,结果如图5和表3所示。
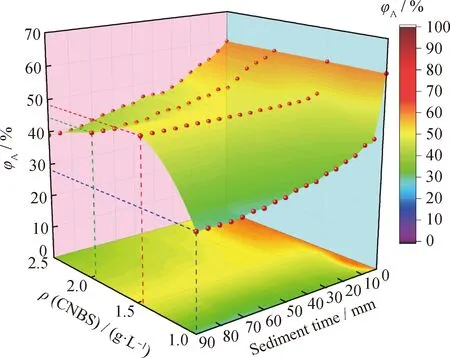
φA—The water volume fraction in the oil phase图5 表面活性剂CNBS浓度对模拟乳状液乳化稳定性的影响Fig.5 Effect of concentration of the surfactant CNBSon stability of the simulated emulsionConditions: ρ(Salinity)=32 g/L;φ(Total water)=60%
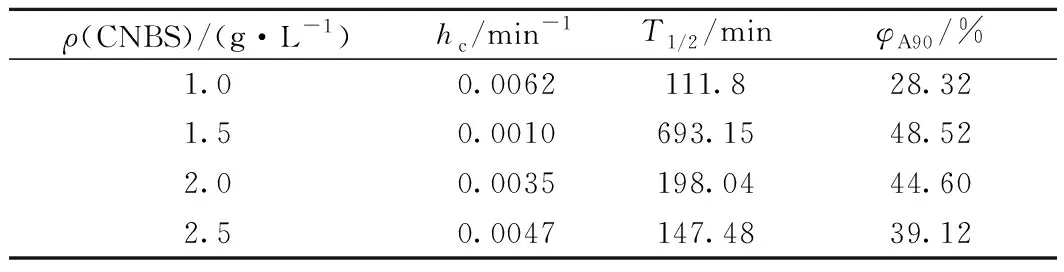
表3 表面活性剂浓度对模拟乳状液乳化稳定动力学参数的影响Table 3 Effect of surfactant concentration on parametersregarding the emulsion-stabilizing kinetics ofthe simulated emulsion
由图5可知:随着静沉时间的延长,不同质量浓度生物基表面活性剂的模拟乳状液油相含水率φA下降幅度开始较大,随后降幅较小;在静沉初期,随生物基两性离子型表面活性剂质量浓度增大,模拟乳状液油相含水率φA增大;当静沉时间为90 min,生物基两性离子型表面活性剂质量浓度为1.5 g/L时,模拟乳状液油相含水率φA最大。这是由于当表面活性剂质量浓度较低时,吸附在油/水界面上的表面活性剂分子较少,分子处于平躺或斜躺状态,形成的界面膜稳定性较差;当表面活性剂浓度大于临界胶束浓度时,其在油/水界面达到饱和吸附,形成稳定的界面膜。当表面活性剂浓度大于临界浓度时,一方面,表面活性剂在水相易于形成胶束,促进水相乳化,不利于W/O型乳状液的形成;另一方面,随着表面活性剂浓度增大,表面活性剂在溶液中形成胶束,模拟乳状液体系的黏度增大,一定程度上阻止表面活性剂分子进一步在油/水界面的定向排列[20]。由表3的动力学参数可知:当生物基两性离子型表面活性剂质量浓度为1.5 g/L时,模拟乳状液破乳速率常数最小,为0.0010 min-1;半衰期T1/2和90 min时油相含水率φA90达到最大值,分别为693.15 min和48.52%,油/水体系主要形成W/O型乳状液。在该实验测量浓度范围内,φA90大于0,说明油/水体系主要形成W/O型乳状液。当生物基两性离子型表面活性剂质量浓度低于1.5 g/L时,随着表面活性剂质量浓度的增大,模拟乳状液破乳速率常数减小,半衰期T1/2和油相含水率φA90均升高;当表面活性剂质量浓度高于1.5 g/L,随着表面活性剂质量浓度的增大,模拟乳状液破乳速率常数增大,半衰期T1/2和油相含水率φA90均降低,这表明,表面活性剂浓度是影响乳状液稳定性的主要因素。
2.4 NaOH质量分数对生物基两性离子型表面活性剂乳化稳定动力学的影响
固定矿化度为32 g/L、总含水体积分数为60%、生物基两性离子型表面活性剂质量浓度为1.5 g/L,考察NaOH质量分数对生物基两性离子型表面活性剂形成的二元模拟乳状液稳定动力学的影响,结果如图6和表4所示。

φA—The water volume fraction in the oil phase图6 NaOH质量分数对模拟乳状液乳化稳定性的影响Fig.6 Effect of NaOH mass fraction on emulsifyingstability of the simulated emulsionConditions: ρ(Salinity)=32 g/L;φ(Total water)=60%; ρ(CNBS)=1.5 g/L
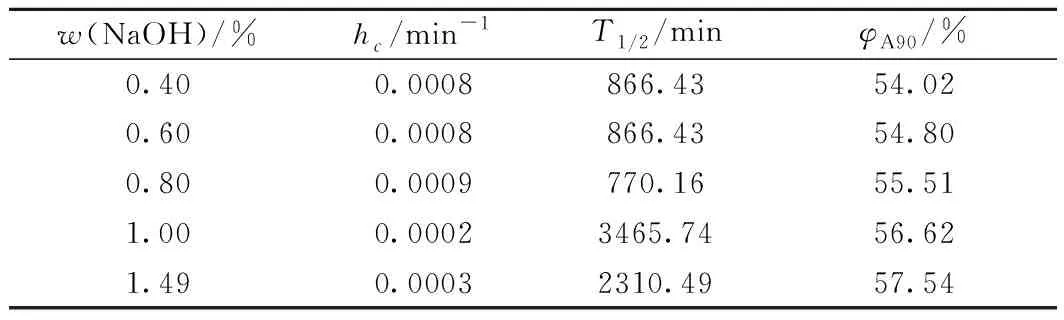
表4 NaOH质量分数对乳状液乳化稳定动力学参数的影响Table 4 Effect of NaOH mass fraction on parametersregarding the emulsion-stabilizing kinetics ofthe simulated emulsion
由图6可知:随着NaOH的加入,乳状液体系的φA增加幅度较小;且随着静沉时间的延长,NaOH在二元模拟乳状液体系的φA变化较小,实验所测范围内模拟乳状液的φA范围为53%~60%。这是由于当生物基两性离子型表面活性剂质量浓度为1.5 g/L,形成的模拟乳状液比较稳定(见表3)。当体系中加入NaOH后,一方面NaOH通过电荷之间的相互作用,使溶液中的表面活性剂离子与溶液中无机离子达到平衡,同时影响生物基两性离子型表面活性剂在水相分布能力和油/水界面的分布能力,使油/水界面张力降低;另一方面NaOH与原油中的酸性物质反应形成的表面活性物质也会吸附到油滴表面,与吸附在油/水界面上的生物基两性离子型表面活性剂发生协同吸附[21],增加界面膜上吸附的分子密度,提高了界面膜的稳定性,多方面的协同作用增加了乳状液的稳定性。但是由于表面活性剂分子在油/水界面已达到饱和吸附,形成的表面活性物质在油/水界面有效吸附量较小,且受原油中酸性物质含量的影响,导致NaOH质量分数对生物基两性离子型表面活性剂形成的二元模拟乳化体系的乳化稳定动力学性能影响较小。从表4也可以看出,随着NaOH质量分数增大,φA90和破乳速率常数hc变化均较小,且当NaOH质量分数在0~1.49%范围内,φA90大于0,体系仍主要是W/O型乳状液。然而,半衰期T1/2变化很大,当NaOH质量分数为0.40%时,半衰期T1/2为866.43 min;当NaOH质量分数为1.00%时,半衰期T1/2达到最大,为3465.74 min。这表明,在二元体系中,NaOH与生物基两性离子型表面活性剂协同形成较稳定的模拟乳状液。但是NaOH质量分数过高会伤害地层,因此,针对该研究体系,NaOH适宜的质量分数为1.00%。
2.5 部分水解聚丙烯酰胺浓度对生物基两性离子型表面活性剂乳化稳定动力学的影响
固定矿化度为32 g/L、总含水体积分数为60%、表面活性剂质量浓度为1.5 g/L、碱质量分数为1.00%,考察HPAM质量浓度对模拟三元乳状液稳定动力学的影响,结果见图7和表5所示。
由图7可以看出,随着静沉时间的延长,φA逐渐下降,其中HPAM质量浓度为2000 mg/L的体系降低速率最快。这表明,随着HPAM的加入,生物基两性离子型表面活性剂形成的乳状液乳化稳定性下降。从表5也可以看出,随着HPAM质量浓度增大,破乳速率常数hc增大,半衰期T1/2减小,这是由于HPAM除影响乳化体系的油、水分离过程外,还会影响乳状液的形成。这是因为,在乳状液制备过程中,随着HPAM质量浓度增大,水相溶液黏度逐渐增大,会消耗一定量的机械能,导致促进乳状液生成的能量减少。另外,随着HPAM质量浓度增大,表面活性剂分子向油/水界面扩散的速率降低,溶液界面张力增大(图3);同时模拟乳状液体系黏度的增大,导致供乳状液生成的能量和乳化液滴运动速率和碰撞机率降低[22]。当HPAM质量浓度为900 mg/L时,φA90最大,这是由于当HPAM质量浓度小于900 mg/L时,提高HPAM质量浓度可以促进乳状液生成和稳定;当HPAM质量浓度大于900 mg/L时,提高HPAM质量浓度会减弱乳状液的生成。因此,采用强碱三元复合驱油体系提高原油采收率时,结合驱油体系的黏度和界面张力,针对该生物基两性离子型表面活性剂形成的强碱三元复合驱油体系,选择适宜的HPAM质量浓度为900 mg/L。
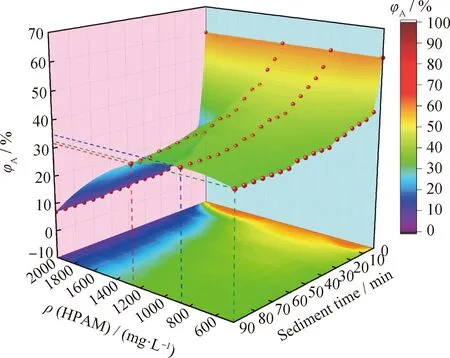
φA—The water volume fraction in the oil phase图7 聚合物质量浓度对模拟乳状液乳化稳定性的影响Fig.7 Effect of polymer mass concentration on stability ofthe simulated emulsionConditions: ρ(Salinity)=32 g/L;φ(Total water)=60%;ρ(CNBS)=1.5 g/L; w(NaOH)=1.00%
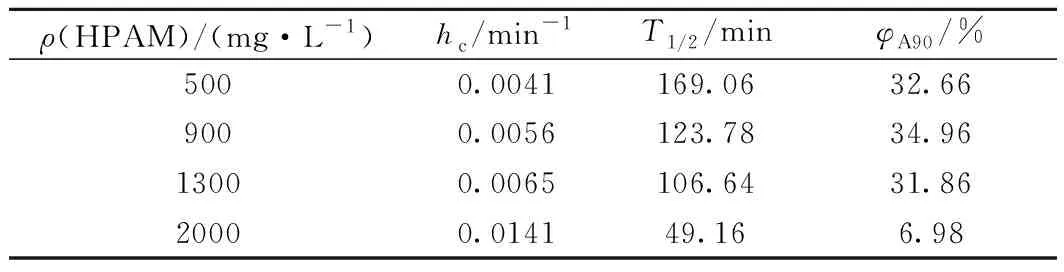
表5 HPAM质量浓度对三元模拟乳状液乳化稳定参数的影响Table 5 Effect of HPAM mass concentration on stabilityparameters regarding the ternary simulated emulsion
2.6 生物基两性离子型表面活性剂的界面微观特性
生物基两性离子型表面活性剂在不同体系中的界面活性以及乳化稳定动力学研究结果表明,该活性剂在油/水界面的分布是影响界面张力和乳液稳定性的关键因素。为了进一步研究其在油/水界面的微观特性,对油/水、油/水/CNBS、油/水/CNBS/NaCl和油/水/CNBS/NaCl/NaOH 4种体系形成的油/水界面的微观特性进行分子模拟及模拟结果分析。研究油/水/表面活性剂体系的界面时,按照“90%~90%”原则进行界面厚度计算,计算油相和水相的密度分布见图8(a),其中油相密度的90%与水相密度90%之间的距离为界面厚度[23]。基于此方法统计所模拟的体系油相和水相密度沿Z轴分布情况并计算界面厚度,见图8。根据式(4)计算油/水界面能,结果见表6。
由图8和表6可知:纯油/水体系的油/水界面膜厚度为0.3795 nm;而加入生物基两性离子型表面活性剂后,油/水/CNBS体系的油/水界面厚度增加到0.5948 nm,且界面能由-2241.14 kJ/mol降至-2379.91 kJ/mol。表明,随着生物基两性离子型表面活性剂的加入,形成的模拟乳状液的稳定性增强。向油/水/CNBS体系中加入NaCl,油/水/CNBS/NaCl体系的油/水界面厚度由0.5948 nm降至0.5739 nm,油/水/CNBS/NaCl体系的界面能由-2379.91 kJ/mol降至-2464.24 kJ/mol(见表6)。向油/水/CNBS/NaCl体系中加入NaOH,油/水/CNBS/NaCl/NaOH体系的油/水界面厚度和界面能进一步下降,分别降至0.5422 nm和-2517.86 kJ/mol。这进一步表明,随着NaCl和NaOH的加入,油/水/CNBS/NaCl体系和油/水/CNBS/NaCl/NaOH体系越稳定,形成的乳状液稳定性增强。这是因为,在水相中加入NaCl或NaOH后,离子浓度发生了变化,导致界面层被压缩,油/水界面膜厚度变小,但压缩后界面层的界面能更低,界面的稳定性得到增强。
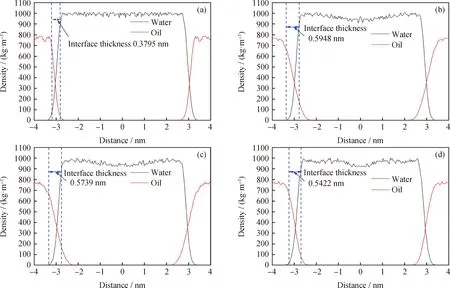
图8 模拟体系中油分子和水分子沿z轴密度分布曲线Fig.8 z-Axis density distribution of water and oil molecules in the simulation system(a) Oil/Water system; (b) Oil/Water/CNBS system; (c) Oil/Water/CNBS/NaCl system; (d) Oil/Water/CNBS/NaCl/NaOH system

表6 模拟体系界面能计算结果Table 6 Calculation results of the interfacial energy in the simulation system
3 结 论
(1)通过测定界面张力和分子动力学模拟技术研究了生物基两性离子型表面活性剂在油/水界面的性质和分布,界面张力测定结果表明,在矿化度为32 g/L、NaOH质量分数为2.5%的条件下,该生物基两性离子型表面活性剂的质量浓度为1.29 g/L的溶液的油/水界面张力最低可达9.60×10-4mN/m。分子模拟结果表明,在油/水体系中加入该生物基两性离子型表面活性剂可将油/水界面膜厚度由0.3795 nm提高至0.5948 nm。
(2)NaCl和NaOH使油/水界面膜厚度和界面能均降低。
(3)乳化稳定动力学研究结果表明,该生物基两性离子型表面活性剂形成的模拟乳状液以W/O型为主,表面活性剂质量浓度是影响乳状液稳定动力学的关键因素,当表面活性剂浓度接近其临界胶束浓度时,形成的模拟乳状液稳定动力学参数半衰期和油相含水率均最大,破裂速率常数最小,此时形成的乳状液最稳定。
