亚麻籽胶-大豆分离蛋白乳状液微滴聚集体的制备及其流变特性
2019-08-12马宁宁许朵霞肖俊松曹雁平孙宝国
王 旭 马宁宁 李 昕 凌 月 许朵霞 肖俊松 曹雁平 孙宝国
(北京食品营养与人类健康高精尖创新中心 北京工商大学食品学院 北京市食品添加剂工程技术研究中心食品添加剂与配料北京高校工程研究中心 北京市食品风味化学重点实验室食品质量与安全北京实验室 北京 100048)
高脂肪含量的食品虽然是导致肥胖的主因,但是,减少脂肪含量,会劣变食品流变等特性,影响其口感与饱腹感,成为开发低脂食品的瓶颈。采用新方法提高食品体系的流变特性,具有重要的研究价值。基于乳状液微滴间异型聚集效应,形成具有特定三维空间网络结构的微聚集体,成为提高食品乳状液体系流变特性的新途径[1-2]。
蛋白质、油脂、多糖是食品体系中重要的3类生物大分子,是影响食品结构和质构的主要因素。在实际体系中3种分子往往共存,由于两种分子之间的相互作用,此时体系的稳定性和质构特性并非这3种分子作用的简单加和[3-4]。水包油体系乳状液的异型聚集为提高食品乳状液体系流变特性提供了研究思路。本研究基于乳状液微滴间静电组装,构建大豆分离蛋白和亚麻籽胶两种乳状液异型微聚集体,考察其粒径大小与分布、zeta-电位、物理稳定性、微观结构、剪切流变与微流变特性,确定最佳混合比例,构建具有高流变特性同时具有良好稳定性的异型微聚集体,为脂肪模拟物的研究提供思路。
1 材料与方法
1.1 材料与设备
亚麻籽胶(FG,纯度≥99%),新疆利世得生物科技有限公司;中链甘油三酸酯 (MCT,C8-C10),奎斯特(上海)国际有限公司;大豆分离蛋白(SPI,纯度≥90%),美国 Davisco国际食品公司;NaOH、HCl、NaH2PO4、Na2HPO4,国药集团化学试剂有限公司。
HD-1型高速乳化均质机,北京华远航实验设备厂;集热式恒温加热磁力搅拌器,河南省予华仪器有限公司;M-110EH型微射流仪,加拿大Microfluidics公司;Zetasizer Nano-ZS90激光粒度仪,英国Malvern公司;Modular Compact Rheometer剪切流变仪,法国Formulaction公司;微流变仪,法国Formulaction公司;pH计,梅特勒-托利多仪器(上海)有限公司;尼康80 i显微镜,日本尼康公司。
1.2 试验方法
1.2.1 大豆分离蛋白SPI/MCT乳状液的制备 准确称取一定量的大豆分离蛋白 (SPI),溶解于5 mmol/L磷酸盐缓冲溶液(pH 7.0)中,50℃搅拌2 h,溶胀过夜,使用前于50℃搅拌30 min,确保SPI充分溶解,制备SPI溶液(1%),形成水相。将溶解好的SPI溶液用1 mol/L HCl调节pH值至3.0。准确称取一定量的MCT(10%),作为油相。以高速乳化均质机19 000 r/min剪切 5 min,形成粗乳状液;粗乳状液通过微射流进一步均质得到SPI/MCT乳状液,均质压力50 MPa,均质3次。
1.2.2 亚麻籽胶FG/MCT乳状液的制备 准确称取一定量的亚麻籽胶(FG),溶解于5 mmol/L磷酸盐缓冲溶液(pH 7.0)中,于50℃搅拌2 h,溶胀过夜,使用前50℃搅拌30 min,确保FG充分溶解,制备FG溶液 (0.6%),形成水相。将溶解好的FG溶液用1 mol/L HCl调节pH值至3.0。准确称取一定量的MCT(10%),作为油相。在高速乳化均质机19 000 r/min剪切5 min,形成粗乳状液,将其通过微射流进一步均质得到FG/MCT乳状液,均质压力为50 MPa,均质3次。
1.2.3 FG乳状液-SPI乳状液微聚集体的制备将1%的SPI乳状液与0.6%的FG乳状液按不同比例分别混合(0∶10,1∶9,2∶8,3∶7,4∶6,5∶5,6∶4,7∶3,8∶2,9∶1,10∶0),混合均匀,用1 mol/L HCl将混合乳状液pH值调至3.0,形成不同组成的FG乳状液-SPI乳状液微聚集体。
1.2.4 FG乳状液-SPI乳状液微聚集体Zeta-电位分析 采用Nano-ZS90激光粒度仪,分析FG乳状液-SPI乳状液微聚集体Zeta-电位。为减小多重光散射对测量的误差,样品在分析测试前用5 mmol/L磷酸盐缓冲液(pH 3.0)稀释400倍。每个样品分析重复3次,结果以平均值表示。
1.2.5 FG乳状液-SPI乳状液微聚集体粒径分析 采用激光粒度仪测定FG乳状液-SPI乳状液微聚集体粒径。乳状液(或其稀释液)的粒径是衡量乳状液微聚集体的尺寸分布。为减小多重光散射对测量的误差,样品在分析测试前用5 mmol/L磷酸盐缓冲液(pH 3.0)稀释400倍。每个样品分析重复3次,结果以粒径平均值(nm)表示。
1.2.6 FG乳状液-SPI乳状液微聚集体物理稳定性分析 应用Lumisizer稳定性分析仪,通过加速分层和量化沉淀、悬浮的方法(STEP-Technology)快速测定乳状液的稳定性。不稳定性指数(Instability index)是在离心的过程中,平行的近红外光照射在样本试管上,通过记录样品不同位置的透射率分布的变化,确定乳状液粒子的迁移过程。取乳状液约0.4 mL,均匀注射至样品试管底部,温度设定为25℃,离心转数为2 500 r/min,样品的透射率的特征线每30 s记录1次,共255次。
1.2.7 FG乳状液-SPI乳状液微聚集体剪切流变特性分析 采用安东帕流变仪 (MCR-301)测定FG乳状液-SPI乳状液微聚集体在剪切作用力条件下的流变学特性。根据样品特性,选择型号为CP-50-1的不锈钢平板转子,测量时的平板转子间距设定为0.1 mm。加样时注意保持样品均匀,防止气泡。剪切速率为2~200 s-1,测量温度为25℃。每个样品重复3次。
1.2.8 FG乳状液-SPI乳状液微聚集体微流变特性分析 采用Rheolaser Master微流变仪分析FG乳状液-SPI乳状液微聚集体微流变特性,微流变仪通过多散斑扩散波光谱学理论分析软物质的微流变特性,通过专利运算法计算对应相关时间的粒子均方根位移(MSD)。将20 mL不同比例的FG乳状液-SPI乳状液倒入样品池内,测量温度为25℃,放入仪器内测量。通过广义的斯托克斯爱因斯坦关系式,计算对应频率下的黏性指数(MVI)和弹性指数(EI)。
1.2.9 FG乳状液-SPI乳状液微聚集体微观结构分析 采用尼康80 i显微镜分析FG乳状液-SPI乳状液微聚集体的微观结构。取1滴FG乳状液-SPI乳状液置于载玻片上,用60倍油镜观察,调节显微镜焦距至形成清晰的画面后,拍照。分析软件为显微镜摄影图像处理软件NIS-Elements。
1.3 数据分析方法
数据统计分析用SPSS 12.0 for Windows软件(美国 SPSS公司)进行方差分析(ANOVA),显著性水平为0.05,所有试验均重复3次。
2 结果与分析
2.1 FG乳状液微滴含量对FG乳状液-SPI乳状液微聚集体Zeta-电位的影响
不同含量的亚麻籽胶(FG)乳状液微滴对FG乳状液-SPI乳状液微聚集体Zeta-电位的影响如图1所示。随着FG乳状液微滴含量的增大,FG乳状液-SPI乳状液微聚集体的Zeta-电位值由正变为负,当FG乳状液微滴含量小于60%时,乳状液微聚集体微滴带正电荷;当FG乳状液微滴含量为60%时,乳状液微聚集体的Zeta-电位值接近0;FG乳状液微滴含量大于60%时,FG乳状液-SPI乳状液微聚集体微滴带负电荷。这表明带异型电荷的FG乳状液微滴与SPI乳状液微滴之间通过静电相互作用发生聚集。静电相互作用是影响FG乳状液-SPI乳状液微聚集体的主要作用力。在静电相互作用下,带负电荷的FG-乳状液微滴吸附至SPI乳状液微滴上,使得体系的Zeta-电位下降。随着FG乳状液含量的继续增加 (80%和90%),Zeta-电位值不再显著降低,与FG乳状液的Zeta-电位相比,无显著性差异。推测可能是因为足量的FG乳状液微滴与SPI乳状液微滴产生静电吸附作用,使得微聚集体的zeta-电位不再发生显著变化。
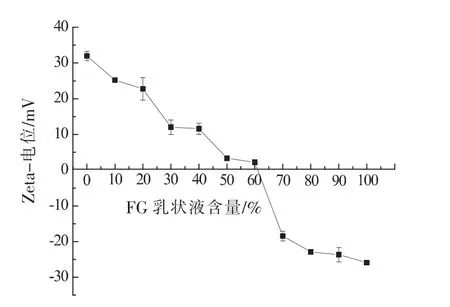
图1 FG乳状液含量对FG乳状液-SPI乳状液微聚集体Zeta-电位的影响Fig.1 Effect of FG emulsion content on the zeta-potential of the heteroaggregated emulsions of FG-coated droplets and SPI-coated droplets
2.2 FG乳状液微滴含量对FG乳状液-SPI乳状液微聚集体粒径的影响
不同含量的FG乳状液微滴对FG乳状液-SPI乳状液微聚集体粒径的影响如图2所示。随着FG乳状液微滴含量的增加,FG乳状液-SPI乳状液微聚集体的粒径呈先增大后减小的趋势,这主要是因为带有负电荷的FG乳状液微滴吸附至SPI乳状液微滴上,形成微聚集体使粒径变大。当FG乳状液微滴含量小于30%时,乳状液粒径变化较小,这主要是SPI占主导地位,只有小部分的FG乳状液微滴通过静电相互作用与SPI乳状液微滴吸附,形成少部分的微聚集体。而后,随着FG乳状液微滴的增多,带负电荷的FG乳状液微滴可与带正电荷的SPI乳状液微滴相互作用(微滴间和游离FG、SPI分子间)形成具有特定结构的空间网络结构的微聚集体。当FG乳状液微滴含量为60%时,乳状液微聚集体的粒径最大,FG乳状液-SPI乳状液微聚集效应最强。随着FG乳状液微滴含量的增加,FG乳状液微滴占主导地位,FG乳状液-SPI乳状液微聚集效应减弱,表明带异型电荷的FG乳状液-SPI乳状液聚集效应的最佳比例为 6∶4。
2.3 FG乳状液微滴含量对FG乳状液-SPI乳状液微聚集体稳定性的影响
采用Lumisizer稳定性分析仪,通过不稳定性指数(Instability Index)分析不同含量的FG乳状液微滴对FG乳状液-SPI乳状液微聚集体稳定性的影响。不稳定性指数越小,乳状液越稳定。从图3可以看出,随着FG乳状液微滴含量的增加,FG-SPI乳状液微聚集体的不稳定性指数先增大后减小再增大。FG乳状液含量较少或较多 (0~20%,80%~100%)时,乳状液的不稳定性指数较小,表明乳状液稳定性较好,这可能是因为乳状液微滴-微滴间相互作用较弱,对乳状液的稳定性影响较小[5]。当FG乳状液含量分布于30%~70%时,乳状液的不稳定性指数明显增大,表明乳状液微滴间相互作用较强时,乳状液的物理稳定性被破坏。通常乳状液界面聚电解质之间静电相互作用强度以及在界面形成的复合物的性质取决于其质量分数、本身表面带电基团的分布、分子结构的稳定以及所带电荷的分布及密度等[6-7]。此外,从热力学方面考虑,进一步开拓这个新方法面临的主要问题是乳状液微聚集体在制备过程中的絮凝问题,即在多糖乳状液微滴的加入过程中,其含量的过小或过大引起的乳状液不稳定现象[8-9]。由此可知,并不是所有应用聚电解质微滴及其分子间的相互作用都能提高乳状液的稳定性,乳状液体系及乳化剂含量选择不当,可能会导致絮凝,最终导致乳状液的不稳定[10]。当FG乳状液含量为60%时,乳状液的不稳定性指数(<0.2)相对较小,较稳定。
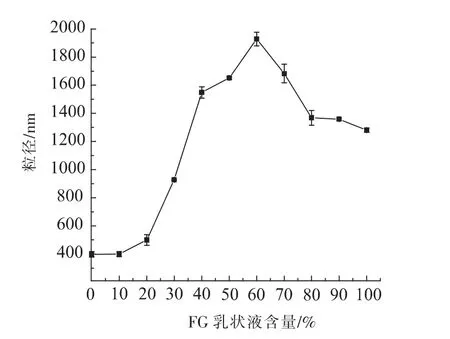
图2 FG乳状液含量对FG乳状液-SPI乳状液微聚集体粒径的影响Fig.2 Effect of FG emulsion content on the droplet size of the heteroaggregated emulsions of FG-coated droplets and SPI-coated droplets
2.4 FG乳状液-SPI乳状液微聚集体剪切流变特性
不同含量的FG乳状液微滴对FG乳状液-SPI乳状液微聚集体流变学特性的影响如图4所示。随着剪切速率的增加,FG乳状液-SPI乳状液的黏度降低,表明样品具有假塑性流体特性。这是因为随着剪切速率增加,乳状液微聚集体内部结构打开,分子按照剪切速率的方向线性排列[11-12]。从图4可看出,当体系不含有FG时,SPI乳状液黏度随剪切速率的曲线趋于平整,表明SPI乳状液接近牛顿流体。当FG乳状液浓度增加时,剪切稀化的特性变得更为明显。这是因为随着剪切速率的增大,聚集体结构被破坏,剪切变稀,样品的黏度和剪切应力减小[13-14]。60%FG乳状液-40%SPI乳状液微聚集体体系黏度比单一的SPI、FG乳状液显著增加,可能是因为二者在该混合比例时,粒径较大,形成特定的空间结构,从而提高黏度值[15-16]。

图3 FG乳状液含量对FG乳状液-SPI乳状液微聚集体不稳定指数变化的影响Fig.3 Effect of FG emulsion content on the instability index of the heteroaggregated emulsions of FG-coated droplets and SPI-coated droplets
图5是所有乳状液体系在剪切速率为95.8 s-1时的黏度,此剪切速率是模拟人体口腔咀嚼速率(100 s-1左右为人体口腔咀嚼速率)[17-18]。同一剪切速率下,FG乳状液含量为60%时的FG乳状液-SPI乳状液微聚集体体系黏度最大,表明含60%FG乳状液的体系具有稳定的空间结构,在此剪切速率下体系对剪切具有一定的抗性,具有很好的剪切流变黏性[19]。
2.5 FG乳状液-SPI乳状液微聚集体微流变特性
采用Formulation微流变分析仪,通过颗粒均方根位移(MSD)分析不同含量的FG乳状液微滴对FG乳状液-SPI乳状液微聚集体微流变特性的影响(图6)。颗粒的布朗运动是由颗粒均方根位移(MSD)与时间关系曲线来表征的[20]。MSD曲线反应样品的黏弹性特征。在纯黏性流体 (牛顿流体)中,粒子MSD与时间呈线性增长;而在一个黏弹性流体中,粒子的均方根位移受到限制,粒子被困在三维微观结构网络中,从而在MSD与时间的关系曲线中形成一个平台区[21]。
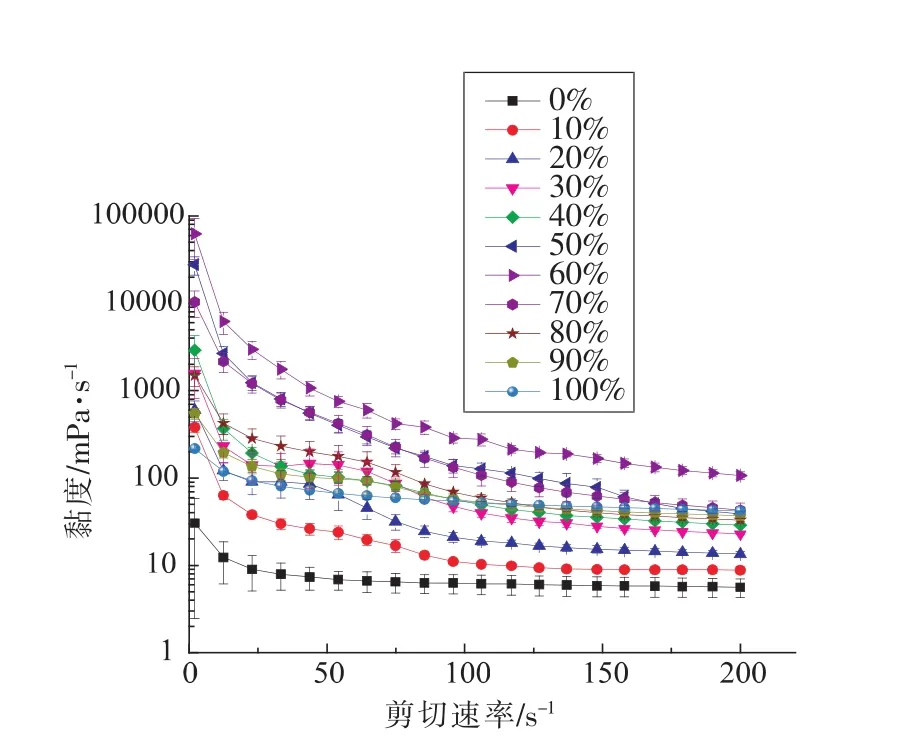
图4 FG乳状液含量对FG乳状液-SPI乳状液微聚集体黏度随剪切速率变化的影响Fig.4 Effect of FG emulsion content on mean viscosity with changing shear rate of the heteroaggregated emulsions of FG-coated droplets and SPI-coated droplets
由图6可知,乳状液微聚集体样品在短的去相关时间段,60%FG乳状液-40%SPI乳状液微聚集体体系的MSD最小,表明此比例条件下二者微滴间的作用力最强,平台区与时间轴所形成的面积最小,该体系的黏弹性最高。弹性因子(EI)与样品的最终流变特征相关,如凝胶网络尺寸、硬度、凝胶化过程的速度、剪切后恢复速度等[22]。从图7看出,含60%FG乳状液的体系EI最大,体系的弹性最大。MSD曲线平台区后的斜率是样品的宏观黏度指数(MVI),斜率越低,粒子在给定的去相关时间内运动的均方位移越小,意味着粒子长去相关时间内运动的布朗运动速度越慢。粒子移动的越慢,样品的黏度就越强。另一方面,粒子移动的越快,样品的黏度越弱。MVI是计算斜率值的倒数,它的变化是与黏度的变化一致的。MVI与样品的最终特性相关,如增稠剂的效果、质地、口感、流动性、长期稳定性等。图7显示含60%FG乳状液的体系MVI值最大,黏度最大。FG乳状液含量对FG乳状液-SPI乳状液微聚集体MVI与EI的影响均呈现先增大后减小的趋势,与上述剪切流变分析结果一致。
2.6 FG乳状液-SPI乳状液微聚集体微观结构

图5 FG乳状液含量对FG乳状液-SPI乳状液微聚集体黏度的影响Fig.5 Effect of FG emulsion content on mean viscosity of the heteroaggregated emulsions of FG-coated droplets and SPI-coated droplets

图6 FG乳状液含量对FG乳状液-SPI乳状液微聚集体均方根位移曲线的影响Fig.6 Effect of FG emulsion content on the mean square displacement(MSD) curves of the heteroaggregated emulsions of FG-coated droplets and SPI-coated droplets
为了进一步观察FG乳状液-SPI乳状液微聚集体的形成情况,采用10×100倍光学显微镜观察其微观结构。图8分别是SPI乳状液(a),60%FG乳状液-40%SPI乳状液微聚集体(b)以及FG乳状液(c)。从图8a可看出,SPI乳状液微滴粒径小,分布均匀,吸附油滴充分;图8c中FG乳状液吸附油滴的效果不如SPI,液滴粒径较大。由图8b可看出60%FG乳状液-40%SPI乳状液形成均匀的微聚集体,在空间上形成特定的网络结构。模拟聚集体的三维结构得出如图9所示的模型,两种乳状液微滴静电吸附,形成一个类似足球状的微聚集体。

图7 FG乳状液含量对FG-SPI微聚集体弹性指数和宏观黏度指数的影响Fig.7 Effect of FG emulsion content on the EI (a) and MVI (b) values of the heteroaggregated emulsions of FG-coated droplets and SPI-coated droplets

图8 FG乳状液-SPI乳状液微聚集体的微观结构Fig.8 Microstructures of SPI emulsion (a),heteroaggregated emulsions of 60%FG-coated droplets and 40%SPI-coated droplets (b),FG emulsion (c)

图9 FG乳状液-SPI乳状液微聚集体的三维结构模型Fig.9 Three-dimensional structure model of the heteroaggregated emulsions of FG-coated droplets and SPI-coated droplets
3 结论
本研究结果表明,60%FG乳状液-40%SPI乳状液异型聚集时,粒径最大,zeta-电位接近0,体系的稳定性系数较小,两种乳状液发生异型聚集,二者之间的稳定效应主要依靠空间位阻效应。剪切流变和微流变学特性表征了60%FG乳状液-40%SPI乳状液体系的高弹性。从微观结构推测,形成了一种特定的空间网络结构,两种微滴牢牢结合在一起。本研究通过异型聚集效应,制备高流变特性的FG乳状液-SPI乳状液微聚集体,为开发油脂模拟物提供数据。
